Alkohole polihydroksylowe
Alkohole polihydroksylowe
Alkohole polihydroksylowe, tak jak alkohole monohydroksylowe:
nie ulegają dysocjacji elektrolitycznej;
nie przewodzą prądu elektrycznego;
odczyn ich wodnych roztworów jest obojętny.
Właściwości fizyczne alkoholi polihydroksylowych
Zapoznaj się z filmem, a dowiesz się, w jaki sposób ilość grup hydroksylowych wpływa na właściwości fizyczne związku chemicznego.

Film dostępny pod adresem /preview/resource/RxIQgXyf1mtwB
Film nawiązujący do treści materiału dotyczącej wpływu obecności większej liczby grup hydroksylowy w cząsteczkach na ich właściwości fizyczne.
Przeanalizuj poniższy wykres i wyjaśnij, jak zmienia się temperatura wrzenia i topnienia alkoholi polihydroksylowych w szeregu homologicznym.
Do wyjaśnienia tego problemu skorzystaj również z innych źródeł informacji.
- 1. zestaw danych:
- Alkohol: glikol etylenowy
- Temperatura topnienia[°C]: -13; Podpis osi wartości: Temperatura (°C)
- Temperatura wrzenia[°C]: 197; Podpis osi wartości: Temperatura (°C)
- 2. zestaw danych:
- Alkohol: gliceryna
- Temperatura topnienia[°C]: 18; Podpis osi wartości: Temperatura (°C)
- Temperatura wrzenia[°C]: 290; Podpis osi wartości: Temperatura (°C)
- 3. zestaw danych:
- Alkohol: erytrytol
- Temperatura topnienia[°C]: 118; Podpis osi wartości: Temperatura (°C)
- Temperatura wrzenia[°C]: 329; Podpis osi wartości: Temperatura (°C)
- 4. zestaw danych:
- Alkohol: ksylitol
- Temperatura topnienia[°C]: 94; Podpis osi wartości: Temperatura (°C)
- Temperatura wrzenia[°C]: 216; Podpis osi wartości: Temperatura (°C)
- 5. zestaw danych:
- Alkohol: sorbitol
- Temperatura topnienia[°C]: 96; Podpis osi wartości: Temperatura (°C)
- Temperatura wrzenia[°C]: 296; Podpis osi wartości: Temperatura (°C)
- 6. zestaw danych:
- Alkohol: perseitol
- Temperatura topnienia[°C]: 185; Podpis osi wartości: Temperatura (°C)
- Temperatura wrzenia[°C]: 272; Podpis osi wartości: Temperatura (°C)
Właściwości chemiczne alkoholi polihydroksylowych
Alkohole polihydroksylowe ulegają tym samym reakcjom chemicznym, co alkohole monohydroksylowe:
reagują z metalami aktywnymi
W wyniku reakcji etano-,-diolu z sodem powstaje etano-,-diolan sodu i wodór:

reagują z kwasami nieorganicznymi
W wyniku reakcji etano-,-diolu z kwasem azotowym() powstaje diazotan() etano-,-diolu i woda:
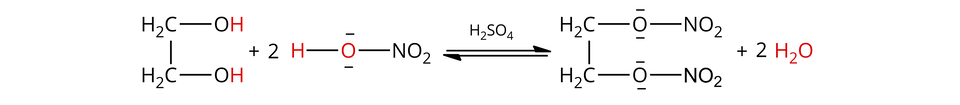
reagują z kwasami organicznymi
W wyniku reakcji etano-,-diolu z kwasem octowym powstaje octan etano-,-diolu i woda:

reagują z tlenkami metali ciężkich – pod wpływem tlenku miedzi() utleniają się na gorąco do związków karbonylowych
W wyniku reakcji etano-,-diolu z tlenkiem miedzi() w podwyższonej temperaturze powstaje oksaloaldehyd, miedź i woda:

reagują z zakwaszonym roztworem dichromianu() potasu, utleniając się do kwasów karboksylowych
W wyniku reakcji etano-,-diolu z dichromianem() potasu w środowisku kwasu siarkowego() powstaje kwas szczawiowy, siarczan() potasu, siarczan()
chromu() i woda:
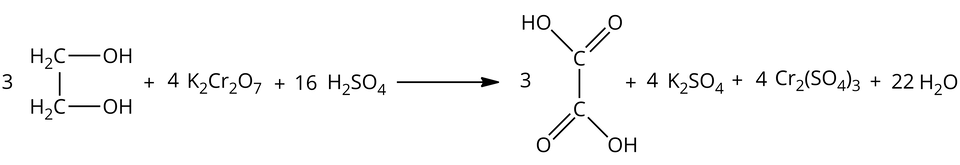
ulegają dehydratacji pod wpływem środowiska kwasowego
W wyniku reakcji etano-,-diolu w środowisku kwasowym powstaje acetaldehyd i woda:

reagują z i
W wyniku reakcji etano-,-diolu z chlorowodorem powstaje ,-dichloroetan i woda:

Czy potrafisz wymienić reakcje, jakim ulegają alkohole polihydroksylowe? Jakie produkty można otrzymać? W poniższym wirtualnym laboratorium można sprawdzić, jakim reakcjom ulega propano-,,-triol. Zaplanuj i przeprowadź eksperymenty, korzystając ze sprzętu, szkła laboratoryjnego i odczynników chemicznych, które pozwolą Ci rozwiązać poniższy problem badawczy. Hipotezy, obserwacje, wyniki i wnioski zanotuj w formularzu. Po wykonaniu eksperymentów rozwiąż poniższe zadania.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DANQL2D7L
Czy potrafisz wymienić reakcje, jakim ulegają alkohole polihydroksylowe? Jakie produkty można otrzymać? Zapoznaj się z opisem przeprowadzonych eksperymentów, a następnie wykonaj polecenia.
Analiza eksperymentu: Badanie reaktywności alkoholi polihydroksylowych.
Problem badawczy: Jakim reakcjom ulegają alkohole polihydroksylowe?
Hipoteza: Propano-,,-triol reaguje z sodem, z kwasami organicznymi oraz ulega dehydratacji pod wpływem stężonego kwasu siarkowego().
Sprzęt laboratoryjny:
cylinder miarowy – podłużne szklane naczynie laboratoryjne w kształcie walca z umieszczoną na ściance podziałką objętości. Służy do odmierzania cieczy;
bibuła do osuszania – kawałek białej chłonnej bibuły;
krystalizator – płaskie naczynie laboratoryjne, które służy do procesu krystalizacji;
pęseta – narzędzie o sprężystych ramionach używane do chwytania przedmiotów, których mały rozmiar utrudnia lub uniemożliwia manipulację za pomocą rąk;
zlewka – naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych;
probówki – podłużne naczynia szklane do przeprowadzania prostych reakcji chemicznych;
pipety Pasteura – wąska rurka do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
palnik gazowy – rodzaj sprzętu z regulacją płomienia, umożliwiający podgrzewanie substancji chemicznych;
trójnóg – urządzenie w kształcie pierścienia, zaopatrzone w trzy wkręcane nogi, mocowane prostopadle do jego powierzchni, służące do ustawiania nad palnikiem naczyń laboratoryjnych, przeznaczonych do podgrzania;
łapa do probówek – rodzaj trzymaka służący do uchwycenia probówki.
Odczynniki chemiczne:
propano-,,-triol (gliceryna);
alkoholowy roztwór fenoloftaleiny;
sód;
kwas etanowy (octowy);
kwas siarkowy() stężony.
Przebieg eksperymentów:
Eksperyment
Odmierzono za pomocą cylindra miarowego centymetrów sześciennych propano-,,-triolu.
Odmierzoną ilość propano-,,-triolu wprowadzono do krystalizatora.
Dodano kilka kropli alkoholowego roztworu fenoloftaleiny.
Wprowadzono mały kawałek sodu (pamiętano o osuszeniu z nafty).
Eksperyment
Do probówki wprowadzono po centymetry sześcienne propano-,,-triolu i kwasu etanowego.
Dodano kilka kropli stężonego kwasu siarkowego().
Probówkę wstawiono do zlewki z gorącą wodą.
Po kilku minutach przelano ciecz z probówki do zlewki z zimną wodą.
Eksperyment
Do probówki wprowadzono propano-,,-triol.
Dodano kilka kropli stężonego kwasu siarkowego().
Obserwacje:
Sód pływa w postaci kulki, która zmniejsza swoją wielkość – sód roztwarza się; wydziela się bezbarwny, bezwonny gaz. Roztwór po dodaniu alkoholowego roztworu fenoloftaleiny zmienił kolor na malinowy.
Wyczuwalny, charakterystyczny zapach.
Wyczuwalny, charakterystyczny zapach.
Wyniki:
Propano-,,-triol ulega reakcji z sodem, w wyniku czego powstaje związek o odczynie zasadowym.
Propano-,,-triol ulega reakcji z kwasem etanowym, w wyniku czego powstaje związek o charakterystycznym zapachu.
Propano-,,-triol ulega reakcji w środowisku stężonego kwasu siarkowego(), w wyniku czego powstaje związek o charakterystycznym zapachu.
Wnioski:
Propano-,,-triol reaguje z sodem, ponieważ obserwowane jest roztwarzanie metalu. W wyniku reakcji chemicznej powstaje propano-,,-triolan sodu o odczynie zasadowym, co jest potwierdzone poprzez malinowe zabarwienie roztworu z fenoloftaleiną. Powstającym bezbarwnym i bezwonnym gazem jest wodór.
Propano-,,-triol reaguje z kwasem etanowym, w wyniku czego powstaje trietanian propano-,,-triolu.
Propano-,,-triol pod wpływem stężonego kwasu siarkowego() ulega dehydratacji, w wyniku czego powstaje propenal.
Hipoteza została potwierdzona.
Zapisz równania reakcji chemicznych, które miały miejsce w powyższym eksperymencie.
propano-jeden,dwa,trzy-triolan sodu + 1. propano-jeden,dwa,trzy-triol, 2. trietanian propano-jeden,dwa,trzy-triolu, 3. wodór, 4. propenal, 5. woda, 6. propano-jeden,dwa,trzy-triolan sodu, 7. woda → 1. propano-jeden,dwa,trzy-triol, 2. trietanian propano-jeden,dwa,trzy-triolu, 3. wodór, 4. propenal, 5. woda, 6. propano-jeden,dwa,trzy-triolan sodu, 7. woda + wodorotlenek sodu
propano-jeden,dwa,trzy-triol + kwas etanowy → 1. propano-jeden,dwa,trzy-triol, 2. trietanian propano-jeden,dwa,trzy-triolu, 3. wodór, 4. propenal, 5. woda, 6. propano-jeden,dwa,trzy-triolan sodu, 7. woda + 1. propano-jeden,dwa,trzy-triol, 2. trietanian propano-jeden,dwa,trzy-triolu, 3. wodór, 4. propenal, 5. woda, 6. propano-jeden,dwa,trzy-triolan sodu, 7. woda
propano-jeden,dwa,trzy-triol pod wpływem kwasu siarkowego(sześć) → 1. propano-jeden,dwa,trzy-triol, 2. trietanian propano-jeden,dwa,trzy-triolu, 3. wodór, 4. propenal, 5. woda, 6. propano-jeden,dwa,trzy-triolan sodu, 7. woda
Produktem jednego z doświadczeń jest związek o podanym wzorze półstrukturalnym:

Odróżnianie alkoholi polihydroksylowych od monohydroksylowych
Alkohole monohydroksylowe można odróżnić od alkoholi polihydroksylowych za pomocą reakcji z wodorotlenkiem miedzi(II). Pozytywny wynik tej reakcji obserwuje się w przypadku alkoholi polihydroksylowych, w których występują co najmniej dwie grupy –OH przy sąsiadujących atomach węgla. Przeprowadż opisaną reakcję w poniższym laboratorium i wykonaj ćwiczenia.
Przeprowadź doświadczenie w laboratorium chemicznym. Rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz swoje obserwacje i wyniki, a następnie sformułuj wnioski.
Szafa laboratoryjna
Analiza doświadczenia: Odróżnianie alkoholu monohydroksylowego od polihydroksylowego.
Problem badawczy: W jaki sposób można odróżnić alkohol monohydroksylowy od polihydroksylowego?
Hipoteza: Za pomocą próby Trommera można odróżnić alkohol monohydroksylowy od polihydroksylowego.
Odczynniki chemiczne: gliceryna (propano-,,-triol), siarczan miedzi – woda , wodorotlenek sodu, etanol, woda destylowana.
Sprzęt laboratoryjny:
dwie zlewki – naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych;
dwie probówki – podłużne naczynie szklane do przeprowadzania prostych reakcji chemicznych;
pipety Pasteura – wąska rurka do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki.
Przebieg doświadczenia:
Przygotowano w dwóch zlewkach -molowy roztwór wodorotlenku sodu oraz -molowy roztwór siarczanu miedzi. Masa molowa hydratu wynosi . Masa molowa jest równa .
Otrzymano wodorotlenek miedzi. W tym celu: przygotowano dwie probówki. Wlano do obu probówek po 5 centymetrów sześciennych -molowego roztworu wodorotlenku sodu. Następnie wlano do obu probówek kilka kropli -molowego roztworu siarczanu miedzi.
Do otrzymanego osadu w probówce numer 1 wlano 3 centymetry sześcienne propano-,,-triolu i wstrząśnięto.
Do drugiej probówki wlano 3 centymetry sześcienne etanolu i wstrząśnięto probówką.
Obserwacje:
Przygotowany wodorotlenek miedzi wytrącił się w postaci galaretowatego niebieskiego osadu. W probówce z gliceryną następuje zmiana zabarwienia z błękitnego na szafirowy oraz roztworzenie osadu wodorotlenku miedzi. W probówce z etanolem nie zaobserwowano objawów reakcji – wciąż widoczny jest niebieski osad.
Wyniki:
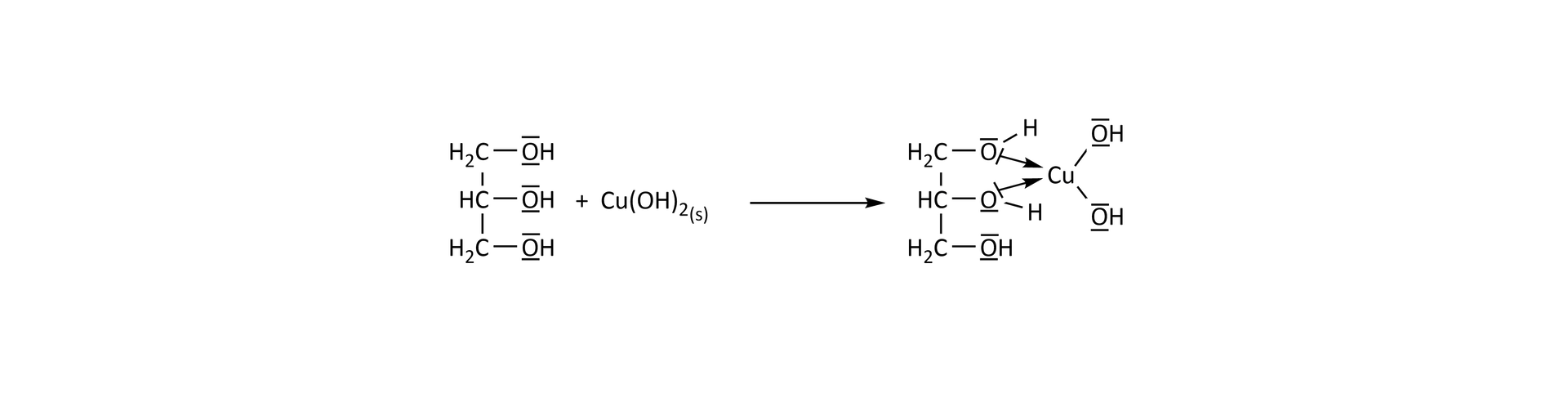
Gliceryna reaguje z wodorotlenkiem miedzi tworząc glicerynian miedzi. Grupy hydroksylowe gliceryny są donorami par elektronowych. Między tymi grupami a atomami miedzi powstają wiązania koordynacyjne. Utworzony kompleks jest łatwo rozpuszczalny w wodzie.
Wnioski:
Jest to reakcja charakterystyczna dla alkoholi polihydroksylowych. Etanol jest alkoholem monohydroksylowym i nie reaguje z wodorotlenkiem miedzi. Za pomocą próby Trommera można odróżnić alkohol monohydroksylowy od polihydroksylowego – hipoteza potwierdziła się.
Zaznacz wzory półstrukturalne alkoholi, które po dodaniu do świeżo strąconego wodorotlenku miedzi spowodują jego roztworzenie, a roztwór przyjmie szafirowe zabarwienie.
Poniższy schemat przedstawia moment doświadczenia, w którym drugi z reagentów nie został jeszcze dodany do probówki. Pod każdą probówką umieść odpowiednie obserwacje po dodaniu drugiego reagenta.