Właściwości chemiczne fenoli
Właściwości kwasowe fenolu
W myśl teorii Brønsteda‑Lowry’ego, fenol pełni funkcję kwasu. Jest kwasem silniejszym od wody (, ), ale słabszym od kwasu węglowego ( ). Należy do elektrolitów słabych – tylko niewielki procent jego cząsteczek dysocjuje na jony, a reszta zostaje w roztworze w postaci niezdysocjowanej.
Czy wiesz, z czego wynikają kwasowe właściwości fenolu? Zapoznaj się z poniższym filmem, a następnie rozwiąż poniższe ćwiczenia.

Film dostępny pod adresem /preview/resource/RhUTSv2A70xRa
Film tłumaczy właściwości kwasowe fenolu.
Opisz, z czego wynikają właściwości kwasowe fenolu?
Porównanie mocy fenolu z innymi kwasami
Fenol wykazuje właściwości kwasowe, ponieważ w wyniku procesu dysocjacji elektrolitycznej powstaje anion fenolanowy i kation hydroniowy.

Czy potrafisz stwierdzić, na podstawie wartości stałej dysocjacji, który kwas jest najmocniejszy? Zapoznaj się z filmem, spróbuj rozwiązać samodzielnie zawarte w nim zadania, a następnie odpowiedz na poniższe pytania.

Film dostępny pod adresem /preview/resource/RaPBamGThSqdn
Film udziela odpowiedzi na pytanie, czy fenol jest mocnym kwasem.
K indeks dolny, a, koniec indeksu dolnego, równa się, jeden przecinek osiem, razy, dziesięć indeks górny, minus, pięć, koniec indeksu górnego dla kwasu octowego
K indeks dolny, a, koniec indeksu dolnego, równa się, jeden przecinek osiem, razy, dziesięć indeks górny, minus, cztery, koniec indeksu górnego dla kwasu mrówkowego
K indeks dolny, a, koniec indeksu dolnego, równa się, jeden przecinek cztery, razy, dziesięć indeks górny, minus, pięć, koniec indeksu górnego dla kwasu propionowego
K indeks dolny, a, koniec indeksu dolnego, równa się, jeden przecinek trzy, razy, dziesięć indeks górny, minus, pięć, koniec indeksu górnego dla fenolu.
Najmocniejszym z podanych kwasów jest: Możliwe odpowiedzi: 1. fenol., 2. kwas mrówkowy., 3. kwas propionowy., 4. kwas octowy.
K indeks dolny, a, koniec indeksu dolnego, równa się, jeden przecinek osiem, razy, dziesięć indeks górny, minus, pięć, koniec indeksu górnego dla kwasu octowego
K indeks dolny, a, koniec indeksu dolnego, równa się, jeden przecinek osiem, razy, dziesięć indeks górny, minus, cztery, koniec indeksu górnego dla kwasu mrówkowego
K indeks dolny, a, koniec indeksu dolnego, równa się, jeden przecinek cztery, razy, dziesięć indeks górny, minus, pięć, koniec indeksu górnego dla kwasu propionowego
K indeks dolny, a, koniec indeksu dolnego, równa się, jeden przecinek trzy, razy, dziesięć indeks górny, minus, pięć, koniec indeksu górnego dla fenolu.
Najsłabszym z podanych kwasów jest: Możliwe odpowiedzi: 1. kwas mrówkowy., 2. kwas octowy., 3. fenol., 4. kwas benzoesowy.
Reakcje z metalami i zasadami
Fenol reaguje z metalami aktywnymi i mocnymi zasadami. W reakcjach tych powstają fenolany, czyli sole fenolu posiadające anion , gdzie -Ar to grupa arylowa. Przykładowe reakcje fenolu z sodem i wodorotlenkiem potasu zaprezentowano poniżej.

W reakcji fenolu z roztworem wodorotlenku potasu powstaje fenolan potasu, który, jako sól słabego kwasu i mocnej zasady, ulega hydrolizie anionowej. Wodny roztwór tego związku ma odczyn zasadowy, co potwierdza jonowy skrócony zapis tego procesu.

Wykrywanie fenoli
Reakcją charakterystyczną dla fenoli jest reakcja z solami żelaza(III), w której tworzą się związki zabarwiające roztwór na kolor fioletowy (lub granatowy). Powstające fenolany żelaza(III) mają charakter związków koordynacyjnych. Reakcja z jonami żelaza(III) pozwala na wykrywanie nawet śladowych ilości fenolu.
Reakcje fenolu jako związku aromatycznego
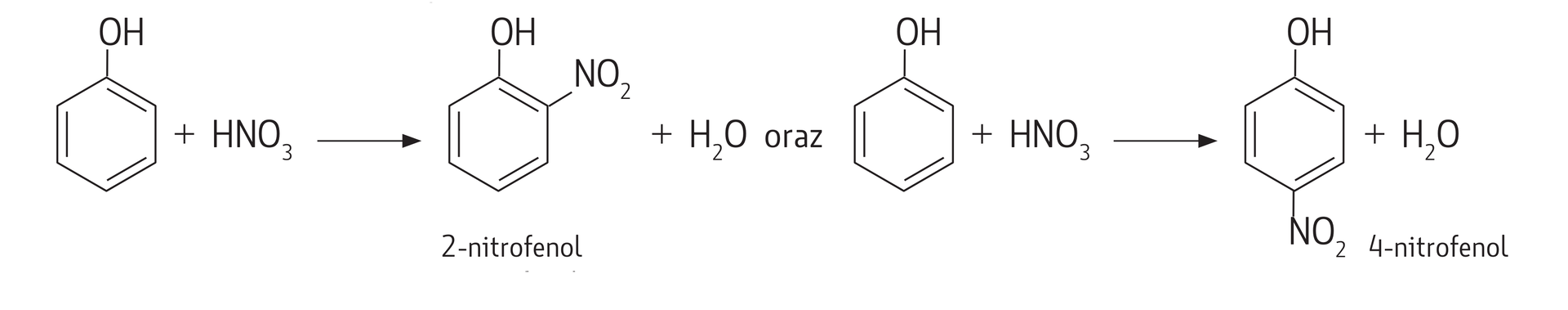
Fenol jest związkiem aromatycznym i dlatego ulega również reakcjom charakterystycznym dla tych związków, np. bromowaniu i nitrowaniu. Reakcje te zachodzą dużo łatwiej niż w przypadku benzenu:
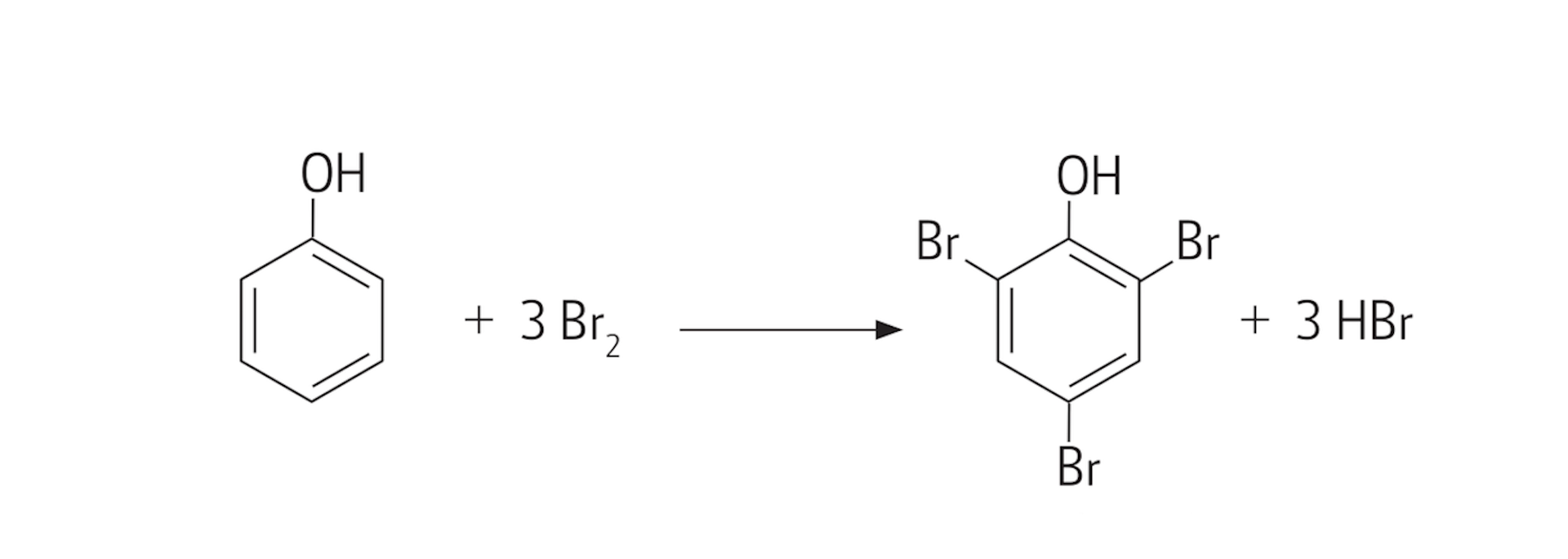
bromowanie (bez katalizatora) – powstaje 2,4,6‑tribromofenol;

nitrowanie (rozcieńczony ) – powstaje mieszanina 2‑nitrofenolu i 4‑nitrofenolu.
Grupa –OH w cząsteczce fenolu, jako podstawnik pierwszego rodzaju, kieruje następny podstawnik na pozycje 1,2 i 1,4 (powstają dwa produkty organiczne z przewagą izomeru 1,4).

Spróbuj rozwiązać poniższe ćwiczenia, które opierają się na reakcjach fenolu jako związku zawierającego pierścień aromatyczny.
Uczeń przeprowadził doświadczenie opisane poniższym równaniem reakcji. Opisz, co zaobserwował uczeń podczas wykonywania tego eksperymentu.
Zapisz równania reakcji nitrowania fenolu. Wyjaśnij, dlaczego w efekcie tego procesu powstaje mieszanina dwóch związków?