Porównanie alkoholi i fenoli
Porównanie alkoholi i fenoli
Alkohole i fenole to związki, w których cząsteczkach występuje grupa hydroksylowa -OH, przyłączona do atomu węgla. Różnica polega na tym, że w alkoholach atom węgla buduje alifatyczny łańcuch węglowy, a jego orbitalom atomowym przypisuje się stan hybrydyzacji . W fenolach natomiast, atom węgla, związany z grupą hydroksylową, buduje pierścień aromatyczny. Stan hybrydyzacji orbitali atomowych tego atomu węgla to zatem . Schematycznie alkohole i fenole oznacza się odpowiednio jako: oraz , gdzie to łańcuch węglowodorowy, a to pierścień aromatyczny. Aby odróżnić alkohole od fenoli, stosuje się szereg metod, z którymi zapoznasz się w tym materiale.
Właściwości fizyczne
Wraz ze wzrostem długości łańcucha węglowodorowego alkoholu, maleje jego lotność oraz rozpuszczalność w wodzie. Im dłuższy łańcuch węglowodorowy, tym większa masa alkoholu, a tym samym potrzebne jest więcej energii, aby zmienić stan skupienia. Ponadto, im więcej atomów węgla posiada alkohol, tym mniejszy jest efekt obecności tlenu, co prowadzi do osłabienia wiązania w .
Fenole stosunkowo łatwo ulegają reakcji substytucji elektrofilowej, której produkty odznaczają się odmiennymi właściwościami. Przykładowo -metylofenol charakteryzuje się mniejszą rozpuszczalnością w wodzie niż fenol, a ,,-trinitrofenol to związek występujący w postaci żółtych kryształów, w odróżnieniu od przezroczystych kryształów fenolu.
Właściwości fizyczne alkoholi zmieniają się wraz z ilością atomów węgla w cząsteczce. Im większa ich liczba w łańcuchu, tym większa masa molowa, a tym samym mniej lotny homolog, co prowadzi do konieczności dostarczenia większej energii, np. w celu doprowadzenia odpowiedniego alkoholu o dłuższym łańcuchu do wrzenia. Ponadto wraz z większą liczbą atomów węgla w łańcuchu zmniejsza się hydrofilowość rozpatrywanej cząsteczki – a zatem obniża się rozpuszczalność w rozpuszczalnikach polarnych. Wpływ na ich właściwości fizyczne ma również rozgałęzienie łańcucha węglowodorowego. Cząsteczki o liniowo połączonych atomach węgla w łańcuchu będą wymagały do dostarczenia większej energii w celu doprowadzenia ich do temperatury wrzenia. Przykładowo czterowęglowy alkohol tert-butylowy (-metylopropan--ol: - pod ciśnieniem ) posiada mniejszą temperaturę wrzenia niż jego izomer alkohol n-butylowy (butan--ol: - pod ciśnieniem ). W przypadku fenoli właściwości fizyczne zmieniają się wraz z rodzajem występujących w pierścieniu aromatycznym podstawników i z tego względu mogą być bardzo zróżnicowane. Poniżej przedstawiono porównanie tych właściwości na przykładzie typowych przedstawicieli obu grup, czyli etanolu i fenolu.
Występowanie grupy hydroksylowej w cząsteczkach alkoholi i fenoli nie powoduje ich podobieństwa we właściwościach fizycznych. Alkohole i fenole wykazują duże różnice pod kątem charakterystyki fizycznej, ze względu na różną budowę. Alkohole to pochodne węglowodorów alifatycznych, a fenole – pochodne węglowodorów aromatycznych. Należą więc one do grup o odmiennych właściwościach fizykochemicznych.
Sprawdzanie odczynu
Alkohole nie ulegają dysocjacji elektrolitycznej pod wpływem wody – odczyn ich wodnego roztworu jest więc obojętny. Z kolei fenole to słabe kwasy, które ulegają dysocjacji elektrolitycznej pod wpływem wody. Odczyn ich wodnych roztworów jest kwasowy.
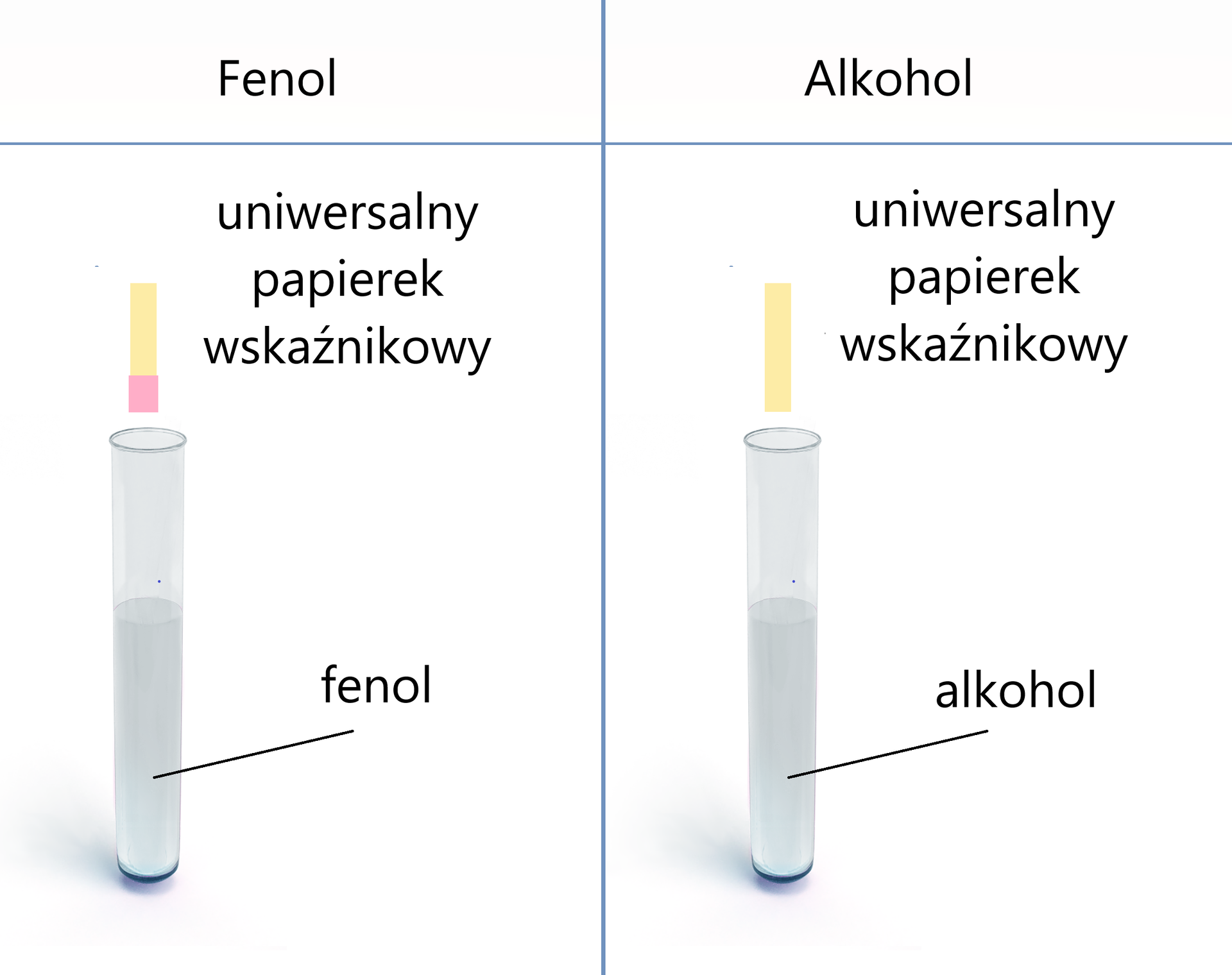
Poniżej przedstawiono porównanie zachowania roztworu fenolu oraz etanolu wobec uniwersalnego papierka wskaźnikowego.
Zapoznaj się z opisem ilustracji przedstawiającej porównanie zachowania roztworu fenolu oraz etanolu wobec uniwersalnego papierka wskaźnikowego.
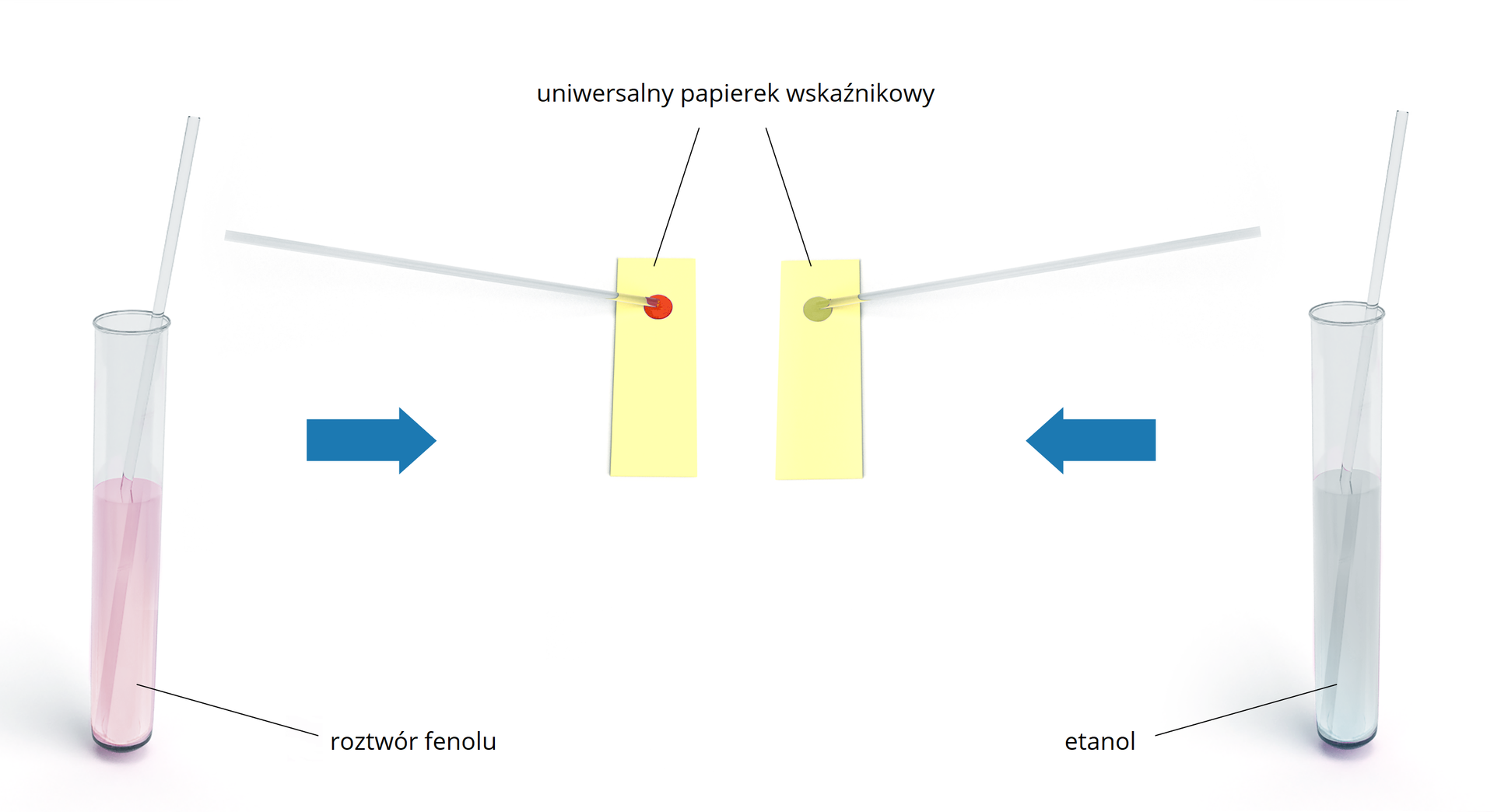
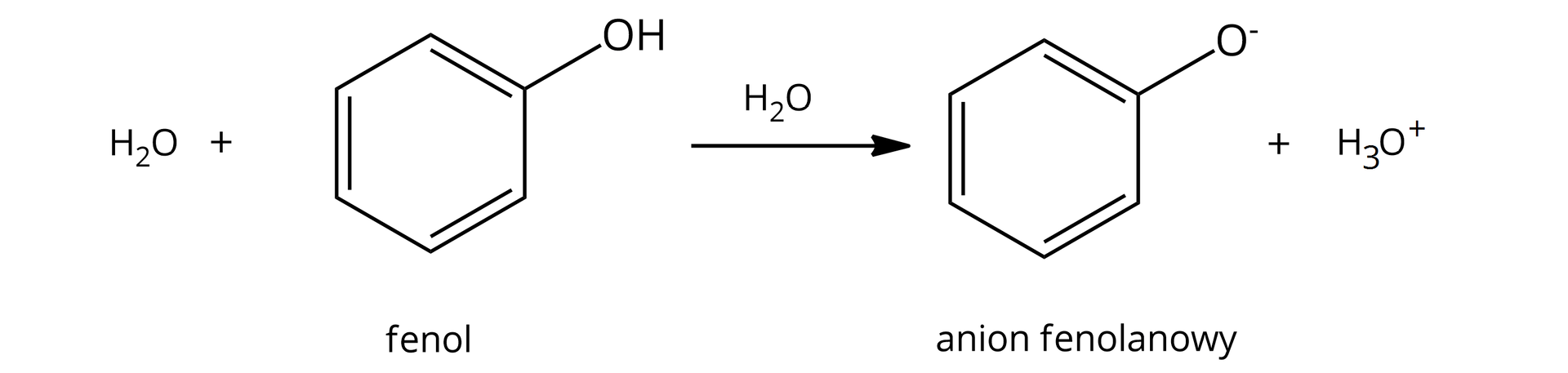
Uniwersalny papierek wskaźnikowy w roztworze fenolu barwi się na kolor jasnoczerwony, co świadczy o odczynie kwasowym. Fenol ulega dysocjacji zgodnie z poniższym równaniem:
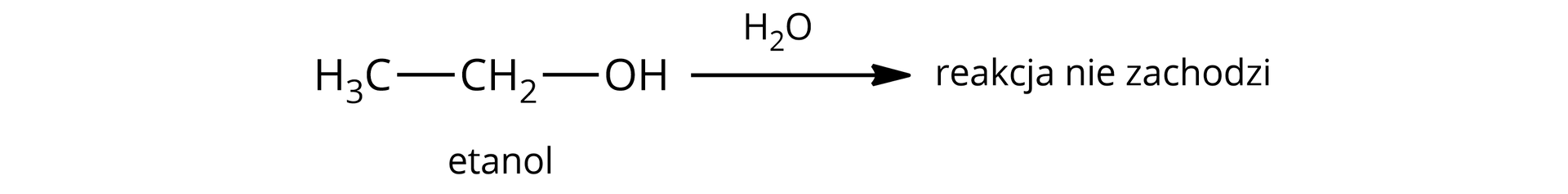
W przypadku etanolu papierek wskaźnikowy pozostaje żółty, co wskazuje na odczyn obojętny. Etanol nie dysocjuje już w wodzie, ponieważ jego stała dysocjacji kwasustała dysocjacji kwasu jest niższa niż stała dysocjacji kwasu dla wody, co oznacza, że etanol wykazuje jeszcze słabsze właściwości kwasowe niż woda.
związek | wartość w 25°C | wartość w 25°C |
fenol | 1,3 · 10Indeks górny -10-10 | 9,9 |
woda | 1,8 · 10Indeks górny -16-16 | 15,7 |
etanol | 1,3 · 10Indeks górny -16-16 | 15,9 |
Użycie wskaźnika kwasowo‑zasadowego, np. uniwersalnego papierka wskaźnikowego, oranżu metylowego czy wskaźnika uniwersalnego pozwala na odróżnienie alkoholi od fenoli. Należy jednak pamiętać, że w przypadku fenolu jego roztwór musi być stężony i przygotowany w gorącej wodzie, ponieważ rozpuszcza się on jedynie w wysokiej temperaturze. Co więcej – ani alkohole, ani związki aromatyczne, zawierające ugrupowanie fenolowe, nie mogą być związane z innymi grupami kwasowymi lub zasadowymi, które wpływają na odczyn całego związku chemicznego.
Reakcja z
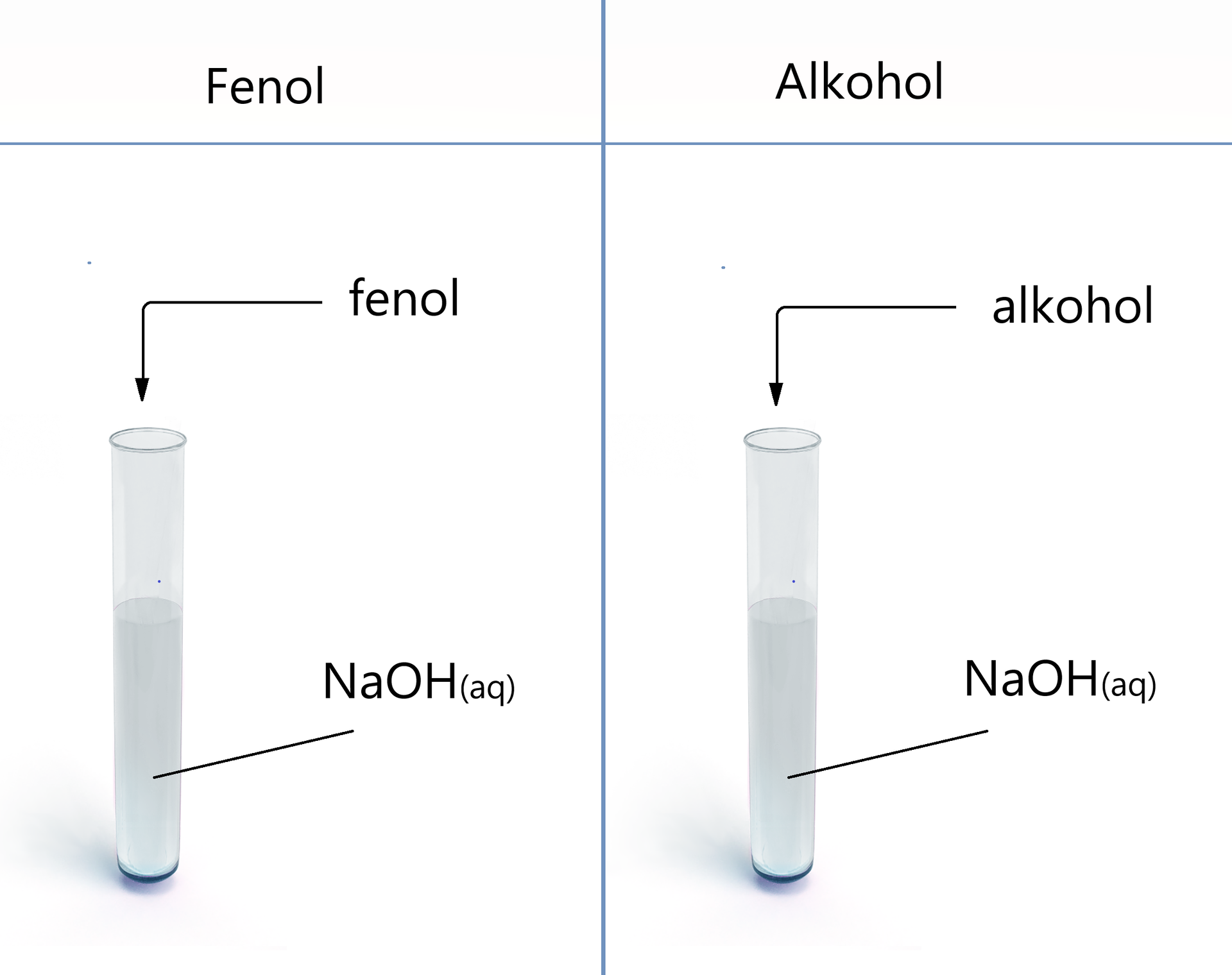
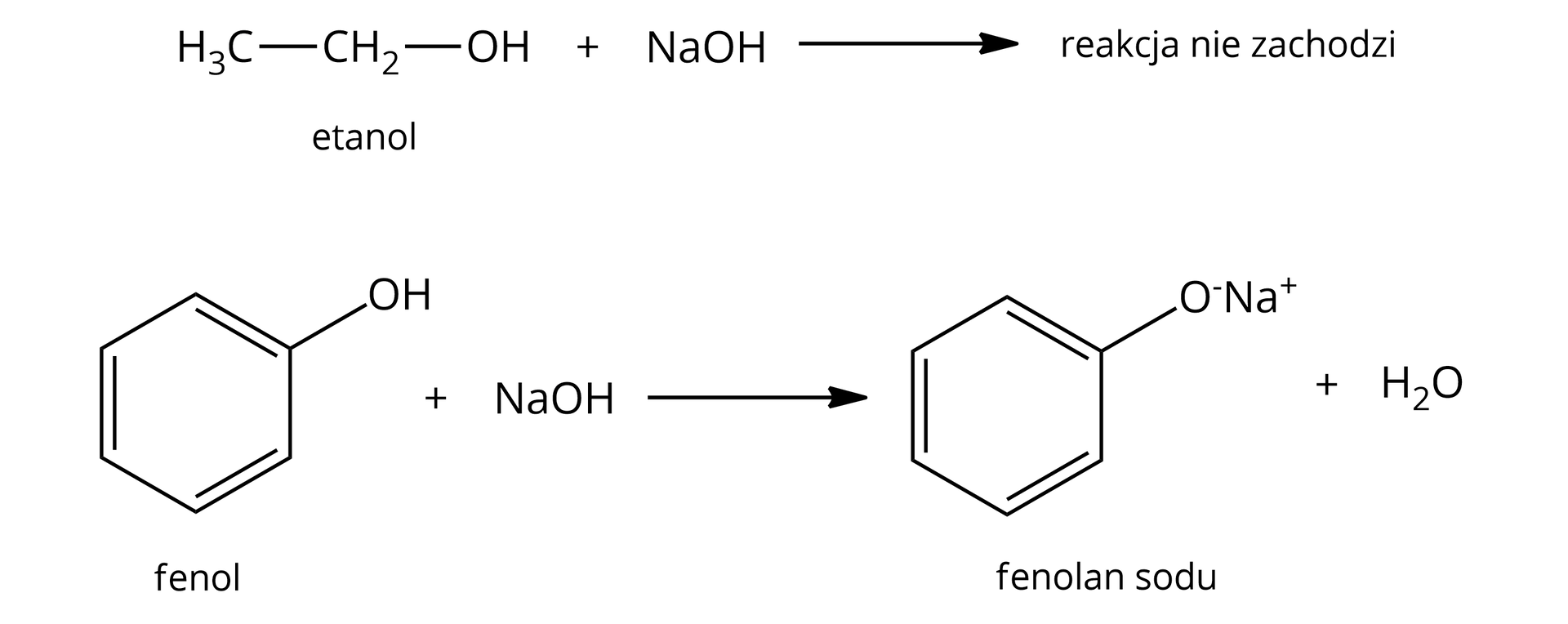
Fenol, jako słaby kwas, reaguje z wodnymi roztworami mocnych zasad, np. , zgodnie z poniższym równaniem reakcji:

Produktem reakcji fenolu (benzenolu) z wodorotlenkiem sodu jest sól – fenolan sodu (benzenolan sodu).
Alkohole mają właściwości kwasowe, ale na tyle słabe, że można je wykazać jedynie w reakcji z metalami aktywnymi, ponieważ tylko te wypierają wodór z alkoholu. Alkohole więc nie reagują z zasadami, jak choćby lub .
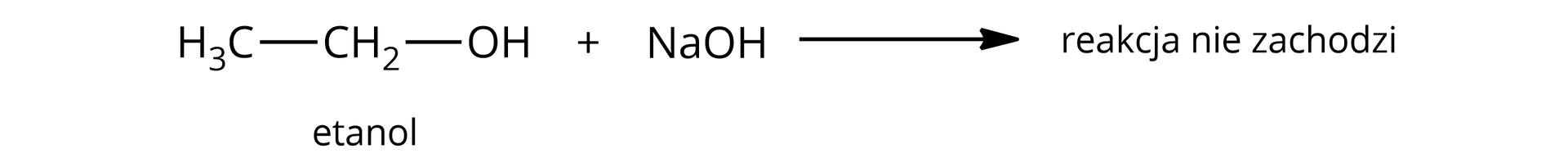
Fenol posiada zatem silniejsze właściwości kwasowe niż alkohole.
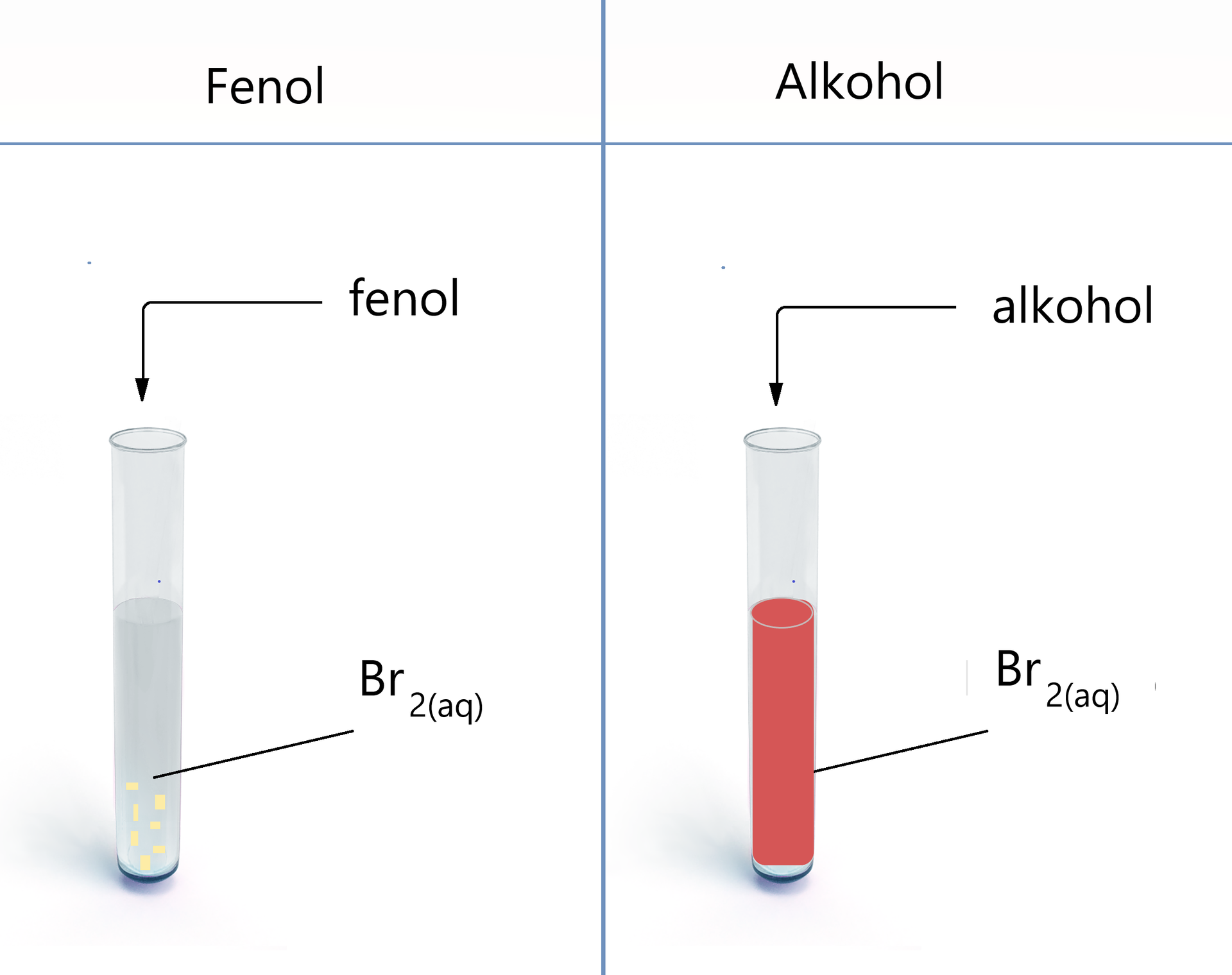
Reakcja charakterystyczna dla fenoli: zachowanie wobec
Najszybszą metodą na odróżnienie alkoholi od fenoli jest przeprowadzenie próby z wodnym roztworem chlorku żelaza(III). Jest to jakościowa metoda potwierdzająca obecność ugrupowania fenolowego w cząsteczce. Związki aromatyczne zawierające grupę , bezpośrednio związaną z pierścieniem w reakcji z , tworzą charakterystyczne związki koordynacyjnezwiązki koordynacyjne o barwie ciemnofioletowej. Zabarwienie roztworu zależy jednak od stężenia chlorku żelaza(III).
Poniżej przedstawiono wynik połączenia roztworów fenolu oraz .
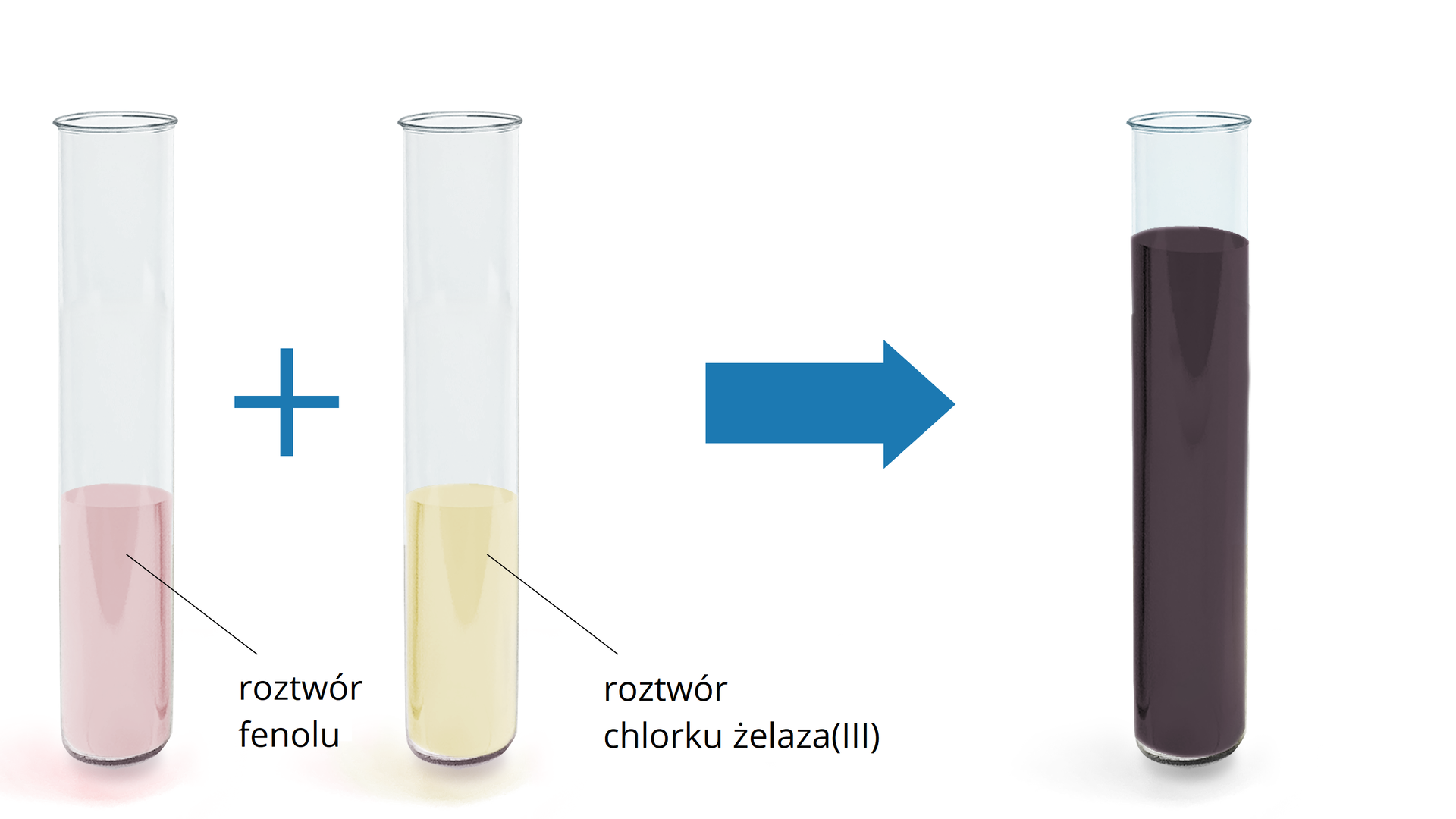
Równanie reakcji powstawania powyższego związku koordynacyjnego o barwie fioletowej można przedstawić następująco:
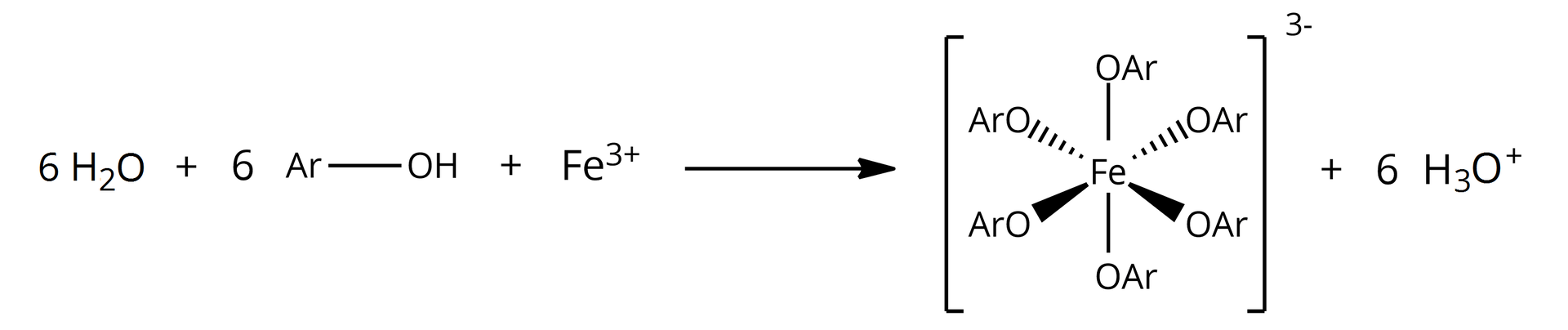
Jakie są różnice w reaktywności pomiędzy alkoholami i fenolami? Zapoznaj się z grafiką interaktywną, która przedstawia podsumowanie rozbieżności pomiędzy tymi związkami, a następnie przejdź do wykonania zadań.
W oparciu o wiadomości zdobyte w „Przeczytaj” i w grafice interaktywnej, uzupełnij schematy doświadczeń, przeciągając pola z odczynnikami w wybrane miejsce tablicy interaktywnej.
Pamiętaj, że nie wszystkie odczynniki muszą być wykorzystane.
wskaźnikowy, uniwersalny papierek
wskaźnikowy, stężony kwas siarkowy(VI), stężony kwas siarkowy(VI), fenol (aq), fenol (aq), fenol (aq), fenol (aq), etanol, etanol, etanol, etanol, świeżo strącony Cu(OH)2, FeCl3 (aq), FeCl3 (aq), Br2 (aq), Br2 (aq), błękit bromotymolowy, błękit bromotymolowy
W oparciu o wiadomości zdobyte w „Przeczytaj” i w grafice interaktywnej, wykonaj ćwiczenia.
Zapisz obserwacje do każdego z powyższych schematów reakcji w tabeli zamieszczonej pod poleceniem.
Zapisz obserwacje do każdej reakcji w tabeli zamieszczonej pod poleceniem.
Zapisz wnioski wynikające z zastosowania każdej z metod odróżniania alkoholi od fenoli.
Na podstawie zdobytej wiedzy o alkoholach i fenolach, przeprowadź odpowiednie reakcje chemiczne alkoholi i fenoli w wirtualnym laboratorium, obserwuj ich przebieg oraz porównaj otrzymane wyniki. Zwróć uwagę na różnice w reaktywności obu grup związków i sformułuj wnioski. Następnie rozwiąż ćwiczenia.
W jaki sposób porównasz właściwości fenolu i alkoholi? Wśród sprzętu laboratoryjnego oraz odczynników chemicznych znajdują się te niezbędne do przeprowadzenia eksperymentu. Zaplanuj eksperyment chemiczny, przeprowadź go, zapisz obserwacje, wyniki i wnioski. Zapisz odpowiednie równania reakcji chemicznych.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D8HT48V3E
Zapoznaj się z opisem doświadczenia, w którym porównano właściwości fenolu i alkoholu.
Analiza eksperymentu: Porównanie fenolu i alkoholi: metanolu i etanolu pod względem ich właściwości chemicznych
Problem badawczy: Czy badane w doświadczeniu fenol i alkohole reagują z wodnym roztworem wodorotlenku sodu oraz kwasem bromowodorowym?
Hipoteza: Fenol w odróżnieniu od etanolu reaguje z wodnym roztworem wodorotlenku sodu, natomiast metanol w odróżnieniu od fenolu reaguje z kwasem bromowodorowym.
Sprzęt laboratoryjny:
cztery probówki – podłużne naczynia szklane do przeprowadzania prostych reakcji chemicznych;
cztery pręciki szklane służący do mieszania cieczy;
łyżeczka – długi trzonek wykonany ze szkła, porcelany lub metalu zakończony z jednej strony łyżeczką. Służy do nabierania sypkich substancji chemicznych;
pipety Pasteura – wąska rurka do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki.
Odczynniki chemiczne:
etanol;
metanol;
fenol;
woda destylowana;
wodny roztwór oranżu metylowego;
alkoholowy roztwór fenoloftaleiny;
roztwór wodorotlenku sodu;
roztwór chlorku żelaza.
Przebieg eksperymentu:
Eksperyment
Aby przygotować odpowiedni roztwór, do jednej z probówek wsypano fenol, a następnie wlano do niego wodę.
Zawartość zamieszano pręcikiem szklanym.
Do drugiej probówki wlano pięć centymetrów sześciennych etanolu.
Do obu probówek dodano jednym centymetrze sześciennym ilość roztworu wodorotlenku sodu. Obie probówki zamieszano szklanym pręcikiem.
Następnie za pomocą szklanych bagietek zawartość wymieszano.
Niewielkie ilości roztworów naniesiono za pomocą bagietek na uniwersalne papierki wskaźnikowe.
Eksperyment
Do jednej z probówek dodano dwa centymetry sześcienne metanolu, a do drugiej fenol.
Do probówki, w której znajdował się fenol, dodano wodę.
Następnie do obu probówek dodano wodny roztwór chlorku żelaza.
Eksperyment
Aby przygotować odpowiedni roztwór, do jednej z probówek wsypano fenol, a następnie dodano pięć centymetrów sześciennych wody.
Zawartość zamieszano pręcikiem szklanym.
Do drugiej probówki wlano dwa centymetry sześcienne metanolua następnie dodano pięć centymetrów sześciennych wody.
Probówkę z fenolem umieszczono w drewnianej łapie, po czym ogrzano w płomieniu palnikai ostudzono.
Niewielkie ilości roztworów naniesiono za pomocą bagietek szklanych na uniwersalne papierki wskaźnikowe.
Obserwacje:
Eksperyment : fenol nie do końća rozpuszcza się w wodzie o temperaturze pokojowej, papierek w przypadku fenololu przybrał jasnozielone zabarwienie, natomiast w przypadku etanolu – ciemnoniebieskie;
Eksperyment : w probówce z metanolem nie zaobserwowano zmian, a w probówce z fenolem po dodaniu żółtego roztworu chlorku żelaza roztwór o fioletowym zabarwieniu, tak zwanym fiołkowym;
Eksperyment : papierek w przypadku fenololu przybrał pomarańczowo‑czerwone zabarwienie, natomiast w przypadku etanolu – żółte.
Wyniki:
Eksperyment : mieszanina wodnego roztworu fenolu i wodorotlenku sodu ma słabo zasadowy charakter, z kolei mieszanina etanolu z wodnym roztworem wodorotlenku sodu wykazuje charakter silnie zasadowy, zatem fenol reaguje z wodnym roztworem wodorotlenku sodu, a pH roztworu otrzymanego w wyniku reakcji fenolu z wodorotlenkiem sodu, w warunkach prowadzenia eksperymentu, wynosi ok. (odczyn zasadowy). Etanol nie reaguje z wodnym roztworem wodorotlenku sodu, a pH otrzymanego roztworu wynosi ok. (równe jest w przybliżeniu pH użytego w doświadczeniu wodnego roztworu wodorotlenku sodu);
Eksperyment : fenol reaguje z chlorkiem żelaza w środowisku wodnym, tworząc dobrze rozpuszczalny w wodzie związek kompleksowy o fioletowym zabarwieniu. Metanol nie reaguje z chlorkiem żelaza.
Eksperyment : po ogrzaniu fenol dobrze rozpuszcza się w wodzie, a odczyn wodnego roztworu fenolu jest kwasowy, natomiast metanol jest dobrze rozpuszczalny w wodzie, a jego wodny roztwór ma obojętny odczyn.
Wnioski:
Hipoteza została potwierdzona – fenol wykazuje inne właściwości chemiczne niż alkohole (metanol i etanol).
W oparciu o wynik doświadczenia ustal, który ze związków chemicznych - metanol czy fenol, wykazuje silniejsze właściwości kwasowe. Odpowiedź krótko uzasadnij.
W oparciu o odpowiednie obliczenia uzasadnij uzyskany wynik eksperymentu, w którym określono zachowanie się fenolu wobec wodnego roztworu wodorotlenku sodu. Załóż, że w czasie trwania eksperymentu użyto wodnego roztworu o stężeniu oraz wodnego roztworu zawierającego stechiometryczną ilość fenolu, a eksperyment prowadzono w temperaturze .