Właściwości fizyczne alkoholi monohydroksylowych
Właściwości fizyczne alkoholi monohydroksylowych
Poniżej przedstawiono właściwości fizyczne wybranych, nasyconych, alifatycznych alkoholi. Czy wszystkie alkohole mają te same cechy fizyczne?
Zapoznaj się z opisem grafiki dotyczącej właściwości fizycznych wybranych, nasyconych, alifatycznych alkoholi. Czy wszystkie alkohole mają te same cechy fizyczne?
Przeanalizuj poniższy wykres i wyjaśnij, jak zmienia się temperatura wrzenia i topnienia alkoholi w szeregu homologicznym.
- 1. zestaw danych:
- Alkohol: metanol
- Temperatura topnienia[°C]: -97.7; Podpis osi wartości: Temperatura (°C)
- Temperatura wrzenia[°C]: 64.65; Podpis osi wartości: Temperatura (°C)
- 2. zestaw danych:
- Alkohol: etanol
- Temperatura topnienia[°C]: -114.1; Podpis osi wartości: Temperatura (°C)
- Temperatura wrzenia[°C]: 78.30; Podpis osi wartości: Temperatura (°C)
- 3. zestaw danych:
- Alkohol: dekan‑1-ol
- Temperatura topnienia[°C]: 6.9; Podpis osi wartości: Temperatura (°C)
- Temperatura wrzenia[°C]: 230; Podpis osi wartości: Temperatura (°C)
- 4. zestaw danych:
- Alkohol: dodekan‑1-ol
- Temperatura topnienia[°C]: 23.5; Podpis osi wartości: Temperatura (°C)
- Temperatura wrzenia[°C]: 259; Podpis osi wartości: Temperatura (°C)
Rozpuszczalność
Obecność silnie spolaryzowanego wiązania determinuje właściwości fizyczne i chemiczne alkoholi. Silna polaryzacja wiązania sprawia, że cząsteczki alkoholi są dipolami.

Istnienie wolnych par elektronowych atomu tlenu w cząsteczce alkoholu oraz jego silna elektroujemność umożliwiają tworzenie wiązań wodorowych pomiędzy cząsteczkami alkoholi i wody, a także pomiędzy cząsteczkami alkoholi.
Im krótszy łańcuch węglowy cząsteczki alkoholu, tym bardziej polarny jest jej charakter. Wraz ze wzrostem liczby atomów węgla w łańcuchu, czyli wzrostem wpływu tego łańcucha na właściwości związku, maleje rozpuszczalność w wodzie i reaktywność alkoholi. Dzieje się tak dlatego, że długi łańcuch węglowodorowy staje się dominującą częścią cząsteczki alkoholu. Wyższe alkohole równie dobrze rozpuszczają się w rozpuszczalnikach organicznych, np. w heksanie i innych węglowodorach. Wraz ze wzrostem liczby grup w cząsteczce alkoholu, wzrasta ich rozpuszczalność w wodzie.
Zmiany właściwości alkoholi w szeregu homologicznymszeregu homologicznym przedstawiono na poniższych wykresach.
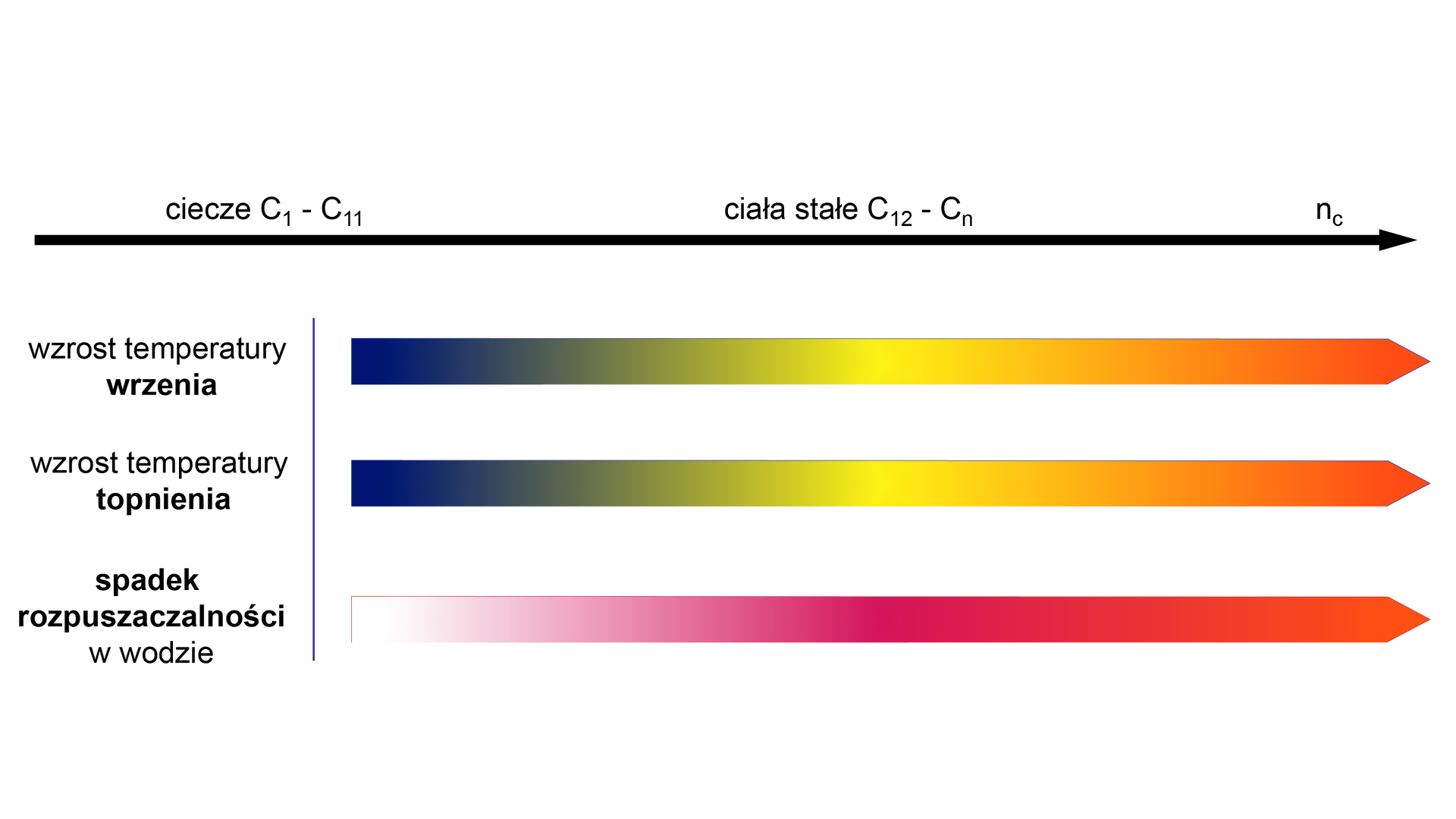
Pierwsze cztery, w szeregu homologicznym, nasycone alkohole monohydroksylowe mieszają się z wodą w każdym stosunku. Wynika to z ich zdolności do tworzenia z cząsteczkami wody wiązań wodorowych, z czym związane jest zjawisko kontrakcjizjawisko kontrakcji.
Kontrakcja
Mieszając etanol z wodą otrzymujemy mieszaninę, której objętość jest mniejsza od sumy objętości składników. Ta właściwość alkoholi wynika właśnie ze zjawiska kontrakcjikontrakcji.

Obecność grup prowadzi do asocjacji cząsteczek alkoholu, dzięki czemu nasycone alkohole monohydroksylowe mają temperatury wrzenia i topnienia odpowiednio wyższe od temperatur wrzenia i topnienia węglowodorów o tej samej liczbie atomów węgla w cząsteczce.
Dwa rodzaje oddziaływań, które wpływają na podwyższenie temperatur wrzenia i topnienia w cząsteczkach alifatycznych alkoholi w stosunku do odpowiednich alkanów, to wiązania wodorowe oraz oddziaływania dipol–diopl.

Aby poznać i zrozumieć właściwości alkoholi związane z rozpuszczalnością i temperaturą wrzenia, przeprowadź poniższe wirtualne laboratorium. Zwróć uwagę na zależność temperatury wrzenia od budowy cząsteczek alkoholi. Następnie przeanalizuj otrzymane wyniki i rozwiąż polecenia zamieszczone pod laboratorium.
Wykorzystując wirtualne laboratorium, przeanalizuj, jak zmieniają się właściwości fizyczne alkoholi w szeregu homologicznym. Przeprowadź badanie rozpuszczalności alkoholi w wodzie oraz oznacz ich temperatury wrzenia, a następnie rozwiąż przedstawione zadania.
W wirtualnym laboratorium badano, w jaki sposób zmieniają się właściwości fizyczne alkoholi w szeregu homologicznym. W tym celu przeprowadzono badania rozpuszczalności alkoholi w wodzie oraz oznaczono ich temperatury wrzenia.
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D9F7U3V1N
Na podstawie badania rozpuszczalności alkoholi w wodzie sformułuj wniosek, który określi zależność pomiędzy rozpuszczalnością alkoholi w wodzie a wzrostem długości łańcucha węglowego w ich cząsteczce.