Słownik
Słownik
związki organiczne, które powszechnie występują w organizmach żywych, zawierające w cząsteczce co najmniej jedną grupę karboksylową i co najmniej jedną grupę aminową
związki chemiczne pierwiastka węgla z wyłączeniem tlenków i siarczków węgla, kwasu węglowego i jego nieorganicznych pochodnych
organiczne związki acykliczne, związki łańcuchowe, węglowodory i ich pochodne o cząsteczkach, w których atomy węgla są połączone ze sobą w otwarte proste (liniowe) lub rozgałęzione łańcuchy
alkohol, gdzie grupa funkcyjna – grupa hydroksylowa – jest przyłączona do pierwszorzędowego atomu węgla (atom węgla, który jest połączony z jednym atomem węgla w cząsteczce). Przykładem alkoholu pierwszorzędowego jest propan‑1-ol
reakcja przyłączenia cząsteczki wodoru do danego związku chemicznego; jest to reakcja redukcji
substancja, która wprowadzona do mieszaniny reakcyjnej przyspiesza reakcję chemiczną, ale nie zużywa się w niej. Katalizator można odzyskać po zakończeniu reakcji chemicznej
reakcja polegająca na eliminacji grupy karboksylowej z cząsteczki kwasu karboksylowego, jego soli czy estru; w wyniku reakcji powstaje również tlenek węgla(IV)
sól, która zawiera w sieci krystalicznej swojej cząsteczki wodę, np.: (siarczan(VI) wapnia – woda (1/2))
związki organiczne, których cząsteczki zawierają grupę funkcyjną karboksylową () oraz długi łańcuch węglowodorowy; są naturalnymi składnikami tłuszczy
kwas, który w roztworze wodnym tylko częściowo dysocjuje na jony. Stopień dysocjacji elektrolitycznej słabych kwasów jest mniejszy od 1. Przykładem takiego kwasu może być kwas węglowy
kwas, który w roztworze wodnym całkowicie dysocjuje na jony. Stopień dysocjacji elektrolitycznej mocnych kwasów jest równy 1. Przykładem takiego kwasu może być kwas azotowy(V)
liczba wyrażona w procentach lub w ułamku, ukazująca stosunek cząsteczek, które rozpadły się na jony podczas dysocjacji elektrolitycznej, do liczby cząsteczek wprowadzonej do roztworu
kwasy karboksylowe, które posiadają długi łańcuch węglowy
kwasy karboksylowe nie zawierające podwójnych wiązań między atomami węgla w cząsteczce
kwasy karboksylowe zawierające przynajmniej jedno wiązanie podwójne między atomami węgla w cząsteczce
rodzaj izomerii geometrycznej, w której podstawniki znajdują się po tej samej stronie płaszczyzny wiązania podwójnego lub pierścienia
sole wyższych kwasów karboksylowych
przyłączenie do związku mniej nasyconego atomów wodoru w celu uzyskania związku bardziej nasyconego
reakcja chemiczna, w której brom przyłącza się do cząsteczki związku chemicznego
rozpad substancji na jony pod wpływem rozpuszczalnika (najczęściej wody)
dysocjacja zachodząca w więcej niż jednym etapie. Na każdym etapie wydajność dysocjacji jest inna, a wydajność kolejnych dysocjacji jest coraz mniejsza. Przykładem substancji dysocjującej stopniowo, jest kwas szczawiowy ()
kwas organiczny zawierający więcej niż jedną grupę karboksylową. elektrolit (gr. ḗlektron „bursztyn”, lytós „rozpuszczalny”) – substancja, która ulega dysocjacji elektrolitycznej oraz jest zdolna do przewodzenia prądu elektrycznego
substancja, która w małym stopniu dysocjuje, np. kwas octowy
stała równowagi chemicznej procesu dysocjacji. Jest charakterystyczna dla danego elektrolitu, a jej wartość jest bezwymiarowa
atom lub grupa atomów, które stanowią odgałęzienie od łańcucha głównego w związku organicznym
zdolność atomu danego pierwiastka do przyciągania elektronów. Elektroujemność może być wyrażona w postaci bezwymiarowych liczb w skali Paulinga
związek organiczny mający grupę funkcyjną: karboksylową. Atomy węgla połączone są w postaci otwartego i prostego lub rozgałęzionego łańcucha
(łac. resonare „odbijać się echem”, mezomeria – gr. mesos „pomiędzy”; meros „część”) zjawisko, które dotyczy delokalizacji wolnych par elektronów (p) niewiążących oraz elektronów pi wiążących. Wzory rezonansowe są równoważne i pokazują tzw. graniczne struktury związku chemicznego
atom lub grupa atomów w związkach organicznych, która decyduje o właściwościach danego związku oraz jego przynależności do danej klasy związków
efekt przesunięć elektronów walencyjnych (delokalizacji chmur elektronowych), spowodowany różnicą elektroujemności powiązanych ze sobą atomów różnych pierwiastków, czego konsekwencją jest polaryzacja wiązania, która skutkuje pojawieniem się cząstkowych ładunków delta+ i delta- na tych atomach. Efekt indukcyjny może być przenoszony na odległość dwóch – trzech wiązań
(niem. essigäther „octan etylu” essig „ocet” i Äther „eter”) związek organiczny, powstający w wyniku działania kwasów na alkohole lub fenole
atom lub grupa atomów, która powoduje pojawienie się charakterystycznych cech w danym związku chemicznym
grupa funkcyjna , która występuje w estrach pochodzących od kwasów organicznych
(arab. al‑kuhl „delikatny proszek”) związki organiczne, pochodne węglowodorów, których cząsteczki zawierają grupę hydroksylową , związaną bezpośrednio z atomem węgla o hybrydyzacji
związki organiczne, mono-, di- i polihydroksylowe pochodne benzenu oraz alkilobenzenów, których cząsteczki zawierają grupy hydroksylowe (), związane z atomami węgla pierścienia benzenowego
, związek organiczny, podstawowy węglowodór aromatyczny
związki organiczne, których cząsteczki zawierają grupę karboksylową ()
woski naturalne, mieszaniny gł. estrów monohydroksylowych alkoholi alifatycznych o długich łańcuchach z kwasami tłuszczowymi o długich łańcuchach węglowodorowych, a także alkoholi i kwasów tłuszczowych oraz węglowodorów
tłuszcze właściwe, lipidy proste, biochem. estry glicerolu z kwasami tłuszczowymi długołańcuchowymi o parzystej liczbie atomów węgla (acyloglicerole)
w ujęciu kinetycznym — stan, do którego dąży układ w miarę przebiegu reakcji odwracalnej
substancje zdolne do pochłaniania pary wodnej i wody
Le Chateliera i Brauna reguła, reguła przeciwdziałania: reguła głosząca, że układ będący w stanie równowagi chemicznej, poddany działaniu czynnika z zewnątrz, reaguje w taki sposób, żeby zmniejszyć wpływ tego czynnika i osiągnąć nowy stan równowagi możliwie niezbyt odległy od stanu równowagi wyjściowej
katalizator [gr.] substancja, która zwiększa szybkość reakcji chemicznej, nie naruszając stanu końcowej równowagi i właściwości termodynamicznych układu i pozostając w stanie niezmienionym po zakończeniu reakcji
organiczna grupa funkcyjna o wzorze sumarycznym ; wchodzi w skład wielu związków organicznych

reakcja zachodząca pomiędzy substancją rozpuszczoną a rozpuszczalnikiem (w tym przypadku wodą); ulegają jej związki organiczne i nieorganiczne
w chemii: rodzaj reakcji; dochodzi w niej do połączenia substratów w większą cząsteczkę; powstaje tzw. produkt główny; wynikiem reakcji mogą być również małe cząsteczki produktu/produktów o drugorzędnym znaczeniu
rodzaj sprzętu laboratoryjnego; jej zadaniem jest pośredniczenie w ogrzewaniu lub chłodzeniu zanurzonego naczynia laboratoryjnego i jego zawartości; na łaźni wodnej można ogrzewać różne naczynia; najczęściej stosuje się kolby okrągłodenne, mające długie i wąskie szyjki
sole zbudowane z metali i wyższych kwasów tłuszczowych; kwasy tłuszczowe mają od 12 do 20 atomów węgla; przykładami takich kwasów są: kwas palmitynowy, kwas stearynowy i kwas oleinowy; ich powszechnie wykorzystywaną właściwością jest zmniejszanie napięcia powierzchniowego, dzięki temu są używane jako środki myjące i piorące
związki chemiczne, które powstają podczas oddziaływania alkoholu na kwas w procesie reakcji zwanej estryfikacją
alkohole posiadające w swojej cząsteczce więcej niż jedną grupę hydroksylową
grupa funkcyjna, powstająca przez oderwanie się przynajmniej jednej grupy hydroksylowej, zazwyczaj od kwasu karboksylowego
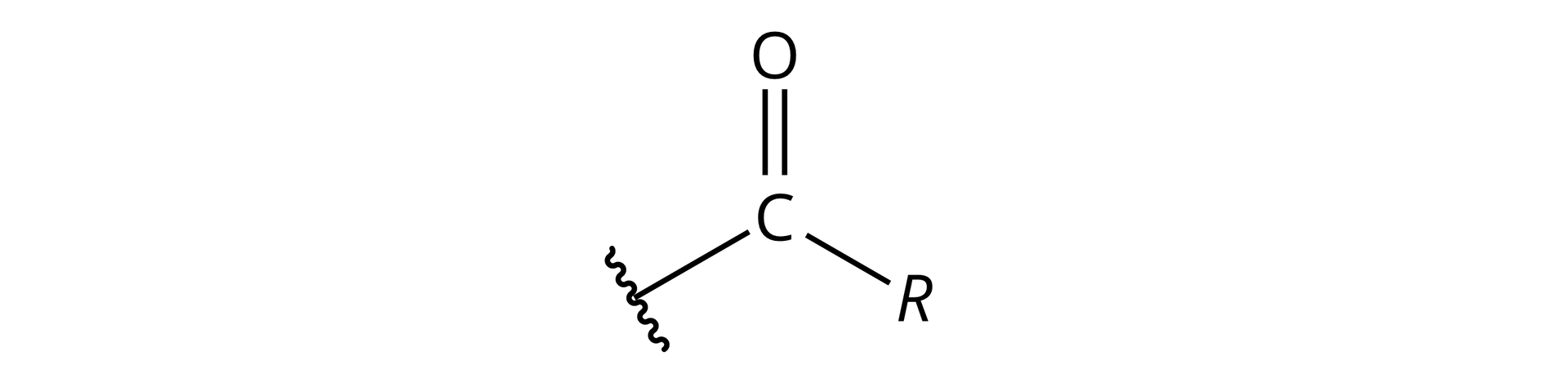
atom tlenu w grupie karbonylowej, czyli grupie funkcyjnej, składającej się z atomu węgla połączonego wiązaniem podwójnym z atomem tlenu
(gr. glykys „słodki”) alkohol polihydroksylowy, zawierający trzy grupy hydroksylowe; jego nazwa systematyczna to propano-,,-triol; powszechnie znany jest również pod nazwą gliceryna.
kwasy karboksylowe, które zawierają długie łańcuchy węglowe, zbudowane z ponad atomów węgla
woda bromowa, czyli wodny roztwór bromu
to reakcja addycji elektrofilowej wodoru do węglowodorów nienasyconych, posiadających wiązania wielokrotne pomiędzy atomami węgla, pod wpływem katalizatora, którym może być pallad, platyna lub nikiel
jedna z możliwości rozmieszczenia atomów lub grup atomów wokół wiązania podwójnego w izomerii geometrycznej; oznacza, że po dwóch stronach wiązania podwójnego te same atomy lub grupy atomów rozmieszczone są w tym samym kierunku; przeciwieństwem jest konfiguracja trans, oznaczająca rozmieszczenie po dwóch stronach wiązania podwójnego tych samym atomów lub grup atomów w różnych kierunkach

reakcja addycji, czyli łączenia, w której związek posiadający niedomiar elektronów (elektrofil) przyłącza się do związku chemicznego posiadającego nadmiar elektronów bez powstawania produktów ubocznych
estry glicerolu oraz wyższych nienasyconych kwasów tłuszczowych