Otrzymywanie amin alifatycznych i aromatycznych
Otrzymywanie amin
AminyAminy alifatyczne można otrzymać w szeregu różnych reakcji chemicznych. Poniżej opisano kilka z nich.
Aminy alifatyczne pierwszorzędowe to takie, w których grupa aminowa jest połączona z jednym atomem węgla. Powstają one w wyniku takich reakcji jak:
w reakcji halogenków alkilowychhalogenków alkilowych z nadmiarem amoniaku:
Przykład:
w reakcji nitryli z wodorem wobec katalizatora (np. , , ) lub z
Przykład:
w reakcji amidów z
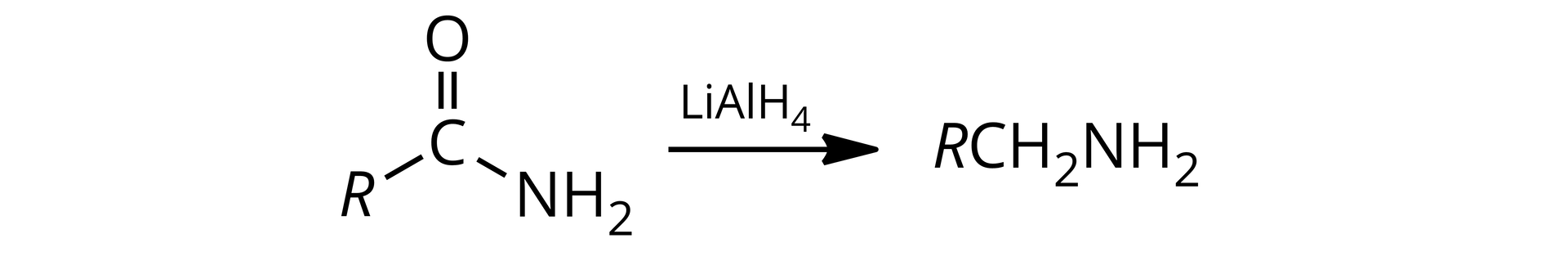
Przykład:
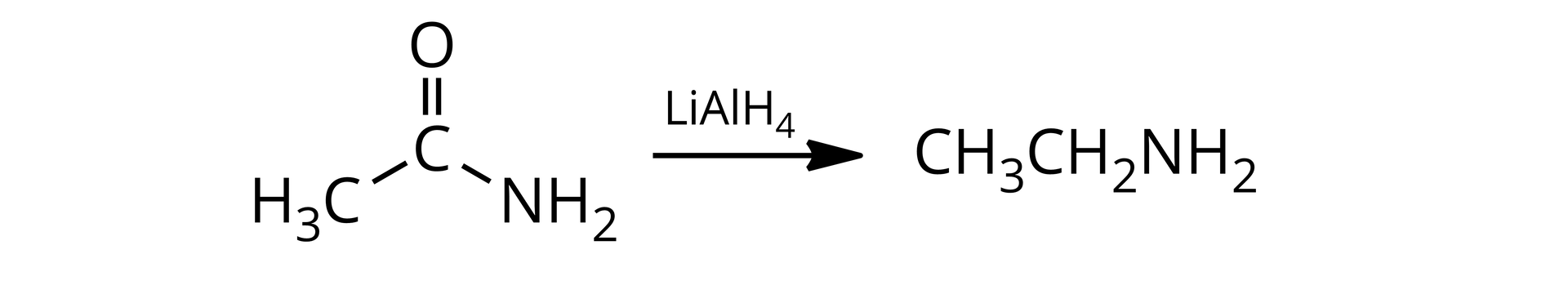
w reakcji nitrozwiązków z czynnikiem redukującym takim jak np.: wodór w obecności katalizatora (np. , , ), metali (np. , , ) w obecności kwasu chlorowodorowego lub
Przykład:
w reakcji azydków z wodorem wobec katalizatora (np. , , ) lub z
Przykład:
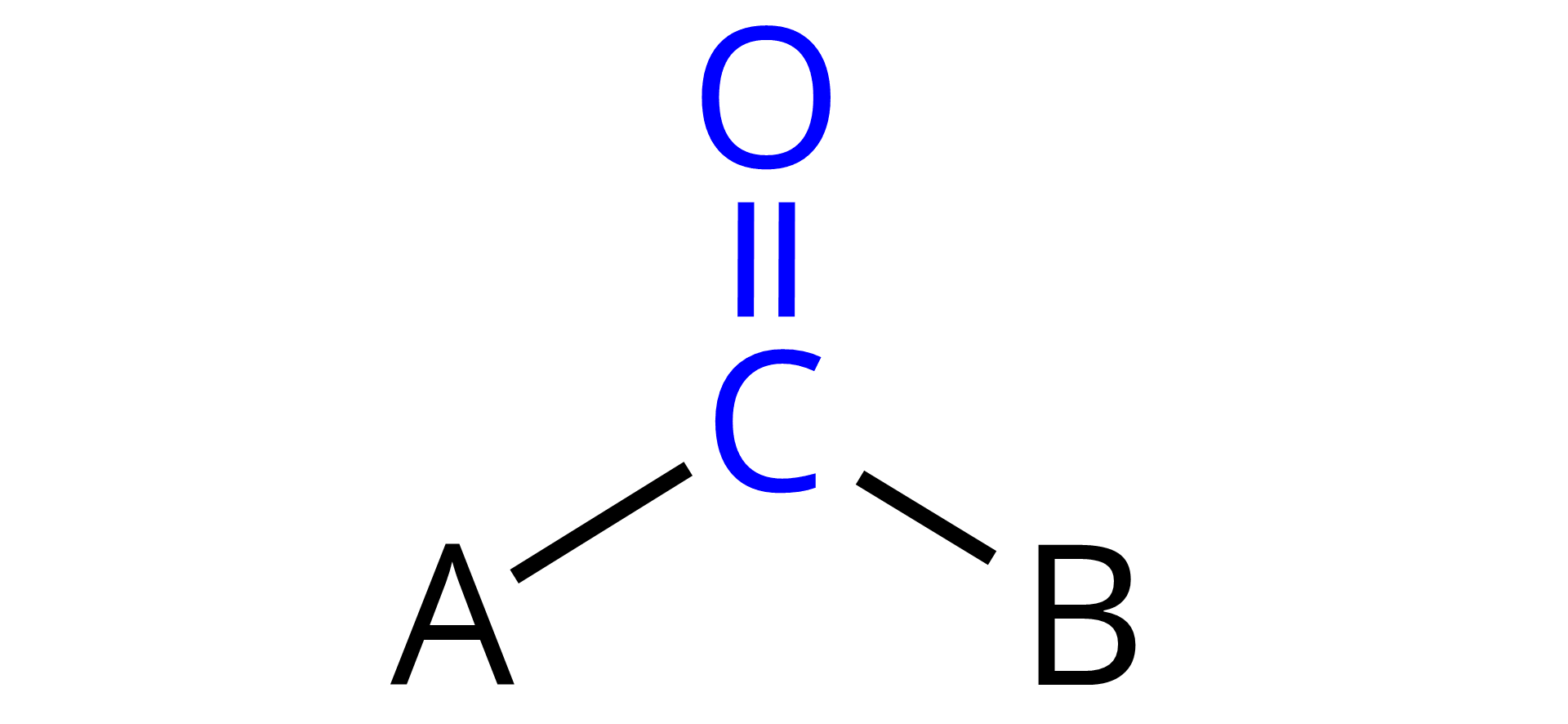
w reakcji związku karbonylowegokarbonylowego (zawierającego grupę karbonylową ) z wodorem w obecności katalizatora (np. , , ) i amoniaku
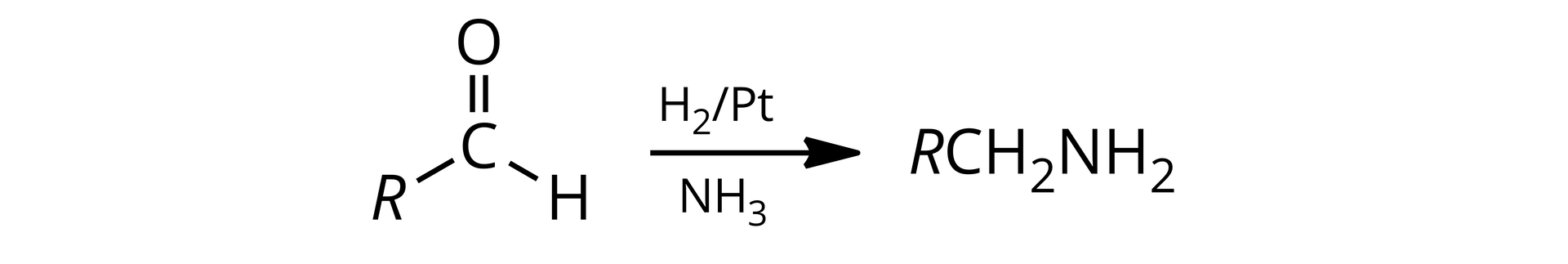
Przykład:
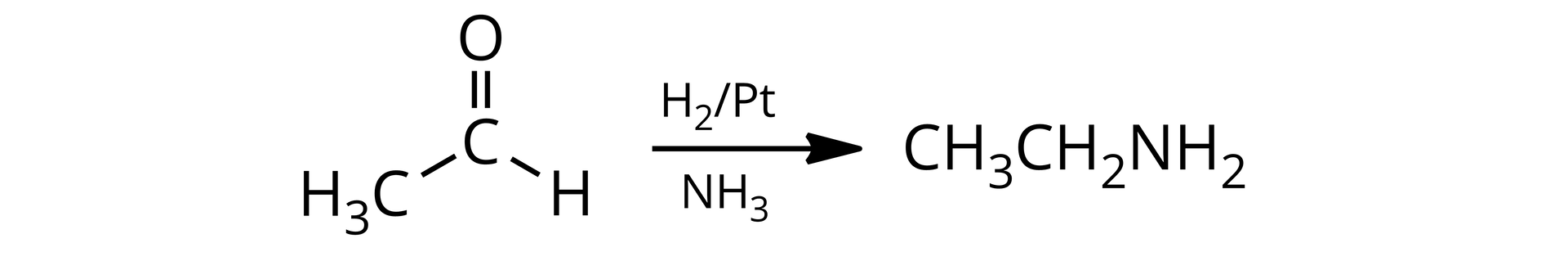
Aminy alifatyczne drugorzędowe powstają w:
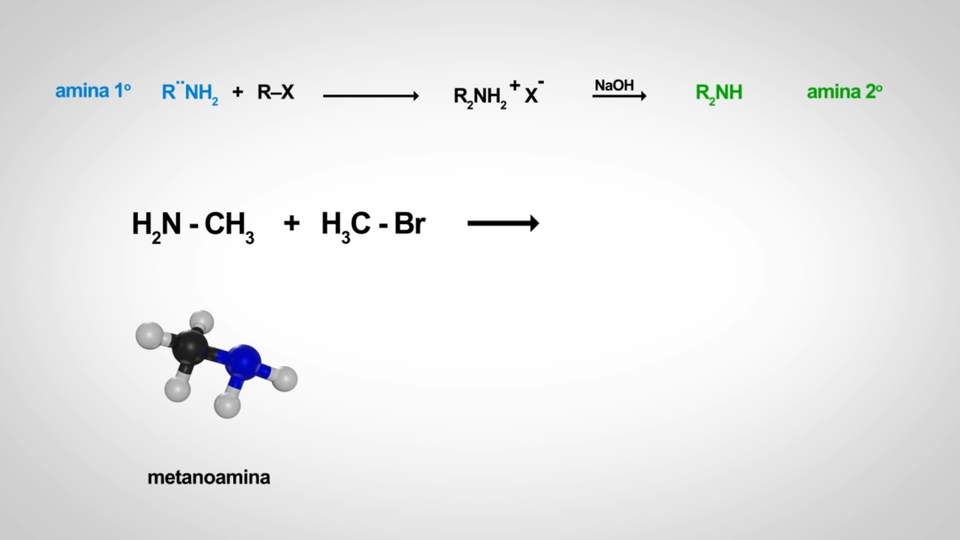
reakcji amin pierwszorzędowych z halogenkami alkilowymi:
Przykład:
w reakcji związku karbonylowegokarbonylowego (zawierającego grupę karbonylową ) z wodorem w obecności katalizatora (np. , , ) i aminy
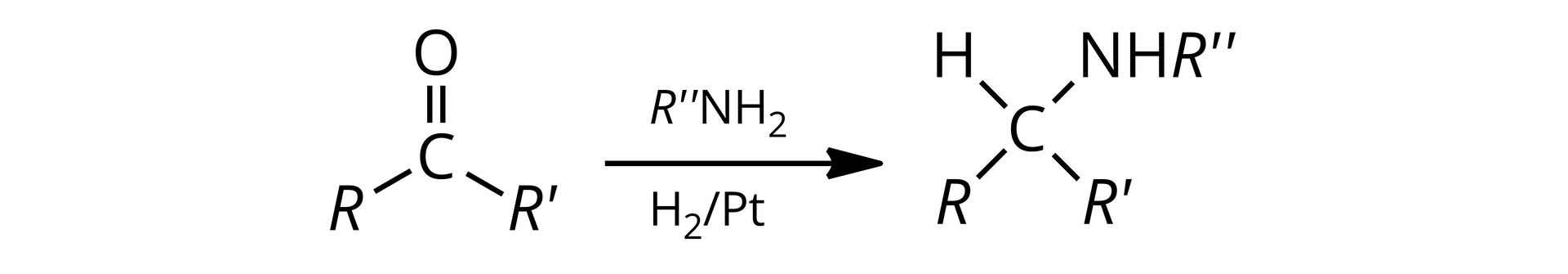
Przykład:
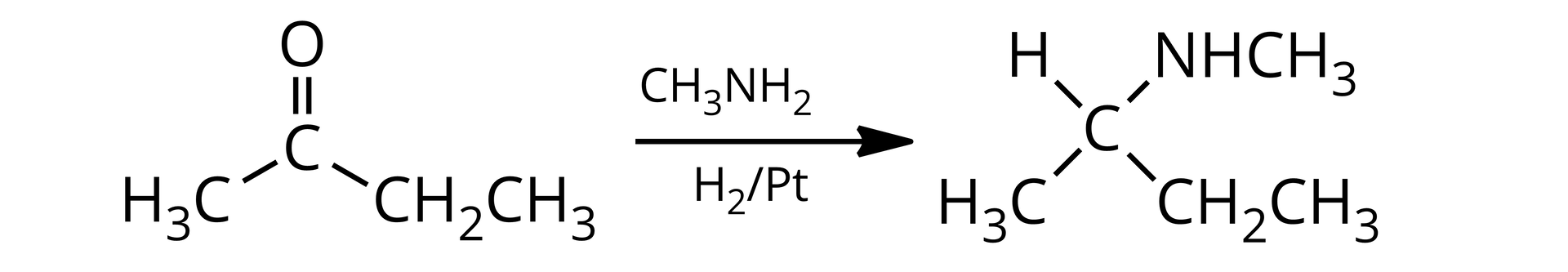
Aminy alifatyczne trzeciorzędowe powstają w:
reakcji amin drugorzędowych z halogenkami alkilowymi w obecności amoniaku:
Przykład:
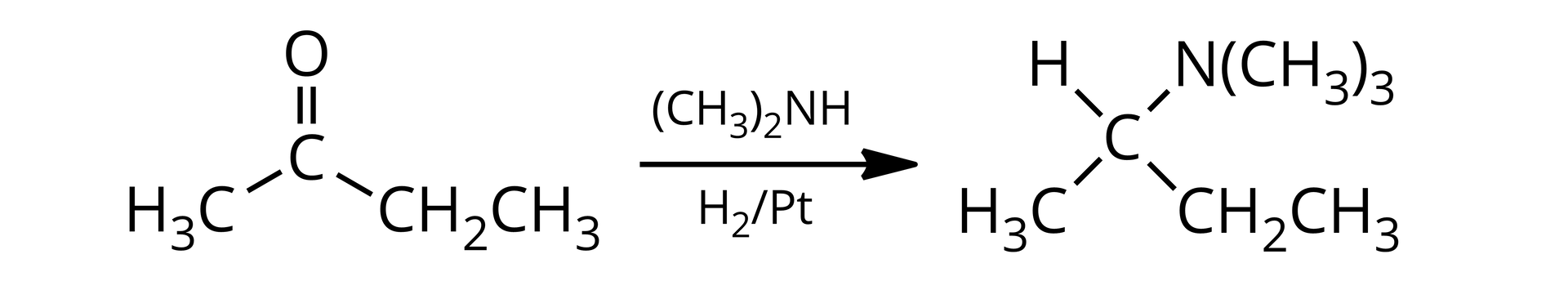
w reakcji związku karbonylowegokarbonylowego (zawierającego grupę karbonylową ) z wodorem w obecności katalizatora (np. , , ) i aminy
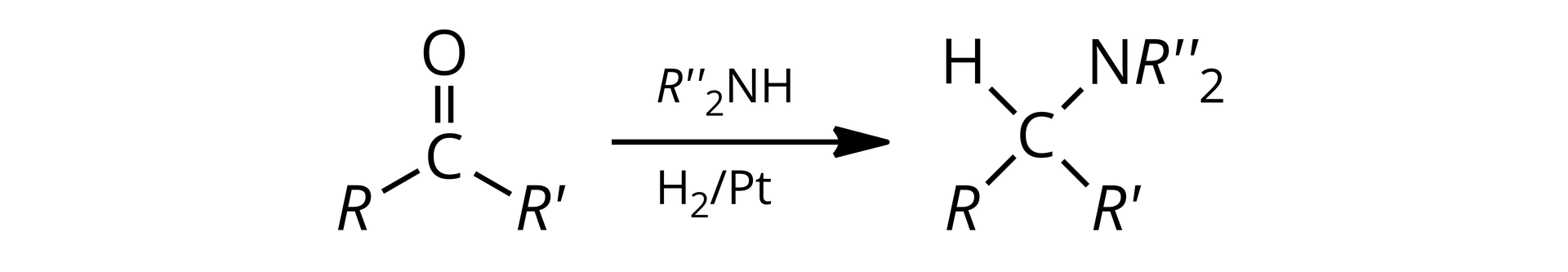
Przykład:
Poprzez reakcje odpowiedniego halogenku alkilowego z amoniakiem lub odpowiednią aminą, nie można otrzymać danej aminy bez domieszek amin o wyższej rzędowości. Jest to związane z mechanizmem reakcji. Aminy wykazują dobrą reaktywność, dlatego w mieszaninie poreakcyjnej otrzymujemy mieszaninę amin o różnych rzędowościach.
Zapoznaj się z animacją dotyczącą amin alifatycznych, z zawartymi informacjami, a następnie rozwiąż ćwiczenia.
Film dostępny pod adresem /preview/resource/R6lhPfvNnD6eW
Animacja stanowi przegląd metod otrzymywania amin alifatycznych.
Wyjaśnij, dlaczego stosowany jest nadmiar amoniaku w reakcji z halogenkiem alkilu?
Czym są aminy aromatyczne?

Najprostszą aminą aromatyczną jest fenyloamina, powszechnie zwana aniliną. Związek ten jest oleistą, bezbarwną cieczą o charakterystycznym zapachu zepsutych ryb, która na powietrzu brunatnieje. Zmiana barwy aniliny związana jest z jej utlenieniem utlenieniem przez tlen atmosferyczny, czego wynikiem są barwne zanieczyszczenia. Anilina słabo rozpuszcza się w wodzie, ale dobrze w alkoholu, eterze i benzenie. Jest substancją toksycznąsubstancją toksyczną.
Właściwości chemiczne aniliny
Anilina i inne aminy aromatyczne wykazują słabszy charakter zasadowy niż aminy alifatyczne. Ich odczynodczyn jest prawie obojętny, a zasadowość maleje wraz ze wzrostem rzędowościrzędowości amin.
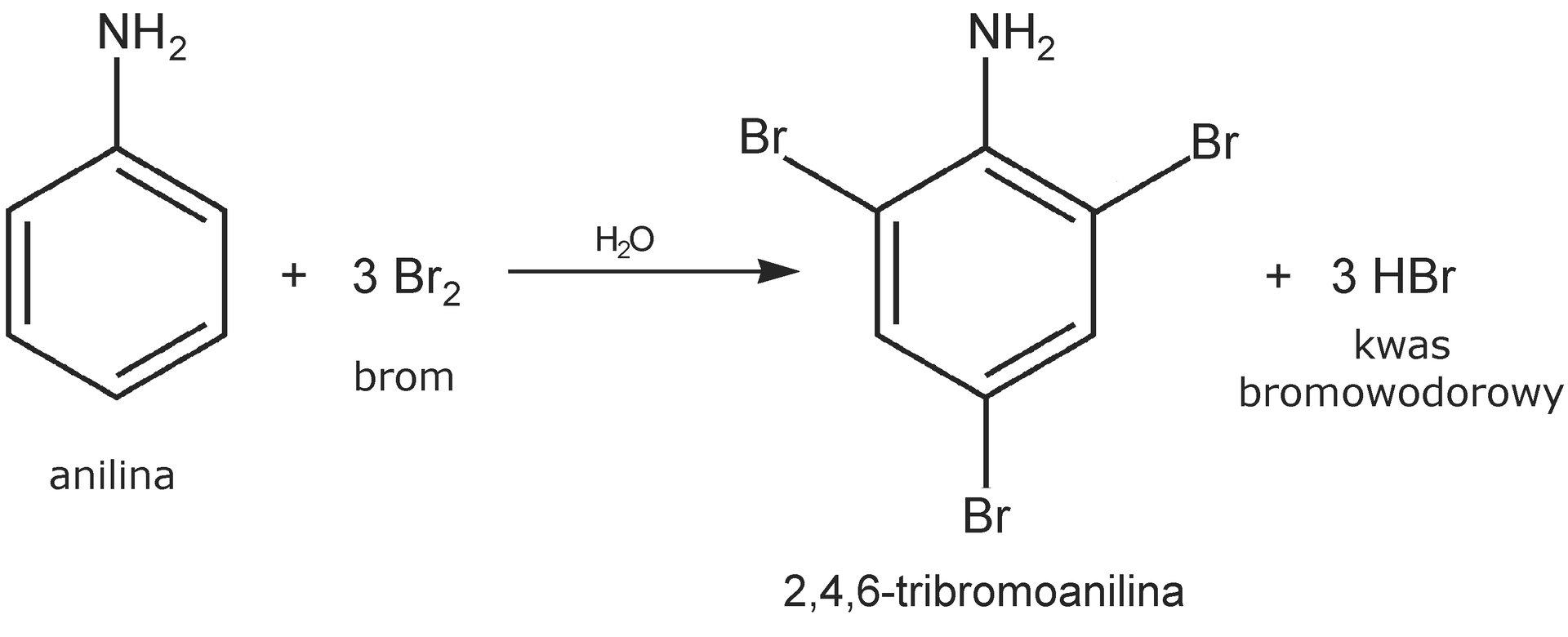
Anilina jako słaba zasada może reagować z kwasami w wyniku czego powstają sole. Obecność grupy aminowej powoduje zwiększenie reaktywności pierścienia aromatycznego podczas substytucji elektrofilowej. Anilina ulega reakcji polisubstytucji elekrofilowej.
Należy pamiętać, że grupa obecna w cząsteczce aniliny jako silnie aktywujący podstawnik pierwszego rodzaju, kieruje w reakcjach substytucji elektrofilowej następny podstawnik na pozycję orto i para, ale np. podczas nitrowania powstaje również –nitroanilina. W silnie kwaśnym środowisku reakcji następuje protonowanie grupy aminowej, która w tej formie () jest podstawnikiem drugiego rodzaju.
Nitrowanie aniliny nie jest praktyczną reakcją do otrzymania jej nitropochodnych. W silnie kwasowym środowisku, grupa aminowa przyjmuje proton, skutkuje to powstaniem jonów anilinowych . Wynikiem przeprowadzenia reakcji nitrowania aniliny są trzy izomery meta, orto oraz para, oraz wydzielenie smoły.
Otrzymywanie aniliny
Anilina powstaje w wyniku redukcjiredukcji nitrobenzenu, którą prowadzi się wodorem atomowym in statu nascendi (w chwili tworzenia, powstawania). Ogólny zapis tego procesu przedstawia równanie:

Atomowy wodór otrzymuje się w reakcji cynku lub żelaza z kwasem solnym. Dlatego pełny zapis redukcji nitrobenzenu przeprowadzanej za pomocą np. cynku i kwasu solnego, wygląda następująco:
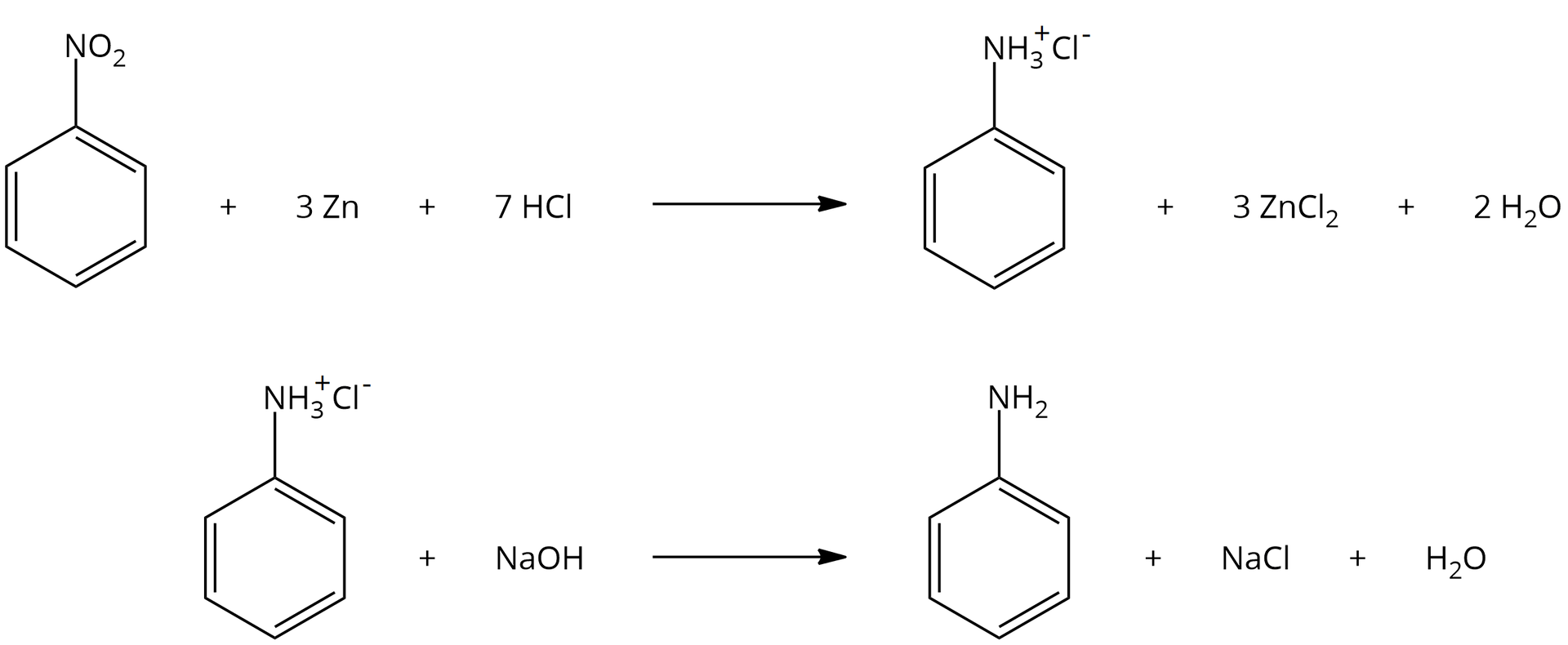
Inne aromatyczne aminy również otrzymuje się przez redukcję odpowiedniego nitrozwiązku. Dzieje się tak chociażby w przypadku otrzymywania –toluidyny.
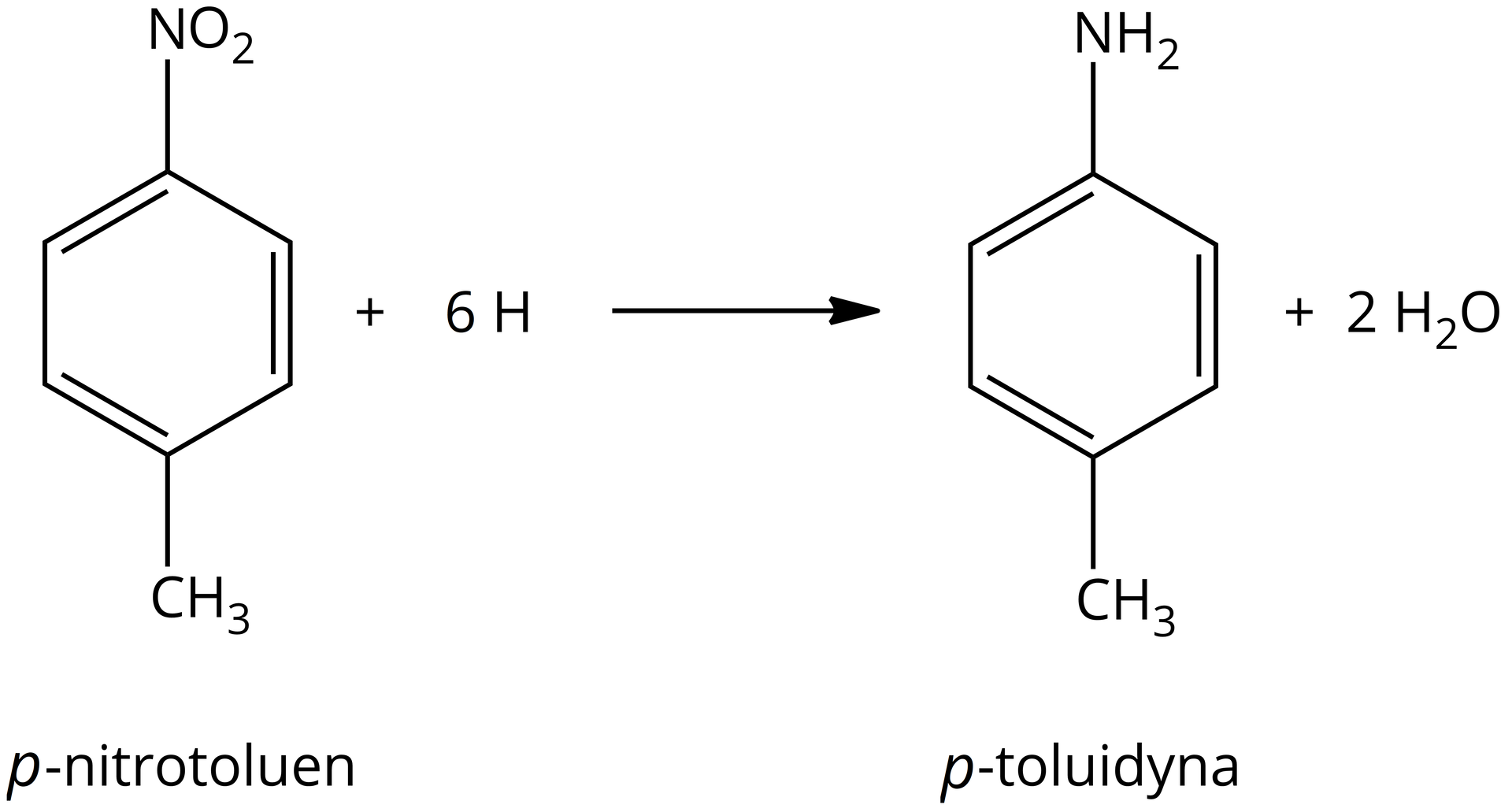
Zastanawiałeś się kiedyś, w jaki sposób otrzymuje się aminy aromatyczne i dlaczego stosuje się inne metody niż w przypadku amin alifatycznych?

Film dostępny pod adresem /preview/resource/Rq9uQoQmJabZp
Animacja dotyczy metod otrzymywania amin alifatycznych.