Właściwości amin
Z czego wynika reaktywność amin?
Spójrz na poniższe wzory kilku wybranych amin:
Jak myślisz, co je łączy?
Wszystkie aminy posiadają w swojej budowie atom azotu z wolną parą elektronową. Reaktywność amin wynika z możliwości jej wykorzystania i utworzenia wiązań z innymi pierwiastkami przez atom azotu.
Aminy są reaktywne dzięki wolnej parze elektronowej atomu azotu, która jest zdolna do tworzenia wiązań koordynacyjnych (donorowo‑akceptorowych).
Reakcje amin z wodą
Reakcja aminamin z wodą pozwala wykazać ich zasadowy odczyn. Powstają wówczas sole amoniowe oraz aniony wodorotlenkowe. Zauważ, że zgodnie z teorią kwasów i zasad Brönsteda i Lowry’ego amina pełni funkcję zasady, ponieważ przyjmuje atom wodoru od cząsteczki wody, która wg tej teorii jest kwasem, czyli dawcą protonu.
amina pierwszorzędowa

amina drugorzędowa

amina trzeciorzędowa

amina aromatyczna

W powstających kationach wiązanie koordynacyjne powstaje pomiędzy atomem azotu (donorem pary elektronowej) a atomem wodoru (akceptorem pary elektronowej), pochodzącym od wody.
Reakcje amin z kwasami
Powyższe równania – zapisane zgodnie z teorią Brönsteda i Lowry’ego – potwierdziły, że aminy są zasadami. Reagują więc z kwasami tworząc sole. Tworzenie soli z kwasami nieorganicznymi i organicznymi polega na odwracalnym przyłączaniu protonu do wolnej pary elektronów atomu azotu, jak pokazano na wzorach ogólnych amin o różnej rzędowości, gdzie R oznacza grupę węglowodorową:

Wzory chemiczne, powstających w reakcjach z kwasami produktów, można zapisać na trzy sposoby, jak pokazano w poniższych równaniach reakcji etyloaminy oraz aniliny z kwasem solnym.
Powstałe w tych reakcjach sole poddaje się działaniu mocnych zasad (np. lub ), uzyskując wówczas aminy, które jako słabsze zasady są wypierane z soli przez mocniejszą zasadę.
Reakcja etyloaminy z kwasem solnym:

Reakcja chlorowodorku etyloaminy z wodorotlenkiem sodu

Reakcja aniliny z kwasem solnym

Reakcja chlorowodorku aniliny z wodorotlenkiem sodu

Warto również wspomnieć o reakcjach amin z kwasem azotowym(III) (), którego roztwór przygotowuje się „na świeżo” (np. poprzez reakcję z ) ze względu na jego nietrwałość. Z tego samego powodu reakcje prowadzi się oziębiając układ. Służą one do wykrywania amin o różnej rzędowości.
W zależności od rodzaju użytej aminy, powstają różne produkty:
Aminy I‑rzędowe
alifatyczne
RMVPezcebiLDJ  Równanie reakcji aminy alifatycznej I‑rzędowej z kwasem azotowym(III)Źródło: GroMar Sp. z o.o, licencja: CC BY-SA 3.0.
Równanie reakcji aminy alifatycznej I‑rzędowej z kwasem azotowym(III)Źródło: GroMar Sp. z o.o, licencja: CC BY-SA 3.0.aromatyczne

Aminy II‑rzędowe

aromatyczne

Aminy III‑rzędowe
alifatyczne - reakcja nie zachodzi
aromatyczne

Otrzymywanie amin II‑rzędowych oraz III‑rzędowych
Aminy I‑rzędowe wykorzystuje się do otrzymania amin II‑rzędowych w reakcji z odpowiednim halogenkiem alkilowymhalogenkiem alkilowym oraz amoniakiemamoniakiem. W analogiczny sposób otrzymywane są aminy III‑rzędowe, z tą różnicą, że substratem jest odpowiednia amina II‑rzędowa, tak jak na poniższych przykładach otrzymywania dimetyloaminy oraz trimetyloaminy.

Zróżnicowanie reaktywności amin alifatycznych
Reaktywność amin I- oraz II- rzędowych o zbliżonych masach cząsteczkowych jest porównywalna. Natomiast aminy III‑rzędowe są mniej reaktywne od amin I- i II- rzędowych. Jest to spowodowane występowaniem trzech podstawników przy atomie azotu. Takie rozmieszczenie podstawników utrudnia dostęp protonu do wolnej pary elektronowej atomu azotu. Jest to tzw. zawada steryczna.
Reakcje substytucji elektrofilowej amin aromatycznych
Aminy aromatyczne są mniej reaktywnymi zasadami niż aminy alifatyczne. Wynika to z oddziaływania wolnej pary elektronowej atomu azotu z chmurą elektronów pierścienia aromatycznego. Powoduje to obniżenie zdolności atomu azotu do przyłączenia protonu.
Grupa aminowa () to grupa elektronodonorowagrupa elektronodonorowa, wzbogacająca pozycje orto i para w elektrony, jest więc podstawnikiem I rodzaju. Grupa aminowa tak silnie aktywuje pierścień, że w reakcjach substytucji (podstawienia) nie jest potrzebny katalizator.
Do typowych reakcji podstawienia (substytucji elektrofilowej) amin aromatycznych należy bromowanie aniliny (fenyloaminy):
rozcieńczonym roztworem bromu

W wyniku reakcji powstają monobromopochodne orto i para.
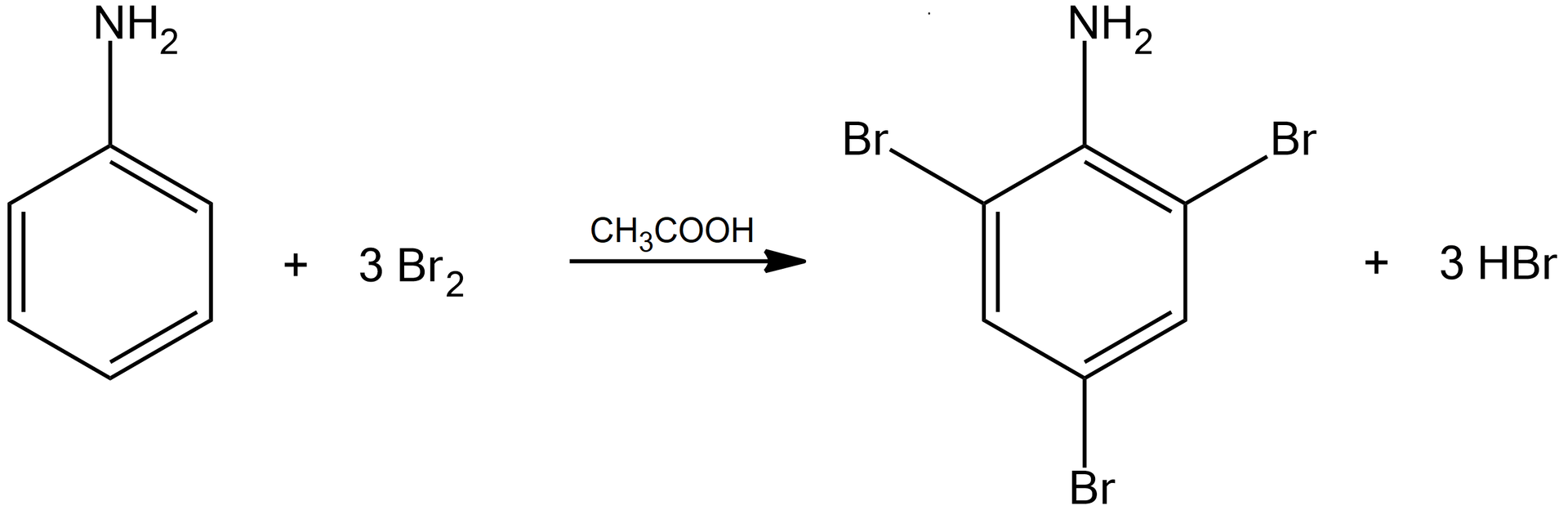
stężonym roztworem bromu

W wyniku reakcji powstaje tribromopochodna. Wszystkie pozycje orto i para są podstawione atomami bromu. Obie reakcje zachodzą bez udziału katalizatora.
Jak wykazać, że anilina jest słabą zasadą? Wśród sprzętu laboratoryjnego oraz odczynników chemicznych znajdują się te niezbędne do przeprowadzenia eksperymentu. Następnie zaplanuj doświadczenie chemiczne, przeprowadź je, zapisz obserwacje, wnioski oraz odpowiednie równania reakcji chemicznych.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D4S2UOVXR
Zadanie: Wykaż doświadczalnie, że anilina jest słabą zasadą.
Sprzęt laboratoryjny:
probówki, podłużne naczynie szklane do przeprowadzania prostych reakcji chemicznych;
pipety Pasteura, wąska rurka pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
pręcik szklany, służący do mieszania substancji chemicznych;
drewniana łapa, rodzaj trzymaka służący do uchwycenia probówki lub małej kolby stożkowej.
Odczynniki chemiczne:
anilina;
stężony kwas solny;
20% roztwór zasady sodowej (NaOH).
Wykonanie:
Za pomocą pipety wlano do probówki 1 cmIndeks górny 33 aniliny a następnie dodano 1 cmIndeks górny 33 HCl (również odmierzonego pipetą).
Zamieszano roztwór pręcikiem szklanym. Probówkę ochłodzono zimną wodą (wprowadzono probówkę trzymaną w łapie drewnianej).
Następnie do tej samej probówki wlano 3 cmIndeks górny 33 NaOH (odmierzonego za pomocą pipety).
Obserwacje:
Po zadaniu aniliny kwasem solnym wytrąca się kremowy osad, który roztwarza się po dodaniu NaOH w probówce znika kremowy osad i pojawiają się dwie warstwy - warstwa oleistej cieczy na górze oraz bezbarwna warstwa na dole.
W poniższym arkuszu wymień zestaw niezbędnych odczynników chemicznych oraz szkła laboratoryjnego, zapisz wnioski, obserwacje oraz instrukcje poprawnego przeprowadzenia doświadczenia pt. „Badanie reaktywności aniliny.”
Zadanie: Wykaż doświadczalnie, że anilina jest słabą zasadą.
Sprzęt laboratoryjny:
probówki, pipety Pasteura, pręcik szklany, drewniana łapa.
Odczynniki chemiczne:
anilina, HCl, NaOH.
Wykonanie:
1. Za pomocą pipety wlej do probówki 1 centymetr sześcienny aniliny, a następnie dodaj 1 centymetr sześcienny stężonego kwasu chlorowodorowego (również odmierzonego pipetą). 2. Zamieszaj roztwór pręcikiem szklanym. Probówkę możesz ochłodzić zimną wodą (wprowadź probówkę trzymaną w łapie drewnianej). 3. Następnie do tej samej probówki wlej 3 centymetry sześcienne 20% roztworu zasady sodowej (odmierzonego za pomocą pipety).
Obserwacje:
Po zmieszaniu aniliny z kwasem solnym wytrąca się kremowy osad, który roztwarza się po dodaniu zasady sodowej. Pojawia się warstwa oleistej cieczy.
Wnioski:
Anilina jest zasadą, ponieważ reaguje z kwasem solnym dając sól. Jest natomiast słabą zasadą, ponieważ zostaje wyparta z soli przez mocną zasadę.
Zapisz równanie reakcji aniliny z kwasem solnym.
Dopasuj nazwy wszystkich reagentów w zapisanych równaniach reakcji chemicznych spośród niżej wymienionych do odpowiednich reagentów.
A. chlorowodorek aniliny;
B. kwas chlorowodorowy;
C. anion chlorkowy;
D. anilina (fenyloamina);
E. kation aniliniowy;
F. chlorek aniliniowy.
Zapisz równanie reakcji chlorowodorku aniliny z zasadą sodową w formie jonowej skróconej.
Fenyloamina, zwana inaczej aniliną, łatwo ulega reakcji bromowania. Czy wiesz, jak przeprowadzić taką reakcję? Czy umiesz zapisać równanie tej reakcji chemicznej? Czy potrafisz nazwać powstający produkt? Zapoznaj się z animacją, a następnie sprawdź swoją wiedzę i rozwiąż poniższe zadania.

Film dostępny pod adresem /preview/resource/Rm8MH3OQPq9HG
Animacja dotyczy przebiegu bromowania aniliny.
Zapisz równanie reakcji chemicznej (w formie cząsteczkowej) aniliny z stężonym wodnym roztworem bromu.