Właściwości redukujące cukrów złożonych
Właściwości cukrów złożonych
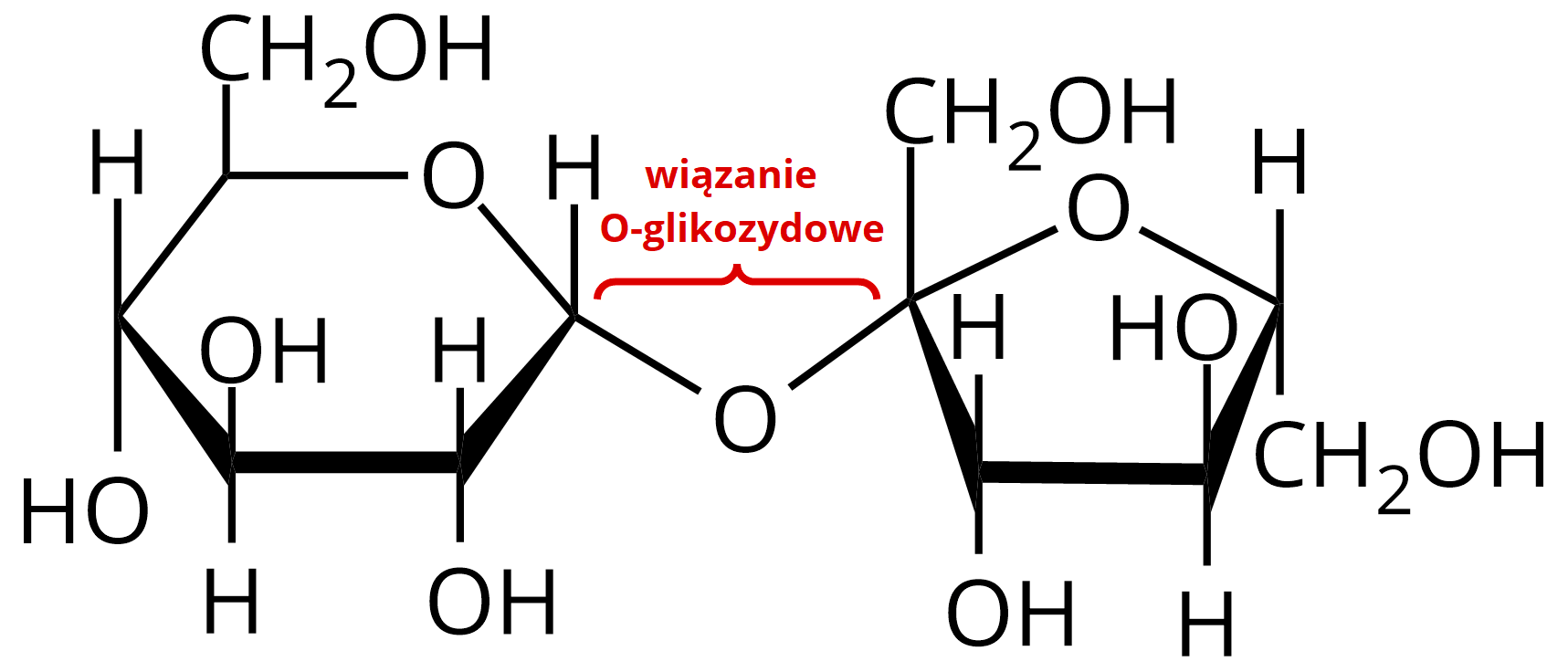
-glikozydowym.
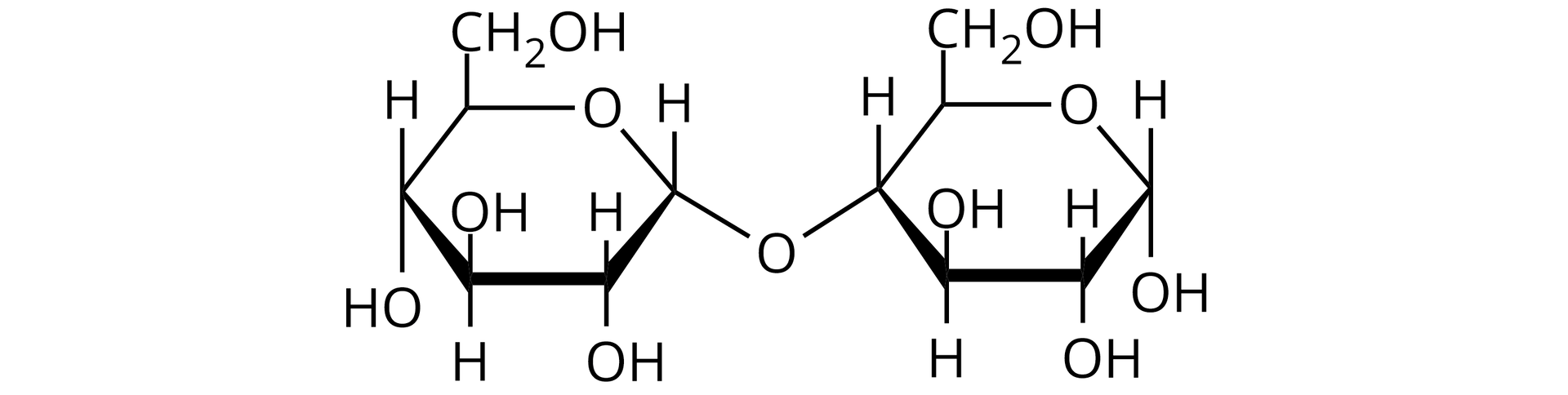
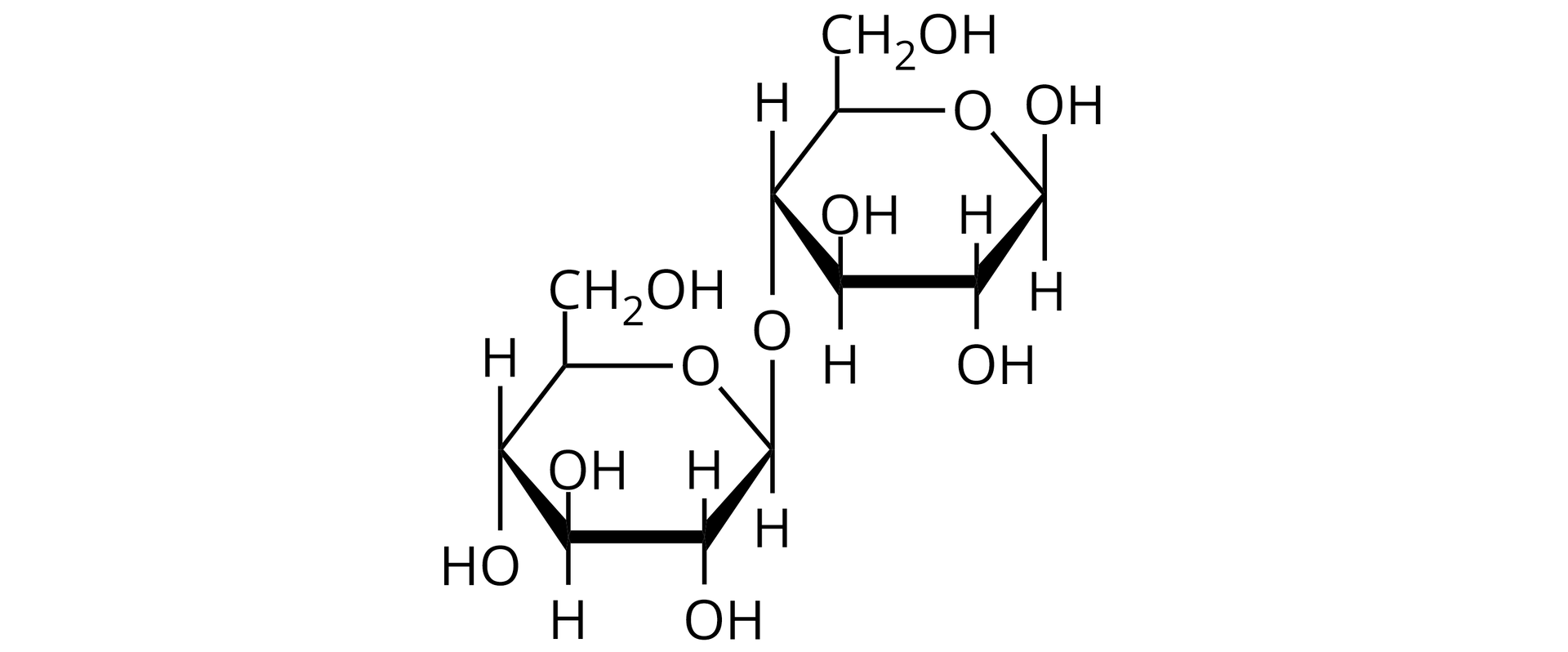
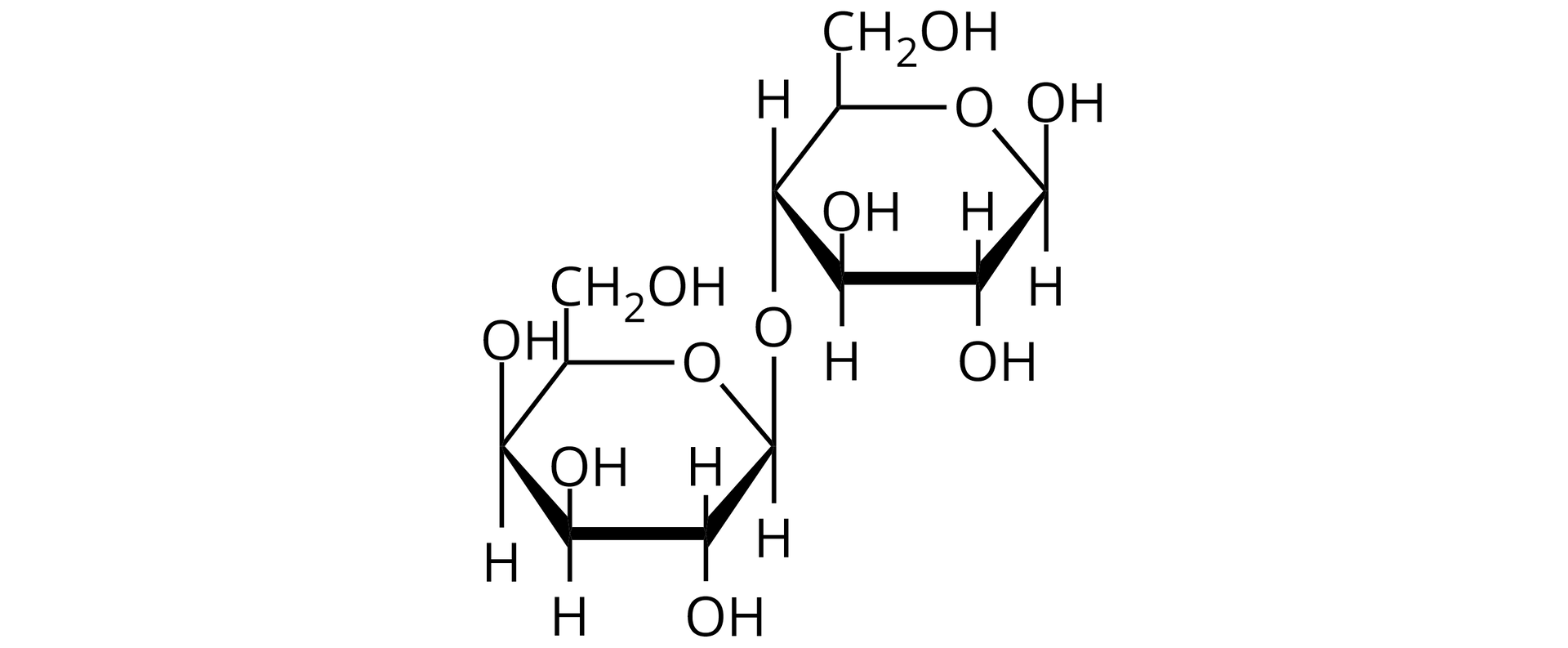
Disacharydy powstają z dwóch reszt monosacharydowych (identycznych lub różnych), połączonych wiązaniem
–glikozydowym.
W zależności od tego, które grupy monosacharydów zostały zaangażowane w tworzenie wiązania glikozydowego, disacharyd wykazuje lub nie wykazuje właściwości redukujących.
Disacharydy należą do cukrów hydrolizujących i są glikozydami.
Ze względu na obecność grup – disacharydy mogą tworzyć estry.
Zapoznaj się z informacjami podanymi w animacji dotyczącej cukrów. Zwróć uwagę, które z nich należą do cukrów redukujących, a które nie. Następnie wykonaj poniższe zadania.

Film dostępny pod adresem /preview/resource/RTAok4lT0EQwf
Film nawiązujący do treści materiału dotyczącej wykazywania właściwości redukujących przez niektóre cukry złożone.
Wypisz nazwy reakcji charakterystycznych, które można wykonać, aby odróżnić cukry redukujące od nieredukujących.
Disacharydy redukujące
W grupie tej znajdują się: maltoza, celobioza, laktoza.
Cukry te:
dają pozytywny wynik w próbie Tollensa i Trommera;
tworzą glikozydy z alkoholami lub fenolami.
Disacharydy nieredukujące
Do disacharydów nieredukujących zalicza się sacharozę, co oznacza, że daje negatywne wyniki w próbach Tollensa, Trommera i Fehlinga. Sacharoza, podobnie jak większość disacharydów, jest ciałem stałym o barwie białej, bez zapachu i o słodkim smaku. Bardzo dobrze rozpuszcza się w wodzie.
Przeprowadź eksperyment w laboratorium chemicznym. Rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz swoje obserwacje i wyniki, a następnie sformułuj wnioski.XD
Szafa laboratoryjna
Zapoznaj się z doświadczeniem w laboratorium chemicznym. Rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu sformułuj wnioski oraz wykonaj ćwiczenia.
Sprzęt laboratoryjny:
probówki – podłużne naczynie szklane do przeprowadzania prostych reakcji chemicznych;
łyżka do spaleń – długi trzonek wykonany z ogniotrwałego materiału zakończony z jednej strony łyżeczką; służy do spalania substancji;
zlewka () – naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych;
cylinder miarowy – podłużne szklane naczynie laboratoryjne w kształcie walca z umieszczoną na ściance podziałką objętości służące do odmierzania cieczy;
trójnóg – metalowy pierścień wsparty na trzech metalowych nogach (prętach), umożliwiający postawienie naczyń laboratoryjnych nad palnikiem;
zapałki – służący do rozpalania ognia, specjalnie w tym celu przygotowany patyczek z drewna;
palnik – rodzaj sprzętu z regulacją płomienia, umożliwiający podgrzewanie substancji chemicznych.
Odczynniki:
glukoza;
fruktoza;
celuloza;
skrobia;
sacharoza;
woda destylowana;
etanol.
Problem badawczy:
Czy dwucukry i polisacharydy mają podobne właściwości do cukrów prostych?
Hipoteza:
Cukry złożone mają odmienne właściwości w porównaniu z cukrami prostymi.
Przebieg doświadczenia:
Dla każdego z cukrów przygotowano zestaw: sucha probówka, probówka z wodą, probówka z alkoholem.
Dodano cukru do czystej probówki, określono jego stan skupienia, barwę, zapach, smak. Następnie wlano wody i oceniono rozpuszczalność.
Następnie przy pomocy łyżki do spalań przeprowadzono próbę palności każdej z substancji.
Stworzono łaźnię wodną i umieszczono probówki z wodą w ogrzanej wodzie. Oceniono rozpuszczalność każdej substancji w tym przypadku.
Dodano cukier do probówki z alkoholem i zapisano obserwacje.
Obserwacje i wyniki:
Właściwość | glukoza | fruktoza | sacharoza | skrobia | celuloza |
|---|---|---|---|---|---|
stan skupienia | stały | stały | stały | stały | stały |
barwa | biała | biała | biała | biała | biała |
zapach | bezwonny | bezwonny | bezwonny | bezwonny | bezwonny |
smak | słodki | słodki | słodki | bez smaku | bez smaku |
rozpuszczalność | dobrze | dobrze | dobrze | słabo | nie rozpuszcza się |
rozpuszczalność | bardzo dobrze | bardzo dobrze | bardzo dobrze | pęcznieje | nie rozpuszcza się |
rozpuszczalność w alkoholu | brak | brak | brak | brak | brak |
palność | topi się, | topi się, | topi się, | palna | palny |
Wspólną cechą monocukrów i dwucukrów jest słodki smak, dobra rozpuszczalność w wodzie oraz topienie się pod wpływem wysokiej temperatury w odróżnieniu od cukrów złożonych, które nie posiadają smaku, nie rozpuszczają się w wodzie i są palne. Różnice te wynikają z większej złożoności budowy chemicznej skrobi i celulozy. Wspólną cechą wszystkich cukrów jest znikoma rozpuszczalność w etanolu oraz podobny kolor i brak zapachu. W związku z tym można stwierdzić, że cukry proste wykazują pewne właściwości odmienne od właściwości cukrów złożonych, co potwierdza postawioną hipotezę.
Zapoznaj się z poniższym audiobookiem, w którym przedstawiono podobieństwa oraz różnice w budowie i właściwościach cukrów prostych i złożonych. Następnie wykonaj zamieszczone pod nim ćwiczenia utrwalające.
Badanie obecności grup funkcyjnych w cząsteczkach cukrów
Stefan Sękowski (żyjący w latach 1925–2014) był legendarnym popularyzatorem chemii i autorem kultowej serii książek dla młodzieży, na której wychowało się już kilka pokoleń polskich chemików. Niewielkiego formatu książeczki zawierały opisy doświadczeń, które można samodzielnie przeprowadzić w domu. Wysłuchaj fragmentu jednej nich, zatytułowanej „Na przełaj przez chemię” a następnie wykonaj poniższe zadania.
Czy każdy cukier jest słodki?
Jeśli poliżesz odrobinę miodu lub kostkę cukru, to poczujesz wyraźny, miły, słodki smak. Odpowiadają za niego liczne grupy hydroksylowe, obecne w cząsteczkach cukrów: glukozy i sacharozy. Natomiast papier czy mąka ziemniaczana, zawierające wielocukry – celulozę i skrobię, tego smaku nie wykazują. Wydaje się to dziwne, bo przecież celuloza i skrobia, jako cukry, także zawierają w swojej strukturze grupy hydroksylowe. Nie mogą one jednak oddziaływać z receptorami smaku na powierzchni języka, ponieważ wspomniane cukry nie rozpuszczają się w wodzie. Co prawda, skrobia rozpuszcza się w gorącej wodzie, jednak nie tworzy z nią roztworu rzeczywistego, a jedynie układ koloidalny.
Jak można wykrywać glukozę?
Otóż jedną z charakterystycznych reakcji glukozy jest redukowanie przez nią pewnych związków miedzi(II) i srebra. Jest to związane z obecnością grupy aldehydowej (–CHO) w cząsteczce tego cukru. Ale pamiętaj, że w podobnej reakcji uczestniczą również i inne związki, jak na przykład metanal.
Aby się o tym przekonać, postaraj się o jedną ampułkę glukozy do zastrzyków. Jeżeli jej nie masz, weź łyżeczkę stołową miodu i rozpuść go w 50 cm3 ciepłej, destylowanej wody.
Teraz przygotuj odczynniki używane do wykrywania glukozy. Będzie to odczynnik Trommera i odczynnik Tollensa. Nazwy tych odczynników pochodzą od nazwisk odkrywców owych metod wykrywania cukrów.
Odczynnik Trommera to świeżo strącony wodorotlenek miedzi(II) z dodatkiem nadmiaru roztworu wodorotlenku sodu. Otrzymasz go mieszając 5 cm3 rozcieńczonego wodnego roztworu siarczanu(VI) miedzi(II) z 5 cm3 10% wodnego roztworu wodorotlenku sodu. W wyniku reakcji w probówce powstaje bezpostaciowy, jasnoniebieski osad. Widzisz? Nie zapomnij, jak ważne jest użycie nadmiaru zasady – inaczej dalsze reakcje mogą się nie udać.
Aby otrzymać odczynnik Tollensa, musisz przede wszystkim zaopatrzyć się w odrobinę azotanu(V) srebra(I) AgNO3. Związek ten możesz przygotować ze starych zużytych materiałów fotograficznych lub kupić w aptece jako tak zwany lapis.
Ze stałego azotanu(V) srebra(I) i wody destylowanej wykonaj 10% roztwór tej soli. Bezpośrednio przed doświadczeniem, do roztworu dodaj kroplę wodnego roztworu amoniaku. Początkowo strąca się ciemny osad, który w miarę dodawania kolejnych porcji wodnego roztworu amoniaku ulega rozpuszczeniu. Następnie wytrąca się już brunatny tlenek srebra Ag2O, roztworzając się następnie w wodzie amoniakalnej. Powstaje klarowny roztwór wodorotlenku diaminasrebra(I). Uwaga: tak przygotowanego roztworu nie wolno przechowywać. Resztę bezpośrednio po zakończeniu doświadczenia należy rozłożyć, dodając kwasu azotowego(V). Pamiętaj, stare amoniakalne roztwory soli srebra są bardzo niebezpieczne, bo powstają w nich związki silnie wybuchowe.
Gdy oba odczynniki masz już gotowe, przygotuj dużą zlewkę z gorącą wodą. Do probówki z odczynnikiem Trommera, czyli osadem wodorotlenku miedzi(II), dodaj 2–3 cm3 roztworu glukozy bądź miodu. Całość dokładnie wymieszaj wstrząsając probówką (zwracając uwagę na ewentualne zmiany). Na końcu wstaw probówkę do zlewki z gorącą wodą.
Teraz bardzo starannie umyj mydłem i wodą jedną probówkę, po czym przepłucz ją wodą destylowaną lub zupełnie świeżą deszczówką. Wlej do niej do połowy jej wysokości przygotowany wcześniej odczynnik Tollensa, po czym dodaj 2–3 cm3 roztworu glukozy lub wodnego roztworu miodu. Całość wstrząśnij, aby się wymieszała i wstaw probówkę do tej samej zlewki z gorącą wodą.
Obserwuj teraz swoje probówki. Pierwsze obserwacje dotyczące probówki z odczynnikiem Trommera masz już pewnie za sobą. Oto po dodaniu roztworu glukozy do zawiesiny Cu(OH)2 niebieski osad roztworzył się i powstał piękny, klarowny, szafirowy roztwór. — Ale ja ten kolor już znam! – mówisz — Taki sam efekt otrzymaliśmy po zmieszaniu wodorotlenku miedzi(II) z gliceryną. — Masz rację. Pamiętasz też na pewno, że był on wskaźnikiem tego, że w cząsteczce glicerolu obecne są grupy hydroksylowe, przyłączone do sąsiadujących ze sobą atomów węgla. Wynika z tego, że i glukoza zawiera w swoich cząsteczkach sąsiadujące grupy OH – jest więc poliolem.
Obserwujmy obie probówki w trakcie ogrzewania. W pierwszej zachodzą jakieś zmiany. Widzisz? Początkowo ciemnoszafirowy płyn powoli jaśnieje, a na dnie zaczyna się gromadzić drobniutki, subtelny proszek o ciemnopomarańczowej barwie. Ale również i w drugiej z probówce coś się dzieje. Tu dla odmiany początkowo jasny, przezroczysty płyn Tollensa ściemniał i stracił swą przejrzystość. W miarę upływu czasu, na ścianach drugiej probówki, od wnętrza pojawia się połyskująca metaliczna lustrzana warstewka.
Uprzedzam Cię jednak z góry, że ta warstewka jest świetnym detektywem. Wykryje ona natychmiast mniejszy brud na ściankach probówki. Jeżeli więc po 5–10 minutach ogrzewania wewnętrzne ścianki probówki zaczną przypominać zebrę, to tak zostanie ukarana Twoja niestaranność przy myciu probówek. Z kolei probówka dokładnie wymyta pokryje się jednolitą, piękną lustrzaną powłoką.
W probówce pierwszej, na jej dnie, zebrało się już sporo drobniutkiego osadu. Odsącz go i przemyj wodą. Otrzymany czerwono–pomarańczowy osad jest tlenkiem miedzi(I) Cu2O. Natomiast lustrzaną warstewkę na ściankach drugiej probówki utworzyło czyste metaliczne srebro. Ponieważ przechodzenie jonów metali w atomy metali nazywamy redukcją, mamy prawo stwierdzić, że nasza glukoza odznacza się właśnie właściwościami redukującymi. Tak jak wspomniałem wcześniej, jest to związane z obecnością grupy aldehydowej w jej cząsteczce.
Kolej na sacharozę
Dwucukier – sacharoza – jest specjalnie rozpowszechniony w świecie roślin. Sporą jego ilość zawiera sok z trzciny cukrowej, buraka cukrowego, czy też sok klonu. Z tych właśnie surowców człowiek od lat otrzymuje słodkie kryształki cukru.
Sacharoza jest dwucukrem zbudowanym z reszt glukozy oraz fruktozy. — Skoro sacharoza zawiera glukozę, to powinna się udać z nią reakcja z odczynnikiem Trommera oraz z odczynnikiem Tollensa – kombinujesz. No cóż, warto spróbować. Do dzieła zatem!
W dwóch probówkach sporządź po 10 cm3 5% wodnego roztworu sacharozy. Do pierwszej probówki dodaj świeżo strąconego osadu wodorotlenku miedzi(II) z nadmiarem wodorotlenku sodu, a do drugiej odczynnik Tollensa. W pierwszej probówce znowu obserwujesz roztwarzanie się niebieskiego osadu i powstawanie ciemnoniebieskiego, szafirowego roztworu. — Cząsteczka sacharozy zawiera więc w swojej strukturze sąsiadujące grupy hydroksylowe, wcale mnie to nie dziwi – mówisz. Probówki włóż do zlewki z gorącą wodą. Mijają minuty i kwadranse, a w obu probówkach z sacharozą nic się nie dzieje. Zawartość pierwszej probówki wciąż pozostaje szafirowa, a drugiej bezbarwna. — Czyli sacharoza nie zawiera glukozy? – pytasz z rozgoryczeniem. Z chemicznego punktu widzenia – nie. Cząsteczka glukozy, łącząc się z cząsteczką fruktozy i wydzielając przy tym cząsteczkę wody, tworzy nową cząsteczkę dwucukru. Cząsteczka sacharozy nie posiada jednak w swojej strukturze grupy aldehydowej, więc nie wykazuje właściwości redukujących.
Ale jest sposób i na to, aby z sacharozy otrzymać mieszaninę związków, które wykażą redukujące właściwości. Wystarczy tylko do wodnego roztworu sacharozy dodać odrobinę kwasu, na przykład solnego, siarkowego(VI) lub azotowego(V), a całość gotować około 2–3 minuty. Po takim zabiegu sacharoza redukować będzie i związki srebra, i związki miedzi. Stop. Przejęzyczyłem się – po zagotowaniu sacharozy z kwasem już jej nie ma w roztworze, bo każda cząsteczka disacharydu – sacharozy – pobierając wodę rozpada się na cząsteczkę glukozy i cząsteczkę fruktozy, a to znaczy, że uległa hydrolizie.
Ten swoisty rozpad cząsteczek sacharozy na glukozę i fruktozę zwany jest inwersją. Cukrem inwertowanym, czyli mieszaniną monosacharydów powstałych w wyniku hydrolizy sacharozy, jest miód i właśnie dlatego może on redukować zarówno jony miedzi, jak i srebra.
Zadaniem ucznia było doświadczalne zidentyfikowanie zawartości czterech probówek, w których znajdowały się:
wodny roztwór etanolu;
wodny roztwór etanalu;
wodny roztwór glicerolu;
wodny roztwór glukozy.
Jedynymi substancjami, które uczeń posiadał, były wodorotlenek sodu i wodny roztwór siarczanu(VI) miedzi(II). Połączył je, dzięki czemu otrzymał niebieską, galaretowatą zawiesinę wodorotlenku miedzi(II):
Uczeń wprowadził otrzymany wodorotlenek do czterech probówek, a następnie dodał badane substancje. Obserwacje umieścił w tabeli. Następnie probówki ogrzał i również zapisał obserwacje.
Przeanalizuj przedstawioną poniżej tabelę, zawierającą zapisane obserwacje, a następnie wpisz nazwy identyfikowanych substancji.
Podsumowanie
Cukry redukujące | Cukry nieredukujące |
|---|---|
mogą występować w postaci łańcuchowej | nie mogą występować w postaci łańcuchowej |
co najmniej jeden anomeryczny atom węgla nie uczestniczy w wiązaniu | wszystkie anomeryczne atomy węgla uczestniczą w wiązaniu |
wykazują zjawisko mutarotacji (ustalenie stanu równowagi pomiędzy anomerami i poprzez formę łańcuchową) | nie wykazują mutarotacji (brak możliwości przechodzenia pomiędzy anomerami i poprzez formę łańcuchową) |
wszystkie monosacharydy i niektóre cukry złożone (np. maltoza, laktoza) | niektóre cukry złożone (np. sacharoza, trehaloza), wszystkie polisacharydypolisacharydy |
w próbie Trommera powstaje ceglastoczerwony osad | w próbie Trommera powstaje czarny osad |
w próbie Tollensa powstaje lustro srebrne | w próbie Tollensa nie powstaje lustro srebrne |