Odziaływanie dipol‑dipol
Czym są dipole?
Pomiędzy cząsteczkami działają siły przyciągania i odpychania. Nazwano je oddziaływaniami międzycząsteczkowymioddziaływaniami międzycząsteczkowymi. Wpływają one znacząco na właściwości substancji, w których występują (np. na temperaturę wrzenia i topnienia, stan skupienia, gęstość). Jednym z przykładów takiego oddziaływania jest oddziaływanie dipol–dipoloddziaływanie dipol–dipol, które występuje w cząsteczkach polarnych. Posiadają one ładunek cząstkowy (dodatni oraz ujemny), skoncentrowany w konkretnym obszarze związku chemicznego. Ponadto takie cząsteczki polarne charakteryzują się również stałym, elektrycznym momentem dipolowym. Ich bieguny (ładunki cząstkowe) decydują o orientacji w przestrzeni względem innych cząsteczek. Oddziaływanie dipol–dipol polega więc na elektrostatycznym przyciąganiu się przeciwnie naładowanych biegunów cząsteczek.
Dipol elektrycznyDipol elektryczny jest układem dwóch ładunków o równych wartościach i przeciwnych znakach, znajdujących się od siebie w pewnej odległości.


Dipol jest więc układem elektrycznie obojętnym, tzn. jego ładunek wypadkowy jest zerowy, ponieważ dodatni ładunek równoważony jest ładunek ujemny. Pomimo tej elektrycznej neutralności, dipol oddziałuje z polem elektrycznym. Jeśli dipol znajdzie się w polu elektrycznym, to na ogół dozna on obrotu.

Jakie są przykłady dipoli?
Do dipoli zalicza się wiele cząsteczekcząsteczek z wiązaniem kowalencyjnym spolaryzowanym. Przykładami mogą być: , , , . Po stronie atomu wodoru znajduje się dodatni biegun dipola, a po stronie atomu fluorowca – ujemny. Takie substancje określa się jako polarne.

Jednak nie wszystkie cząsteczki, w których występuje wiązanie spolaryzowane, są dipolami.

Moment dipolowyMoment dipolowy jest wektorem, zdefiniowanym jako iloczyn ładunku i wektora łączącego ładunek ujemny z dodatnim:
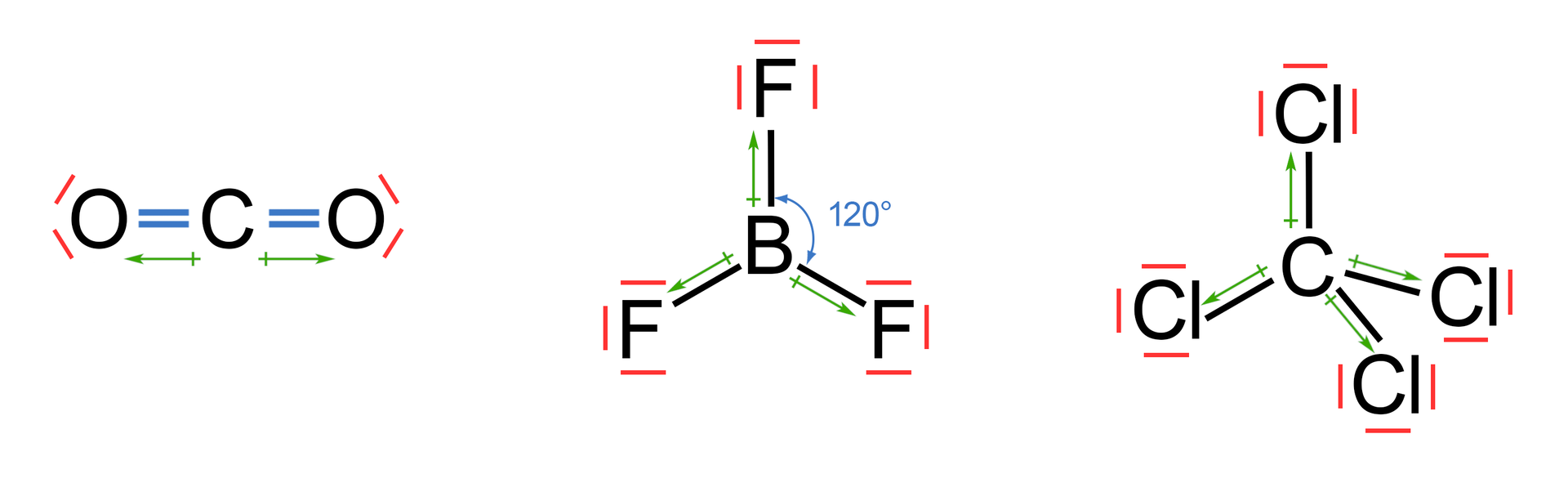
Moment dipolowy cząsteczki jest sumą wektorów momentów dipolowych poszczególnych wiązań w cząsteczce. Jeśli poszczególne momenty dipolowe wiązań znoszą się wzajemnie, to cząsteczka nie posiada wcale momentu dipolowego. Przykładem jest trójatomowa, liniowa cząsteczka . Każde wiązanie jest polarne, jednak eksperymenty pokazują, że cząsteczka tlenku węgla() nie posiada momentu dipolowego. Dzieje się tak, ponieważ dwa dipole wiązania , równe pod względem wielkości oraz zorientowane względem siebie pod kątem , znoszą się wzajemnie. Zerowy moment dipolowy występuje również w cząsteczce czteroatomowej – czy tetraedrycznej .
Cząsteczka o kształcie piramidy, np. amoniak, jest dipolem, ponieważ na atomie azotu, w miejscu występowania wolnej pary elektronowej, jest większa gęstość ładunku ujemnego niż po stronie atomów wodoru.

Silniejszy charakter dipolowy posiadają cząsteczki wody, ponieważ wiązanie jest bardziej spolaryzowane niż wiązanie . Dodatkowo atom tlenu posiada dwie wolne pary elektronowe.

Wyjaśnij różnicę, dlaczego woda jest substancją polarną, a tlenek węgla(IV) nie. Odpowiedź wpisz poniżej:
Ładunki elektryczne o przeciwnych znakach przyciągają się, a o takich samych odpychają, dlatego także dipole mogą się przyciągać lub odpychać, w zależności od wzajemnej orientacji. Bardziej korzystne energetycznie jest przyciąganie, dlatego cząsteczki będące dipolami ustawiają się właśnie w taki sposób. Jest to oddziaływanie dipol–dipol.

Rodzaje odddziaływań między dipolami
Czy wiesz, jakie rodzaje oddziaływań występują między dipolami? Zapoznaj się z poniższym filmem, a następnie rozwiąż zadania.

Film dostępny pod adresem /preview/resource/R1AwIU5EX0jLo
Film opisujący oddziaływania między dipolami
Cząsteczki chlorowodoru są dipolami. Próbkę ciekłego chlorowodoru umieszczono pomiędzy nienaładowanymi okładkami kondensatora. Opisaną sytuację możemy przedstawić schematycznie na poniższej grafice.

Następnie do okładek kondensatora przyłożono napięcie, co spowodowało zgromadzenie się ładunków dodatnich na jednej, a ujemnych na drugiej okładce kondensatora. Czy taka sytuacja, w konsekwencji której pojawiło się jednorodne pole elektryczne między okładkami, wpłynie na orientację przestrzenną cząsteczek chlorowodoru? Zaznacz grafikę przedstawiającą ułożenie cząsteczek chlorowodoru między okładkami naładowanego kondensatora.
Zaznacz poprawną odpowiedź.
Moment dipolowy () jest iloczynem ładunku () i odległości między ładunkami (). Jednostką momentu dipolowego w układzie SI jest iloczyn kulomba () i metra () (zwany potocznie kulombometrem). Moment dipolowy cząsteczki chlorowodoru wynosi , a odległość między ładunkami – . Na podstawie podanych danych doświadczalnych oblicz ładunek cząsteczkowy chlorowodoru.
Wyjaśnij, który związek chemiczny powinien mieć wyższą temperaturę wrzenia, oraz uzasadnij, czym jest to spowodowane.

Jakie są skutki występowania oddziaływań dipol–dipol?
Ciecze, w których występuje silne oddziaływanie międzycząsteczkowe, posiadają duże entalpie parowania oraz wysokie temperatury wrzenia. Dzięki znajomości tej temperatury można uzyskać informacje o względnej sile oddziaływań międzycząsteczkowych.
Substancje polarne są dobrymi rozpuszczalnikami dla innych substancji polarnych (zgodnie z zasadą „podobne rozpuszcza się w podobnym”). Na przykład woda stanowi dobry rozpuszczalnik dla amoniaku.
Oddziaływania dipol–dipol występują pomiędzy grupami polarnymi w białkach, stabilizując ich trzeciorzędową strukturę. Grupy polarne, zawarte w białku, mogą tworzyć oddziaływania dipol–dipol.
