Siły van der Waalsa
Siły van der WaalsaSiły van der Waalsa to wszechobecne, choć stosunkowo słabe oddziaływania międzycząsteczkowe o charakterze elektrostatycznym. Choć indywidualnie są znacznie słabsze od wiązań chemicznych, takich jak kowalencyjne czy jonowe, ich zbiorowe działanie ma fundamentalne znaczenie dla wielu właściwości fizycznych materii, od temperatury wrzenia cieczy po zdolność gekonów do wspinania się po gładkich powierzchniach.

Swoją nazwę zawdzięczają holenderskiemu fizykowi Johannesowi van der Waalsowi [johanesowi wan der walsowi], który w 1873 r. po raz pierwszy je opisał. Siły van der Waalsa występują albo pomiędzy dwoma cząsteczkami, z których jedna jest polarna (jest dipolem), albo pomiędzy dwiema niepolarnymi cząsteczkami typu czy , albo pomiędzy niewiążącymi się atomami gazów szlachetnych, albo także pomiędzy dipolami. Są to siły o charakterze oddziaływań elektrostatycznych. Nie są kierunkowe. Działają tylko na bardzo krótki zasięg. Oddziaływanie jest tym większe, im cząsteczki zbliżają się do siebie.
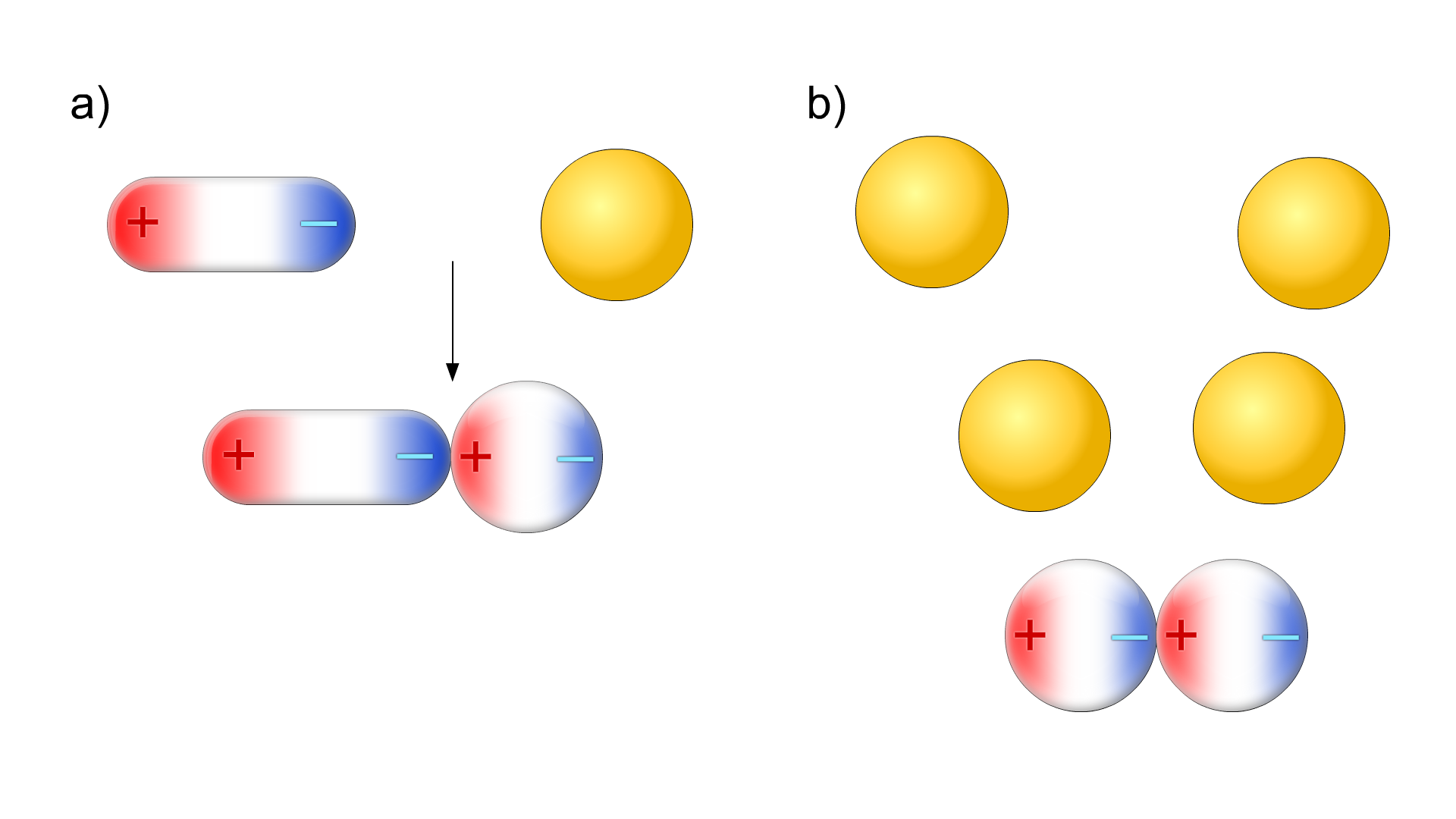
a) dipol-cząsteczka niepolarna
b) cząsteczka niepolarna-cząsteczka niepolarna
Oddziaływania van der Waalsa polegają na słabym oddziaływaniu ze sobą chmury elektronowej indywiduum chemicznego, a więc na przyciąganiu się szybkozmiennych dipoli. Kiedy elektrony walencyjne poruszają się, gęstość ładunku ujemnego na zewnętrznej powłoce atomów ulega szybkim fluktuacjom, co wzbudza również fluktuację w powłoce walencyjnej sąsiednich atomów. W wyniku tego powstają szybkozmienne dipole, które przyciągają się wzajemnie, co zwiększa wzajemną polaryzację elektronową.
Do oddziaływań van der Waalsa można zaliczyć:
przyciąganie trwałych dipoli;
przyciąganie dipola trwałego i indukowanego;
przyciąganie dipola chwilowego i indukowanego.
Za co odpowiadają siły van der Waalsa?
Siły van der Waalsa decydują o wielu istotnych zjawiskach w przyrodzie, takich jak: solwatacja, struktura cieczy i ciał stałych, właściwości gazów rzeczywistych, stan skupienia materii oraz innych. Pełnią bardzo ważną rolę w makromolekułach – np. w polimerach warunkują właściwości polimerów (czyli to, czy cząsteczka polimeru jest giętka, czy sztywna, zależy nie tylko od właściwości makrocząsteczki). Siły van der Waalsa odpowiadają również za występowanie tzw. pochłaniania powierzchniowego, inaczej mówiąc, adsorpcji cząsteczek, czyli odkładania cząsteczek jednej substancji na powierzchni drugiej.

Mimo że są to stosunkowo słabe oddziaływania dla małych cząsteczek (kilkanaście razy słabsze od sił wiązania atomów w cząsteczce), to niekiedy mogą przewyższać siłę wiązania chemicznego. Można to zaobserwować w przypadku długołańcuchowych węglowodorów, które występują w smarach lub tworzywach sztucznych. Widać to również w temperaturach wrzenia – zazwyczaj substancje o dużej masie cząsteczkowej mają wysokie temperatury wrzenia, a substancje o małej masie cząsteczkowej – niskie. Przyczyną tego jest większa liczba elektronów w cząsteczce, czemu odpowiadają większe fluktuacje ładunków cząstkowych, uwarunkowane oscylowaniem elektronów między różnymi położeniami. Na przykład analizując atomy fluorowców, atom fluoru ma tylko dziewięć elektronów, fluktuacje w tej chmurze elektronowej są małe, a oddziaływania międzycząsteczkowe są tak słabe, że temperatura wrzenia gazowego fluoru to -188°C. W atomie bromu jest 35 elektronów, fluktuacje są częstsze, czego efektem jest zmiana temperatury wrzenia. Gazowy brom wrze w 59°C.
Ciała stałe, w których występują głównie siły van der Waalsa, charakteryzują się niższymi temperaturami topnienia i są bardziej miękkie niż te, w których występują inne oddziaływania, tj. wiązanie wodorowe.
Siły Londona
Siły Londona to rodzaj oddziaływań van der Waalsa, są wynikiem wzajemnego przyciągania się wszystkich cząsteczek. Jest to jedyne oddziaływanie, które występuje między atomami gazów szlachetnych i między cząsteczkami niepolarnymi. Niepolarne cząsteczki mogą wykazywać chwilowy moment dipolowy, wynikający z deformacji chmury elektronowej.

Siła oddziaływań Londona wzrasta z liczbą elektronów w cząsteczce, a więc z masą molową związku.
Zmiany właściwości fizycznych związków pod wpływem sił Londona wykazują węglowodory. Wraz ze wzrostem ilości atomów węgla w cząsteczce węglowodoru, zmienia się ich stan skupienia w warunkach pokojowych. Od węglowodorów, które są gazami, poprzez cieczce, aż po węglowodory o dużej ilości atomów węgla, będące ciałami stałymi. W wyniku zwiększania się ilości atomów węgla, cząsteczki te mają większą możliwość oddziaływania ze sobą. Nie są one trwałymi dipolami, ale wraz z ich wzrastającą masą cząsteczkową zwiększa się siła – co przedstawiono na poniższych zdjęciach.
Ważnym czynnikiem, wpływającym na siłę oddziaływań, jest także kształt cząsteczki:
Siły van der Waalsa zależą również od kształtu cząsteczki. Powoduje to różnice w temperaturach wrzenia np. dla związków organicznych. Cząsteczka o wzorze może mieć strukturę liniową lub rozgałęzioną. W zależności od struktury, ma różne temperatury wrzenia.
Substancja zbudowana tylko z cząsteczek liniowych ma wyższą temperaturę wrzenia, niż ta zbudowana z cząsteczek rozgałęzionych. Jest to spowodowane tym, że oddziaływania van der Waalsa są silniejsze dla bardziej zbliżonych do siebie cząsteczek o strukturze liniowej. Poniżej przedstawiono przykłady dwóch izomerów związku o wzorze ogólnym wraz z ich temperaturami wrzenia.
Pentan wrze w temperaturze , a –dimetylopropan w temperaturze . Oddziaływania w przypadku drugiego związku są znacznie słabsze. Im bardziej rozgałęzione związki, tym oddziaływanie Londona jest słabsze.

Duża przyczepność łap gekona do powierzchni wynika nie tylko z obecności lipidów, znajdujących się na ich skórze, oraz sił elektrostatycznych, ale również występujących sił van der Waalsa. Na łapach gekona znajdują się rządki mikroskopijnych włosków, dodatkowo rozszczepionych na końcach w miotełki, które są jeszcze drobniejsze. Zakończone są płaskimi nano‑szpatułkami, co powoduje zwiększenie powierzchni przylegania. Siłą odpowiedzialną za przyklejanie się włosków do powierzchni są właśnie omawiane oddziaływania. Siły van der Waalsa są tymi najsłabszymi, ale nadal odgrywają ważną rolę we właściwościach cząsteczek i w nauce o powierzchni.
Zapoznaj się z poniższym filmem pt. „Siły van der Waalsa”, a następnie rozwiąż zadania.

Film dostępny pod adresem /preview/resource/RxPcxj9aYczSq
Film nawiązujący do treści materiału
Z kolei przyciąganie się dipoli trwałych nazywamy 1. wody, 2. siłami orientacyjnymi Keesoma, 3. sodu, 4. dipol‑dipol, 5. chlorowodoru, 6. ksenonu, 7. chlorkowymi, 8. jon‑dipol, 9. siłami indukcyjnymi Debaya lub po prostu oddziaływaniem typu 1. wody, 2. siłami orientacyjnymi Keesoma, 3. sodu, 4. dipol‑dipol, 5. chlorowodoru, 6. ksenonu, 7. chlorkowymi, 8. jon‑dipol, 9. siłami indukcyjnymi Debaya. Występuje ono m.in. między cząsteczkami ciekłego 1. wody, 2. siłami orientacyjnymi Keesoma, 3. sodu, 4. dipol‑dipol, 5. chlorowodoru, 6. ksenonu, 7. chlorkowymi, 8. jon‑dipol, 9. siłami indukcyjnymi Debaya.
W temperaturze pokojowej fluor i chlor są gazami, brom jest cieczą, a jod to substancja stała. Wytłumacz różnice w stanach skupienia fluorowców.
Siły van der Waalsa są odpowiedzialne za występowanie wielu zjawisk w przyrodzie. Wymień trzy znane Ci, za które odpowiadają te oddziaływania.
Przeanalizuj poniższą symulację interaktywną. Czy potrafisz uzasadnić, jaka jest zależność między liczbą atomów węgla w alkanach a temperaturą wrzenia? Skąd biorą się różnice w temperaturze wrzenia różnych związków?
Zapoznaj się z opisem symulacji interaktywnej. Czy potrafisz uzasadnić, jaka jest zależność między liczbą atomów węgla w alkanach a temperaturą wrzenia? Skąd biorą się różnice w temperaturze wrzenia różnych związków?
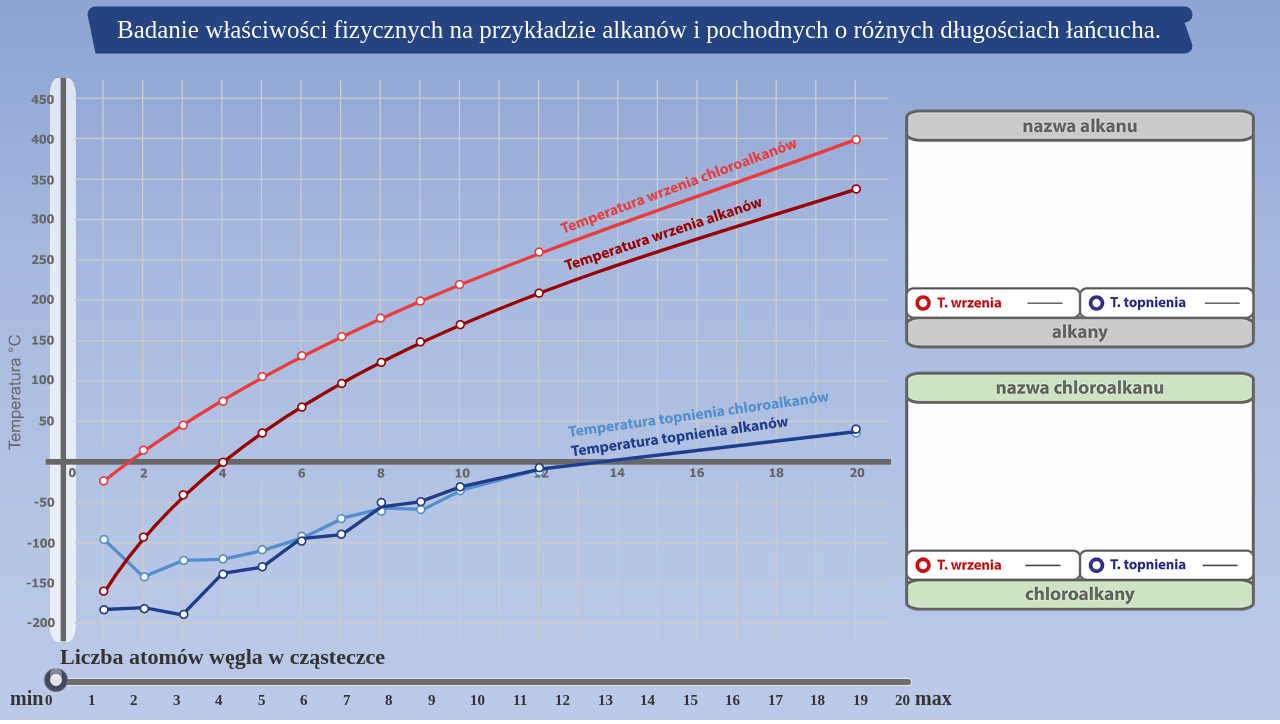
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DDBVRN6HO
Wyjaśnij, jaka jest zależność między liczbą atomów węgla w alkanach a temperaturą wrzenia.
Porównaj temperatury wrzenia alkanów i ich chloropochodnych. Uzasadnij różnice w temperaturze wrzenia tych związków.
Odpowiedz, jaki stan skupienia ma propan i chloropropan w temperaturze .




