Słownik pojęć
to usuwanie materiału z powierzchni w wyniku oddziaływania impulsów laserowych o odpowiedniej gęstości energii (napromienieniu wyrażanym w )
(gr. állos „obcy”, „inny”, trópos „sposób”, „postać”) występowanie tego samego pierwiastka chemicznego w dwóch lub więcej odmianach, znajdujących się w tym samym stanie skupienia. Odmiany alotropowe pierwiastka mogą się różnić między sobą strukturą krystaliczną lub ilością atomów w cząsteczce
, jednostka długości stosowana do wyrażania bardzo małych długości, np. długości fal świetlnych, rozmiarów atomów i cząsteczek; ; nazwa angstrem od nazwiska szwedzkiego fizyka i astronoma A.J. Ångströma, który ją wprowadził w 1868 r.
(gr. ánodos „w górę”) jon o ujemnym ładunku elektrycznym
(łac. arōma, -ătis „przyprawa”) związki wykazują aromatyczność, kiedy są płaskie – powstają w wyniku sprzężenia się wiązań podwójnych; najprostszym związkiem organicznym jest benzen
cząsteczka, w której występują dwa przeciwnie naładowane bieguny
stan, w którym elektron bierze udział w tworzeniu więcej niż jednego wiązania chemicznego
układ dwóch ładunków punktowych o równych wartościach i przeciwnych znakach, znajdujących się w pewnej odległości od siebie
kwas deoksyrybonukleinowy; wielkocząsteczkowy biopolimer obecny we wszystkich komórkach organizmów, w których jest nośnikiem informacji genetycznej
(gr. ḗlektron „bursztyn”) cząstka elementarna o ładunku ujemnym; znajduje się w chmurze elektronowej, otaczającej jądro atomu lub w stanie wolnym
elektrony wartościowości, elektrony zapełniające w atomie danego pierwiastka tzw. orbitale walencyjne, tzn. orbitale o największej dla tego atomu wartości energii (w stanie podstawowym)
(siła wiązania) energia potrzebna do rozerwania cząsteczki na pojedyncze atomy
jest to cząstka elementarna nie mająca ładunku elektrycznego
model stosowany w opisie metali i opisuje zbiór elektronów walencyjnych, poruszających się między kationami metali
helowce; pierwiastki chemiczne, które tworzą grupę układu okresowego: hel (), neon (), argon (), krypton (), ksenon () i radon ()
odmiana alotropowa węgla, grafit jest kruchy oraz przewodzi prąd elektryczny
są to związki chemiczne o cząsteczkach nieróżniących się od siebie ani masą, ani liczbą atomów, ani rodzajem, natomiast mające różny sposób lub kolejność połączeń tych atomów lub też rozmieszczeniem ich w przestrzeni
atom lub grupa atomów obdarzona dodatnim lub ujemnym ładunkiem elektrycznym
(gr. katin „idący w dół”) jon o dodatnim ładunku elektrycznym
równoległościan, który stanowi podstawowy, powtarzający się okresowo w przestrzeni element sieci przestrzennej; kształt i rozmiary komórki elementarnej określają stałe sieciowe: długości krawędzi: , , , i kąty: , , między nimi
typ komórki elementarnej, w której indywidua chemiczne znajdują się w narożach sześcianu i na środkach ścian
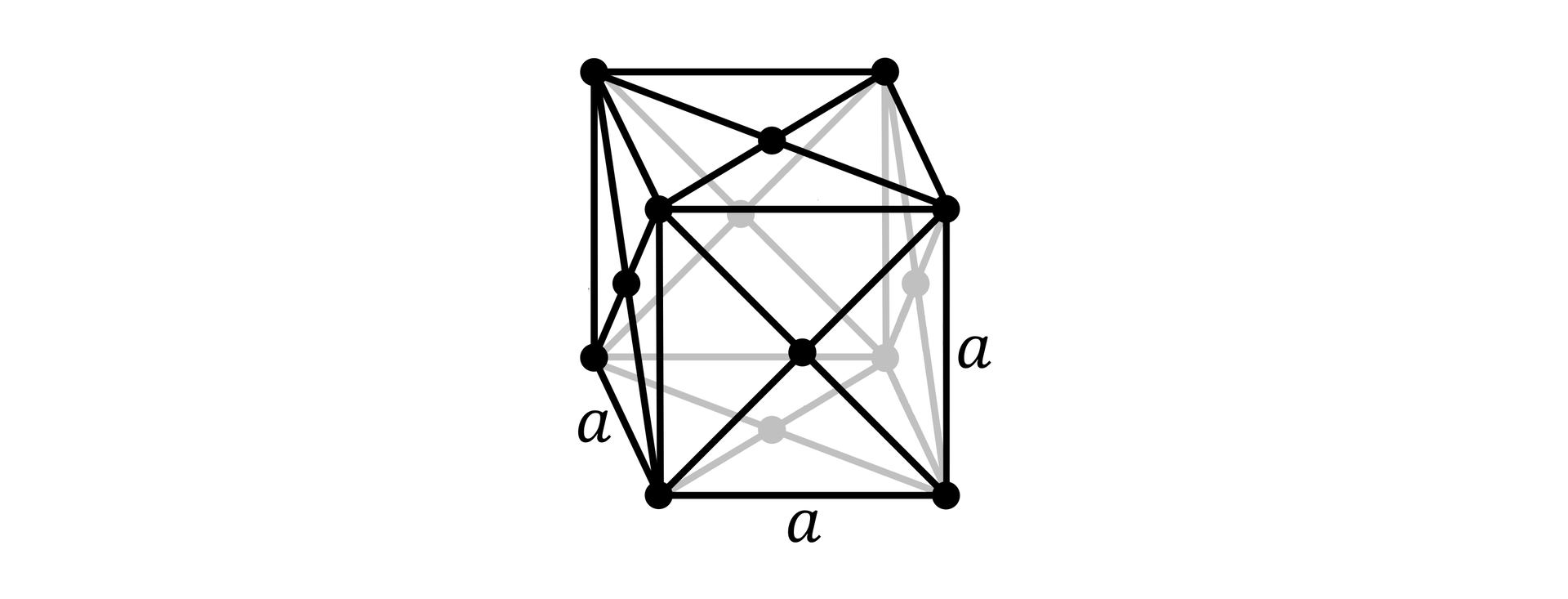
typ komórki elementarnej, w której indywidua chemiczne znajdują się w narożach sześcianu i w jego środku
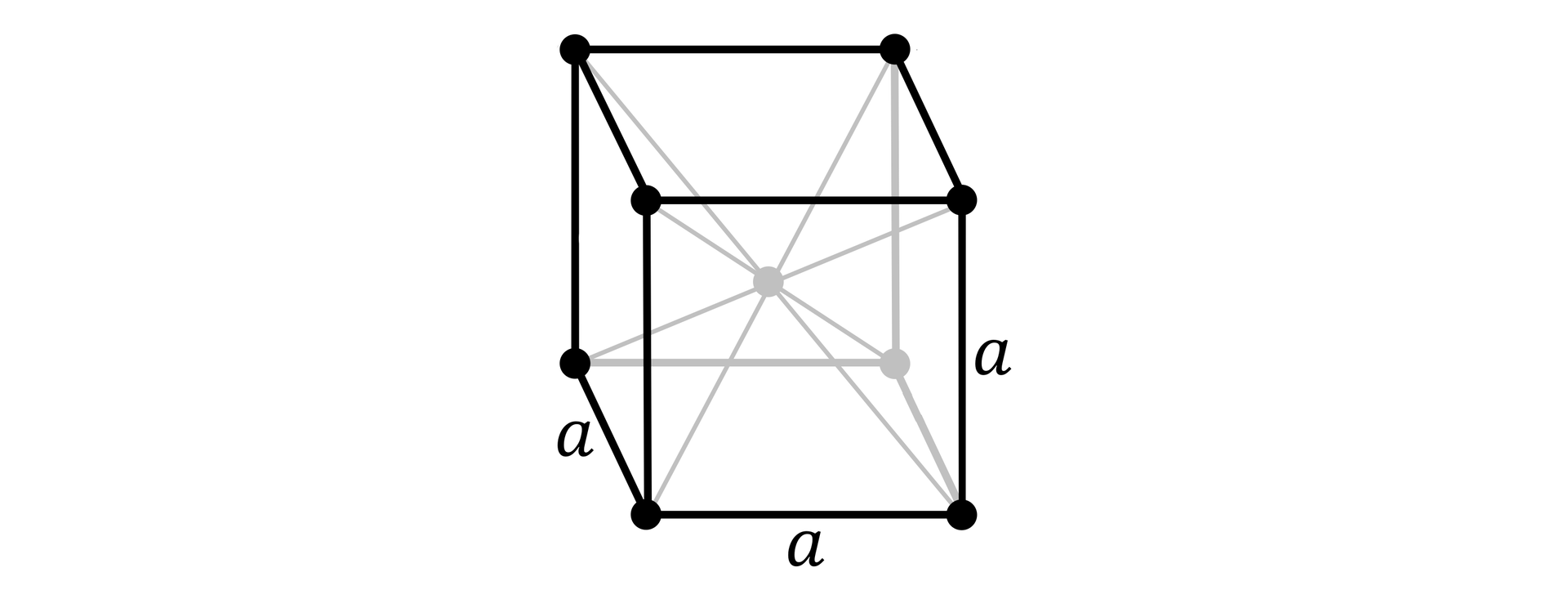
kryształ, w którym sieć krystaliczną tworzą dobrze zdefiniowane cząsteczki powiązane słabymi oddziaływaniami międzycząsteczkowymi (np. siłami van der Waalsa), natomiast nie występują w niej wiązania jonowe ani wodorowe
struktury, w których występuje więcej niż jeden rodzaj oddziaływań między indywiduami
kryształy, w których węzły sieci krystalicznej są obsadzone przez jony – kationy i aniony, o równoważnej ilości ładunków elektrycznych (dzięki czemu kryształ jonowy jako całość jest elektrycznie obojętny); tworzą je głównie sole składające się z pierwiastków o dużej różnicy elektroujemności, np. , – związki o dominującym charakterze jonowym wiązań
kryształy mające w węzłach sieci krystalicznej obojętne elektrycznie atomy; wiązania tworzą pary elektronów walencyjnych pochodzących od dwóch sąsiednich atomów, elektrony te stanowią wspólną własność obydwu atomów; takie wiązania przejawiają wyraźną kierunkowość, a typowym przykładem jest diament; cechy kryształów kowalencyjnych to duża twardość oraz małe przewodnictwo elektryczne
kryształy, w których elektrony walencyjne są wspólne dla wszystkich jonów w krysztale i tworzą gaz elektronowy, wypełniający przestrzeń pomiędzy dodatnimi jonami; kryształy metaliczne są doskonałymi przewodnikami elektryczności i ciepła; przykładem kryształów metalicznych są kryształy tworzone przez metale alkaliczne
liczba najbliższych indywiduów chemicznych, otaczających dany atom lub jon
(gr. makrós „bardzo duży, wielki”, łac. molecula „cząsteczka”) są to cząsteczki chemiczne złożone z kilku tysięcy atomów
inaczej współczynnik sprężystości podłużnej lub moduł sprężystości podłużnej – jest to wielkość określająca własności sprężyste ciała stałego, oznaczana symbolem , charakteryzująca podatność materiału na odkształcenia podłużne przy rozciąganiu, ściskaniu lub zginaniu
wektor o kierunku zgodnym z osią dipola, umownym zwrocie od ładunku ujemnego do dodatniego; jego wartość jest równa iloczynowi ładunku i odległości między ładunkami.
właściwość niektórych ciał stałych, będących nadprzewodnikami polegająca na zaniku oporu elektrycznego po oziębieniu ich do temperatury , niższej od temperatury krytycznej
to substancje, które wykazują jedną z cech: albo nie są kowalne, albo są słabymi przewodnikami prądu. Do typowych niemetali należą: fluorowce, tlen, azot, siarka, fosfor oraz helowce
estry nukleozydów i kwasu ortofosforowego(V); w nukleozydach reszta hydroksylowa () części cukrowej jest połączona z cząsteczką kwasu ortofosforowego() wiązaniem estrowym; stanowią składniki kwasów nukleinowych (DNA i RNA), niezbędne są też w metabolizmie i przekazywaniu sygnałów w komórce
elektrostatyczne oddziaływanie cząsteczek polarnych, odpowiednio zorientowanych wobec siebie
(gr. di- „dwa razy”, gr. pólos „biegun”) ten typ oddziaływania występuje między dwoma cząsteczkami, które w jednym fragmencie cząsteczki posiadają nadmiar elektronów, dlatego występuje na nich częściowy ładunek ujemny, a w drugim fragmencie występuje deficyt elektronów, co prowadzi do powstania w tym miejscu częściowego ładunku dodatniego
oddziaływanie , słabe oddziaływanie chmury elektronowej między pierścieniami aromatycznymi
przyciąganie oraz odpychanie, występujące pomiędzy atomami sąsiadujących cząsteczek
w przestrzeni trójwymiarowej powierzchnia, w obrębie której potencjał elektryczny jest równy (ma jednakową wartość)
to proces polegający na przepływie ciepła i tym samym na przekazywaniu energii kinetycznej bezładnego ruchu cząsteczek ośrodka, z części układu o wyższej temperaturze do cząsteczek z części układu o temperaturze niższej
zjawisko przepływu prądu elektrycznego przez dany ośrodek pod wpływem zewnętrznego pola elektrycznego. Wartości przewodności elektrycznej właściwej dzielą ciała stałe na: przewodniki (), półprzewodniki () i izolatory ()
każda substancja dobrze przewodząca prąd elektryczny
układ krystalograficzny, w którym wszystkie boki komórki krystalicznej mają identyczną długość () oraz wszystkie kąty są proste ()
słabe oddziaływania międzycząsteczkowe, związane z kwantową naturą powłok elektronowych, elektrycznie obojętnych atomów lub cząsteczek oraz z ruchem elektronów w cząsteczce
jest to dziesięciostopniowa skala określająca względną twardość minerałów. Została stworzona przez Friedricha Mohsa w roku

umowna skala elektroujemności pierwiastków opracowana przez L.C. Paulinga w r.
takie ułożenie, w którym każde indywiduum chemiczne otoczone jest przez dwanaście indywiduów
struktury, w których występuje jedynie jeden rodzaj oddziaływań między indywiduami
temperatura, w której dana substancja stała zmienia stan skupienia na ciekły
(gr. tetrakys „czterokrotnie”) czworościan foremny

punkty przecięcia krawędzi komórek elementarnych w sieci kryształu
rodzaj oddziaływania elektrostatycznego pomiędzy atomem wodoru a atomem pierwiastka elektroujemnego o wolnych parach elektronowych; to oddziaływanie może być międzycząsteczkowe lub wewnątrzcząsteczkowe