Badanie właściwości fizycznych substancji tworzących kryształy jonowe, kowalencyjne, molekularne i metaliczne
Uwzględniając rodzaj wiązań, który decyduje o właściwościach fizycznych kryształów wyróżniamy:
Kryształy molekularne
Kryształy molekularneKryształy molekularne są zbudowane z odrębnych cząsteczek, które weszły w interakcję dzięki oddziaływaniom międzycząsteczkowym (van der Waalsa). Takie struktury tworzą związki organiczne lub zestalone gazy. Wspomniane oddziaływania między cząsteczkami są słabe, co skutkuje m.in. stosunkowo małą twardością kryształów molekularnych i niską temperaturą topnienia. Przykładowymi związkami chemicznymi, które tworzą analizowane kryształy są jod oraz naftalen (popularnie nazywany naftaliną). Dodatkowo warto wspomnieć, że kryształy molekularne:
nie przewodzą prądu elektrycznego,
nie ulegają dysocjacji jonowej,
słabo rozpuszczają się w wodzie i innych rozpuszczalnikach polarnych,
dobrze rozpuszczają się w niepolarnych rozpuszczalnikach (np. benzen, benzyna),
mają niskie temperatury topnienia,
są bardzo reaktywne.
W kryształach molekularnych niektórych niepolarnych substancji, oddziaływania między drobinami są na tyle słabe, że pojedyncze cząsteczki mogą odrywać się od kryształu (ciała stałego), zmieniając tym samym stan skupienia na gazowy. Opisana przemiana to sublimacja. Przykładem substancji, która stosunkowo łatwo ulega sublimacji jest jod. Proces odwrotny do sublimacji to resublimacja.
Kryształy kowalencyjne
W kryształach kowalencyjnychkryształach kowalencyjnych (atomowych) atomy są ze sobą związane za pomocą wiązań kowalencyjnych. Podobnie jak w kryształach jonowych, także w kryształach atomowych traci sens pojęcie cząsteczki. W analizowanych układach nie można bowiem wyróżnić pojedynczych cząsteczek – cały kryształ kowalencyjny (atomowy) trzeba traktować jako jedną olbrzymią cząsteczkę. Sztandarowym przykładem kryształu kowalencyjnego jest diament. W sieci krystalicznej diamentu, każdy atom węgla łączy się z czterema innymi atomami węgla za pomocą wiązań kowalencyjnych. Regularna sieć przestrzenna diamentu sprawia, że jest on najtwardszą znaną substancją – przypisuje mu się twardość 10 w skali Mohsa. Wykorzystanie wszystkich elektronów walencyjnych atomów węgla do utworzenia wiązań kowalencyjnych powoduje, że diament jest izolatorem elektrycznym. Podobny układ występuje w krzemie i germanie.
Dodatkowo, kryształy kowalencyjne:
nie ulegają dysocjacji jonowej,
mają wysoką temperaturę topnienia,
są niereaktywne.


Kryształy jonowe
Kryształy jonowe są tworzone tylko przez związki chemiczne o budowie jonowej, m.in. tlenki i sole metali i grupy układu okresowego. W stanie stałym związki te tworzą jonowe sieci krystaliczne, w których na przemian rozmieszczone są jony dodatnie i ujemne.
Przykładowymi związkami chemicznymi, które tworzą kryształy jonowekryształy jonowe są:
tlenki metali alkalicznych, np.: tlenek sodu, tlenek potasu,
wodorotlenki metali alkalicznych, np. wodorotlenek litu,
sole metali alkalicznych, np.: chlorek sodu, jodek potasu.
Analizowane kryształy zbudowane są z jonów rozmieszczonych równomiernie w sieci krystalicznej. Jony te działają na siebie siłami przyciągania elektrostatycznego, których wartości są dość znaczne. Dlatego też kryształy związków o wiązaniu jonowym wykazują specyficzne właściwości fizyczne tj.:
posiadają wysokie temperatury wrzenia, np. chlorek sodu wrze w temperaturze ,
posiadają wysokie temperatury topnienia, np. chlorek sodu topi się w temperaturze (proces topienia związku jonowego wymaga użycia dużych ilości energii w celu zerwania wszystkich wiązań jonowych w krysztale),
odznaczają się stosunkowo dużą twardością,
w stanie stopionym i w roztworze wodnym przewodzą prąd,
najczęściej dobrze rozpuszczają się w rozpuszczalnikach polarnych.

Związki jonowe są na ogół twarde, ale kruche. Dlaczego? Potrzeba dużej siły mechanicznej, takiej jak np. uderzenie kryształu młotkiem, aby doprowadzić do przesunięcia jednej warstwy jonów budującej kryształ, względem drugiej warstwy. W takiej sytuacji, zbliżają się do siebie jony o tym samym ładunku (patrz rysunek poniżej). Jony te odpychają się, powodując tym samym rozbicie (rozkruszenie) kryształu.

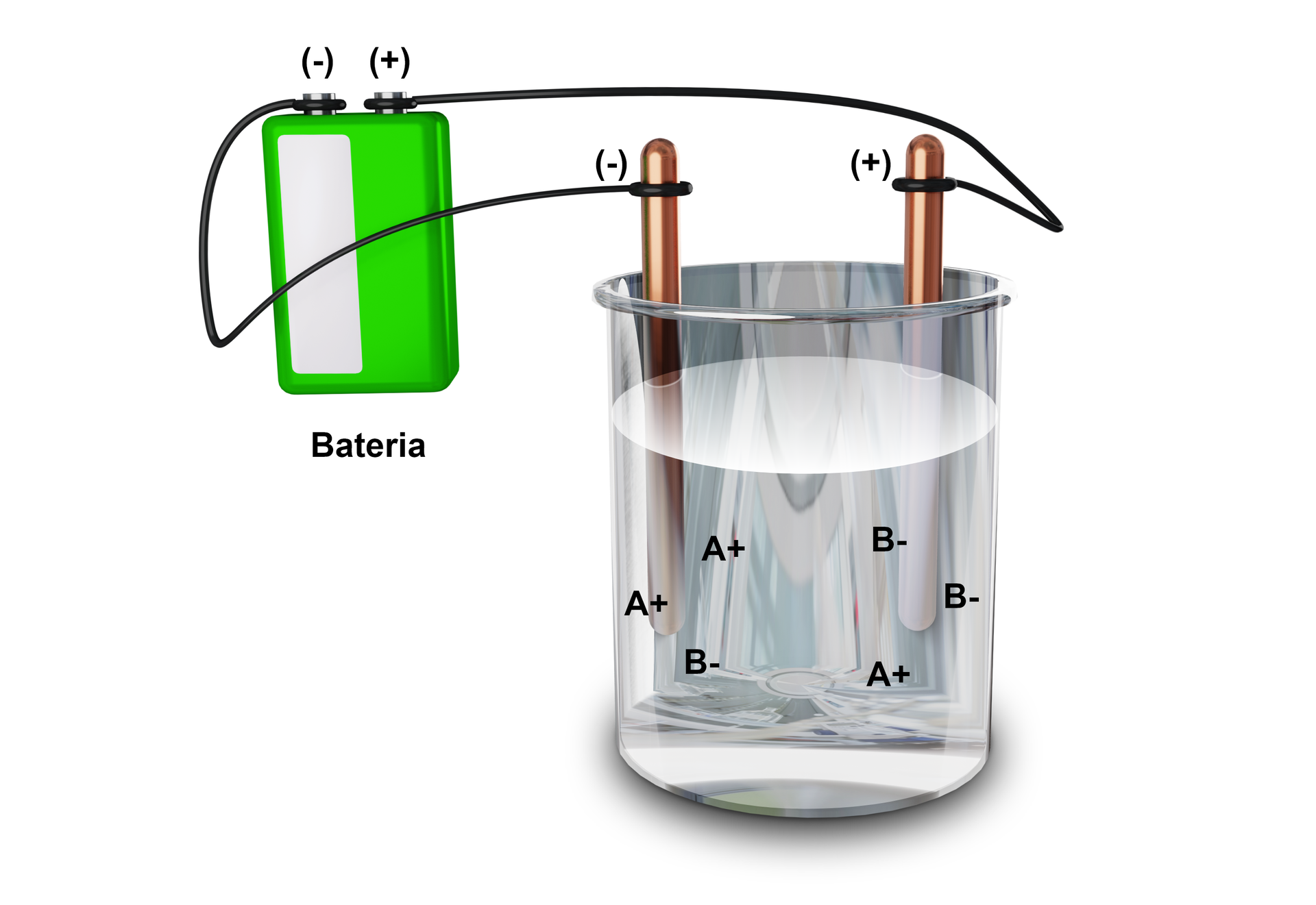
Badanie przewodnictwa kryształów jonowych
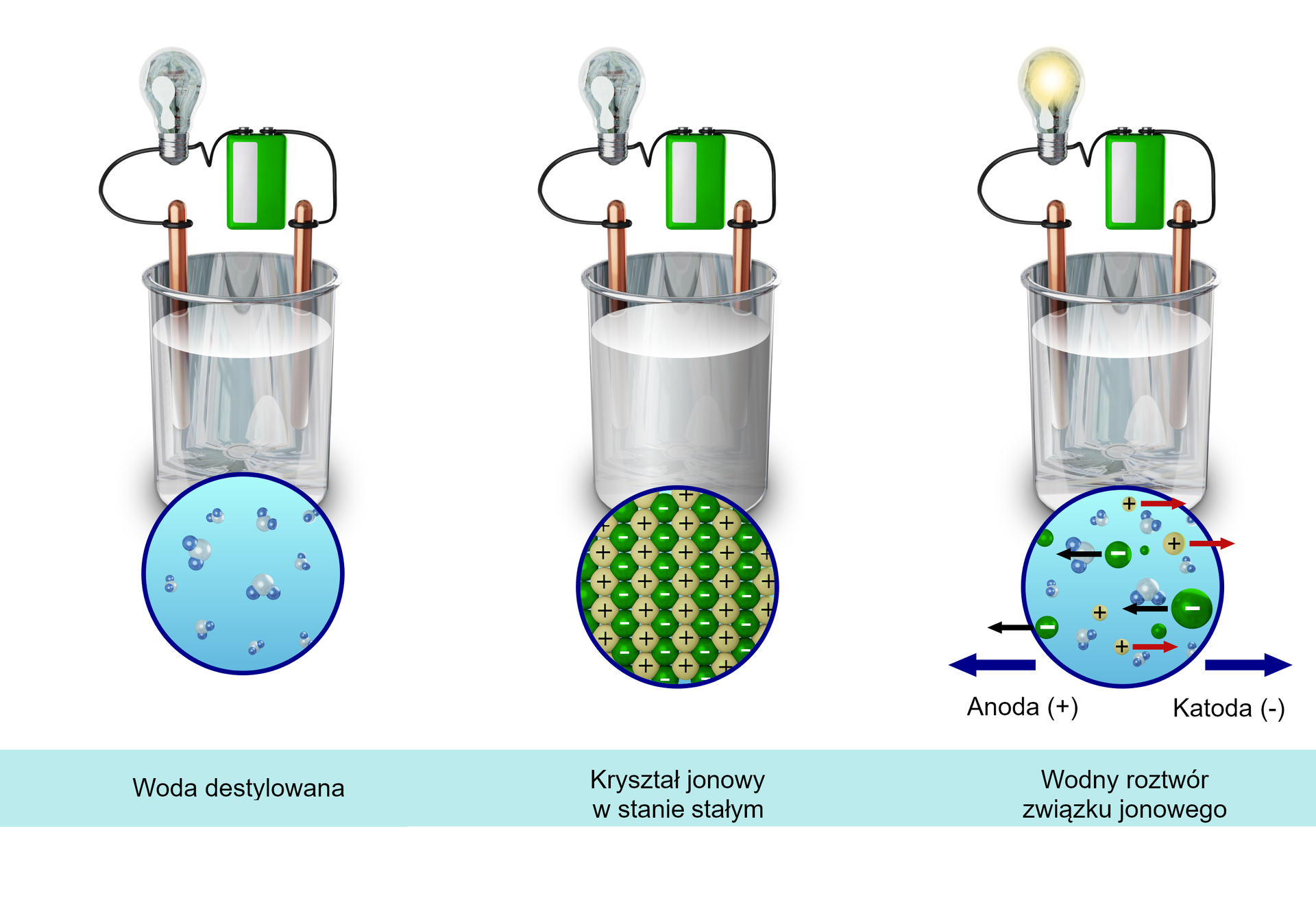
Inną charakterystyczną właściwością związków jonowych jest ich przewodnictwo elektryczne. Poniższy rysunek przedstawia trzy eksperymenty, w których dwie elektrody podłączone do żarówki są umieszczone w zlewkach zawierających trzy różne substancje. Przeanalizuj schemat i zapisz wynikające z niego obserwacje i wnioski.
Inną charakterystyczną właściwością związków jonowych jest ich przewodnictwo elektryczne. Zapoznaj się z opisem rysunku przedstawiającego trzy eksperymenty, w których dwie elektrody podłączone do żarówki są umieszczone w zlewkach zawierających trzy różne substancje. Zapisz wynikające z niego obserwacje i wnioski.
Rozpuszczalność kryształów
Kryształy jonowe, np. chlorku sodu, siarczanu() miedzi() – czy siarczanu() żelaza() – , są łatwo rozpuszczalne w rozpuszczalnikach polarnych w przeciwieństwie do kryształów kowalencyjnych, np. kryształów diamentu.
Kryształy o wiązaniach metalicznych
Kryształy metaliczneKryształy metaliczne występują w czystych metalach i ich stopach. W sieci kryształu metalicznego węzły sieci przestrzennej są obsadzone przez gęsto upakowane dodatnie rdzenie atomowe pozbawione elektronów walencyjnych. Odłączone od rdzenia elektrony tworzą tzw. “gaz elektronowy”, czyli zdelokalizowaną chmurę ładunku ujemnego.

Obecność „chmury elektronowej” zapewnia kryształom metalicznym przewodnictwo elektronowe. Z kolei kationowa budowa sieci krystalicznej zapewnia metalom plastyczność, której nie mają kryształy jonowe. Sieć taka charakteryzuje się m.in. dobrą przewodnością cieplną i elektryczną oraz kowalnością (zdolnością do przyjmowania przez metal dowolnych kształtów, co jest wynikiem braku ukierunkowania wiązań metalicznych). Przemieszczanie się kationów w sieci krystalicznej metalu, w wyniku działania siły zewnętrznej, nieznacznie wpływa na oddziaływania między elementami struktury kryształu (kationami) – jądra atomowe w tym typie kryształów przemieszczają się łatwo względem siebie nawzajem.

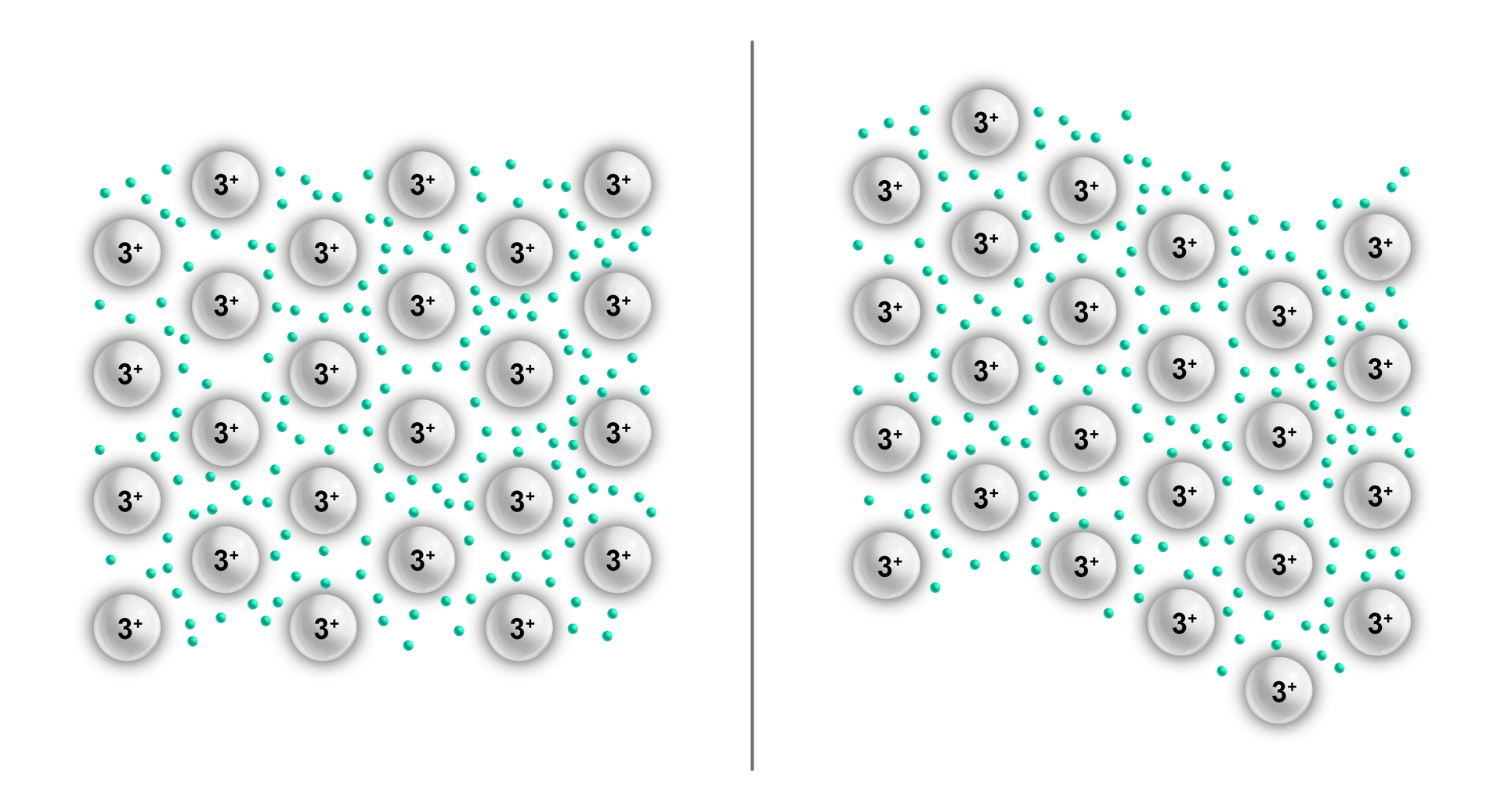
Kryształy metaliczne charakteryzuje:
połysk metaliczny;
dobre przewodnictwo cieplne dzięki zrębom atomowym, które drgając przekazują sobie energię;
dobre przewodnictwo elektryczne;
ciągliwość;
wysokie temperatury topnienia (wyjątek: litowce, gal, ind, rtęć).

Podsumowanie właściwości kryształów
rodzaj właściwości | kowalencyjne (atomowe) | jonowe | metaliczne | molekularne (cząsteczkowe) |
|---|---|---|---|---|
właściwości mechaniczne | duża wytrzymałość, duża twardość | duża wytrzymałość, duża twardość | wytrzymałość różna dla różnych metali, na ogół duża, ciągliwość | mała twardość, mała wytrzymałość |
właściwości termiczne | temperatury topnienia wysokie, mały współczynnik rozszerzalności cieplnej | temperatury topnienia wysokie, mały współczynnik rozszerzalności cieplnej | temperatury topnienia różne, duży współczynnik rozszerzalności cieplnej | temperatury topnienia niskie, duży współczynnik rozszerzalności cieplnej |
przewodnictwo elektryczne | w stanie oczyszczonym nie przewodzą prądu elektrycznego | w stanie stałym źle przewodzą prąd elektryczny, w stanie stopionym i roztworach wodnych wykazują przewodnictwo | przewodniki prądu elektrycznego | nie przewodzą prądu elektrycznego (izolatory) |
Laboratorium
Przeprowadź eksperyment w laboratorium chemicznym. Sformułuj własną hipotezę. W formularzu zanotuj swoje obserwacje, a następnie sformułuj wyniki i wnioski.
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D9XK79LR4
Analiza eksperymentu: Badanie właściwości fizycznych substancji, które tworzą kryształy jonowe, kowalencyjne, molekularne i metaliczne.
Problem badawczy:
Czy kryształy jonowe, kowalencyjne, molekularne i metaliczne rozpuszczają się w wodzie?
Czy kryształy jonowe, kowalencyjne, molekularne i metaliczne rozpuszczają się w rozpuszczalniku organicznym?
Czy kryształy jonowe, kowalencyjne, molekularne i metaliczne charakteryzują się takimi samymi temperaturami topnienia?
Hipoteza: Kryształy jonowe, kowalencyjne, molekularne i metaliczne, charakteryzują się zróżnicowaną rozpuszczalnością w wodzie i w rozpuszczalnikach organicznych oraz różnymi temperaturami topnienia.
Sprzęt laboratoryjny:
zlewki o pojemności – naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych;
cylinder miarowy o pojemności – naczynie laboratoryjne o kształcie otwartego z jednej strony walca, stosowane do odmierzania określonej objętości cieczy;
pręciki szklane (bagietki szklane) – sprzęt laboratoryjny o kształcie prostego pręta szklanego, czasami zakończonego z jednej strony małą rączką, a z drugiej małą łopatką;
łyżki laboratoryjne – długi trzonek wykonany ze szkła, porcelany lub metalu zakończony z jednej strony łyżeczką, służy do nabierania sypkich substancji chemicznych;
kapilara szklana – rurka szklana o bardzo małym przekroju wewnętrznym;
aparatura do wyznaczania temperatury topnienia – automatyczny miernik temperatury topnienia; w celu wykonania pomiaru do urządzenia wprowadzana jest kapilara z badaną próbką, która jest następnie ogrzewana z określoną prędkością, aż do stopienia próbki.
Odczynniki chemiczne: woda destylowana, chloroform, cyna, sacharoza, jod, chlorek sodu, siarczan wapnia‑woda, tlenek krzemu, siarka.
Przebieg eksperymentu:
Część
Niewielką ilość badanej substancji wprowadzić do zlewki, a następnie wlać do niej około wody destylowanej.
Zawartość zlewki wymieszać bagietką.
Powtórzyć punkty i dla pozostałych substancji zamieszczonych w wirtualnym laboratorium.
Część
Niewielką ilość badanej substancji wprowadzić do zlewki, a następnie wlać do niej około chloroformu.
Zawartość zlewki wymieszać bagietką.
Powtórzyć punkty i dla pozostałych substancji zamieszczonych w wirtualnym laboratorium.
Część
Umieścić kapilarę z niewielką ilością badanej substancji w aparaturze do wyznaczania temperatury topnienia.
Ustalić temperaturę topnienia badanej substancji odczytując wskazania aparatury.
Powtórzyć punkty i dla pozostałych substancji zamieszczonych w wirtualnym laboratorium.
Obserwacje:
Część : Sacharoza oraz chlorek sodu tworzą z wodą destylowaną mieszaniny jednorodne. Pozostałe substancje badane w laboratorium (cyna, jod, siarczan wapnia‑woda, tlenek krzemu i siarka, tworzą z wodą destylowaną mieszaniny niejednorodne.
Część : Jod i siarka tworzą z chloroformem mieszaniny jednorodne (jod tworzy z chloroformem fioletowy roztwór). Pozostałe substancje badane w laboratorium (sacharoza, chlorek sodu, cyna, siarczan wapnia‑woda i tlenek krzemu, tworzą z chloroformem mieszaniny niejednorodne.
Część : Każda z wymienionych substancji uległa stopieniu podczas ogrzewania w aparaturze.
Wyniki:
Sacharoza i chlorek sodu rozpuszczają się w wodzie. Jod i siarka rozpuszczają się w chloroformie.
W trakcie pomiarów odnotowano następujące temperatury topnienia:
dla cyny;
dla sacharozy;
dla jodu;
dla chlorku sodu;
dla siarczanu wapnia–woda;
dla tlenku krzemu;
dla siarki.
Wnioski:
W wirtualnym laboratorium badano trzy substancje tworzące kryształy molekularne (sacharoza, jod i siarka), jedną substancję tworzącą kryształy kowalencyjne (tlenek krzemu), dwie substancje tworzące kryształy jonowe (chlorek sodu i siarczan wapnia‑woda oraz jedną substancję tworzącą kryształy metaliczne (cyna).
Wszystkie analizowane substancje, niezależnie od rodzaju tworzonych kryształów, różniły się rozpuszczalnością w wodzie i chloroformie. W wodzie dobrze rozpuszczały się jedynie chlorek sodu (kryształy jonowe) i sacharoza (kryształy molekularne). Z kolei w chloroformie dobrze rozpuszczały się jedynie jod i siarka (kryształy molekularne). Analizowane substancje różniły się również temperaturami topnienia, przy czym najniższymi ich wartościami charakteryzowały się substancje tworzące kryształy molekularne, a najwyższymi te, które tworzyły kryształy jonowe i kowalencyjne.
Postawiona hipoteza została potwierdzona – kryształy jonowe, kowalencyjne, molekularne i metaliczne, charakteryzują się zróżnicowaną rozpuszczalnością w wodzie i w rozpuszczalnikach organicznych oraz różnymi temperaturami topnienia.
Czy wszystkie kryształy rozpuszczają się w benzynie? Przeprowadź eksperyment w laboratorium chemicznym i zweryfikuj własną hipotezę. W formularzu zanotuj swoje obserwacje i wyniki, a następnie sformułuj wnioski.
Szafa laboratoryjna
Badanie rozpuszczalności wybranych związków w benzynie
Czy wszystkie kryształy rozpuszczają się w benzynie? Przeprowadzono eksperyment w laboratorium chemicznym i zweryfikowano hipotezę. W formularzu zanotowano obserwacje i wyniki, a następnie sformułowano wnioski.
Analiza eksperymentu:
Badanie rozpuszczalności kryształów o różnej budowie w rozpuszczalniku niepolarnym – na przykładzie benzyny.
Problem badawczy:
Czy wszystkie typy kryształów rozpuszczają się w rozpuszczalnikach niepolarnych?
Hipoteza:
Fosfor czerwony i grafit rozpuszczają się w rozpuszczalnikach niepolarnych, a chlorek sodu i sacharoza nie ulegają rozpuszczeniu.
Sprzęt laboratoryjny:
cztery zlewki (); bagietka; łyżka laboratoryjna; pipety Pasteura; kolba Erlenmeyera.
Odczynniki chemiczne:
chlorek sodu (sól kuchenna); cukier spożywczy (sacharoza); fosfor czerwony; węgiel (grafit); benzyna.
Przebieg eksperymentu:
Przy pomocy wagi odważono po gramy substancji i wsypano do zlewek, zgodnie z poniższymi punktami:
do zlewki – chlorek sodu;
do zlewki – sacharoza;
do zlewki – fosfor czerwony;
do zlewki – grafit.
Następnie, za pomocą pipet Pasteura, odmierzono po benzyny i wlano do każdej ze zlewek.
Zawartość każdej zlewki wymieszano dokładnie za pomocą bagietki.
Zapisano obserwacje, wyniki i wnioski.
Obserwacje:
Fosfor czerwony bardzo dobrze rozpuścił się w rozpuszczalniku, a grafit tylko w bardzo niewielkim stopniu. Natomiast chlorek sodu i sacharoza nie uległy rozpuszczeniu w ogóle.
Wyniki:
Część kryształów kowalencyjnych uległa rozpuszczeniu w rozpuszczalniku niepolarnym, natomiast kryształy jonowe i molekularne wcale.
Wnioski:
Kryształy o różnej budowie wykazują zróżnicowane zachowanie w rozpuszczalnikach niepolarnych. W rozpuszczalnikach niepolarnych rozpuszczają się fosfor czerwony i w nieznacznym stopniu grafit (kryształy kowalencyjne). Chlorek sodu (kryształy jonowe) oraz sacharoza (kryształy molekularne), jako związki polarne, nie uległy rozpuszczeniu w niepolarnym rozpuszczalniku.
Czy wiesz, jak zachowują się kryształy o różnej budowie pod wpływem ogrzewania? Przeprowadź eksperyment w laboratorium chemicznym – wybierz jeden z przykładowych związków, a następnie przy pomocy łyżeczki laboratoryjnej umieść w tyglu nad palnikiem laboratoryjnym. Zweryfikuj własną hipotezę. w formularzu zanotuj obserwacje i wyniki, a następnie sformułuj wnioski.
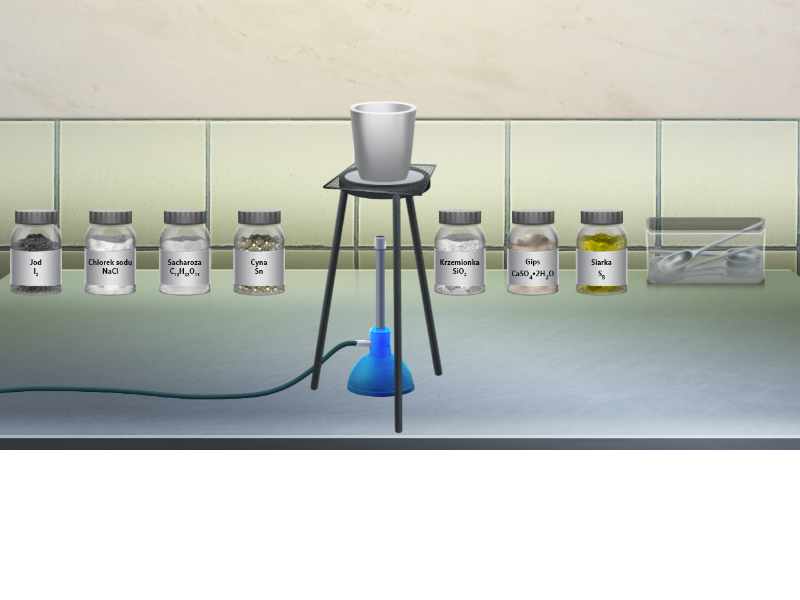
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D9XK79LR4
Czy wiesz, jak zachowują się kryształy o różnej budowie pod wpływem ogrzewania? Zapoznaj się z opisem eksperymentów. Na koniec rozwiąż krótkie zadania.
Analiza eksperymentu:
Jak zachowują się kryształy o różnej budowie pod wpływem ogrzewania
Problem badawczy:
W jaki sposób na wybrane kryształy wpływa ogrzewanie?
Hipoteza:
Kryształy w wyniku ogrzewania ulegają widocznym zmianom fizycznym i/lub fizykochemicznym.
Sprzęt laboratoryjny:
- tygle porcelanowe – sprzęt o kształcie zbliżonym do kubka, który służy do wykonywania operacji na substancjach stałych wymagających stosowania wysokiej temperatury;
- palnik gazowy – rodzaj sprzętu z regulacją płomienia, umożliwiający podgrzewanie substancji chemicznych;
- pierścień do ogrzewania tygli – służy do uchwycenia tygla w celu podgrzania badanych substancji w płomieniu palnika gazowego
- statyw na pierścień; umożliwia stabilizację i utrzymanie pierścienia w odpowiedniej pozycji;
- łapa metalowa – rodzaj regulowanego uchwytu, przy pomocy którego montuje się elementy aparatury;
- łyżeczki – długi trzonek wykonany ze szkła, porcelany lub metalu zakończony z jednej strony łyżeczką. Służy do nabierania sypkich substancji chemicznych.
Odczynniki chemiczne:
- kryształy jodu;
- chlorek sodu;
- sacharoza;
- cyna;
- hydrat siarczanu miedzi;
- gips krystaliczny;
- siarka.
Przebieg eksperymentu:
1. Do porcelanowego tygla nasypano kolejno każdy z badanych odczynników.
2. Umieszczono tygiel nad płomieniem palnika w celu ogrzania.
3. Obserwowano zachodzące zmiany.
Obserwacje:
- Jod, pod wpływem ogrzewania w tyglu nad płomieniem palnika, tworzy fioletowe pary.
- Chlorek sodu – pod wpływem ogrzewania w tyglu, nad płomieniem palnika następuje topnienie (min. ).
- Sacharoza – pod wpływem ogrzewania w tyglu, nad płomieniem palnika topi się wraz ze zmianą barwy z białej na pomarańczową, a następnie ciemnobrązową.
- Cyna – pod wpływem ogrzewania w tyglu, nad płomieniem palnika topi się (min. ).
- Krzemionka – pod wpływem ogrzewania w tyglu, nad płomieniem palnika szary proszek zmienia kolor na jaśniejszy, pojawiają się kropelki bezbarwnej cieczy na ściankach.
- Gips – pod wpływem ogrzewania w tyglu, nad płomieniem palnika kryształki rozpadają się, na ściankach tygla osadzają się kropelki bezbarwnej cieczy.
- Siarka – pod wpływem ogrzewania w tyglu, nad płomieniem palnika topi się i staje się ruchliwą, żółtą cieczą.
Wyniki:
Kryształy ulegają stopieniu w różnych temperaturach, w zależności od ich rodzaju.
Wnioski:
Nie wszystkie kryształy łatwo ulegają topieniu, niektóre z nich wymagają odpowiednio wysokiej temperatury lub od razu zaczynają sublimować.