Budowa kryształów metalicznych
Czym są kryształy metaliczne?
Kryształy metaliczne zbudowane są z kationów metali, a elektronyelektrony powłoki walencyjnej tworzą tzw. gaz elektronowygaz elektronowy (elektrony te są nazywane także elektronami swobodnymi). Strukturę krystaliczną metali można porównać do boi unoszących się na morzu, symbolizujących kationykationy metali, natomiast woda między nimi tworzy gaz elektronowy, w którym elektrony mogą się swobodnie przemieszczać. Dzięki tej właściwości metale są dobrymi przewodnikamiprzewodnikami prądu elektrycznego.

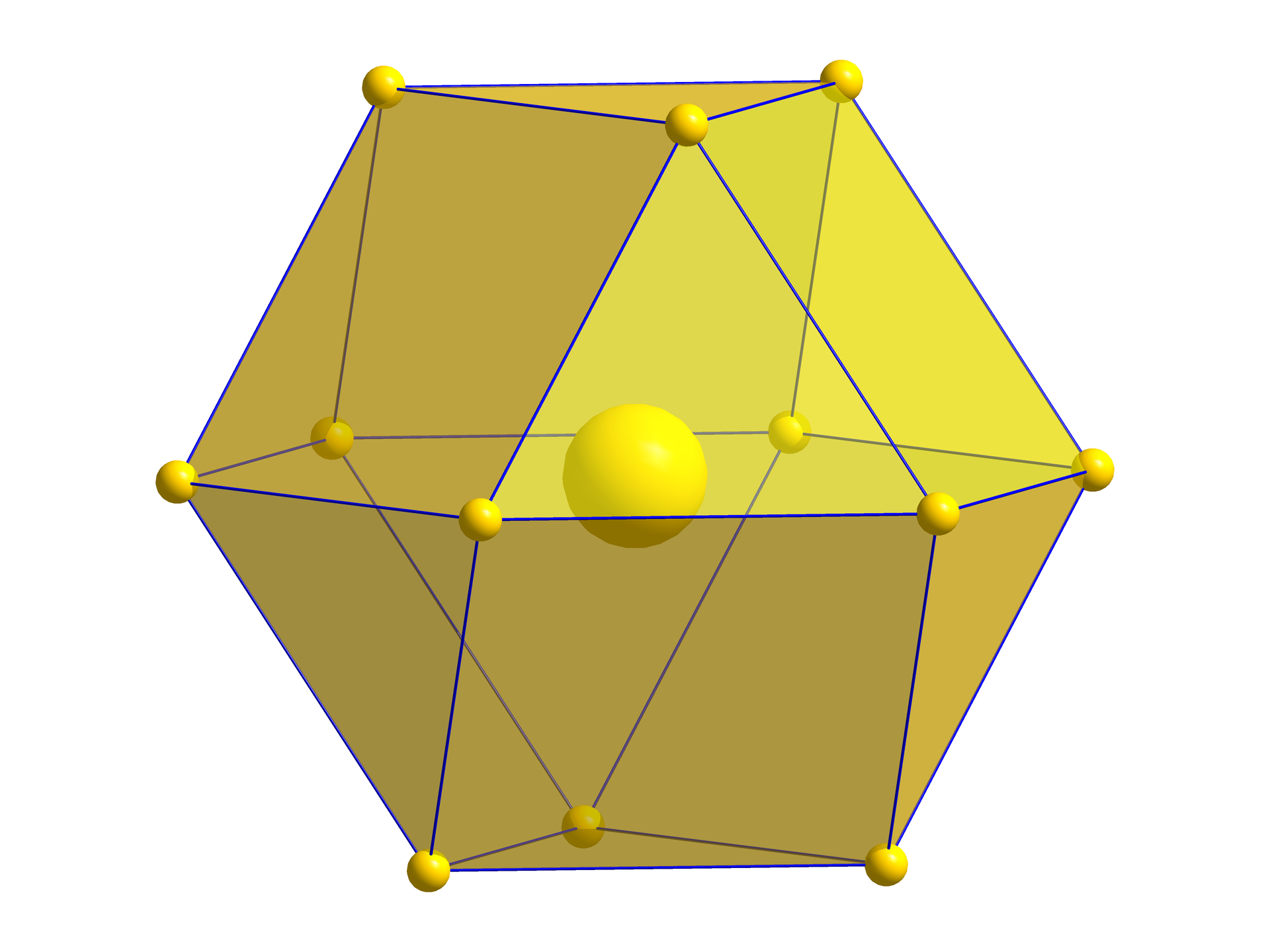
W sieci krystalicznej metali możemy przyjąć, że jony mają kształt kuli. Kule te tworzą strukturę najgęstszego ułożenia atomów, tzw. strukturę zwartą. Są one umieszczone w węzłach sieci, co obrazowo można porównać do ułożenia owoców na półkach w sklepie. Kationy metali ułożone są tak, aby pozostało między nimi jak najmniej „pustego” miejsca, zaś zdelokalizowane elektronyzdelokalizowane elektrony mogą poruszać się w obrębie całego kryształu.

Jakie wyróżniamy typy struktur zwartych?
Czy wiesz, czym różni się budowa heksagonalnie zwarta od regularnie zwartej i jakie kryształy ją posiadają? Zapoznaj się z animacjami i rozwiąż poniższe zadania.

Film dostępny pod adresem /preview/resource/ROSuronNRY9Gt
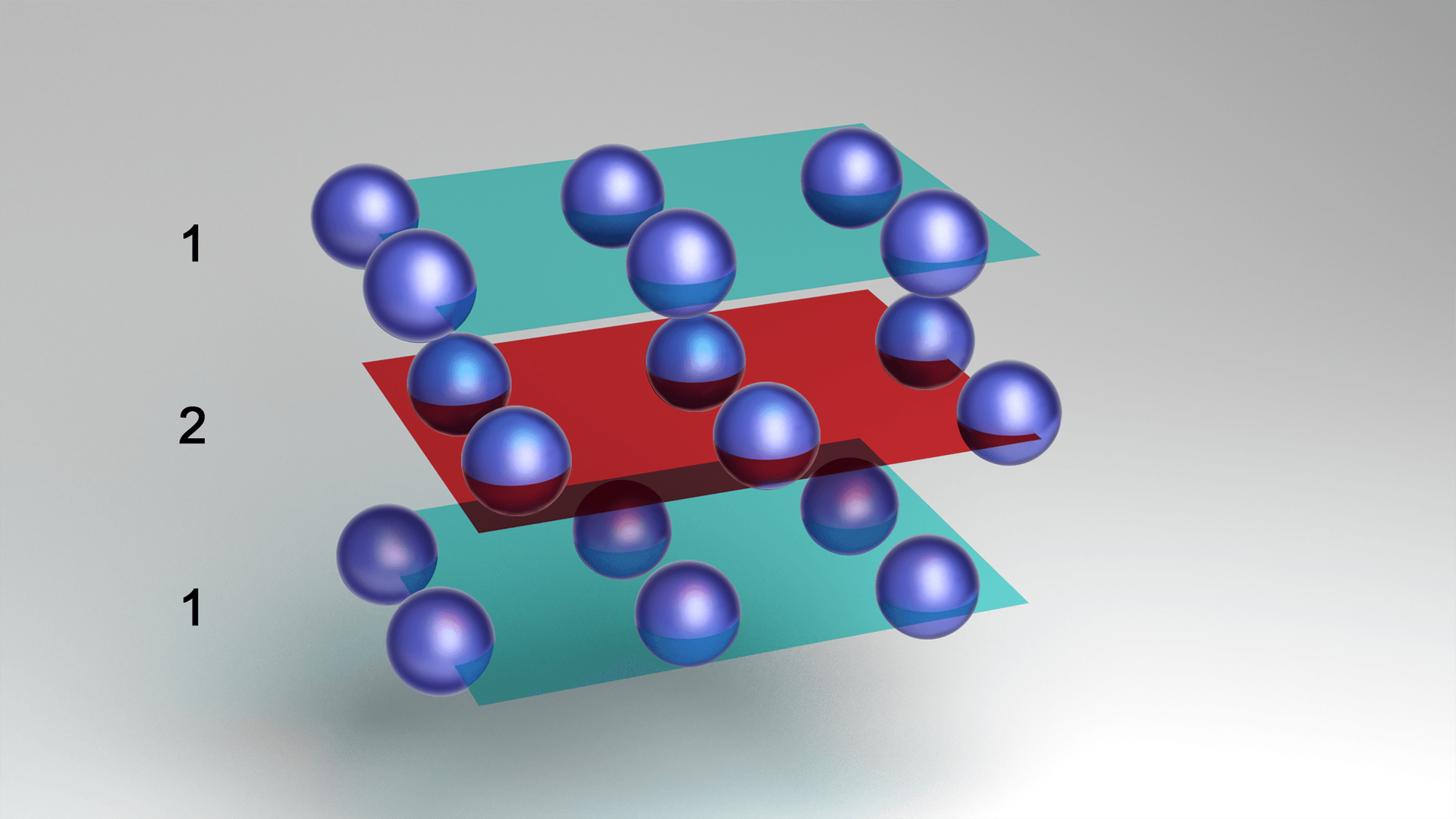
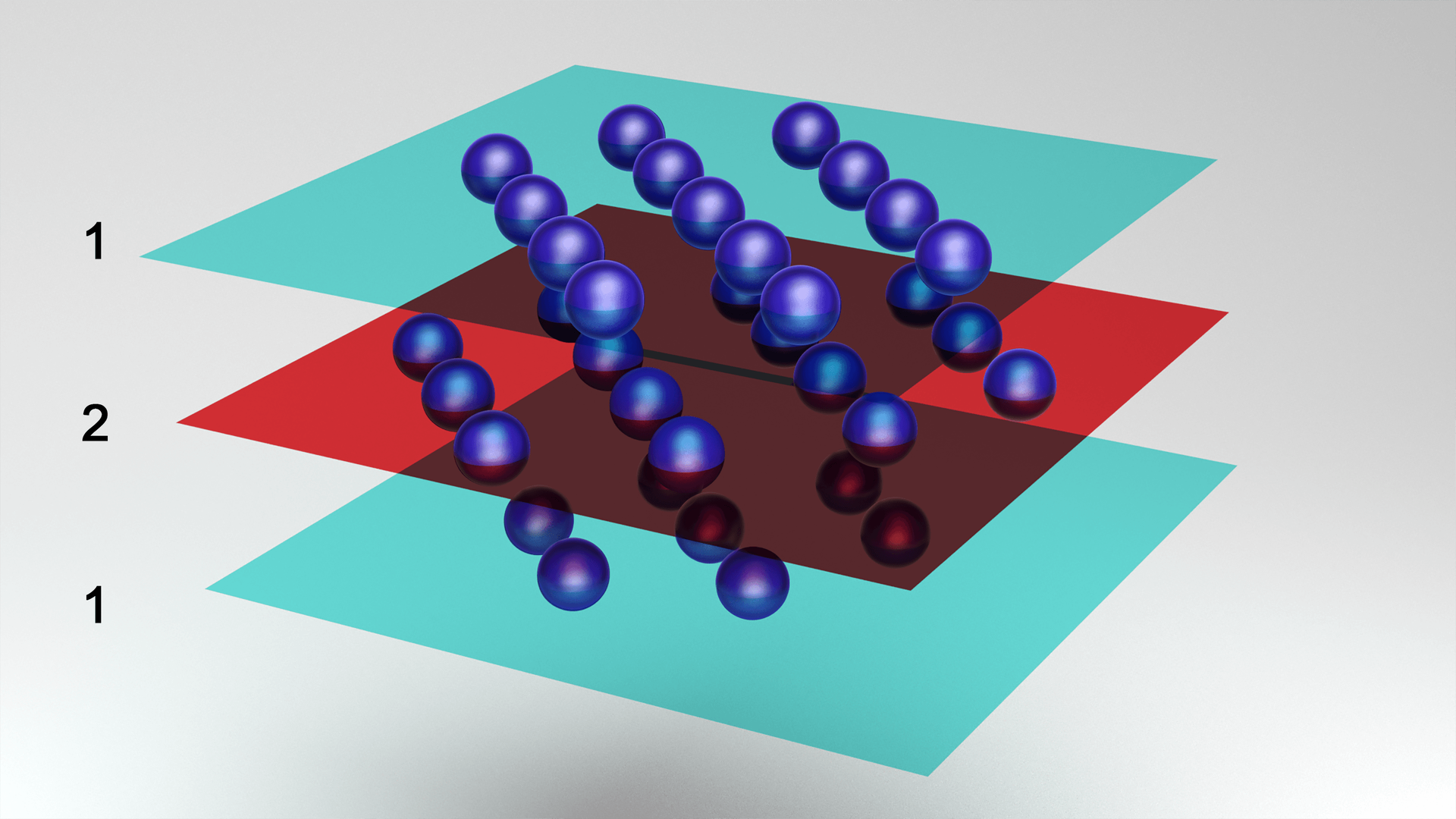
Animacja przedstawia przykład budowy heksagonalnie zwartej. Przykłady: beryl, cynk, magnez. Animacja przedstawia spadające z góry kulki, które tworzą figurę geometryczną. Podstawę figury tworzy sześć układających się w koło kul, na nie spadają trzy kulki, układające się obok siebie, zwieńczenie figury stanowi jedna kulka. Powstaje stożek zbudowany z kulek. Do takiej figury zostaje podłączony zasilacz i żarówka. Żarówka świeci.

Film dostępny pod adresem /preview/resource/RanXbqbApIuze
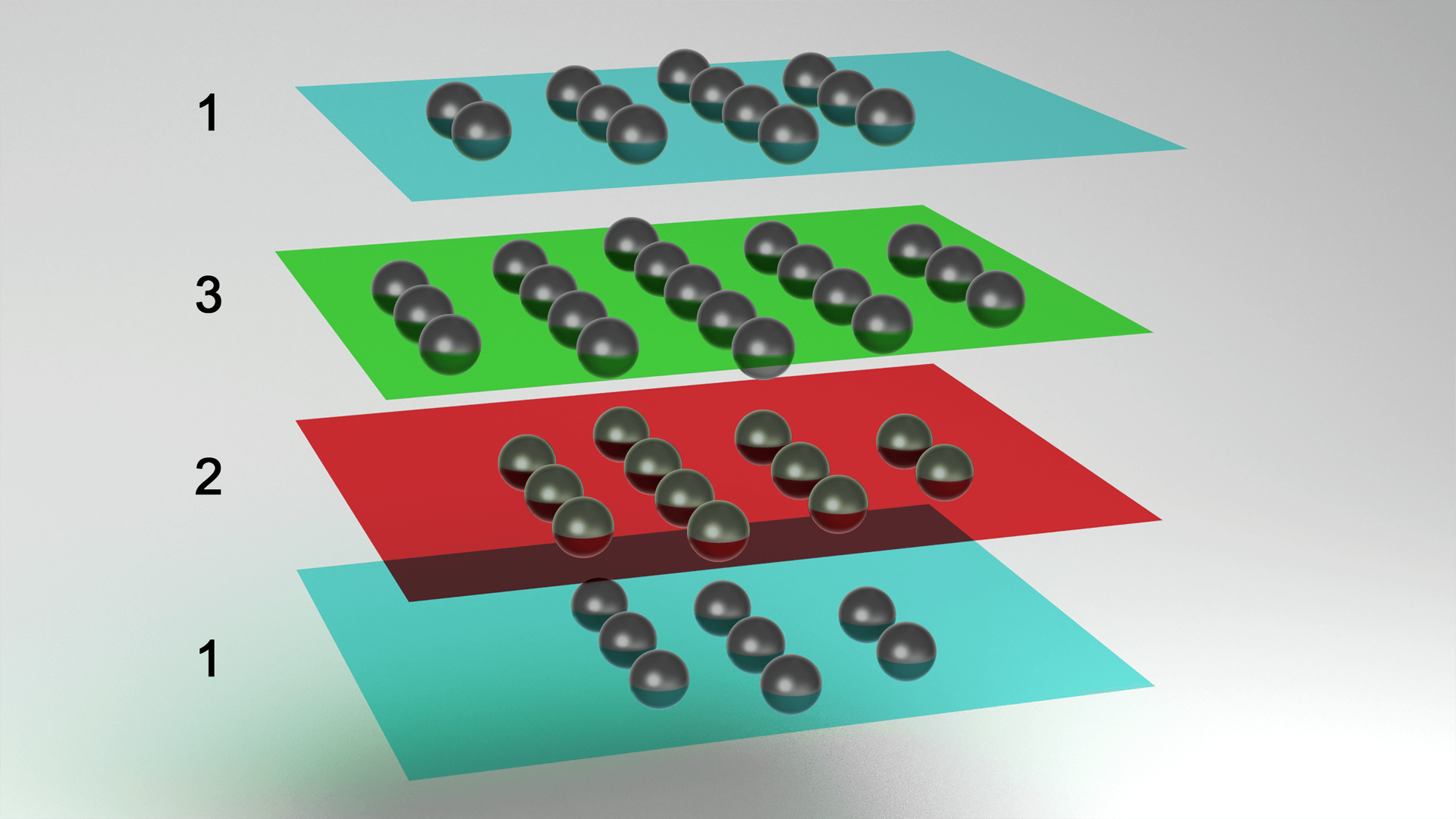
Animacja przedstawia przykład budowy regularnie zwartej. Przykłady: srebro, miedź, złoto. Animacja przedstawia spadające z góry kulki, tworzą one figurę geometryczną. Tworzą one podstawę, którą jest kwadrat. Na nią spadają cztery kulki, zwieńczenie figury stanowi jedna kulka. Powstaje ostrosłup czworokątny zbudowany z kulek. Do takiej figury zostaje podłączony zasilacz i żarówka. Żarówka świeci.
By określić zwartość struktur metalicznych, należy obliczyć ułamek f przestrzeni zajętej przez atomy. Im ten współczynnik jest większy, tym kryształ jest bardziej upakowany. Dzięki wyprowadzeniu zależności, między promieniem jonu r metalu a parametrem a komórki elementarnej, możemy określić, do jakiego typu upakowania należy metal. Wynoszą one odpowiednio:
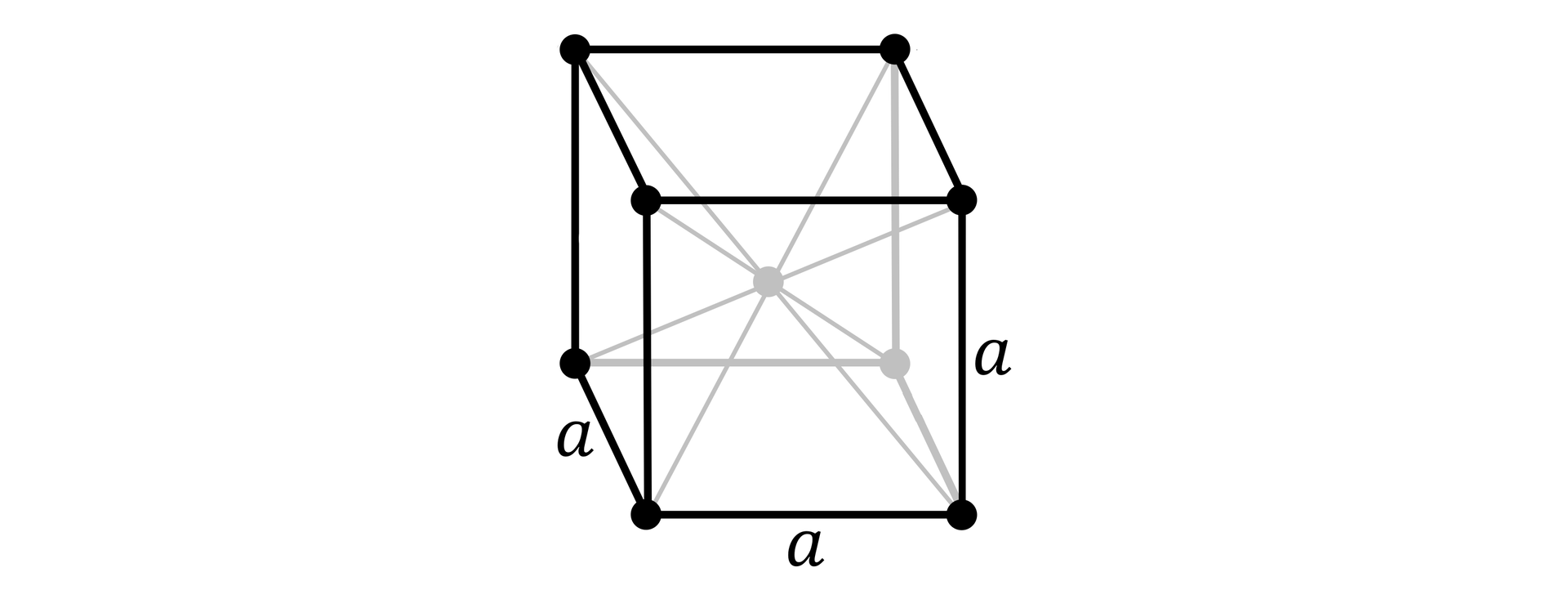
Struktura hcp | |
|---|---|
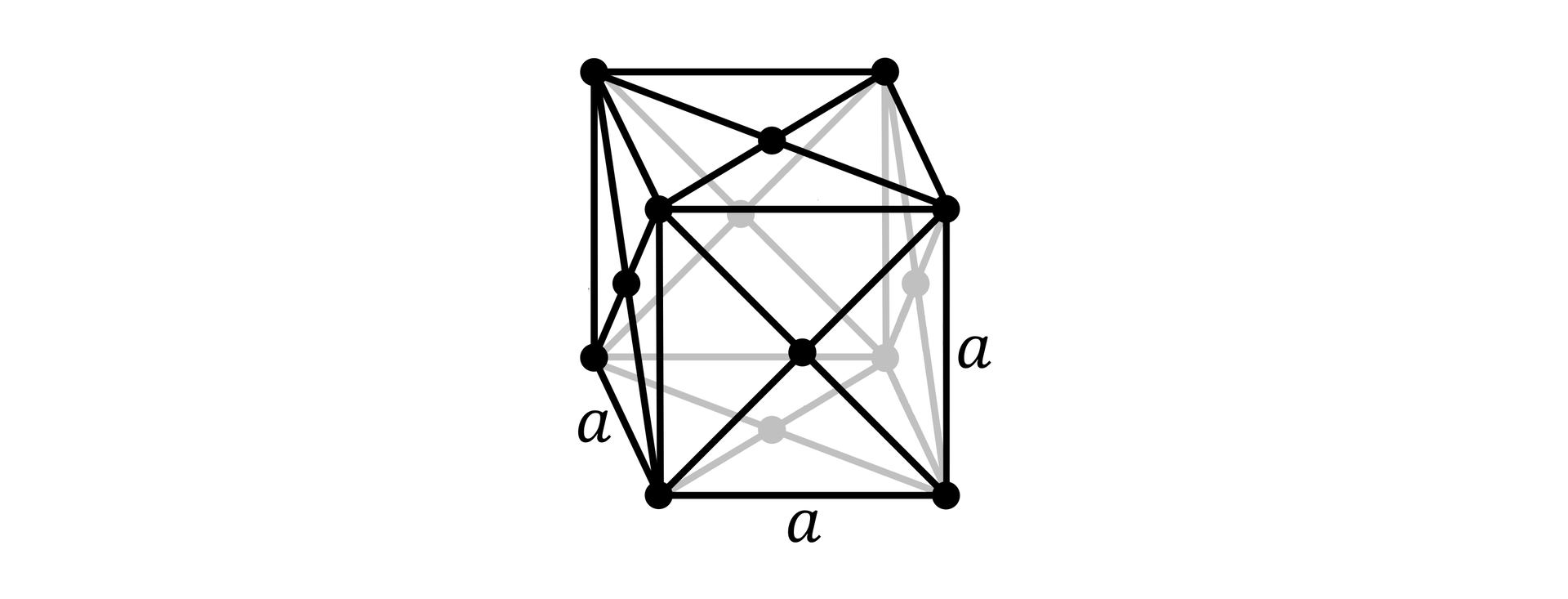
Struktura fcc | |
Struktura bcc |
Promień jonowy platyny () wynosi 1,39 Å. Platyna krystalizuje w układzie regularnym, w typie komórki elementarnej F, w której długość krawędzi a = 3,923 Å.
Zdecyduj, do jakiego typu upakowania, hcp, fcc czy bbc, należy platyna. Odpowiedź potwierdź odpowiednimi obliczeniami.
Przeanalizuj jeszcze raz informacje zawarte wyżej i sporządź mapę pojęciową, która podsumuje budowę kryształów metalicznych.