Podsumowanie
Podstawowymi elementami, z których składa się materia, są atomy. Większość z nich dąży do łączenia się z innymi atomami za pomocą wiązań chemicznych. W zależności od rodzaju tworzonego wiązania, substancje, które z nich powstają, mogą mieć różną budowę i właściwości.
Jak dobrze znasz budowę atomu? Czy potrafisz odczytywać odpowiednie informacje z układu okresowego? Czy potrafisz określać typ wiązań chemicznych w analizowanych związkach? Pracując z tym materiałem, przypomnij sobie zagadnienia dotyczące wewnętrznej budowy substancji, a następnie sprawdź swoją wiedzę, rozwiązując test.
Spróbuj swoimi słowami odpowiedzieć na postawione poniżej pytania. Dane zagadnienie możesz wytłumaczyć swojemu koledze lub koleżance. Następnie rozwiń każdy z kafelków i zweryfikuj poprawność swojej odpowiedzi.
Jak zbudowany jest atom?
W centrum atomu znajduje się dodatnio naładowane jądro atomowe, wokół którego poruszają się ujemnie naładowane cząstki – elektrony. Te poruszające się wokół jądra atomowego tworzą tak zwaną chmurę elektronową.
Jądro atomowe jest zbudowane z protonów (cząstek o ładunku dodatnim) i neutronów (cząstek elektrycznie obojętnych).
Atom jest elektrycznie obojętny. Dlatego liczba elektronów w atomie danego pierwiastka chemicznego jest równa liczbie protonów.
Atomy, które należą do tego samego pierwiastka chemicznego, mają jednakową liczbę elektronów i protonów.

Jak opisujemy atomy?
Do opisu atomów wykorzystujemy liczbę atomową, zwaną również liczbą porządkową (), i liczbę masową ().
Atom opisujemy symbolicznie, stosując zaprezentowaną poniżej notację.

Jak są rozmieszczone elektrony w atomie?
Każdy z elektronów porusza się w odpowiednim obszarze wokół jądra atomowego. Odległość elektronów od jądra atomowego wiąże się z ich energią. Na ogół, im dalej od jądra atomowego znajduje się elektron, tym ma większą energię.
W obrębie chmury elektronowej możemy wskazać zbiory elektronów o zbliżonych energiach. Jednym z ich rodzajów są powłoki elektronowe. Numerujemy je cyframi od do oraz oznaczamy symbolami literowymi (kolejno: , , , , , oraz ).
Umowne rozmieszczenie elektronów w atomie, w obrębie powłok (a także podpowłok elektronowych i orbitali atomowych) to tak zwana konfiguracja elektronowa.
W celu zapisania konfiguracji elektronowej atomu danego pierwiastka chemicznego, musimy ustalić liczbę zawartych w nim elektronów. Następnie elektrony te musimy rozmieścić w obrębie powłok elektronowych (opcjonalnie – podpowłok elektronowych i orbitali atomowych), zgodnie ze wzrastającą energią.
Przykłady:
Konfiguracja elektronowa atomu fosforu – zapis pełny powłokowy:
Konfiguracja elektronowa atomu wapnia – zapis pełny powłokowy:
Elektrony w obrębie powłok elektronowych możemy podzielić ze względu na energię na jeszcze mniejsze zbiory – na tak zwane podpowłoki elektronowe. Liczba podpowłok elektronowych, jakie możemy wyznaczyć w obrębie danej powłoki elektronowej, równa jest numerowi tej powłoki.

W obrębie podpowłok elektronowych można wyznaczyć jeszcze mniejsze zbiory elektronów (o dużo bardziej zbliżonych energiach niż w obrębie podpowłok), które nazywamy orbitalami. W obrębie jednego orbitalu mogą poruszać się maks. dwa elektrony.
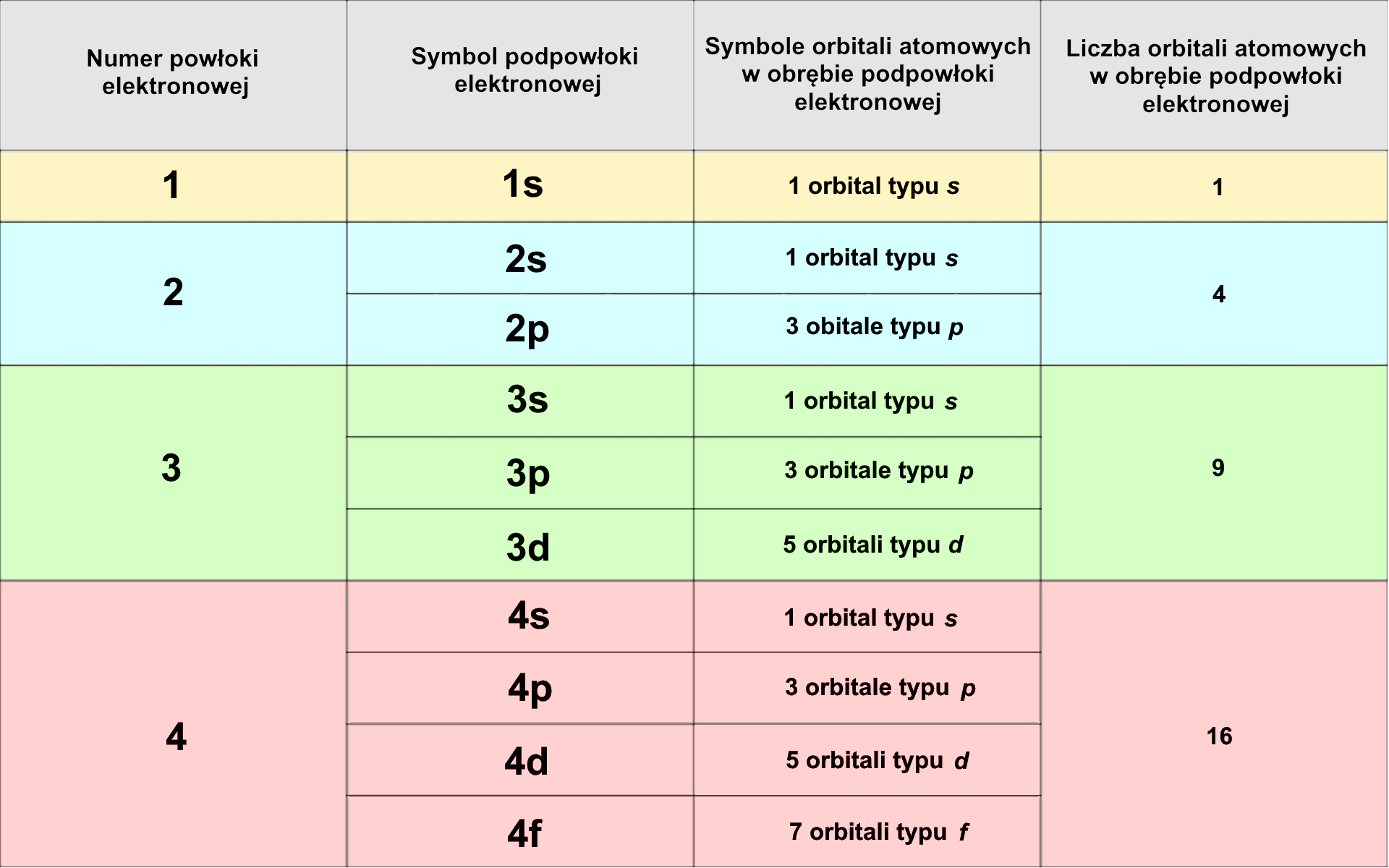
Konfiguracja elektronowa atomu fosforu – zapis pełny podpowłokowy:
Konfiguracja elektronowa atomu wapnia – zapis pełny podpowłokowy:
Co to są elektrony walencyjne? Czy są zawsze elektronami ostatniej powłoki elektronowej?
Elektrony walencyjne to te z elektronów w atomie danego pierwiastka chemicznego, które poruszają się najdalej od jądra atomowego (mają najwyższe wartości energii).
Elektrony walencyjne atomów poszczególnych pierwiastków chemicznych biorą udział w tworzeniu się wiązań i decydują o właściwościach chemicznych pierwiastka.
W poniższej tabeli zamieszczono konfiguracje elektronowe atomów wybranych pierwiastków chemicznych, na których (kolorem czerwonym) wyszczególniono elektrony walencyjne każdego z atomów.
Symbol atomu | Konfiguracja elektronowa zapis powłokowy | Konfiguracja elektronowa zapis podpowłokowy* | Liczba elektronów walencyjnych |
|---|---|---|---|
Indeks górny Konfiguracja elektronowa atomów wybranych pierwiastków chemicznych, ze wskazaniem elektronów walencyjnych
*Gwiazdką wyznaczono formę zapis konfiguracji elektronowej dla osób zainteresowanych. Indeks górny koniecKonfiguracja elektronowa atomów wybranych pierwiastków chemicznych, ze wskazaniem elektronów walencyjnych
*Gwiazdką wyznaczono formę zapis konfiguracji elektronowej dla osób zainteresowanych.
Zwróć uwagę, że w atomach zamieszczonych w powyższej tabeli pierwiastków chemicznych, elektrony walencyjne zajmują ostatnią (najbardziej oddaloną od jądra atomowego) powłokę elektronową.
Opisana sytuacja ma miejsce w atomach pierwiastków chemicznych, które należą do grup pierwszej, drugiej i od do układu okresowego. W atomach tych pierwiastków elektrony walencyjne poruszają się w obrębie jednej powłoki elektronowej – położonej najdalej od jądra atomowego.
W przypadku atomów pierwiastków należących do grup od trzeciej do układu okresowego, elektrony walencyjne należą do dwóch różnych powłok elektronowych. Nadal są to jednak elektrony, które poruszają się najdalej od jądra atomowego.
Co to są izotopy?
Izotopy to atomy tego samego pierwiastka chemicznego, które mają jednakowy ładunek jądra atomowego (identyczną liczbę protonów) oraz taką samą liczbę poruszających się wokół jądra elektronów, a różnią się liczbą neutronów w jądrze atomowym.
Uogólniając, możemy powiedzieć, że izotopy mają taką samą wartość liczby atomowej, ale różnią się wartościami liczb masowych.
Na poniższej grafice przedstawiono uproszczone modele budowy atomów wybranych izotopów wodoru.
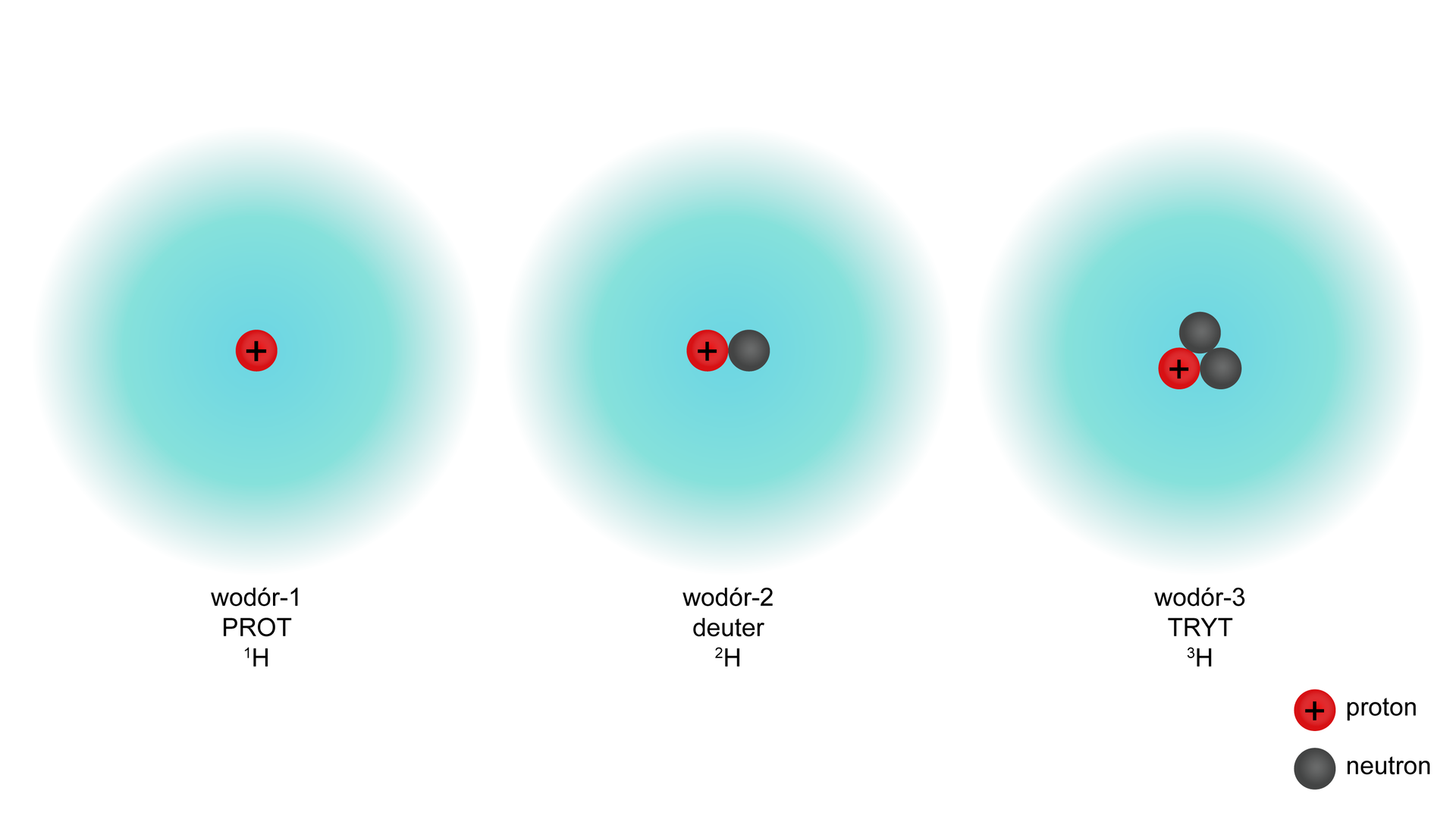
W jakich dziedzinach życia wykorzystujemy izotopy nietrwałe?
Wybrane przykłady zastosowań nietrwałych izotopów omówiono na poniższej grafice interaktywnej. Zapoznaj się z nimi, klikając w odpowiednie cyfry.
W jakich jednostkach wyrażamy masę indywiduów chemicznych?
Atomowa jednostka masy, nazywana inaczej jednostką masy atomowej lub potocznie unitem, jest jednostką masy, używaną do wyrażania mas indywiduów chemicznych (między innymi atomów, jonów, cząsteczek oraz cząstek, które je budują). Jednostka masy atomowej oznaczana jest w skrócie literą “u” (z ang. unit to „jednostka”).
Przy obliczaniu średnich mas atomowych pierwiastków, bierze się pod uwagę skład izotopowy, a konkretnie masy i zawartości procentowe (tak zwane abundancje) poszczególnych izotopów, wchodzących w skład naturalnie istniejącego pierwiastka chemicznego.
Do obliczenia średniej masy atomowej pierwiastka, można wykorzystać wzór:
gdzie:
, , …, – masy poszczególnych izotopów pierwiastka [u];
, , …, – zawartości procentowe poszczególnych izotopów pierwiastka .
Średnie masy atomowe pierwiastków są często zamieszczane w układzie okresowym pierwiastków.
Co to jest układ okresowy pierwiastków?
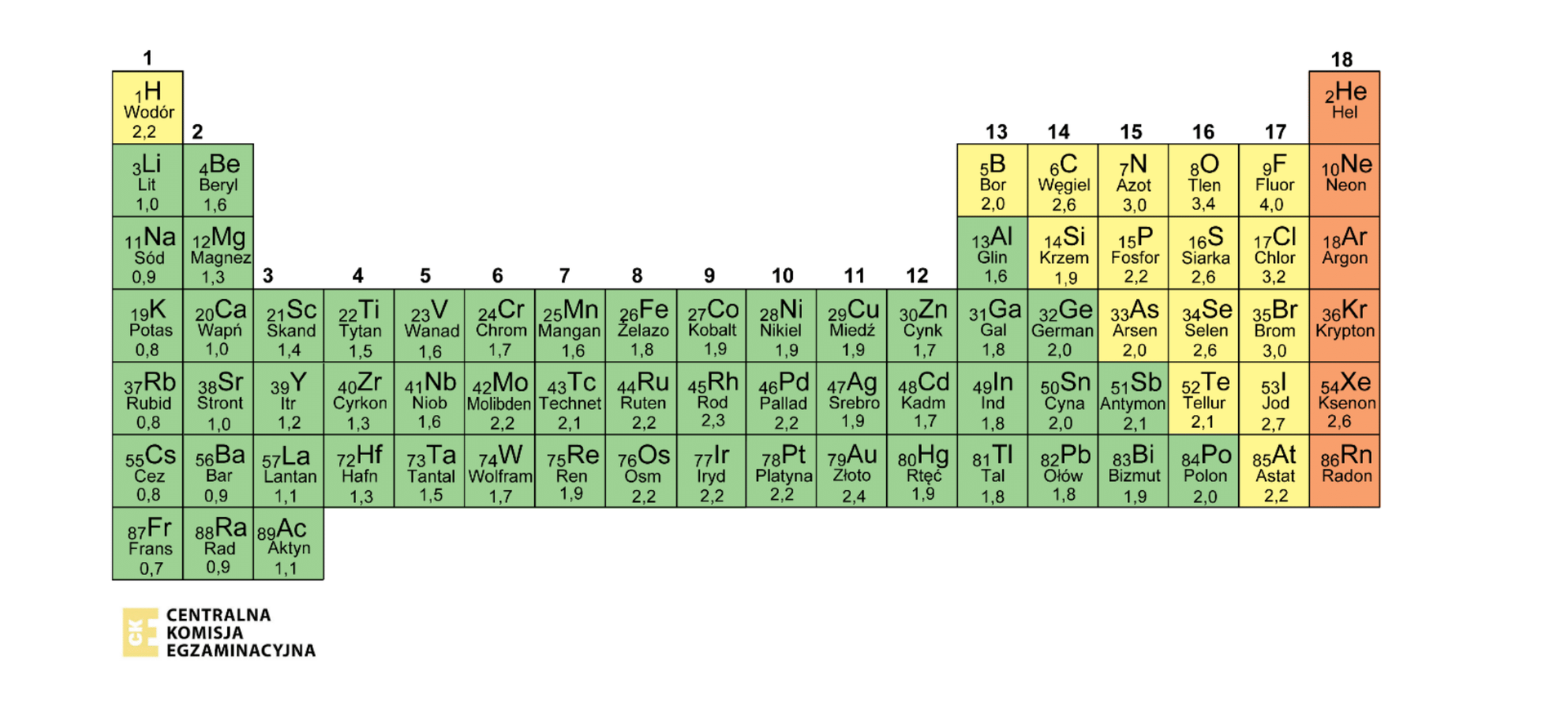
Układ okresowy pierwiastków to zestawienie w tabeli wszystkich pierwiastków chemicznych, uporządkowanych wg rosnącej liczby atomowej. Pionowe kolumny w układzie okresowym określa się mianem grup, a poziome wiersze – okresów. Grupy i okresy są ponumerowane.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DD45RRTDU
Pierwiastki chemiczne, położone głównie w lewej i centralnej części układu okresowego (oprócz wodoru), są metalami, z kolei po prawej stronie znajdują się niemetale.

Pierwiastki chemiczne, które należą do jednej grupy, mają podobne właściwości. Przykładowo – mogą tworzyć podobne typy związków chemicznych z innymi pierwiastkami, a także wykazywać podobne zachowanie wobec tych samych substancji chemicznych (np. wobec wody). Wyjątkiem jest wodór. Chociaż jest położony w grupie metali, to w rzeczywistości jest niemetalem i posiada odmienne właściwości od pozostałych pierwiastków chemicznych z pierwszej grupy układu okresowego.
W okresach układu okresowego następuje na ogół zmiana aktywności pierwiastków chemicznych od aktywnych metali (pierwsza i druga grupa) poprzez mniej aktywne metale i aktywne niemetale do biernych chemicznie helowców (gazów szlachetnych). Opisana zależność jest dobrze widoczna podczas analizy właściwości pierwiastków grup pierwszej i drugiej oraz od do układu okresowego.
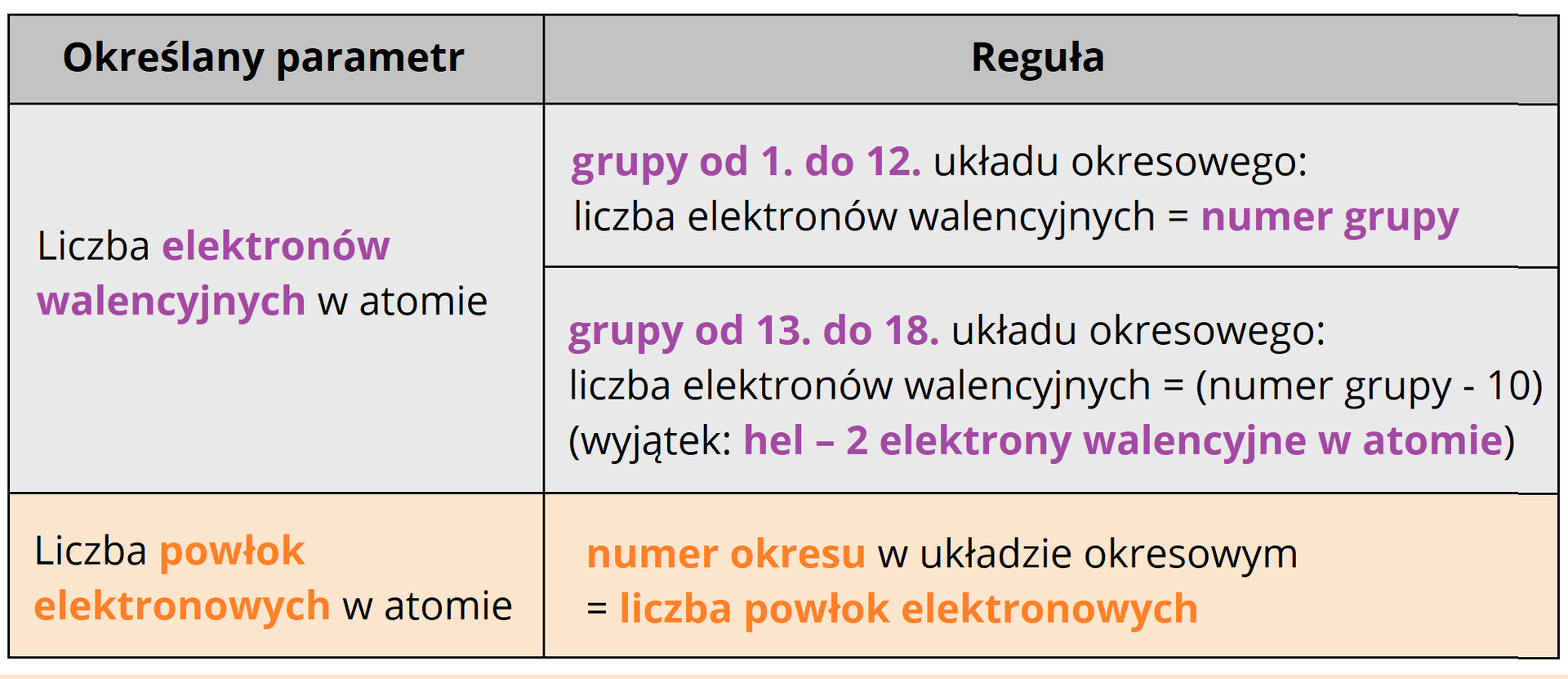
Jaka jest zależność pomiędzy budową atomu a położeniem pierwiastka chemicznego w układzie okresowym?
Budowę atomu można powiązać z jego położeniem w układzie okresowym. Numer okresu informuje bowiem o tym, z ilu powłok elektronowych składa się atom analizowanego pierwiastka, a numery grup pomagają określić liczbę elektronów walencyjnych w atomach poszczególnych pierwiastków chemicznych.
Co to jest wiązanie kowalencyjne (niespolaryzowane)?
Wiązanie kowalencyjne (niespolaryzowane, nazywane czasem wiązaniem atomowym) polega na uwspólnianiu elektronów walencyjnych przez łączące się atomy. Utworzone pary elektronowe, w przypadku wiązania kowalencyjnego (niespolaryzowanego), należą w jednakowym stopniu do obu połączonych atomów. Innymi słowy, uwspólnione elektrony są z taką samą siłą przyciągane przez obydwa atomy, które tworzą wiązanie kowalencyjne (niespolaryzowane).
Wiązania kowalencyjne (niespolaryzowane) występują między atomami pierwiastków chemicznych o zbliżonych wartościach elektroujemności (różnica elektroujemności powinna zawierać się w przedziale od do ). Najczęściej występują więc między atomami tego samego pierwiastka chemicznego (w tak zwanych cząsteczkach homoatomowych).
Atomy mogą łączyć się ze sobą za pomocą wiązań pojedynczych (jedna wiążąca para elektronowa), podwójnych (dwie wiążące pary elektronowe) oraz potrójnych (trzy wiążące pary elektronowe).
Aby „pokazać” wiązania chemiczne w analizowanych drobinach (np. cząsteczkach), rysuje się ich wzory elektronowe. Należy uwzględnić wszystkie elektrony walencyjne każdego z atomów występujących w rozpatrywanej drobinie. W poniższej tabeli zamieszczono wzory elektronowe wybranych cząsteczek, w których występuje wiązanie kowalencyjne (niespolaryzowane).

Co to jest wiązanie kowalencyjne spolaryzowane?
Wiązanie kowalencyjne spolaryzowane jest tworzone pomiędzy atomami, należącymi do różnych niemetali, które w większym stopniu różnią się wartościami elektroujemności (różnica elektroujemności powinna zawierać się w przedziale od do ).
Wiązanie kowalencyjne spolaryzowane polega na uwspólnieniu elektronów walencyjnych przez atomy odpowiednich pierwiastków chemicznych, przy czym wiążąca para elektronowa (bądź pary elektronowe) przesunięta jest w kierunku atomu pierwiastka o większej elektroujemności. Pierwiastek chemiczny, który charakteryzuje się większą wartością elektroujemności, ma bowiem większą zdolność przyciągania elektronów.
W poniższej tabeli zamieszczono wzory elektronowe wybranych cząsteczek, w których występuje wiązanie kowalencyjne spolaryzowane.

Przesunięcie uwspólnionych elektronów w kierunku atomu pierwiastka o większej elektroujemności, często zaznacza się na wzorze elektronowym kreskowym za pomocą umieszczonej na środku odpowiedniego wiązania strzałki. Jej zwrot powinien być skierowany w kierunku symbolu pierwiastka o większej wartości elektroujemności.

Co to jest wiązanie jonowe?
Wiązanie jonowe to elektrostatyczne przyciąganie się jonów o przeciwnych znakach – kationów i anionów. Tworzy się je najczęściej pomiędzy atomem metalu i niemetalu. Atom metalu, w czasie tworzenia wiązania, oddaje elektron bądź elektrony walencyjne i przekształca się w kation. Atom niemetalu, w czasie tworzenia wiązania, przyjmuje elektron bądź elektrony walencyjne od atomu metalu i przekształca się w anion.

Związki chemiczne o budowie jonowej nie tworzą cząsteczek, ale kryształy, zbudowane z naprzemiennie ułożonych jonów – kationów i anionów.

Czym różnią się substancje o budowie jonowej od substancji o budowie kowalencyjnej?
W poniższej tabeli opisano wybrane różnice w budowie i właściwościach substancji o budowie jonowej i kowalencyjnej.
Właściwość | Związki o budowie jonowej | Związki o budowie kowalencyjnej |
|---|---|---|
budowa | kryształy, w których występują naprzemiennie ułożone jony (kationy i aniony) | cząsteczki |
wzór sumaryczny | przedstawia najmniejszy wzór powtarzających się kationów i anionów w krysztale | odzwierciedla skład cząsteczki |
stan skupienia w temperaturze pokojowej | ciała stałe | ciała stałe, ciecze, gazy |
temperatury topnienia i wrzenia | w większości przypadków wysokie | w większości przypadków niskie |
przewodnictwo elektryczne | stopione oraz w roztworach wodnych przewodzą prąd elektryczny | większość nie przewodzi prądu elektrycznego |
Indeks górny Porównanie budowy i wybranych właściwości fizycznych substancji o budowie jonowej i kowalencyjnej Indeks górny koniecPorównanie budowy i wybranych właściwości fizycznych substancji o budowie jonowej i kowalencyjnej
Do czego służą indeks i współczynnik stechiometryczny
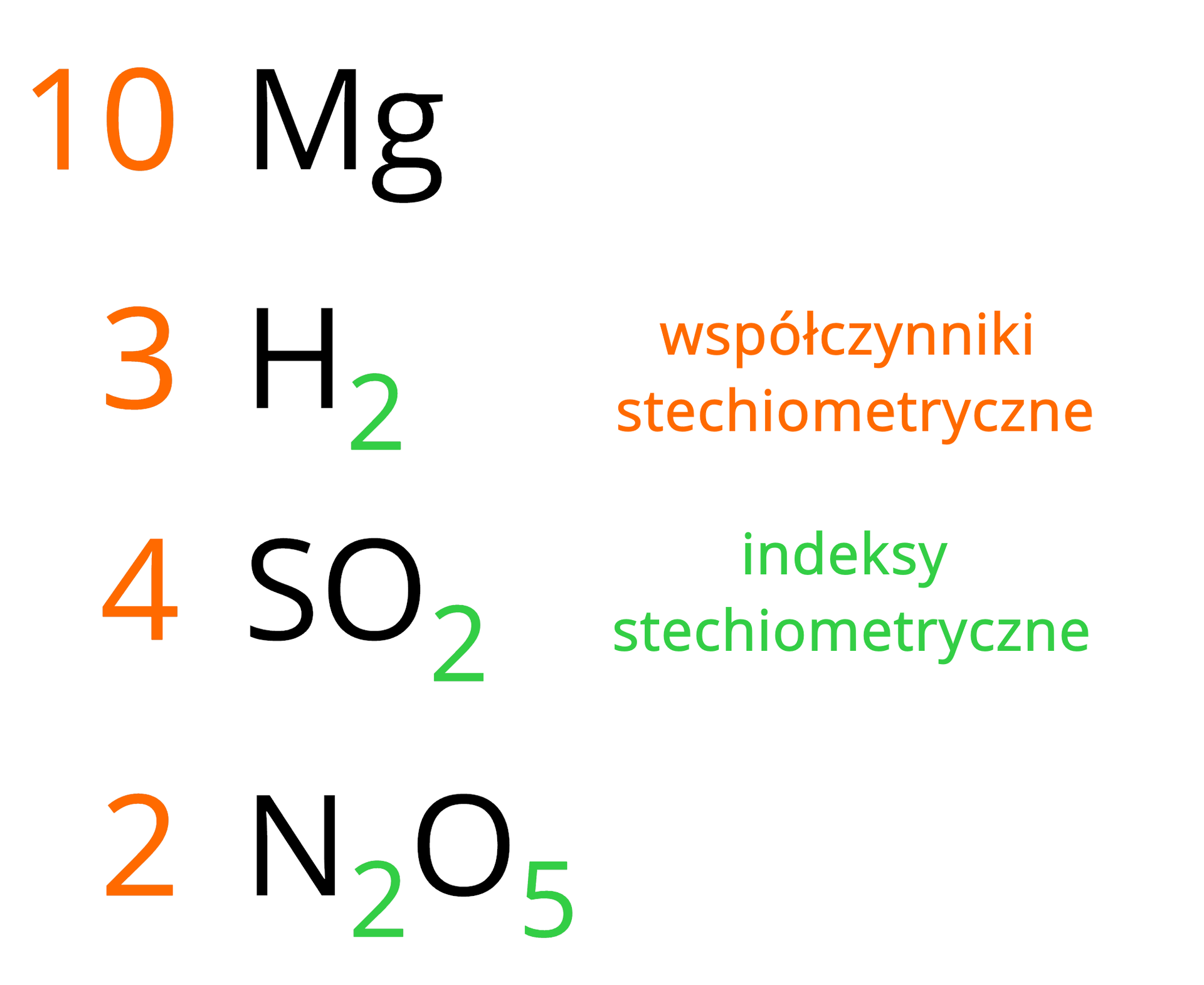
Liczbę atomów pierwiastka w cząsteczce lub w najmniejszym zbiorze powtarzających się jonów (w związku o budowie jonowej) przedstawia się za pomocą indeksu stechiometrycznego. Indeks stechiometryczny to liczba, którą umieszcza się na dole, z prawej strony symbolu pierwiastka we wzorze chemicznym substancji.
Liczbę indywiduów chemicznych (między innymi pojedynczych atomów, cząsteczek, jonów lub najmniejszych zbiorów powtarzających się jonów) opisuje się za pomocą współczynnika stechiometrycznego. Współczynnik stechiometryczny to liczba umieszczana przed symbolem lub wzorem chemicznym.
Co to jest wartościowość?
Wartościowość pierwiastka w związkach chemicznych o budowie kowalencyjnej jest równa liczbie wiązań, które tworzą w cząsteczkach jego atomu z innymi atomami. W związkach o budowie jonowej, wartościowość pierwiastka chemicznego jest liczbowo równa ładunkowi jego jonu w analizowanym związku, z pominięciem znaku ujemnego bądź dodatniego (w zależności od jonu).
Wykorzystując układ okresowy, możemy określić maks. wartościowość niektórych pierwiastków chemicznych w związkach z wodorem oraz z tlenem.
Numer grupy | |||||||
Maksymalna wartościowość pierwiastków względem wodoru |
Numer grupy | |||||||
Maksymalna wartościowość pierwiastków względem tlenu |