Sprawdź, czego się nauczyłeś
Wykonaj poniższe ćwiczenia i zweryfikuj swoją wiedzę. Jeżeli odpowiedzi na któreś pytania stanowią dla Ciebie problem, wróć do właściwego materiału i przeanalizuj ponownie jego treść.
b) F, indeks dolny, dziewięć, koniec indeksu dolnego, indeks górny, osiemnaście, koniec indeksu górnego, strzałka w prawo, O, indeks dolny, osiem, koniec indeksu dolnego, indeks górny, osiemnaście, koniec indeksu górnego, plus luka do uzupełnienia
c)P u, indeks dolny, dziewięćdziesiąt cztery, koniec indeksu dolnego, indeks górny, dwieście trzydzieści dziewięć, koniec indeksu górnego, plus luka do uzupełnienia strzałka w prawo, N b, indeks dolny, czterdzieści jeden, koniec indeksu dolnego, indeks górny, dziewięćdziesiąt pięć, koniec indeksu górnego, plus, I, indeks dolny, pięćdziesiąt trzy, koniec indeksu dolnego, indeks górny, sto czterdzieści dwa, koniec indeksu górnego, plus3 luka do uzupełnienia
d) T h, indeks dolny, dziewięćdziesiąt, koniec indeksu dolnego, indeks górny, dwieście dwadzieścia siedem, koniec indeksu górnego, strzałka w prawo, R a, indeks dolny, osiemdziesiąt osiem, koniec indeksu dolnego, indeks górny, dwieście dwadzieścia trzy, koniec indeksu górnego, plus luka do uzupełnienia
Poniżej przedstawiono przemiany jądrowe w zapisie pełnym i skróconym.
Rozpatrujemy jądra atomowe żelaza oraz astatu . Wskaż jedno, które podlega przemianie alfa i zapisz równanie tej przemiany w pełnej i skróconej formie.
Jądro przechodzi w jądro w wyniku kilku rozpadów promieniotwórczych alfa i beta. Określ liczbę oraz rodzaj rozpadów, zachodzących podczas tego procesu.
Uzupełnij poniższe równanie, a następnie przedstaw je w postaci zapisu uproszczonego. Określ rodzaj przemiany.
Pozytonowa tomografia emisyjna (PET) to metoda obrazowania tkanek, w której wykorzystuje się strumień pozytonów. Ich źródłem może być radioizotop o czasie połowicznego zaniku minut. Otrzymuje się go w wyniku napromieniowania protonami izotopu tlenu . Zapisz równania opisanych reakcji w formie pełnej i skróconej.
Ułóż równanie przemiany w postaci pełnego zapisu i określ jej rodzaj. Znajdź brakujący pierwiastek.
W ciągu godzin uległo rozpadowi początkowej liczby jąder izotopu promieniotwórczego. Ile wynosi czas połowicznego rozpadu tego izotopu?
Stront ulega przemianie z czasem półtrwania wynoszącym lat. Oblicz, ile czasu upłynie, aby z próbki strontu o masie pozostało tego radionuklidu.
Pewien izotop promieniotwórczy rozkłada się zgodnie z danymi przedstawionymi w poniższej tabeli:
Czas [dni] | Masa próbki [mg] |
|---|---|
Wiedząc, że po dniach masa próbki pewnego izotopu zmalała z do , oblicz okres półtrwania tego izotopu.
Przyporządkuj różnicę elektroujemności między atomami do podanych związków chemicznych. Wartości elektroujemności poszczególnych pierwiastków odczytaj z układu okresowego.
Przyporządkuj różnicę elektroujemności między atomami do podanych związków chemicznych. Wartości elektroujemności poszczególnych pierwiastków weź z opisu układu okresowego.

Podaj, jakie wiązania występują w chlorku amonu?
Uczeń uzyskał wartości temperatur wrzenia (pod ciśnieniem atmosferycznym) dwóch badanych substancji. Przyporządkuj je do odpowiednich substancji, wiedząc, że jedną z nich jest tlenek sodu, a drugą tlenek węgla().
Poniżej przedstawiono wzory sześciu związków chemicznych. Zaznacz te, które przedstawiają związki o wiązaniach jonowych.
Wpisz do tabeli, jaki rodzaj wiązania chemicznego (jonowe, kowalencyjne spolaryzowane, kowalencyjne niespolaryzowane, metaliczne) występuje w wymienionych w tabeli związkach.
Oceń, jaką budowę (kowalencyjną czy jonową) posiada chlorek arsenu(), jeśli wiesz, że w temperaturze pokojowej jest cieczą o temperaturze wrzenia . Podaj wzór sumaryczny badanego związku chemicznego.
Budowa: 1. jonowa, 2. kowalencyjna, 3. A l C l indeks dolny, trzy, koniec indeksu dolnego, 4. A s C l indeks dolny, trzy, koniec indeksu dolnego
- Nazwa kategorii: Wiązanie kowalencyjne spolaryzowane
- Elementy należące do kategorii Wiązanie kowalencyjne spolaryzowaneKoniec elementów należących do kategorii Wiązanie kowalencyjne spolaryzowane
- Nazwa kategorii: Wiązanie kowalencyjne niespolaryzowane
- Nazwa kategorii:
- Nazwa kategorii:
- Nazwa kategorii: Koniec elementów należących do kategorii Wiązanie kowalencyjne niespolaryzowane
- Elementy należące do kategorii Wiązanie kowalencyjne niespolaryzowane
- Nazwa kategorii: Wiązanie jonowe
- Nazwa kategorii:
- Nazwa kategorii:
- Nazwa kategorii: Koniec elementów należących do kategorii Wiązanie jonowe
- Elementy należące do kategorii Wiązanie jonowe
- Nazwa kategorii: Wiązanie metaliczne
- Nazwa kategorii:
- Nazwa kategorii:
- Nazwa kategorii: Koniec elementów należących do kategorii Wiązanie metaliczne
- Elementy należące do kategorii Wiązanie metaliczne
Oceń, czy poniższe zdania są prawdziwe czy fałszywe.
Wyjaśnij, w jaki sposób metale przewodzą prąd elektryczny.
By określić zawartość struktur metalicznych, należy obliczyć ułamek f przestrzeni zajętej przez atomy. Im ten współczynnik jest większy, tym kryształ jest bardziej upakowany. Dzięki wyprowadzeniu zależności, między promieniem jonu r metalu a parametrem a komórki elementarnej, możemy określić, do jakiego typu upakowania należy metal. Wynoszą one odpowiednio:
Struktura hcp | |
|---|---|
Struktura fcc | |
Struktura bcc |
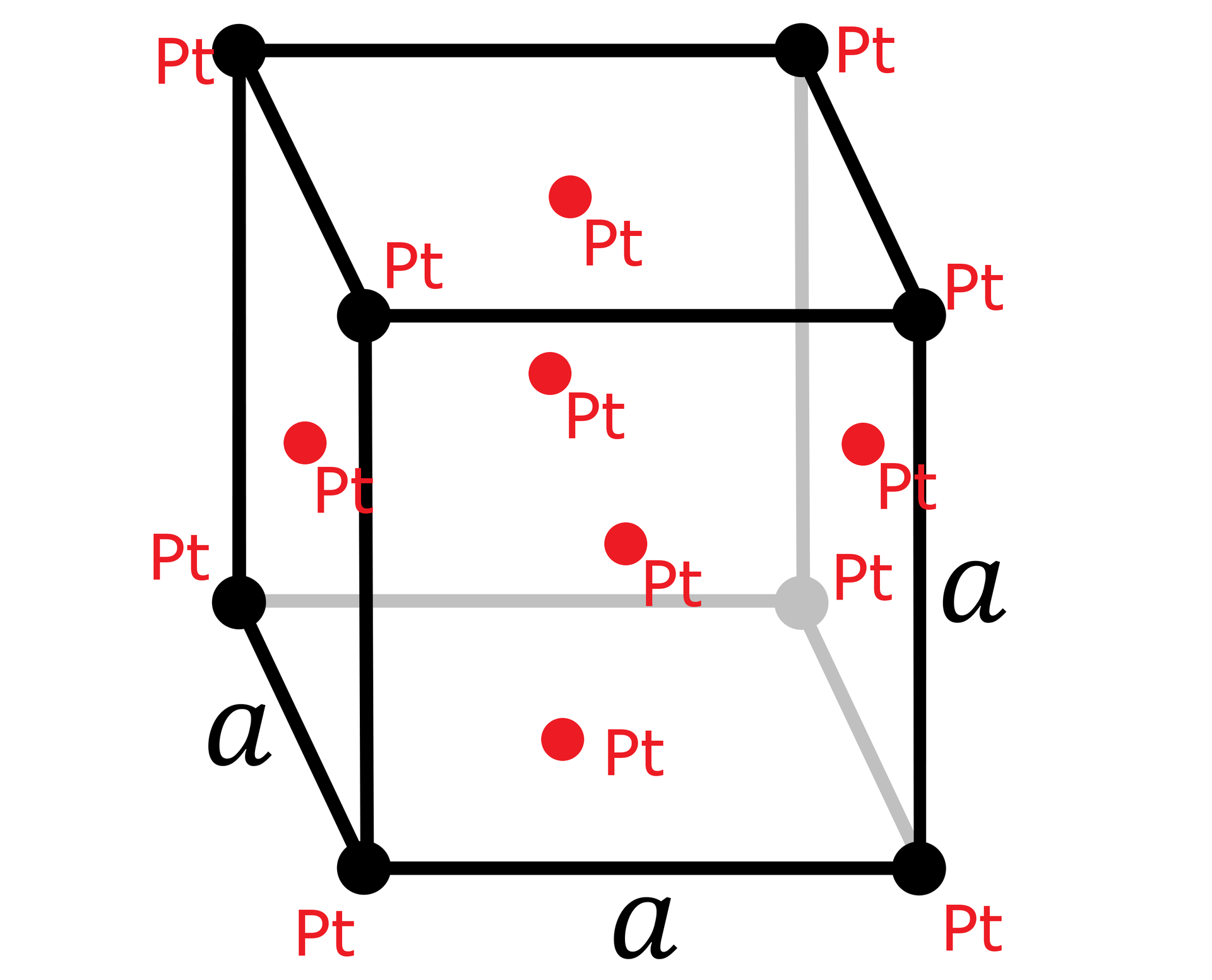
Promień jonowy platyny () wynosi 1,39 Å. Platyna krystalizuje w układzie regularnym, w typie komórki elementarnej F, w której długość krawędzi a = 3,923 Å.
Zdecyduj, do jakiego typu upakowania, hcp, fcc czy bbc, należy platyna. Odpowiedź potwierdź odpowiednimi obliczeniami.
Z dostępnych materiałów stwórz model budowy sieci krystalicznej platyny.