Jakie właściwości fizyczne i chemiczne posiadają alkany?
Jedną z wykorzystywanych w życiu codziennym właściwości substancji jest palność. Na przykład metan to główny składnik gazu ziemnego. Jest wykorzystywany do wytwarzania płomienia w kuchenkach gazowych, ogrzewania wody czy mieszkań. Niestety, co roku media informują o jego wybuchach w kopalniach bądź o czyjejś śmierci z powodu zaczadzenia. Dlaczego tak się dzieje? Jakie jeszcze właściwości mają alkany i dlaczego ich spalanie może być niebezpieczne?
Właściwości fizyczne alkanów
Otrzymywanie metanu oraz sposób jego zbierania.
Problem badawczy
W jaki sposób można zbierać metan powstający w reakcji chemicznej?
Hipoteza
Metan można otrzymać w wyniku reakcji octanu sodu z wodorotlenkiem sodu pod wpływem tlenku wapnia. To gaz o mniejszej gęstości od powietrza i słabo rozpuszczalny w wodzie, dlatego należy go zbierać do probówki lub zlewki napełnionej wodą i odwróconej do góry dnem w naczyniu napełnionym wodą.
Co będzie potrzebne
octanu sodu;
tlenku wapnia;
wodorotlenku sodu;
moździerz;
krystalizator;
dwie probówki;
korek z rurką odprowadzającą;
korek;
statyw;
łapa;
palnik gazowy.
Instrukcja
W moździerzu zmieszano octan sodu, tlenek wapnia i wodorotlenek sodu. Powstałą mieszaninę umieszczono w probówce, zamknięto korkiem z rurką odprowadzającą i umocowano ukośnie w statywie. Drugą probówkę napełniono wodą i umieszczono, odwróconą do góry dnem, w krystalizatorze napełnionym wodą do objętości. Zaczęto ogrzewać probówkę z mieszaniną. Wydzielający gaz zbierano pod wodą do probówki (po ukończeniu zbierania zamknięto probówkę korkiem). Zaobserwowano zachodzące zmiany.
Obserwacje
W wyniku reakcji powstaje bezbarwny, bezwonny gaz, który wypiera wodę z probówki.
Wybrana hipoteza
Metan można otrzymać w wyniku reakcji octanu sodu w wodorotlenkiem sodu, pod wpływem tlenku wapnia. Jest gazem o mniejszej gęstości od powietrza i słabo rozpuszczalny w wodzie, dlatego należy go zbierać do probówki lub zlewki napełnionej wodą i odwróconej do góry dnem w naczyniu napełnionym wodą.
Wnioski
Zebranym gazem jest metan.

Jakie związki chemiczne są potrzebne, aby otrzymać metan?

. Przedstaw dane z tabeli nr 1 w postaci wykresu punktowego, uwzględniając zależność temperatury wrzenia i topnienia alkanów od liczby atomów węgla w ich cząsteczkach. Następnie uzupełnij zdanie.
. Odczytaj w tablicach chemicznych gęstość pierwszych pięciu węglowodorów z szeregu homologicznego alkanów. Następnie uzupełnij zdanie.
Zastanów się i napisz, jaka jest zależność pomiędzy temperaturą wrzenia oraz topnienia i stanem skupienia względem liczby atomów węgla cząsteczkach alkanów.
Podsumowanie właściwości fizycznych alkanów
1. Właściwości fizyczne alkanów o prostych łańcuchach węglowych zmieniają się wraz ze wzrostem liczby atomów węgla w ich cząsteczkach.
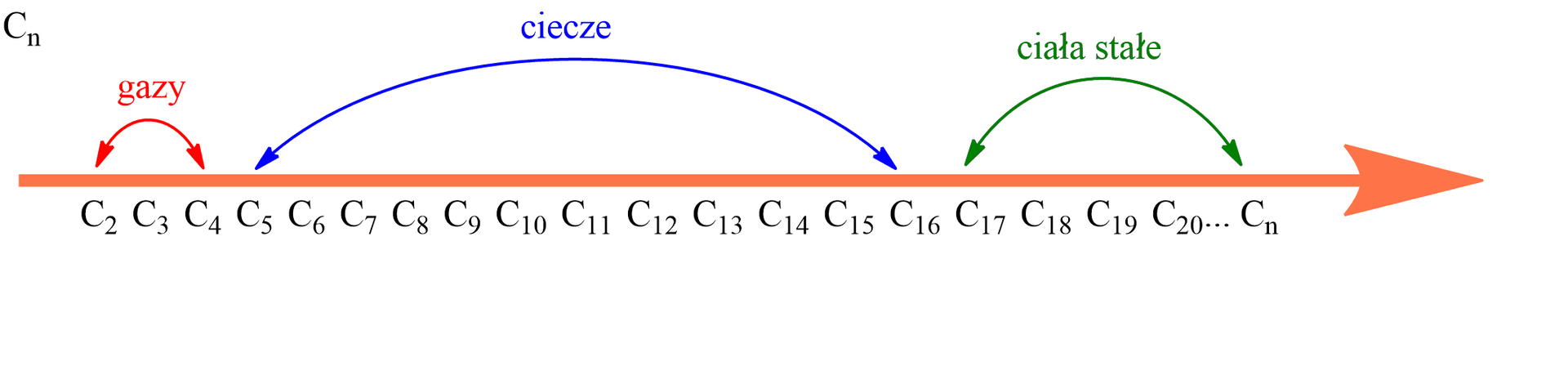
W temperaturze pokojowej alkany o prostych łańcuchach węglowych od metanu do butanu to gazy, od pentanu do heksadekanu to ciecze, natomiast od heptadekanu wszystkie alkany charakteryzują się stałym stanem skupienia.
Wraz ze wzrostem liczby atomów węgla rosną zarówno temperatury wrzenia, jak i topnienia alkanów.

Wraz z długością łańcucha węglowego zwiększa się również gęstość alkanów, jednak pozostaje mniejsza od gęstości wody wynoszącej .

2. Alkany są związkami bezbarwnymi, nie rozpuszczają się w wodzie.

Właściwości chemiczne alkanów
Uwaga!
Doświadczenie chemiczne należy wykonywać wyłącznie pod sprawnym wyciągiem, ponieważ może pojawiać się również toksyczny tlenek węgla(II), tzw. czad.
Problem badawczy
Czy propan i butan są palnymi gazami?
Hipoteza
Propan i butan są palnymi gazami.
Co będzie potrzebne
palnik gazowy (zawierający mieszaninę propan‑butan);
zlewka;
szkiełko zegarkowe;
woda wapienna;
szczypce.
Instrukcja
Należało zapalić palnik gazowy. Za pomocą pokrętła, trzeba było ustawić mały dopływ powietrza. Nad palnikiem trzymać szkiełko zegarkowe, zwilżone wodą. Należało obserwować zachodzące zmiany na szkiełku zegarkowym. Następnie, za pomocą pokrętła, w palniku gazowym ustawiono duży dopływ powietrza. Do wylotu palnika zbliżono kolejne szkiełko zegarkowe, zwilżone wodą wapienną. Zaobserwowano zachodzące zmiany na szkiełku zegarkowym.
Obserwacje
Należało zapalić palnik gazowy. Za pomocą pokrętła, ustawiono mały dopływ powietrza. Nad palnikiem trzeba było trzymać szkiełko zegarkowe, zwilżone wodą. Należało obserwować zachodzące zmiany na szkiełku zegarkowym. Następnie za pomocą pokrętła w palniku gazowym należało ustawić duży dopływ powietrza. Do wylotu palnika zbliżono kolejne szkiełko zegarkowe zwilżone wodą wapienną. Zaobserwowano zachodzące zmiany na szkiełku zegarkowym.
Wnioski
Palnik gazowy jest wypełniony mieszaniną propan‑butan. Alkany te są gazami palnymi. Przy nieograniczonym dostępie powietrza (tlenu), w miejscu zwilżenia wodą wapienną szkiełka zegarkowego, widoczny jest biały osad. Jest to węglan wapnia. Oznacza to, że jednym z produktów spalania, przy nieograniczonym dostępie tlenu, jest tlenek węgla, który reaguje z wodą wapienną. Przy ograniczonym dostępie powietrza (tlenu), na szkiełku pojawia się czarny nalot. Jest to węgiel, czyli sadza.
Zapisz hipotezę, obserwację i wnioski do przeprowadzonego doświadczenia.
Zastanów się i zapisz, jakie dwa alkany występują w składzie mieszaniny palnika gazowego?
Zapisz równania reakcji, jakie zachodzą podczas przeprowadzania doświadczenia .
W wyniku niecałkowitego spalania metanu, np. w piecykach gazowych, powstaje tlenek węgla zwany czadem. Jest to bezbarwny, bezwonny gaz, który w organizmie człowieka ok. razy szybciej łączy się z hemoglobiną niż tlen.
W dodatku to połączenie jest o wiele trwalsze. Dochodzi więc do niedotlenienia tkanek, co w wielu przypadkach prowadzi do śmierci. Jedynym ratunkiem jest natychmiastowa transfuzja krwi.
W pomieszczeniach, w których występuje ryzyko emisji tlenku węgla, montuje się detektory przeznaczone do stałej kontroli obecności tego gazu. Po przekroczeniu określonych wartości stężenia tlenku węgla, w powietrzu zostaje uruchomiony odpowiedni sygnał.

Produktami spalania całkowitego innych alkanów są – tak jak w przypadku propanu i butanu – tlenek węgla i woda. Z kolei podczas spalania niecałkowitego powstają odpowiednio tlenek węgla i woda lub węgiel i woda.
W wyniku spalania całkowitego etanu powstaje zatem:

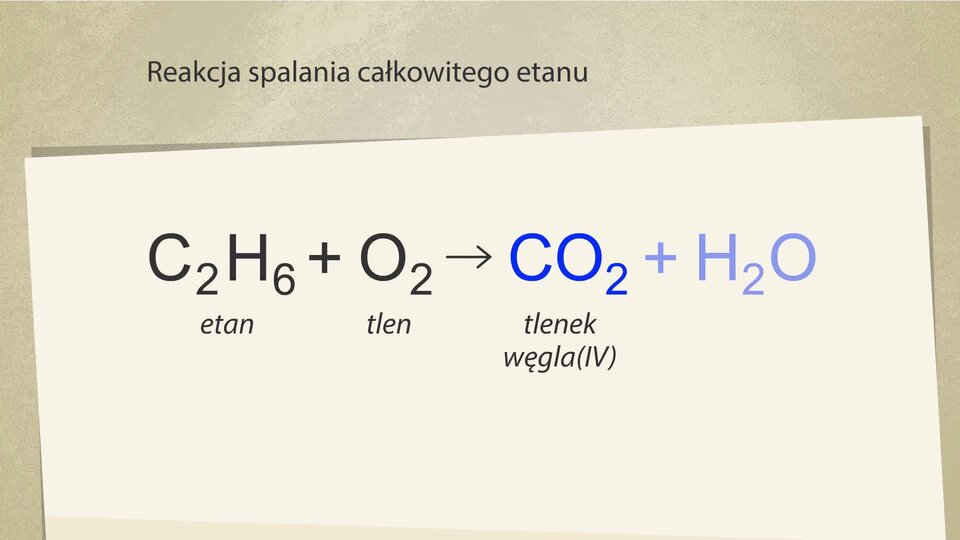
Film dostępny pod adresem /preview/resource/Rq17i7iEDtjmY
Animacja przedstawiająca reakcję spalania całkowitego etanu, gdzie są uzgadniane wartości po stronie substratów i produktów.
Natomiast produktami niecałkowitego spalania etanu są:

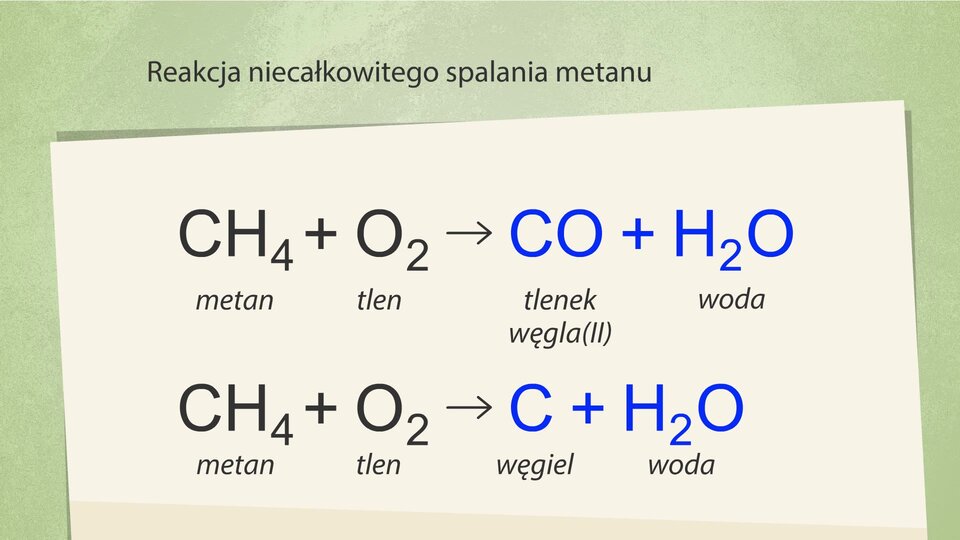
Film dostępny pod adresem /preview/resource/RyFlF2c0pO68V
Animacja przedstawiająca reakcję spalania całkowitego metanu. Wykonywane są obliczenia obrazujące tę reakcję.
Uzupełnij współczynniki stechiometryczne w poniższych równaniach reakcji chemicznych.
Miejsca, w którym uznasz, że współczynnik stechiometryczny wynosi , pozostaw puste.

Film dostępny pod adresem /preview/resource/RsLe6wuVPcwxk
Prezentowane są odpowiednio wymieniane sprzęty laboratoryjne i odczynniki. Eksperymentator wlewa do krystalizatora wodę, dodaje detergent. Eksperymentator wprowadza wężykiem gaz z butli do krystalizatora z wodą. Na powierzchni krystalizatora tworzą się bańki. Po zebraniu większej ilości baniek eksperymentator odstawia butlę. Eksperymentator zbliża do baniek zapalone łuczywko. Pojawia się duży płomień.
Mieszanina metanu z powietrzem w stężeniu objętościowym ma właściwości wybuchowe. Tworzenie się tej mieszaniny wskutek przedostania się metanu do zamkniętych pomieszczeń bywa przyczyną groźnych w skutkach eksplozji, zarówno w budynkach mieszkalnych, jak i kopalniach. Metan jest gazem bezwonnym, dlatego gaz ulatniający się z sieci nawaniany jest związkami siarki. Dzięki temu, przy odkręconym kurku z gazem, można wyczuć charakterystyczny zapach. W mieszaninie o proporcji powyżej , metan pali się płomieniowo. Mieszanina wybuchowa eksploduje np. pod wpływem ognia czy iskry elektrycznej. Dlatego gdy podejrzewasz, że ulatnia się gaz, zamknij jego dopływ i otwórz szeroko okna. Pod żadnym pozorem nie zapalaj ognia ani nie włączaj urządzeń elektrycznych. Jak najszybciej opuść mieszkanie i zawiadom pogotowie gazowe (tel. ).
Uwaga! Należy podkreślić, że niebezpieczeństwo związane z urządzeniami gazowymi stanowi zarówno metan, jak i tlenek węgla. Oba związki chemiczne są gazami bezwonnymi. Metan jednak nie jest gazem toksycznym, lecz wybuchowym, ponieważ gwałtownie się spala. Natomiast tlenek węgla jest trujący i może spowodować śmierć poprzez uduszenie.

Uwaga!
Doświadczenie należy przeprowadzać w okularach ochronnych.
Problem badawczy
Czy węglowodory ciekłe i stałe są palne?
Hipoteza
Węglowodory stałe i ciekłe są palne.
Co będzie potrzebne
palnik gazowy;
dwie parownice;
nafta lub pentan (lub inny dostępny ciekły alkan, np. heksan);
parafina;
szczypce;
trójnóg;
siatka ze spiekiem ceramicznym;
łuczywo.
Instrukcja
W ogrzanej parownicy umieszczono niewielką ilość pentanu (lub nafty). Zapalono go (ją), używając łuczywa. Umieszczono parownicę z niewielką ilością parafiny na trójnogu z siatką ceramiczną i ogrzewano. Po chwili zapalono, używając łuczywa. Zaobserwowano zachodzące zmiany.
Obserwacje
Po ogrzaniu nafty, jej pary się zapaliły. Podczas ogrzewania parafiny najpierw zaobserwowano jej stopienie, a potem również zapalenie się jej par.
Wnioski
Nafta jest mieszaniną ciekłych alkanów (pentan także jest ciekłym alkanem). Parafina z kolei jest mieszaniną stałych węglowodorów. Wszystkie alkany są palne, a temperatura zapłonu wzrasta z liczbą atomów węgla w cząsteczce węglowodoru.

Zapisz wybraną hipotezę, obserwację i wnioski z doświadczenia.
Zastanów się i napisz, jakie możliwe ciekłe alkany można było wykorzystać w tym doświadczeniu?
Sprawdź, w jaki sposób metan zachowuje się wobec wody bromowej.
W tym celu wykonaj doświadczenie. Wybierz hipotezę, napisz obserwacje oraz sformułuj odpowiedni wniosek.
Jeśli nie masz możliwości samodzielnego przeprowadzenia doświadczenia, zapoznaj się z poniższym materiałem filmowym obrazującym jego przebieg.
Sprawdzono, w jaki sposób metan zachowuje się wobec wody bromowej.
W tym celu wykonano doświadczenie. Wybierz hipotezę, zapoznaj się z obserwacjami oraz sformułuj odpowiedni wniosek.
Możesz zapoznać się z filmem ukazującym to doświadczenie.
Problem badawczy:
Czy metan powoduje odbarwienie wody bromowej?
Hipoteza:
Metan nie powoduje odbarwienia wody bromowej.
Co będzie potrzebne:
dwie probówki;
korek;
woda bromowa (roztwór bromu);
metan (np. z małej butli).
Instrukcja:
Doświadczenie przeprowadzono pod dygestorium. Do obu probówek wlano do objętości roztwór bromu (wodę bromową). Do jednej z probówek włożono wężyk z metanem i przepuszczono gaz przez roztwór. Zaobserwowano zachodzące zmiany i porównano obie probówki.
Obserwacje:
Brak objawów reakcji./Brak zmian świadczących o przebiegu reakcji./Brunatny (lub pomarańczowy lub żółty) roztwór nie zmienia swojego zabarwienia.
Wniosek:
Metan nie powoduje odbarwienia wody bromowej./Metan nie reaguje z bromem.

Film dostępny pod adresem /preview/resource/R1Pmw7FoxTWhn
W filmie zaprezentowano przebieg doświadczenia, w którym zbadano reaktywność metanu względem wody bromowej. W filmie przedstawiono niezbędne szkło i sprzęt laboratoryjny do przeprowadzenia doświadczenia.
Napisz obserwacje oraz wniosek do przeprowadzonego doświadczenia.
Zastanów się i napisz, w jakiej postaci metan wprowadzany jest do probówki.
Metan w zwykłych warunkach nie reaguje z bromem. Dopiero pod wpływem wysokiej temperatury lub światła, metan reaguje m.in. z bromem lub chlorem.
Podsumowanie
Właściwości fizyczne alkanów zmieniają się wraz ze wzrostem długości łańcucha węglowego.
Alkany są związkami mało reaktywnymi chemicznie, w temperaturze pokojowej ulegają reakcjom spalania.
Słownik
proces spalania węglowodorów przy nieograniczonym dostępie powietrza (tlenu); jego produktami są tlenek węgla i woda
proces spalania węglowodorów przy ograniczonym dostępie powietrza (tlenu); jego produktami są tlenek węgla (czad) oraz woda lub węgiel (sadza) i woda
mieszanina ciekłych alkanów, których cząsteczki zawierają od do atomów węgla
mieszanina stałych alkanów, zawierających od do atomów węgla
naturalna mieszanina węglowodorów, w skład której wchodzi głównie metan, a także w bardzo małej ilości inne lekkie węglowodory, zwłaszcza etan, propan butan, pentan i heksan