Benzen jako przedstawiciel arenów - budowa
Co wniósł do świata chemii Friedrich August Kekulé von Stradonitz [czyt. kekulẹ fon sztrạ:donıc]?
Był to niemiecki chemik, który pracował na stanowisku profesora na uniwersytecie w Gandawie w Heidelbergu i Bonn. Nazywany jest współtwórcą teorii budowy związków organicznych. Na podstawie prowadzonych badań dowiódł, że węgiel jest czterowartościowy, a jego atomy, występujące w związkach organicznych, mogą brać udział w tworzeniu łańcuchów. Określany jest mianem odkrywcy budowy benzenu.

Zapoznaj się z treścią audiobooka dotyczącego odkrycia budowy cząsteczki benzenu. Dowiesz się, jaki udział w rozwoju chemii organicznej miał Friedrich Kekulé. Następnie rozwiąż poniższe zadania.
Jak zbudowana jest cząsteczka benzenu?
Był ciepły, wrześniowy wieczór. Friedrich Kekule wracał zmęczony po całym dniu pracy. Na szczęście udało mu się zdążyć na ostatni odjazd omnibusa. Zajął jedyne wolne miejsce na końcu. Wiedział, że nareszcie może odpocząć po ciężkim pełnym zajęć dniu. Przez okno przyglądał się wyjątkowo pustym o tej porze ulicom Londynu. Mimo że jeździł tą trasą codziennie, zawsze dostrzegał coś niezwykłego.
Często wracał wspomnieniami do życia, jakie prowadził w Gandawie. Architektura była tym, co go fascynowało – te niesamowite kształty budynków, zdobione fasady, kolumny. We wszystkim widział pewnego rodzaju harmonię. Zaczął jednak myślami podążać w innym kierunku. Marzenia pochłonęły go bez reszty aż przymknął powieki... Nagle, przed oczami zobaczył krążące atomy. Twory te były w nieustannym ruchu, widział wyraźnie, jak dwa mniejsze łączą się ze sobą w pary, jak większe otaczają dwa mniejsze, a jeszcze większe utrzymywały to wszystko w zawrotnym tańcu. Większe atomy tworzyły łańcuch, wciągając mniejsze, ale tylko na końcach łańcucha (...).
Nagle Friedrich obudził się, a w omnibusie nie było ani jednego pasażera. Dojeżdżał już na ostatni przystanek, na którym powinien wysiąść. Zebrał torbę z rzeczami, wysiadł i powolnym krokiem ruszył w stronę swojego domu. Wiedział, że to, co zobaczył, mogło mieć coś wspólnego ze strukturami związków.
Nadeszła wolna niedziela, Kekule spędzał czas na spacerze, korzystając z ostatnich promieni słońca. W powietrzu wyczuwalny był już jesienny chłód. Spacerował po parku, znajdującym się dwie ulice od jego domu. Półmrok, który zaczął wylewać się na ulice Londynu, sugerował aby wracać. Friedrich skierował więc kroki na swoją ulubioną trasę.
Będąc już w domu rozpalił ogień w piecu. Wieczory były już naprawdę zimne. Odwrócił fotel w stronę kominka, rozsiadł się i pogrążył w półśnie. Atomy znowu zaczęły harcować przed jego oczami. Tym razem mniejsze grupy trzymały się skromnie z tyłu. Jego czujność, wyostrzona przez powtarzające się podobne wizje, rozróżniała teraz większe twory o różnorodnym kształcie. Długie szeregi, kilkakrotnie ściśle ze sobą złączone, wiły się i skręcały niczym węże. W pewnym momencie zdziwił się. Jeden z tych węży chwycił swój własny ogon i szyderczo kręcił się przed jego oczami.
Kekule ocknął się, zerwał się z krzesła i od razu pobiegł do swojego biurka. Chciał jak najszybciej zapisać wszystko to, co zobaczył w swoim śnie. Resztę nocy spędził na rozpracowywaniu wniosków z tej wizji.
Od czasu, kiedy Kekule ujrzał oczami wyobraźni tańczące węże, prawie w ogóle nie sypiał. Każdą wolną chwilę pochłaniało mu przeglądanie materiałów naukowych czy rysowanie na kartce układów, które wówczas zobaczył. Kreślił bezładnie po wielu kartkach, szukając odpowiedzi na nurtujące go pytania.
Po kilku tak pracowitych dniach i nieprzespanych nocach, poszukującemu rozwiązania zagadkowej struktury chemikowi przyśniło się sześć małp rozrabiających na drzewie. Nagle, w jednej chwili małpki wyskoczyły w powietrze i utworzyły trudny do rozerwania wirujący, sześciokątny krąg. Każda z nich w jednej łapce trzymała banana. Porażony odkryciem Kekulè, obudził się i natychmiast naszkicował wyśnioną strukturę – sześciokąt. W każdym narożu figury wpisał atom węgla. Naprzemiennie ułożone pojedyncze i podwójne chwyty łapek małp określił jako wiązania pojedyncze i podwójne, a trzymane banany jako wiązania pojedyncze pomiędzy atomami węgla i atomami wodoru. To tworzyło spójną całość – pomyślał. Dumny ze swojego odkrycia – struktury benzenu – odetchnął z ulgą i w końcu położył się spokojnie spać.
https://wiedza.alkahest.umcs.pl/co-wysnil-kekule/ [dostęp 17.02.2020r.]
https://pl.wikipedia.org/wiki/Friedrich_August_Kekulé_von_Stradonitz [dostęp 17.02.2020], licencja: CC BY-SA 3.0.
Reguła Hückla to prosta metoda, pozwalająca na sprawdzenie, czy płaski pierścień badanego związku wykazuje aromatyczność. Oparta jest na wzorze
wyznaczającym liczbę zdelokalizowanych elektronów pi , czyli 4n+2, gdzie n to liczba naturalna. Obowiązuje dla n w granicach 0–6. Czy benzen spełnia tę regułę?
Benzen
Cząsteczka benzenu zbudowana jest z sześciu połączonych ze sobą atomów węgla. Do każdego atomu węgla przyłączony jest atom wodoru.
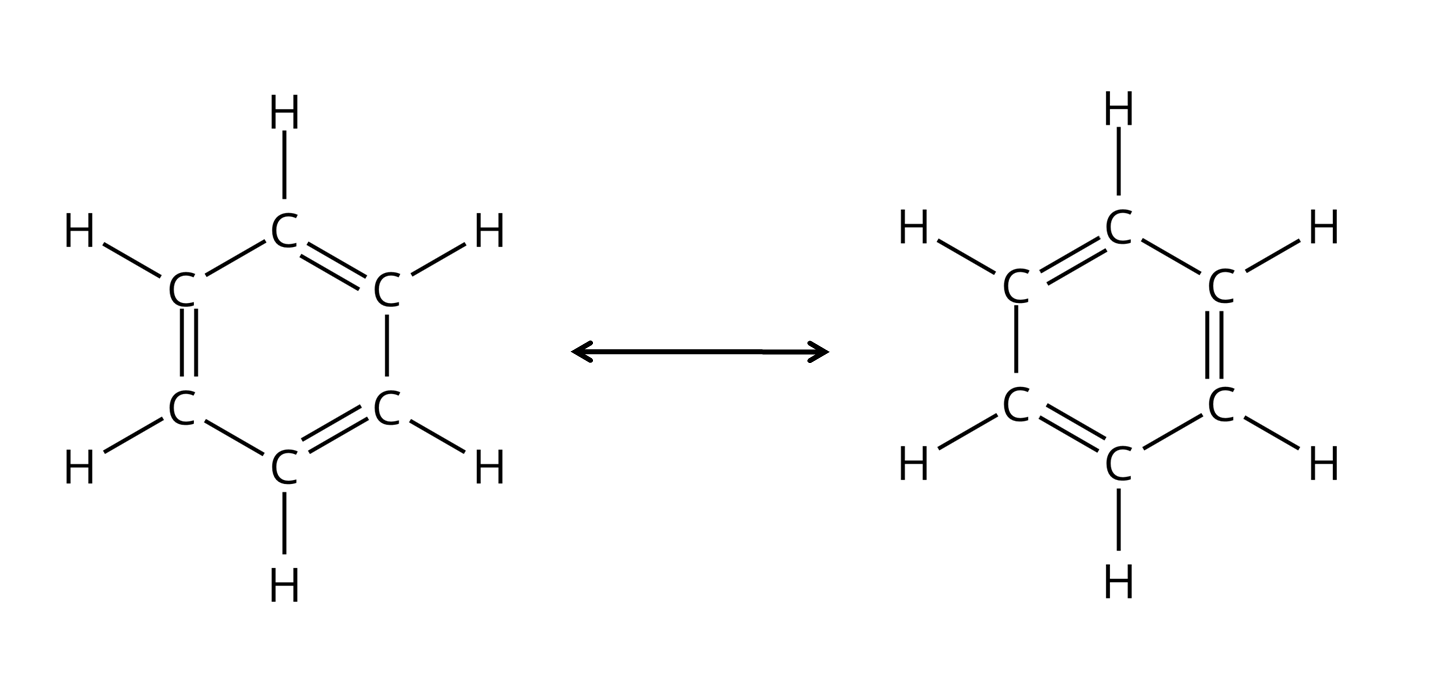
W cząsteczce benzenu występują zdelokalizowane wiązania , które znajdują się między atomami węgla w pierścieniu. Powstają w wyniku rozmycia się chmury elektronowej w okolicy pierścienia, gdzie jest zlokalizowanych sześć elektronów , po jednym od każdego atomu węgla, wchodzącego w skład pierścienia. Delokalizacja tych wiązań jest jedną z charakterystycznych cech związków aromatycznych.
Poza wyżej wymienioną właściwością, związki aromatyczne muszą wykazywać również kilka innych cech: są cykliczne, pierścień odznacza się płaską budową (orbitalom walencyjnym atomów węgla budującym pierścień przypisujemy więc hybrydyzację ), a ponadto dla tych związków musi zostać spełniona . Według niej związki aromatyczne to takie, które spełniają zasadę zdelokalizowanych elektronów , gdzie jest liczbą naturalną lub zerem. Cząsteczka benzenu posiada sześć elektronów . Oznacza to, że , czyli .
Otrzymywanie benzenu
Otrzymywanie benzenu z węgla i odczynników nieorganicznych
Możliwą metodą otrzymywania benzenu jest ciąg przemian rozpoczynajacy się od reakcji węgla ze związkiem nieorganicznym. Przykładem może być reakcja węgla i wapna palonego () prowadząca do otrzymania acetylenku wapnia (węglika wapnia) i tlenku węgla().
Na kolejnym etapie acetylenek wapnia reaguje z wodą. W reakcji tej wydziela się etyn.
Ostatnim krokiem jest opisana wcześniej trimeryzacja etynu w podwyższonej temperaturze i pod odpowiednim ciśnieniem, z zastosowaniem katalizatora, prowadząca do otrzymania benzenu. Spróbuj wykonać opisaną wyżej syntezę w poniższym laboratorium chemicznym.
Na podstawie poniższych informacji wykonaj niezbędne obliczenia i przeprowadź eksperyment w laboratorium chemicznym. Wyliczone wartości uzupełnij i sprawdź w umieszczonym zadaniu. Zapoznaj się z problemem badawczym i zweryfikuj własną hipotezę. W formularzu zanotuj swoje obserwacje i wyniki, a następnie zapisz wnioski.
Do kolby okrągłodennej odmierz aniliny , a następnie dodaj kwasu chlorowodorowego . Następnie odważ azotanu sodu i rozpuść w wody. W kolejnym etapie odmierz kwasu fosforowego i dodaj go do uzyskanej w kolbie okrągłodennej mieszaniny. Po zakończeniu reakcji, przeprowadź destylację prostą powstałego roztworu zwracając uwagę na temperaturę, w której destylują poszczególne składniki roztworu.
Ważne!
Na podstawie licznych badań, benzen został uznany za substancję rakotwórczą. W jego przypadku nie ma czegoś takiego, jak bezpieczny poziom narażenia – nawet niewielkie ilości tej substancji mogą wyrządzić szkody naszemu organizmowi.
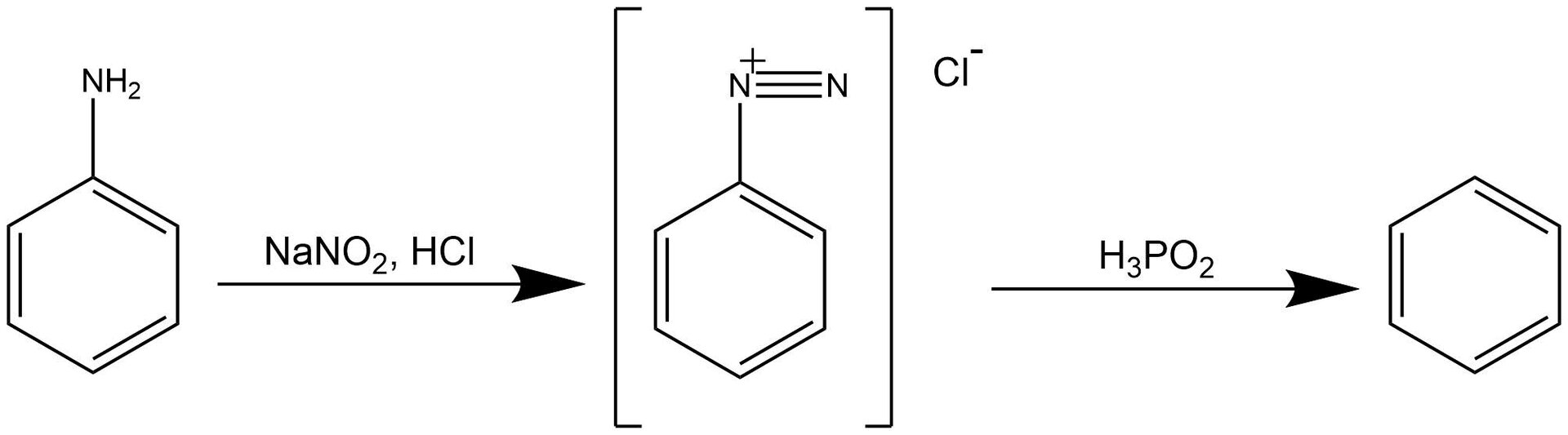
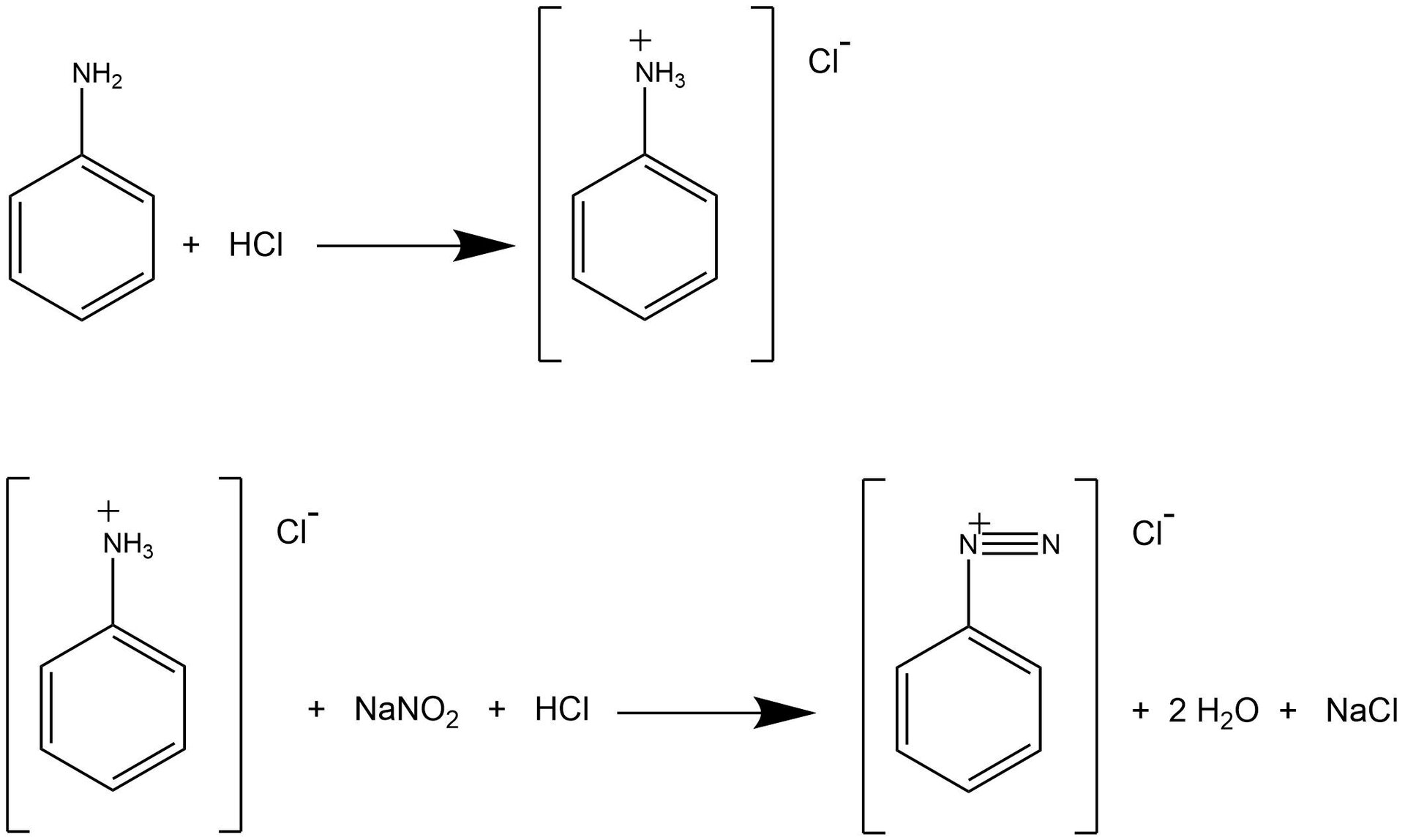
W przedstawionym niżej laboratorium zastosowano metodę otrzymywania benzenu, która składa się z dwóch etapów. W pierwszym etapie zastosowano reakcję diazowania. W wyniku reakcji aminy aromatycznej (anilina) z kwasem azotowym (który został otrzymany w reakcji azotanu sodu z kwasem solnym) otrzymano sól diazoniową. Sole diazoniowe to grupa związków organicznych o wzorze ogólnym . Reakcja ta wymaga zastosowania odpowiednich warunków, aby mogła przebiec prawidłowo. Aromatyczne sole diazoniowe są trwałe w temperaturze od do , dlatego reakcja prowadzona jest w łaźni lodowej. Należy użyć nadmiaru kwasu solnego. Zapewnia on odpowiednie pH reakcji, które jest niezbędne do ustabilizowania soli diazoniowych.
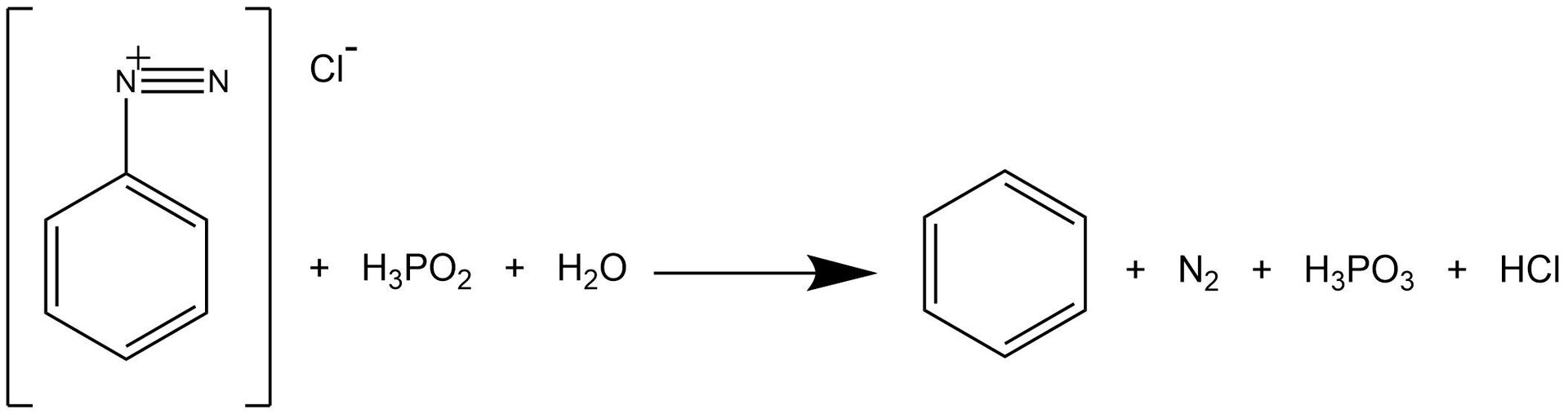
Dopiero po otrzymaniu soli diazoniowej można przejść do kolejnego etapu reakcji – otrzymywania benzenu.
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D28BPTFH4
Na podstawie licznych badań, benzen został uznany za substancję rakotwórczą. W jego przypadku nie ma czegoś takiego, jak bezpieczny poziom narażenia – nawet niewielkie ilości tej substancji mogą wyrządzić szkody naszemu organizmowi. W przedstawionym laboratorium zastosowano metodę otrzymywania benzenu, która składa się z dwóch etapów. W pierwszym etapie zastosowano reakcję diazowania. W wyniku reakcji aminy aromatycznej (anilina) z kwasem azotowym (który został otrzymany w reakcji azotanu sodu z kwasem solnym) otrzymano sól diazoniową. Sole diazoniowe to grupa związków organicznych o wzorze ogólnym . Reakcja ta wymaga zastosowania odpowiednich warunków, aby mogła przebiec prawidłowo. Aromatyczne sole diazoniowe są trwałe w temperaturze od do , dlatego reakcja prowadzona jest w łaźni lodowej. Należy użyć nadmiaru kwasu solnego. Zapewnia on odpowiednie pH reakcji, które jest niezbędne do ustabilizowania soli diazoniowych.
Dopiero po otrzymaniu soli diazoniowej można przejść do kolejnego etapu reakcji – otrzymywania benzenu. Zapoznaj się z przeprowadzonym doświadczeniem i wykonaj ćwiczenia.
Analiza eksperymentu: Otrzymywanie benzenu.
Problem badawczy: Czy możliwe jest otrzymanie benzenu w reakcji soli diazoniowej z kwasem fosforowym?
Hipoteza: Można otrzymać benzen w reakcji soli diazoniowej z kwasem fosforowym.
Sprzęt laboratoryjny:
waga – urządzenie elektryczne służące do wyznaczania mas substancji. Daną substancję umieszcza się na srebrnej tacy umieszczonej na urządzeniu. Masa ważonej substancji wyświetlana jest na wyświetlaczu;
zlewka – naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych;
cylindry miarowe – podłużne szklane naczynia laboratoryjne w kształcie walca z umieszczoną na ściance podziałką objętości. Służą do odmierzania cieczy;
pipety – wąska rurka do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
łyżeczki – długi trzonek wykonany ze szkła, porcelany lub metalu zakończony z jednej strony łyżeczką. Służy do nabierania sypkich substancji chemicznych;
kolba okrągłodenna – szklane naczynie laboratoryjne z zaokrąglonym dnem;
termometr ze szlifem – sprzęt laboratoryjny służący do pomiaru temperatury rozmaitych substancji, zwykle umieszczonych wewnątrz szklanej aparatury;
płaszcz grzewczy – sprzęt laboratoryjny służący do kontrolowanego podgrzewania zawartości kolb okrągłodennych, wykorzystywany często zamiast łaźni laboratoryjnej;
chłodnica Liebiga – rodzaj sprzętu laboratoryjnego pełniący funkcję skraplacza, czyli urządzenia zamieniającego gaz w ciecz lub (rzadko) gaz w ciało stałe;
kolba stożkowa – szklane naczynie laboratoryjne o kształcie stożka z płaskim dnem i wąską szeroką szyjką;
łaźnia lodowa – sprzęt laboratoryjny pośredniczący w chłodzeniu naczyń laboratoryjnych (wraz z ich zawartością). Łaźnia jest naczyniem wypełnionym odpowiednią substancją;
statyw – prostokątny sprzęt laboratoryjny z rzędami otworów, w których umieszczane są probówki.
Odczynniki chemiczne:
anilina;
azotan sodu;
kwas chlorowodorowy ;
kwas fosforowy ;
woda destylowana.
Przebieg eksperymentu.
Wprowadzono aniliny do kolby okrągłodennej, następnie dodano stężonego kwasu chlorowodorowego. Otrzymaną mieszaninę umieszczono w łaźni lodowej.
Przygotowano wodny roztwór azotanu sodu (rozpuszczono azotanu sodu w wody destylowanej). Roztwór wprowadzono do kolby okrągłodennej.
Do uzyskanej w kolbie okrągłodennej mieszaniny dodano kwasu fosforowego.
Po zakończeniu reakcji, przeprowadzono destylację prostą otrzymanego roztworu.
Podczas prowadzenia destylacji, zwrócono uwagę na temperaturę, w której destylują poszczególne składniki roztworu. Po wartości temperatury wrzenia określono, jaki produkt został otrzymany.
Obserwacje: Po dodaniu azotanu mieszanina znajdująca się w kolbie okrągłodennej przyjmuje pomarańczowy kolor. Następnie, po dodaniu kwasu fosforowego można zaobserwować wydzielanie się pęcherzyków bezbarwnego gazu. Podczas prowadzenia destylacji prostej analizowanej mieszaniny pierwszy składnik zaczyna wrzeć i skraplać się w kolbie stożkowej w temperaturze , jest to bezbarwna ciecz.
Wyniki: Otrzymana bezbarwna ciecz to benzen. Zostało to potwierdzone podczas destylacji prostej mieszaniny – temperatura wrzenia benzenu odpowiada temperaturze wrzenia bezbarwnej cieczy zbierającej się w kolbie stożkowej.
Wnioski: Hipoteza została potwierdzona – w reakcji soli diazoniowej z kwasem fosforowego możliwe jest otrzymanie benzenu.
Dokończ poniższe zdanie, wybierając prawidłową odpowiedź.