Kwasy – moc kwasu, otrzymywanie kwasów
Moc kwasu
Cząsteczki kwasów ulegają dysocjacji elektrolitycznej, w wyniku której od cząsteczki kwasu oderwane zostają jony wodoru. To jak chętnie i w jakim stopniu kwasy ulegają dysocjacji elektrolitycznej jest miarą mocy kwasów. Ozdwierciedleniem tego są wartości stałych dysocjacji elektrolitycznej, charakterystyczne dla poszczególnych kwasów. Stała ta zależy od rodzaju rozpuszczalnika i temperatury (ze wzrostem temperatury wartość stałej dysocjacji kwasowej rośnie). Wraz ze wzrostem wartości stałej dysocjacji kwasowej, dysocjacja zachodzi w większym stopniu, więc moc kwasu także rośnie. Szerzej temat dysocjacji elektrolitycznej omówiony jest w innym module.
Moc kwasów beztlenowych
W przypadku kwasów beztlenowych czynnikiem decydującym o mocy kwasu jest wielkość promienia atomowego. Im słabsze wiązanie H–A, tym łatwiej oderwać jon H⁺, a więc kwas jest mocniejszy. Im większy jest promień atomowy niemetalu, połączonego z atomem wodoru, tym dłuższe i słabsze jest wiązanie, a anion reszty kwasowej po oderwaniu jonu wodoru stabilniejszy, a co za tym idzie moc kwasu będzie większa.
Na moc kwasu beztlenowego ma również wpływ elektroujemność niemetalu. Należy ją wziąć pod uwagę porównując moc kwasów HA, w których A to niemetale z tego samego okresu. Wraz ze wzrostem elektroujemności atomu niemetalu w okresie, moc kwasów się zwiększa. Czym większa jest różnica elektroujemności pomiędzy pierwiastkami i w wiązaniu, tym wiązanie jest bardziej spolaryzowane. Większe spolaryzowanie wiązania sprzyja rozpadowi substancji chemicznej na jony. Porównując moc kwasów beztlenowych niemetali z jednej grupy w układzie okresowym, elektoujemność nie odgrywa znaczącej roli.
Podsumowując - w przypadku kwasów beztlenowych
W grupie: moc kwasu rośnie w dół (bo rośnie promień atomowy → słabsze wiązanie H–A).
W okresie: moc kwasu rośnie w prawo (bo rośnie elektroujemność → większa polaryzacja wiązania H–A)
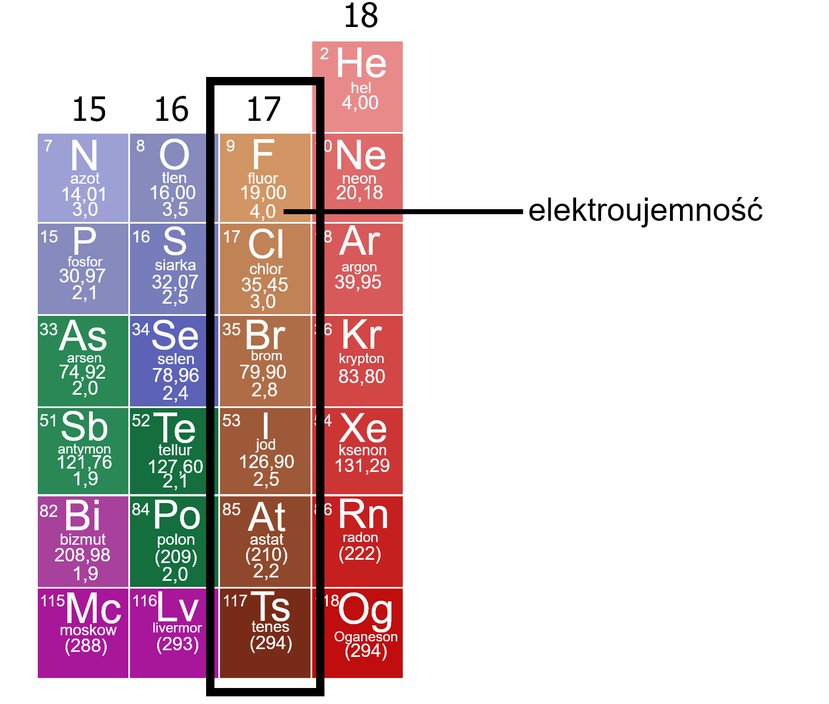
Korzystając z poniższego fragmentu układu okresowego pierwiastków, odczytaj wartości elektroujemności fluorowców oraz zastanów się jak zmienia się promień atomowy w obrębie grupy. Ustal, który z tych niemetali: fluoru, chloru, bromu i jodu tworzy kwasy najmocniejszy, a który z nich najsłabszy.
Moc kwasów tlenowych
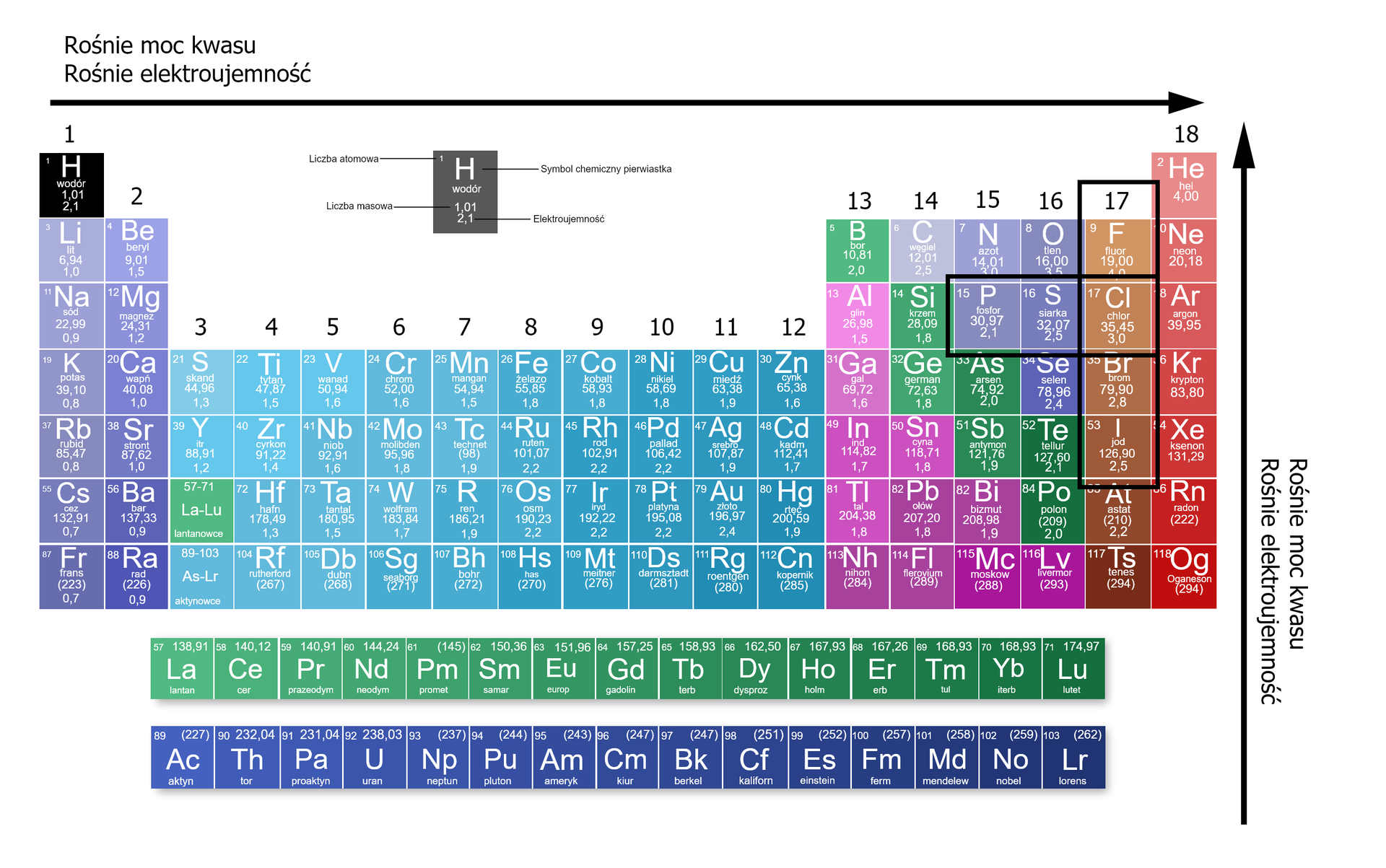
Moc kwasów tlenowych wzrasta wraz ze wzrostem wartości elektroujemności atomów pierwiastka zawartego w reszcie kwasowej – zarówno w grupie, jak i w okresie układu okresowego pierwiastków chemicznych. Im bardziej elektroujemny atom centralny (E), tym silniej przyciąga elektrony, co za tym idzie bardziej polaryzuje wiązanie O–H, a w konsekwencji łatwiej oderwać jon wodoru.
Należy jednak pamiętać, że regułę tę możemy stosować tylko w przypadku porównywania kwasów o tej samej budowie, np. , gdzie jest symbolem pierwiastka. Zatem możemy porównywać ze sobą i , nie zaś np. i . Stąd uniwersalnym kluczem, który umożliwia porównanie mocy kwasów, jest analiza zgodna z wartościami stałych dysocjacji.
Porównując moc kwasów tlenowych tego samego pierwiastka, należy pamiętać, że moc kwasu wzrasta wraz z liczbą atomów tlenu przyłączonych do atomu centralnego (E). Więcej atomów tlenu (zwłaszcza tych, które nie są częścią grupy OH) to silniejszy efekt indukcyjnyefekt indukcyjny, większa polaryzacja wiązań i większa stabilizacja anionu powstałego po oddysocjowaniu H⁺, a co za tym idzie mocniejszy kwas.
Jak otrzymać kwasy?
Czy zastanawiasz się czasem, skąd biorą się kwasy spotykane w chemii i codziennym życiu? Poznanie metod ich otrzymywania to nie tylko sposób na zrozumienie wielu reakcji chemicznych, ale także okazja do uporządkowania wiedzy o właściwościach różnych substancji. Dzięki temu łatwiej jest pojąć, dlaczego jedne kwasy powstają z gazów, inne z tlenków, a jeszcze inne z soli. To fascynujący temat, który warto poznać bliżej!
Reakcja wodorków niemetali z wodą
Metoda ta pozwala na otrzymanie wodnych roztworów kwasów beztlenowych. Dobrze działa w przypadku wodorków, które są rozpuszczalnymi w wodzie gazami, a w cząteczkach których występuje silna polaryzacja wiązań umożliwiająca łatwe oderwanie jonu wodoru.
wodorek niemetalu + H₂O → kwas beztlenowy
HCl Indeks dolny (g)(g) + HIndeks dolny 22O → HCl Indeks dolny (aq)(aq) (kwas chlorowodorowy)
HIndeks dolny 22S Indeks dolny (g)(g) + HIndeks dolny 22O → HIndeks dolny 22S Indeks dolny (aq)(aq) (kwas siarkowodorowy)
Reakcja tlenków kwasotwórczych z wodą
W kontekście otrzymywania kwasów, można wyróżnić tlenki, które mają charakter kwasowy i jednocześnie reagują z wodą. To właśnie te tlenki, w wyniku reakcji z wodą tworzą kwasy.
Potrafisz podać przykład reakcji tlenku z wodą, w wyniku której otrzymasz kwas tlenowy? Umiesz zaplanować takie doświadczenie? W jaki sposób potwierdzisz, że otrzymanym produktem jest kwas? Przeprowadź eksperyment w wirtualnym laboratorium, a na pewno udzielisz odpowiedzi na powyższe pytania. Zapoznaj się z problemem badawczym, zaproponuj hipotezę, zanotuj obserwacje i wyniki oraz sformułuj wnioski.
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D2VEGKVMK
Potrafisz podać przykład reakcji tlenku z wodą w wyniku której otrzymasz kwas tlenowy? Umiesz zaplanować takie doświadczenie? W jaki sposób potwierdzisz, że otrzymanym produktem jest kwas? Zapoznaj się z opisem doświadczenia, a na pewno będziesz znał odpowiedź na powyższe pytania. Zapoznaj się z problemem badawczym, hipotezą, obserwacjami i wynikami oraz sformułowanymi wnioski.
Analiza eksperymentu:
Otrzymywanie kwasów tlenowych w wyniku reakcji odpowiednich tlenków z wodą.
Problem badawczy:
Czy w wyniku reakcji tlenku z wodą można otrzymać kwas tlenowy?
Hipoteza:
W wyniku reakcji tlenku z wodą można otrzymać kwas tlenowy.
Sprzęt laboratoryjny:
statyw na probówki – prostokątny sprzęt laboratoryjny z rzędami otworów, w których umieszczane są probówki;
pipety – wąskie rurki służące do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
łyżeczki – długie trzonki wykonane ze szkła, porcelany lub metalu zakończone z jednej strony łyżeczką.
Odczynniki chemiczne:
wskaźnik uniwersalny; tlenek siarki(); suchy lód; tlenek fosforu(); tlenek krzemu().
Przebieg eksperymentu:
1. Umieszczenie w probówce trzech centymetrów sześciennych wody ze wskaźnikiem uniwersalnym.
2. Przez roztwór w probówce przepuszczono gazowy tlenek siarki().
3. Doświadczenie powtórzono dla pozostałych trzech tlenków wsypując je do roztworu wody ze wskaźnikiem uniwersalnym
Obserwacje:
W probówkach do których dodano: tlenek siarki(), suchy lód oraz tlenek fosforu() roztwór zmienił barwę z zielonego na czerwone. Natomiast w probówce z tlenkiem krzemu() brak zmian.
Wyniki:
W probówkach, w których znalazły się tlenki: siarki(), węgla() oraz fosforu() doszło do spadku pH. W przypadku probówki z tlenkiem krzemu() nie doszło do zmian pH.
Wnioski:
W probówkach, w których nastąpiła zmiana koloru z zielonej na czerwoną jako produkt powstał kwas. Za zmianę zabarwienia odpowiada wskaźnik uniwersalny, który w środowisku kwasowym przyjmuje czerwone zabarwienie. Tlenek krzemu() nie reaguje z wodą, brak widocznych objawów reakcji. Tlenek siarki(), zestalony tlenek węgla() oraz tlenek fosforu() reagują z wodą w wyniku czego powstają odpowiednie kwasy tlenowe. Hipoteza została potwierdzona.
Dlaczego w powyższym doświadczeniu wykorzystujemy wskaźnik kwasowo‑zasadowy?
Reakcje tlenków kwasotwórczych z wodą biegną według następującego schematu:
W wyniku reakcji chemicznej tlenku kwasotwórczego z wodą powstaje odpowiedni kwas tlenowy.
Zapisz równanie reakcji tlenku siarki() z wodą w formie cząsteczkowej.
Wzór tlenku:
Równanie reakcji z wodą:
W wyniku reakcji tlenku siarki() z wodą powstaje kwas siarkowy().
Jak łatwo zauważyć, stopień utlenienia atomu siarki w wyniku reakcji nie zmienia się.
Zapisz równanie reakcji otrzymywania kwasu fosforowego() z odpowiedniego tlenku i wody w formie cząsteczkowej. Zapisz wzór tlenku.
Wzór kwasu:
Stopień utlenienia atomu fosforu:
Wzór tlenku:
Równanie reakcji:
Tlenek węgla() jest bezwodnikiem kwasu węglowego. Kwas węglowy jest kwasem nietrwałym, dlatego też reakcja ta jest odwracalna. Zapisz równanie reakcji tlenku węgla() z wodą.
Równanie reakcji:
Ze względu na nietrwałość kwasu węglowego równanie reakcji zapisywane jest z dwiema strzałkami (reakcja odwracalna).
Jedną z metod otrzymywania kwasu azotowego() jest reakcja tlenku azotu() z wodą. W wyniku tej reakcji chemicznej powstaje mieszanina kwasów –
azotowego() i azotowego().
Kwas azotowy() ulega rozkładowi:
Sumarycznie równania powyższych reakcji chemicznych można zapisać jako:
Reakcja tlenku azotu() z wodą to przykład szczególnej reakcji redoks zwanej reakcją dysproporcjonowania.
Otrzymywanie kwasu przez wypieranie go z jego soli
Kwasy, których nie da się otrzymać w wyniku reakcji odpowiedniego tlenku z wodą, otrzymuje się zazwyczaj z ich soli. Na taką sól działa się innym mocnym kwasem (mocniejszym, niż ten wypierany), w wyniku czego interesujący nas kwas zostaje wyparty z soli.
W wirtualnym laboratorium otrzymaj wybrany przez siebie kwas metodą wypierania go ze swojej soli. Zapoznaj się z problemem badawczym oraz postaw hipotezę badawczą. Sporządź notatkę, w której zapiszesz własne obserwacje, wyniki i wnioski.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D2VEGKVMK
Zadanie: jak otrzymać kwas poprzez wypieranie go z soli.
Analiza eksperymentu: Otrzymywanie kwasu poprzez wypieranie go z jego soli.
Problem badawczy: Czy w reakcji soli z mocnym kwasem zawsze dochodzi do powstania innego kwasu?
Hipoteza: Powstanie kwasu następuje jedynie w wyniku reakcji soli słabego kwasu z mocnym kwasem.
Sprzęt laboratoryjny: probówki - podłużne naczynie szklane do przeprowadzania prostych reakcji chemicznych; pipety - wąska rurka pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki; statyw na probówki - prostokątny sprzęt laboratoryjny z rzędami otworów, w których umieszczane są probówki.
Odczynniki chemiczne: kwas chlorowodorowy; siarczek sodu (ciało stałe); siarczan(IV) potasu (ciało stałe); węglan wapnia (ciało stałe); siarczan(VI) baru (ciało stałe).
Przebieg eksperymentu: Do każdej z probówek dodano małą ilość soli zgodnie z kolejnością położenia na półce. Następnie dodano kwas chlorowodorowy. Probówkę z siarczkiem sodu oraz siarczanem(IV) potasu dodatkowo podgrzewano.
Obserwacje: W probówkach z siarczan(IV) potasu, siarczkiem sodu i węglanem wapnia ciała stałe uległy roztworzeniu, wydzieliły się bezbarwne gazy. Gaz wydzielający się z probówki z węglanem był bezwonny, z probówki z siarczkiem sodu - miał charakterystyczny zapach zgniłych jaj, a z probówki z siarczanem(IV) potasu - charakterystyczny drażniący zapach. W probówce z siarczanem(VI) baru nie zaobserwowano zmian.
Wyniki: W przypadku węglanu wapnia, siarczku sodu i siarczanu(IV) potasu doszło do reakcji z kwasami, czego efektem było wydzielanie się gazów. W przypadku siarczanu(VI) baru nie zaobserwowano żadnej reakcji z kwasami.
Wnioski: Kwas chlorowodorowy jest kwasem mocniejszym od kwasu siarkowego(IV), węglowego i siarkowodorowego dlatego wypiera je z ich soli oraz roztworów ich soli. Nie wypiera jednak kwasu siarkowego(VI), który to jest kwasem mocnym. Hipoteza została potwierdzona.
Równania reakcji chemicznej: 1. Węglan wapnia z kwasem chlorowodorowym: jedna cząsteczka węglanu wapnia + dwie cząsteczki chlorowodoru dają jedną cząsteczkę chlorku wapnia + jedną cząsteczkę wody + jedną cząsteczkę dwutlenku węgla. 2. Siarczek sodu z kwasem chlorowodorowym: jedna cząsteczka siarczku sodu + dwie cząsteczki chlorowodoru daje dwie cząsteczki chlorku sodu + jedna cząsteczka siarkowodoru. 3. Siarczan(IV) potasu z kwasem chlorowodorowym: jedna cząsteczka siarczanu(IV) potasu + dwie cząsteczki chlorowodoru daje dwie cząsteczki chlorku potasu + jedna cząsteczka wody + jedna cząsteczka dwutlenku siarki. 4. Siarczan(VI) baru z kwasem chlorowodorowym: reakcja nie zachodzi.
\ Wypierany kwas jest słabszy niż kwas działający na sól. Reakcja przebiega według schematu:
sól słabego kwasu + mocny kwas → słaby kwas + sól mocnego kwasu
Gdy do roztworu octanu sodu () doda się kwas solny (np. ), to równanie omawianej reakcji chemicznej wygląda następująco:
Jak widać, w wyniku powyższej reakcji otrzymano chlorek sodu oraz kwas octowy (etanowy). Octan (etanian) sodu jest solą złożoną z kationu metalu oraz anionu reszty kwasu octowego, który jest słabym kwasem ( = 1,8 · 10Indeks górny -5-5). Natomiast kwas solny jest kwasem mocnym ( = 1,0 · 10Indeks górny 77; ) , który wyparł kwas słabszy (kwas octowy) z roztworu jego soli.
Jak otrzymać kwas siarkowy(VI) z pierwiastków?1
Przeanalizuj poniższą symulację. Sprawdź, w jaki sposób odbywa się przemysłowe otrzymywanie kwasu siarkowego(), jaka temperatura jest wykorzystywana do tego procesu, a następnie rozwiąż ćwiczenia sprawdzające.
Przeanalizuj opis symulacji. Sprawdź, w jaki sposób odbywa się przemysłowe otrzymywanie kwasu siarkowego(), jaka temperatura jest wykorzystywana do tego procesu, a następnie rozwiąż ćwiczenia sprawdzające.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D2VEGKVMK
