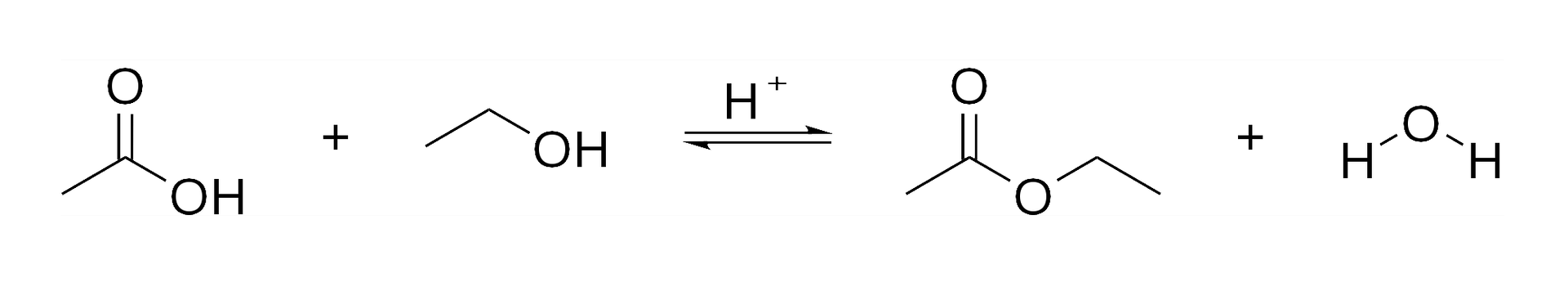
Otrzymywanie estrów
Estryfikacja
Estry powstają w wyniku kondensacji kwasów (organicznych lub nieorganicznych) i alkoholi lub fenoli. Jedną z najpopularniejszych metod jest reakcja kwasu karboksylowego i alkoholu w środowisku kwasu, najczęściej jest to kwas siarkowy().
Jak przebiega proces estryfikacji?
Zapoznaj się z poniższym filmem, a następnie rozwiąż zadania.

Film dostępny pod adresem /preview/resource/RCPi7v8Nydlww
Film omawia rolę kwasu siarkowego(VI) w reakcji estryfikacji na przykładzie reakcji otrzymywania octanu butylu. Przedstawiono również mechanizm reakcji estryfikacji.
Uzasadnij, w jakim celu do mieszaniny reakcyjnej alkoholu i kwasu karboksylowego dodaje się stężony kwas siarkowy(VI).
Na co wpływa dodany nadmiar kwasu siarkowego(VI) do układu reakcyjnego (podczas reakcji estryfikacji)?
={R1VxhFuMh30Y4
Pamiętaj, że proces estryfikacji zachodzi zgodnie z mechanizmem substytucji nukleofilowej.
W wyniku reakcji estryfikacji następuje zastąpienie grupy hydroksylowej , pochodzącej z kwasu karboksylowego, i podłączenie grupy alkoholu. Reakcje można przedstawić następująco;
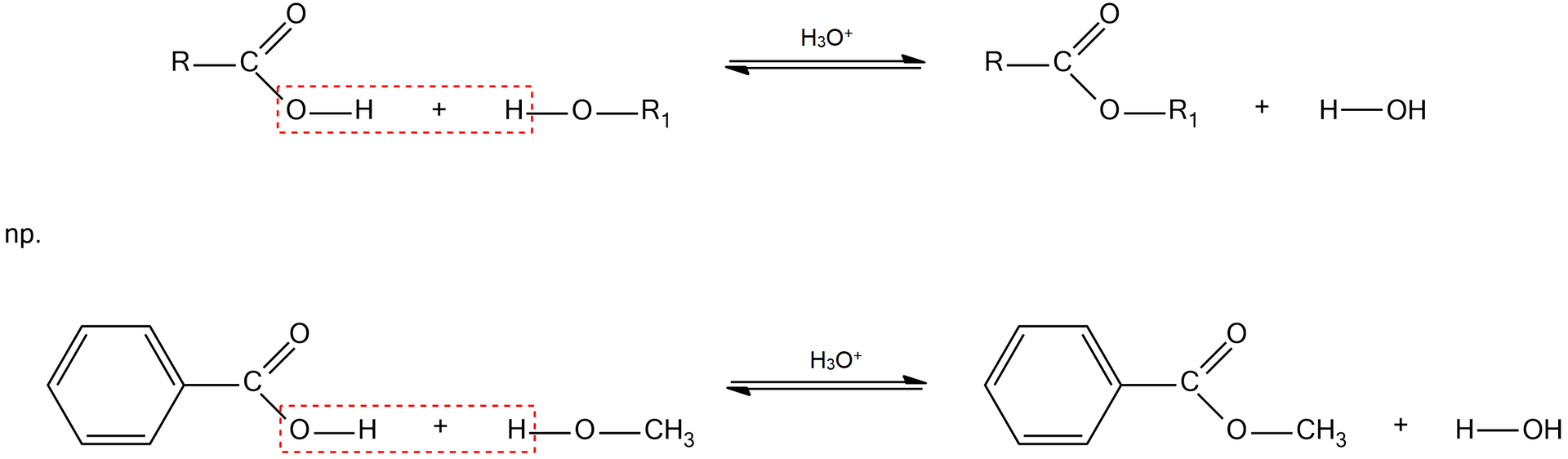
Jak możesz zauważyć w równaniu reakcji, pomiędzy substratami a produktami narysowana jest strzałka w dwie strony. Oznacza to, że reakcja jest odwracalna i przebiega z zachowaniem równowagi chemicznej. Kwas nieorganiczny w tej reakcji pełni rolę katalizatora i jest niezbędny do jej przeprowadzania, jako katalizatora używa się kwasu siarkowego (VI) ze względu na jego właściwości higroskopijne. Po pewnym czasie ustala się stan równowagi – mówiąc prościej, stosunek ilości substratów do produktów jest stały i się nie zmienia – oznacza to, że nie możemy otrzymać produktu np: ze wydajnością. By zwiększyć wydajność reakcji, należy na bieżąco usuwać ester z układu reakcyjnego np.: poprzez destylację. Zwiększenie wydajności reakcji zachodzi zgodnie z regułą przekory. Jak widzisz, w reakcji powstaje również cząsteczka wody. Gdybyśmy do mieszaniny reakcyjnej dodali wody, równowaga chemiczna reakcji przesunęłaby się w stronę substratów. Dlatego używane w nich estry charakteryzują się małą trwałością. Podczas pocenia się nasz organizm wydziela wodę, która powoduje rozkład estru do kwasu karboksylowego i alkoholu.
Estry powstają również w wyniku reakcji chlorków kwasowych z alkoholami.
Alkoholiza to reakcja, której ulegają np. estry, bezwodniki i chlorki kwasowe:
Alkoholiza chlorku kwasowego:
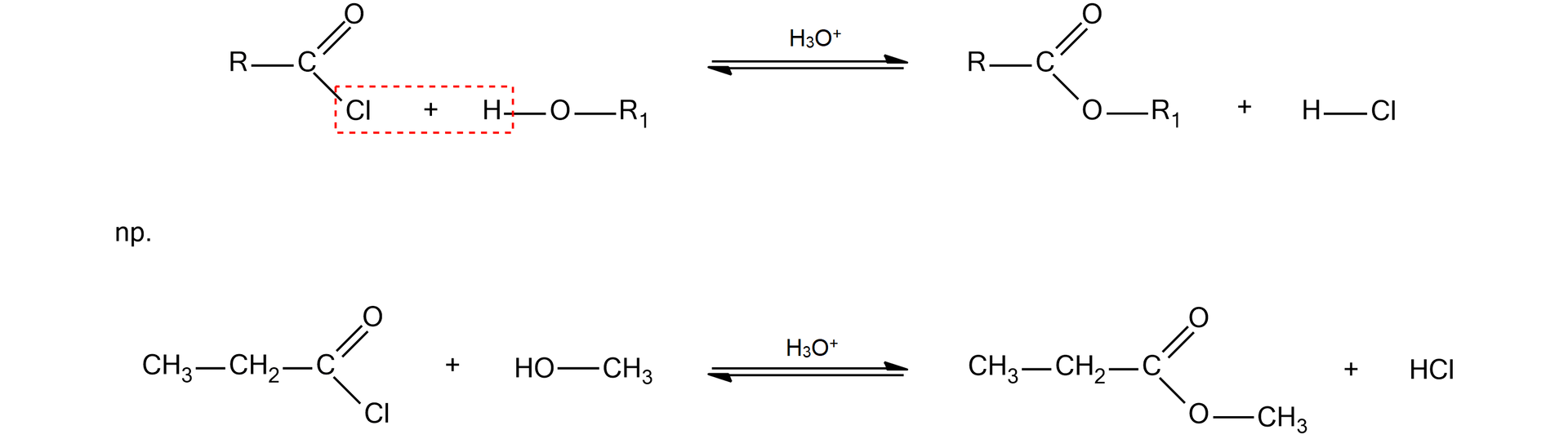
Alkoholiza bezwodnika kwasowego:
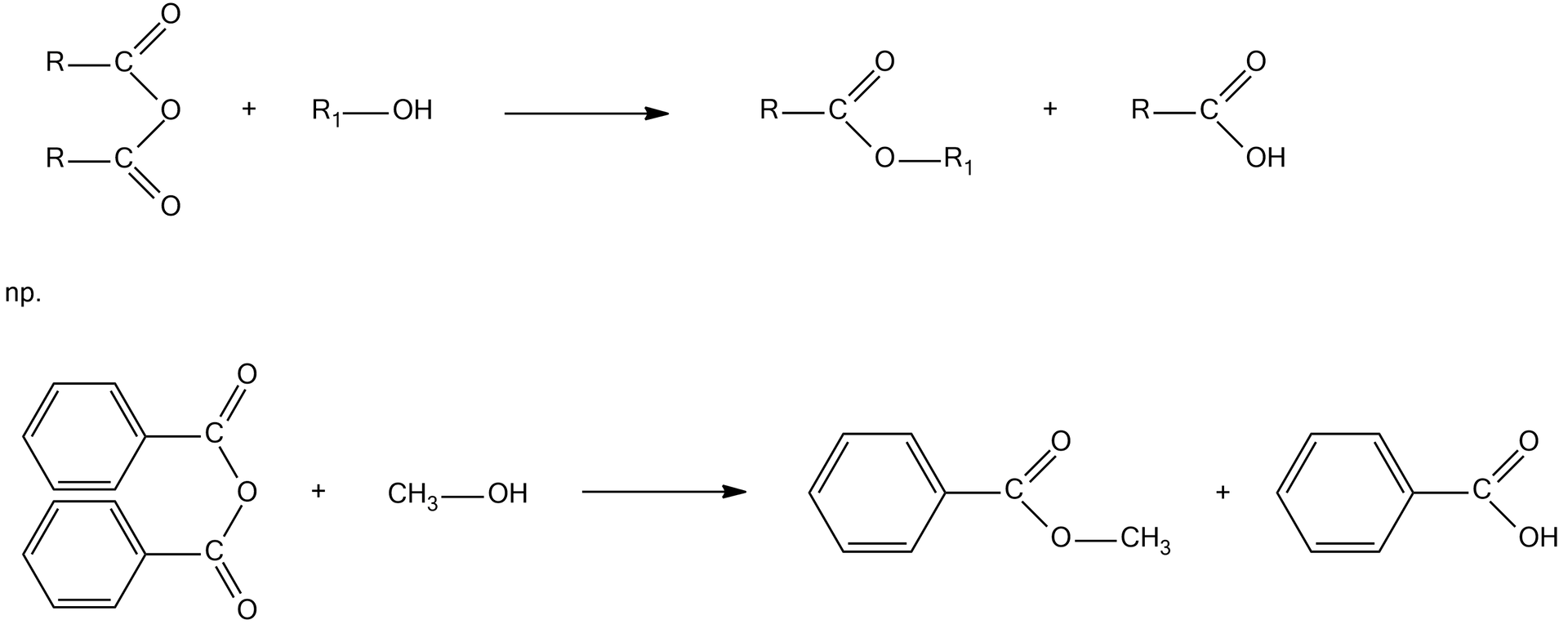
Poniżej spróbuj przeprowadzić reakcje estryfikacji w poniższych wirtualnych laboratoriach oraz rozwiąż ćwiczenia.
Przeprowadź doświadczenie w laboratorium chemicznym. Rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz swoje obserwacje i wyniki, a następnie sformułuj wnioski.
Szafka laboratoryjna
Przeprowadzono doświadczenie mające na celu zbadanie reakcji alkoholi z kwasami. Zapoznaj się z opisem, a następnie wykonaj ćwiczenie.
Analiza doświadczenia: Badanie reakcji alkoholi z kwasami.
Problem badawczy: Jakie produkty otrzymamy w reakcji alkoholi z kwasami?
Hipoteza: Alkohole reagują z kwasami, tworząc estry.
Odczynniki:
etanol,
kwas octowy,
kwas siarkowy().
Sprzęt laboratoryjny:
cztery zlewki – naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych,
łyżka laboratoryjna – długi trzonek wykonany ze szkła, porcelany lub metalu zakończony z jednej strony łyżeczką. Służy do nabierania sypkich substancji chemicznych,
pipety Pasteura – wąska rurka do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki,
palnik – rodzaj sprzętu z regulacją płomienia, umożliwiający podgrzewanie substancji chemicznych,
trójnóg – urządzenie w kształcie pierścienia, zaopatrzone w trzy wkręcane nogi, mocowane prostopadle do jego powierzchni, służące do ustawiania nad palnikiem naczyń laboratoryjnych, przeznaczonych do podgrzania,
dwie szalki Petriego – naczynia laboratoryjne w kształcie okrągłej podstawki (spodka) o szerokim, płaskim dnie i niskich (w stosunku do średnicy) ścianach bocznych, wykonane ze szkła lub przezroczystych tworzyw sztucznych,
drewniane szczypce – rodzaj trzymaka służący do uchwycenia probówki lub małej kolby stożkowej,
trzy probówki – podłużne naczynia szklane do przeprowadzania prostych reakcji chemicznych,
statyw na probówki – prostokątny sprzęt laboratoryjny z rzędami otworów, w których umieszczane są probówki.
Przebieg doświadczenia:
Do probówki wlano etanolu i kwasu etanowego.
Następnie dodano stężonego kwasu siarkowego().
Probówkę ogrzewano w łaźni wodnej. Ostrożnie powąchano powstałą substancję, wachlując ręką powstałe opary w kierunku nosa.
Obserwacje:
Barwa roztworu nie zmienia się.
Jeśli przeprowadzasz doświadczenie w laboratorium chemicznym: W probówce powstała substancja o innym zapachu niż substraty. Jej zapach przypomina zapach kleju lub zmywacza do paznokci.
Wyniki:
Etanol uległ reakcji z kwasem octowym.
Wnioski:
Między alkoholem i kwasem octowym zaszła reakcja, w wyniku której powstała inna substancja. Kwas octowy reaguje z etanolem w obecności kwasu siarkowego(). W wyniku reakcji powstały: octan etylu i woda. W wyniku reakcji kwasów z alkoholami powstają estry – jest to reakcja estryfikacji.
Z dostępnych w wirtualnym laboratorium związków, otrzymaj wszystkie możliwe estry. Sformułuj problem badawczy i zweryfikuj własną hipotezę. W formularzu zanotuj swoje obserwacje i wyniki, a następnie zapisz wnioski. Następnie rozwiąż poniższe zadania.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D4A6XQPM8
W wirtualnym laboratorium badano powstawanie estrów. Zapoznaj się poniższym opisem doświadczenia, a następnie rozwiąż zamieszczone pod nim ćwiczenia.
Analiza eksperymentu:
Otrzymywanie estrów.
Problem badawczy:
Czy w reakcji kwasu karboksylowego z alkoholem w środowisku kwasowym powstają estry?
Hipoteza:
Estry powstają w reakcji odpowiedniego kwasu karboksylowego oraz alkoholu w środowisku kwasowym.
Sprzęt i szkło laboratoryjne:
probówki – podłużne U‑kształtne naczynia szklane służące do przeprowadzania prostych reakcji chemicznych;
pipety – wąskie rurki służące do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
statyw na probówki – prostokątny sprzęt laboratoryjny z rzędami otworów, w których umieszczane są probówki;
łaźnia wodna – może być zmontowana samodzielnie poprzez użycie zlewki wypełnionej wodą i umieszczenie jej w płaszczu grzejnym bądź można wykorzystać w tym celu termostat.
Odczynniki chemiczne:
pentanol; butanol; etanol; kwas octowy, kwas mrówkowy, kwas butanowy, stężony kwas siarkowy().
Przebieg doświadczenia:
1. Dodanie do probówki dwóch centymetrów sześciennych wybranego alkoholu.
2. Następnie dodanie do probówki z alkoholem dwóch centymetrów sześciennych wybranego kwasu karboksylowego.
3. Dodanie do probówki zawierającej mieszaninę alkoholu oraz kwasu karboksylowego kropli stężonego kwasu siarkowego().
4. Ogrzanie mieszaniny w łaźni wodnej.
5. Powtórzenie czynności dla wszystkich dostępnych alhoholi oraz kwasów.
Obserwacje:
Po ogrzaniu zawartości probówek zaobserwowano, że z ich wnętrza ulatniają się charakterystyczne słodkie, owocowe zapachy.
Wyniki:
Otrzymane produkty to octan etylu, octan butylu, octan pentylu, maślan etylu, maślan butylu, maślan pentylu, mrówczan etylu, mrówczan butylu oraz mrówczan pentylu.
Wnioski:
Estry powstają w reakcji odpowiedniego kwasu karboksylowego oraz alkoholu w środowisku kwasowym w warunkach ogrzewania. W doświadczeniu otrzymano dziewięć estrów o różnych zapachach, które ogólnie można określić jako słodkie oraz owocowe.
Jakie znaczenie ma obecność kwasu siarkowego()?