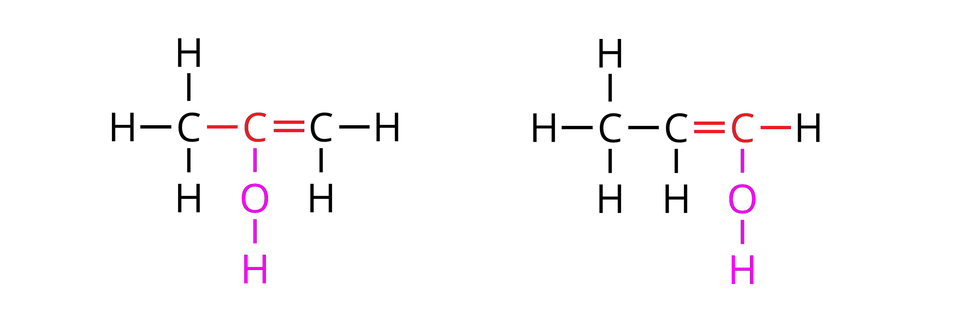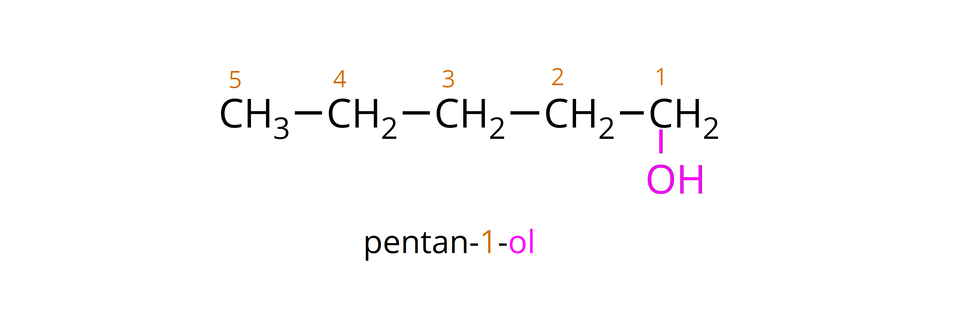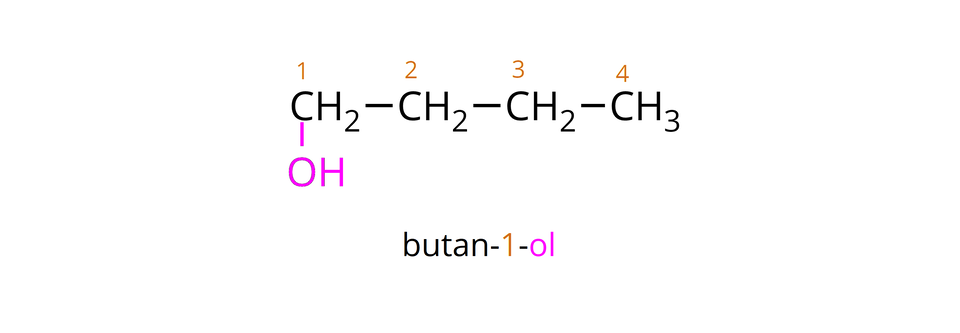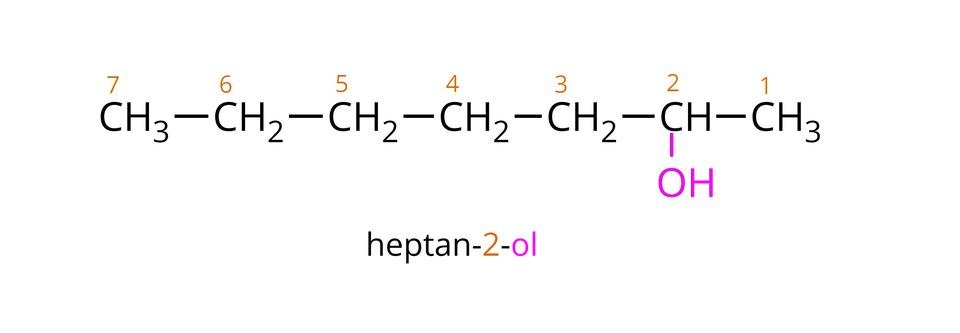Właściwości alkoholi monohydroksylowych
Poniższy materiał stanowi uzupełnienie treści znajdujących się w materiale: https://zpe.gov.pl/a/alkohole–wlasciwosci/D1GBDQith
Nieznajomość pewnego zjawiska fizycznego, dotyczącego etanolu, w drugiej połowie niemal doprowadziło sędziów do uwięzienia na długie lata niewinnego człowieka. O jakie zjawisko dokładnie chodzi i z jakimi właściwościami alkoholi jest ono związane?
budowę alkoholi;
tworzenie nazw alkoholi;
sposób przedstawiania budowy alkoholi za pomocą wzorów;
definicję szeregu homologicznego;
przykłady właściwości substancji zaliczanych do właściwości fizycznych oraz przykłady właściwości zaliczanych do właściwości chemicznych.
projektować i przeprowadzać doświadczenie, które pozwoli na zbadanie rozpuszczalności wybranych alkoholi w wodzie oraz ich temperatur wrzenia;
wyjaśniać wpływ długości łańcucha węglowodorowego w cząsteczkach alkoholi na ich temperatury wrzenia i topnienia oraz na rozpuszczalność w wodzie;
omawiać zmiany wybranych właściwości fizycznych w szeregu homologicznym nasyconych alkoholi monohydroksylowych, o prostych (nierozgałęzionych) łańcuchach węglowych;
projektować i przeprowadzać doświadczenie, za pomocą którego zbadasz odczyn wodnych roztworów wybranych alkoholi;
wskazywać produkty reakcji spalania alkoholi w zależności od dostępności tlenu.
1. Alkohole – budowa
Definicja
Alkohole to pochodne węglowodorów, w których przynajmniej jeden atom wodoru został zastąpiony grupą hydroksylową ().
Jeżeli w cząsteczce alkoholu znajduje się tylko jedna grupa hydroksylowa, to taki alkohol nazywamy monohydroksylowym. Jeśli zaś w cząsteczce alkoholu występują co najmniej dwie grupy hydroksylowe, jest to alkohol polihydroksylowy.
Ogólny wzór alkoholi monohydroksylowych można zapisać jako:
gdzie: – łańcuch węglowodorowy; – grupa hydroksylowa, będąca grupą funkcyjną alkoholi.
AlkoholeAlkohole, podobnie jak węglowodory, z których się wywodzą, mogą być nasycone i nienasycone. Te nasycone to takie, w których cząsteczkach wszystkie atomy węgla połączone są za pomocą wiązań pojedynczych. Nienasycone zaś to z kolei takie, w których cząsteczkach między atomami węgla znajduje się przynajmniej jedno wiązanie wielokrotne (podwójne lub potrójne).
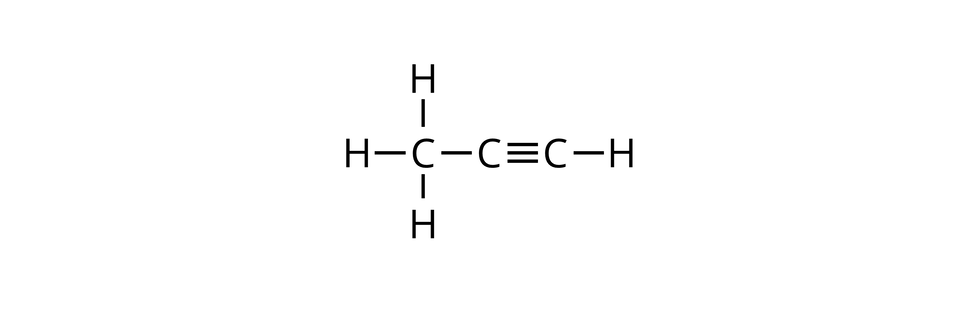
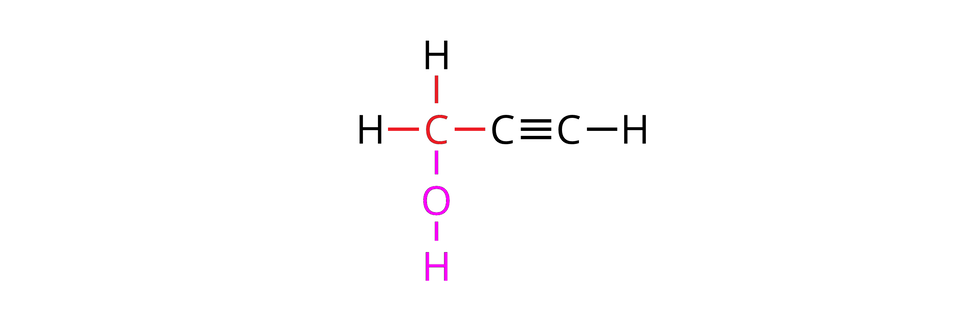
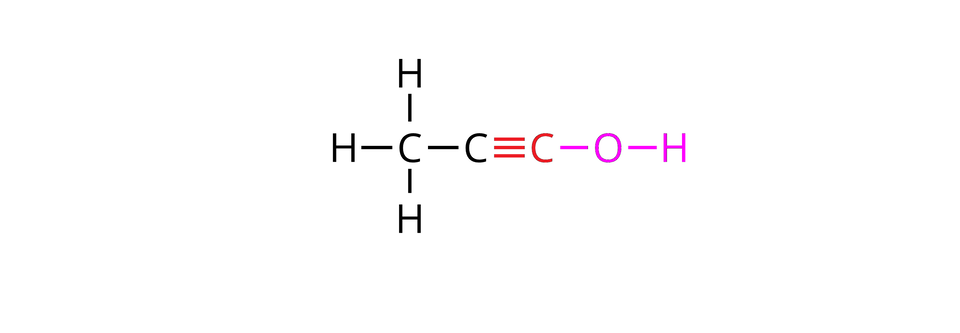
Jednak nie wszystkie pochodne węglowodorów nienasyconych, w cząsteczkach których atom bądź atomy wodoru zastąpione zostały grupami hydroksylowymi, będą zaliczane do grupy alkoholi. Warunkiem klasyfikacji danego związku chemicznego do rodziny alkoholi jest obecność grupy hydroksylowej przy atomie węgla, który z innymi atomami w cząsteczce rozpatrywanego związku jest połączony wyłącznie za pomocą wiązań pojedynczych.
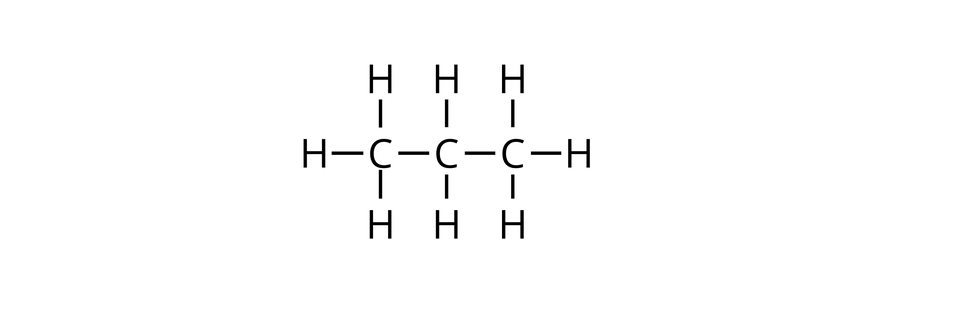
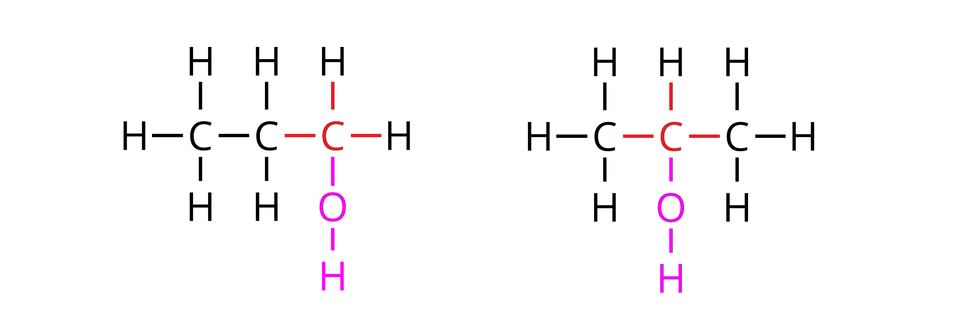
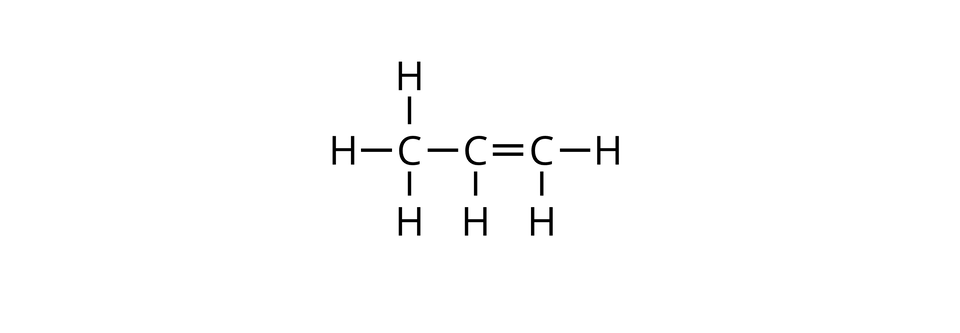
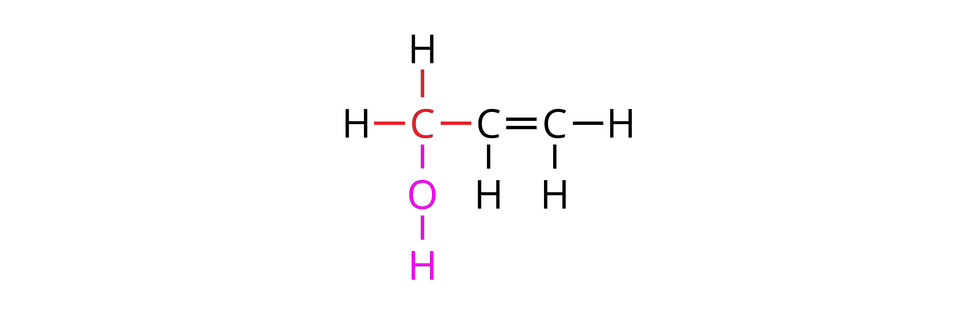
W poniższej galerii znajdują się wzory strukturalne węglowodorów łańcuchowych (alifatycznych), których cząsteczki zbudowane są z trzech atomów węgla oraz wzory strukturalne ich pochodnych, zawierających po jednej grupie hydroksylowej w cząsteczkach. Zapoznaj się ze wzorami zamieszczonymi w galerii, a następnie wykonaj ćwiczenie.
2. Szereg homologiczny alkoholi monohydroksylowych, będących pochodnymi alkanów
Alkohole, podobnie jak węglowodory, tworzą szeregi homologiczneszeregi homologiczne. Ogólny wzór szeregu homologicznego alkanów (węglowodorów nasyconych) ma postać: , gdzie to liczba atomów węgla w cząsteczce. Jeżeli we wzorze zastąpimy jeden atom wodoru jedną grupą hydroksylową (), to uzyskamy wzór ogólny dowolnego szeregu homologicznego nasyconych alkoholi monohydroksylowych (o budowie łańcuchowej):
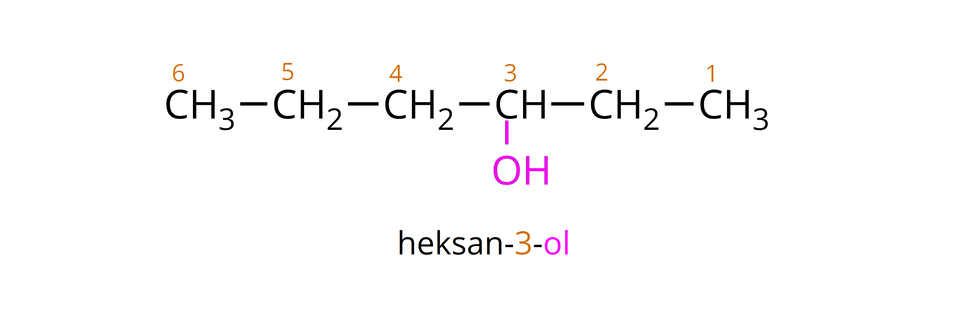
Nazwy systematyczne alkoholi, będących pochodnymi alkanów, tworzymy od nazw sytematycznych alkanów o tej samej liczbie atomów węgla w cząsteczkach, dodając do nich przyrostek . Jeżeli cząsteczka alkoholu zawiera co najmniej trzy atomy węgla, to przed przyrostkiem „–ol”, musimy wpisać cyfrę oznaczającą (położenie) grupy hydroksylowej. Innymi słowy, przed wspomnianym przyrostkiem zapisujemy numer atomu węgla w cząsteczce alkoholu, do którego przyłączona jest grupa . Należy przy tym pamiętać, aby ponumerować atomy węgla w łańcuchu, rozpoczynając od tego ze skrajnych atomów węgla, którego grupa hydroksylowa znajduje się bliżej. W poniższej galerii znajdują się wzory półstrukturalne oraz nazwy systematyczne wybranych nasyconych alkoholi monohydroksylowych, których cząsteczki utworzone są z atomów węgla, połączonych w prosty (nierozgałęziony) łańcuch.
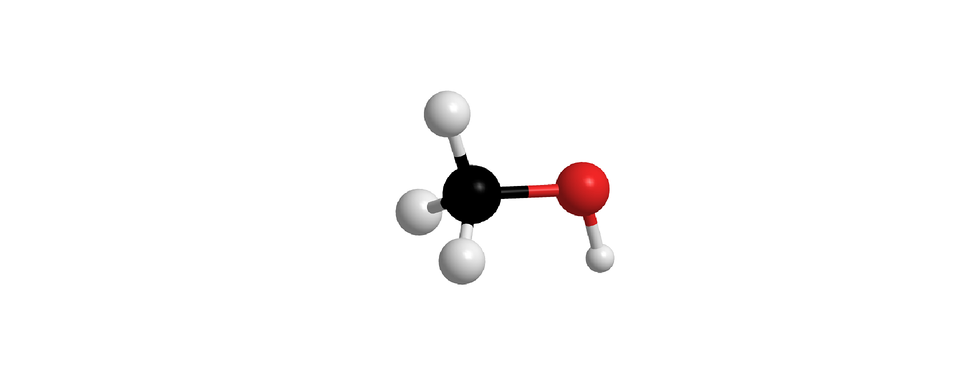
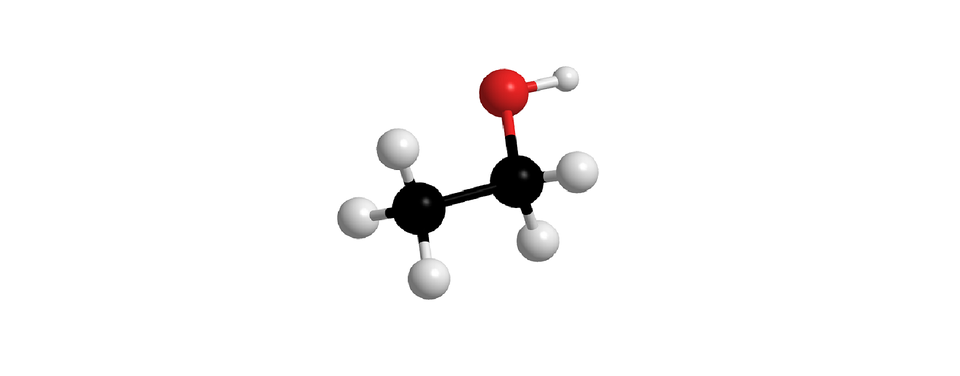
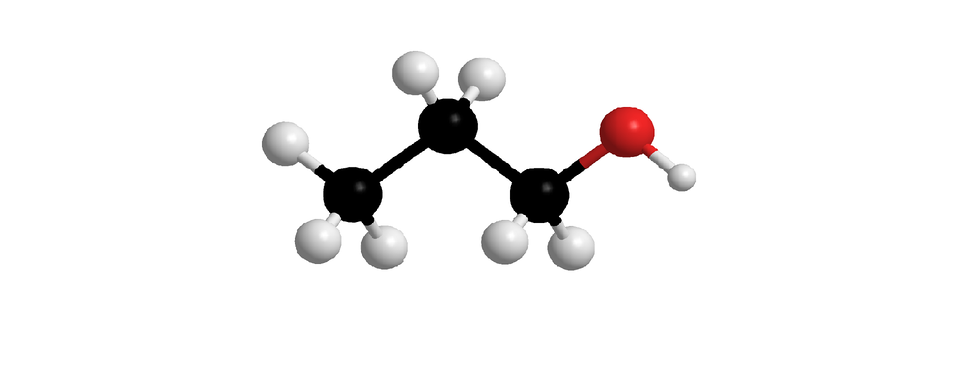
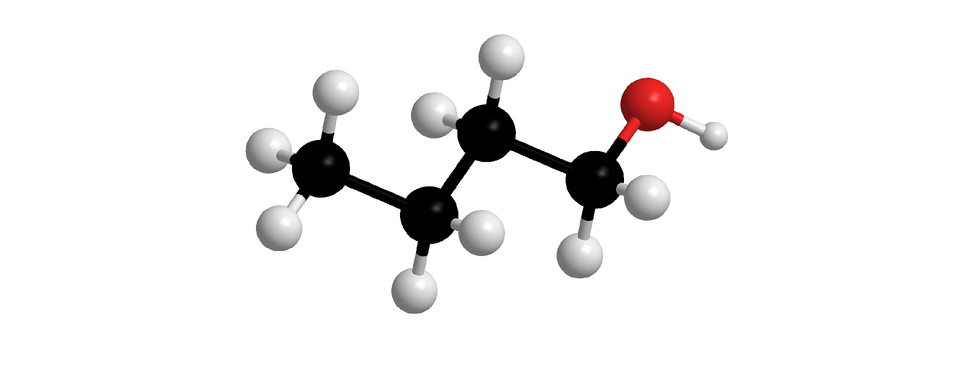
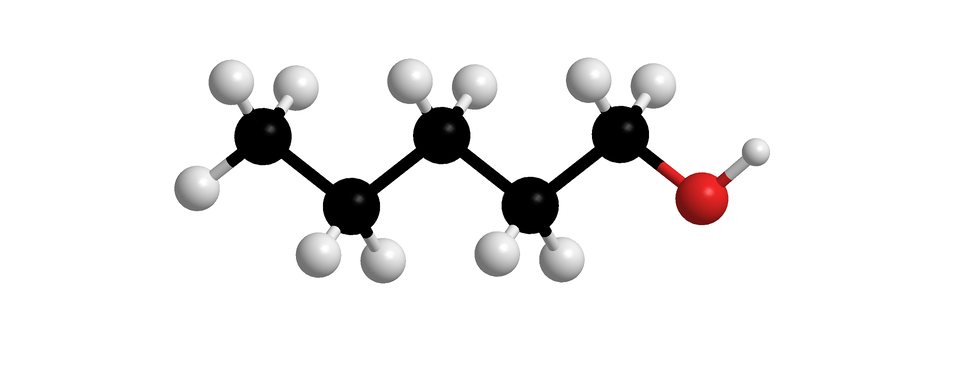
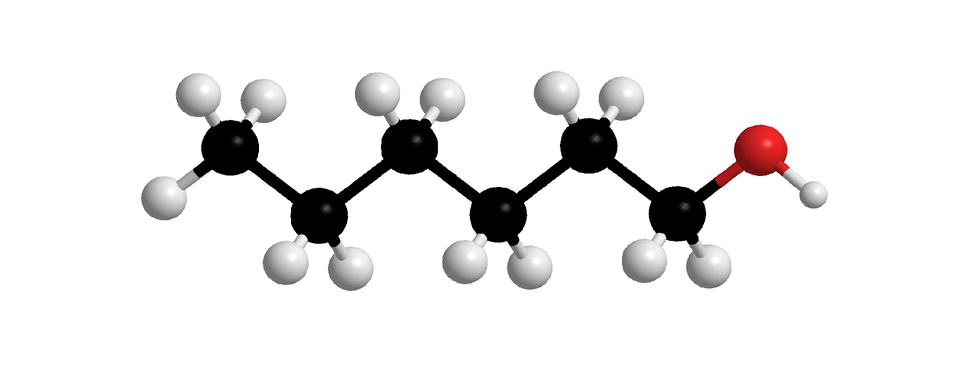
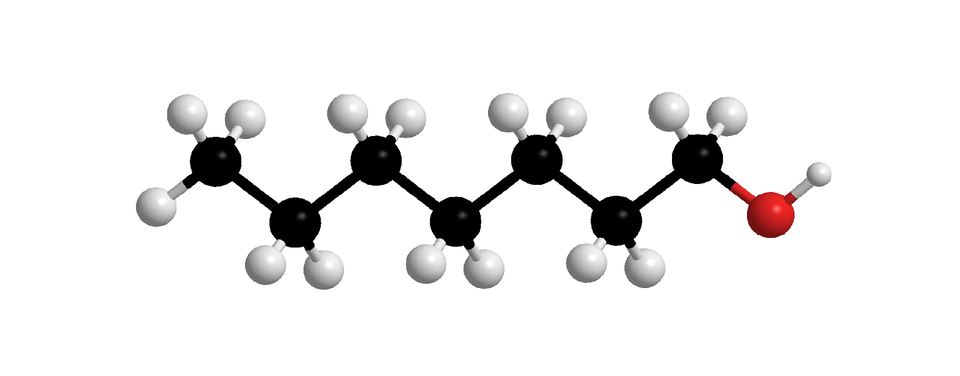
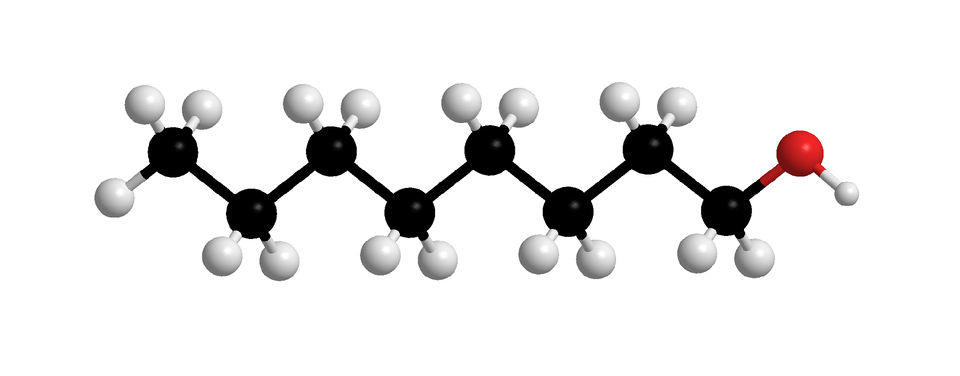
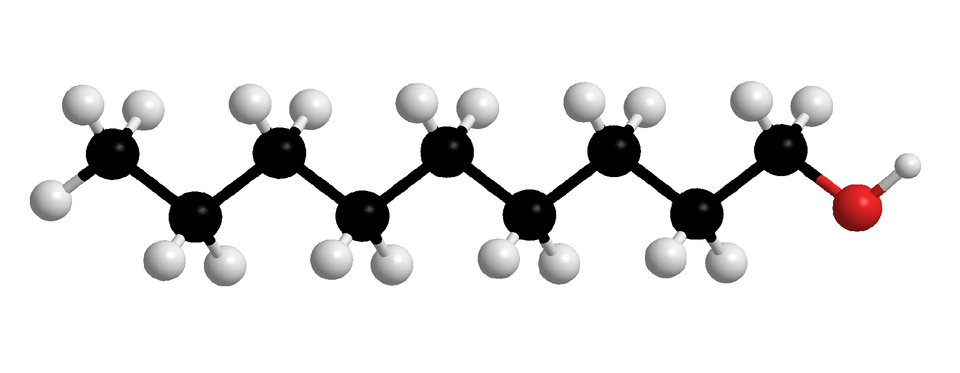
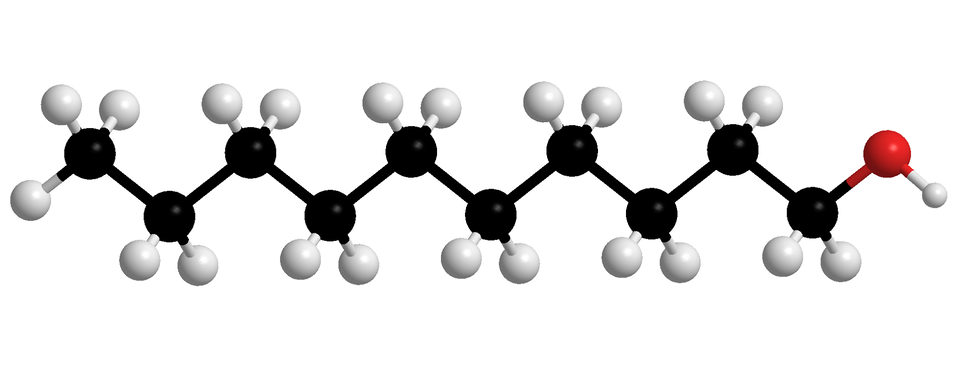
W poniższej tabeli zaprezentowano z kolei nazwy systematyczne i modele cząsteczek nasyconych alkoholi monohydroksylowych, o prostych (nierozgałęzionych) łańcuchach węglowych. W każdej z nich grupa hydroksylowa przyłączona jest do pierwszego atomu węgla. Związki chemiczne wymienione w poniższej tabeli to pierwsze dziesięć alkoholi z szeregu homologicznego nasyconych alkoholi monohydroksylowych.
Liczba atomów węgla w cząsteczce | Wzór uproszczony z uwzględnieniem grupy funkcyjnej | Model cząsteczki | Nazwa |
|---|---|---|---|
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | |||
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | |||
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | |||
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | |||
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | |||
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | |||
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | |||
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | |||
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | |||
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |
Indeks górny źródło: John McMurry, Chemia organiczna, Tom I, 2000. Indeks górny koniecźródło: John McMurry, Chemia organiczna, Tom I, 2000.
Indeks górny Fragment szeregu homologicznego alkan––oli (nasyconych alkoholi monohydroksylowych, w których cząsteczkach, grupa przyłączona jest do pierwszego atomu węgla). W tabeli zamieszczono wzory uproszczone, modele cząsteczek i nazwy alkoholi, których cząsteczki zbudowane są z od jednego do dziesięciu atomów węgla, połączonych w prosty (nierozgałęziony) łańcuch. Indeks górny koniecFragment szeregu homologicznego alkan––oli (nasyconych alkoholi monohydroksylowych, w których cząsteczkach, grupa przyłączona jest do pierwszego atomu węgla). W tabeli zamieszczono wzory uproszczone, modele cząsteczek i nazwy alkoholi, których cząsteczki zbudowane są z od jednego do dziesięciu atomów węgla, połączonych w prosty (nierozgałęziony) łańcuch.
Indeks dolny Modele: GroMar Sp. z o.o. licencja: CC BY‑SA 3.0 Indeks dolny koniecModele: GroMar Sp. z o.o. licencja: CC BY‑SA 3.0
3. Nasycone alkohole monohydroksylowe – właściwości fizyczne
HomologiHomologi, a więc związki chemiczne należące do tego samego szeregu homologicznego, na ogół różnią się właściwościami fizycznymi.
Nasycone alkohole monohydroksylowe, których najprostszym przedstawicielem (pod względem budowy) jest metanol (), to bezbarwne substancje, będące w temperaturze pokojowej cieczami lub ciałami stałymi.
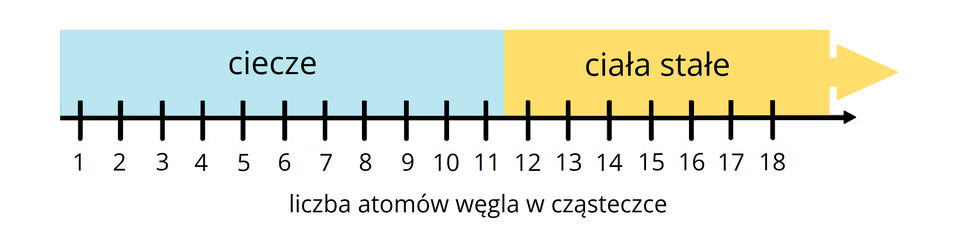
Alkohole, których cząsteczki zbudowane są z od do atomów węgla połączonych w prosty (nierozgałęziony) łańcuch to w temperaturze pokojowej ciecze. Z kolei alkohole, które zawierają w cząsteczkach przynajmniej 12 atomów węgla, połączonych w prosty (nierozgałęziony) łańcuch, to w temperaturze pokojowej ciała stałe.
Wraz ze zmianą liczby atomów węgla w cząsteczkach alkoholi, zmienia się również ich gęstość. Im więcej atomów węgla znajduje się w cząsteczkach, a więc z im dłuższych łańcuchów węglowych zbudowane są cząsteczki alkoholi, tym większa jest gęstość tych alkoholi.
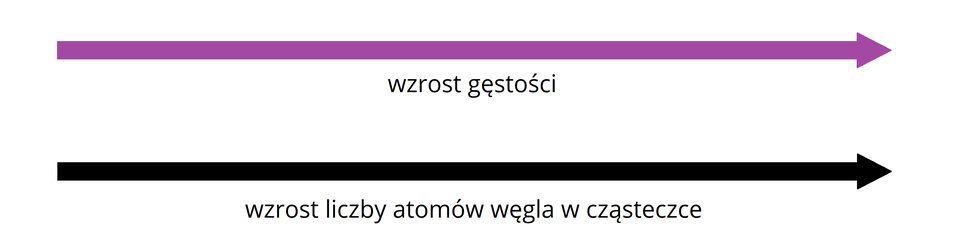
Wzrost liczby atomów węgla w cząsteczkach alkoholi powoduje również pewną zmianę ich temperatur wrzenia i topnienia.
W poniższej tabeli znajdują się zapisane w przypadkowej kolejności nazwy alkoholi oraz odpowiadające im temperatury wrzenia i topnienia. Narysuj wykres słupkowy, który przedstawia zależność temperatur wrzenia i topnienia nierozgałęzionych, nasyconych alkoholi monohydroksylowych od liczby atomów węgla w ich cząsteczkach. Następnie określ ogólną zależność pomiędzy temperaturami wrzenia i topnienia wspomnianych alkoholi a liczbą atomów węgla w ich cząsteczkach.
Nazwa alkoholu | Temperatura wrzenia, | Temperatura topnienia, |
|---|---|---|
heksan––ol | ||
propan––ol | ||
oktan––ol | ||
etanol | ||
butan––ol | ||
nonan––ol | ||
heptan––ol | ||
dekan––ol | ||
metanol | ||
pentan––ol |
Indeks górny Źródło: W. Mizerski, Tablice chemiczne, Warszawa 2004 Indeks górny koniecŹródło: W. Mizerski, Tablice chemiczne, Warszawa 2004
Na słupkowym wykresie interaktywnym przedstawiono zależności pomiędzy temperaturami wrzenia i topnienia wspomnianych alkoholi a liczbą atomów węgla w ich cząsteczkach. Zapoznaj się z poniższym opisem, a następnie wykonaj polecenie.
Temperatura wrzenia ():
atom węgla –
atomy węgla –
atomy węgla –
atomy węgla –
atomów węgla –
atomów węgla –
atomów węgla –
atomów węgla –
atomów węgla –
atomów węgla –
Temperatura topnienia ():
atom węgla –
atomy węgla –
atomy węgla –
atomy węgla –
atomów węgla –
atomów węgla –
atomów węgla –
atomów węgla –
atomów węgla –
atomów węgla –
Musisz wiedzieć, że wszystkie indywidua chemiczne, a więc również cząsteczki, oddziałują ze sobą za pomocą różnorodnych sił i oddziaływań. Jeśli przeanalizujemy cząsteczki alkoholi zbudowane z prostych (nierozgałęzionych) łańcuchów węglowych, to oczywistym jest, że wraz ze wzrostem liczby atomów węgla, rosną masy tych cząsteczek. Ponieważ zwiększa się jednocześnie długość łańcucha węglowego, to rośnie także liczba oddziaływań pomiędzy cząsteczkami, które znajdują się obok siebie. Aby zmienić stan skupienia alkoholu, np. z ciekłego w gazowy, należy dostarczyć takiej temperatury (energii), żeby wszystkie te oddziaływania przezwyciężyć. Dlatego – tak jak zapewne udało Ci się wywnioskować w poleceniu – im dłuższy jest łańcuch węglowy, tym wyższe są temperatury wrzenia i topnienia alkoholi.

Ponieważ wraz ze wzrostem liczby atomów węgla w cząsteczkach analizowanej grupy alkoholi rosną ich temperatury wrzenia, to jednocześnie trudniej jest je przeprowadzić w stan gazowy. Można zatem wnioskować, że maleje ich lotnośćlotność, którą w uproszczeniu możemy określić jako łatwość przechodzenia substancji w stan gazowy.

Liczba atomów węgla w cząsteczkach alkoholi ma również wpływ na rozpuszczalność tych związków chemicznych w wodzie.
Liczba atomów węgla w cząsteczce | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
Nazwa alkoholu | metanol | etanol | propan––ol | butan––ol | pentan––ol | heksan––ol | heptan––ol | oktan––ol | nonan––ol | dekan––ol |
Rozpuszczalność w wodzie, | mieszają się z wodą bez ograniczeń | praktycznie nierozpuszczalne w wodzie | ||||||||
Indeks górny Rozpuszczalność wybranych alkoholi w wodzie w temperaturze pokojowej. Źródło: W. Mizerski, Tablice chemiczne, Warszawa 2004 Indeks górny koniecRozpuszczalność wybranych alkoholi w wodzie w temperaturze pokojowej. Źródło: W. Mizerski, Tablice chemiczne, Warszawa 2004
Pierwsze trzy alkohole z szeregu homologicznego nasyconych alkoholi monohydroksylowych rozpuszczają się w wodzie bez ograniczeń. Rozpuszczalność kolejnych alkoholi w wodzie znacząco maleje wraz ze wzrostem liczby atomów węgla w ich cząsteczkach.
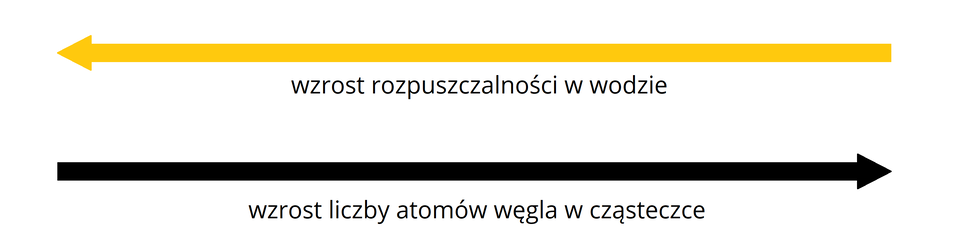
Woda jest rozpuszczalnikiem polarnym. Dlatego też będą się w niej dobrze rozpuszczały substancje o podobnej, polarnej budowiepolarnej budowie. Cząsteczki alkoholi mają budowę zbliżoną do cząsteczki wody.
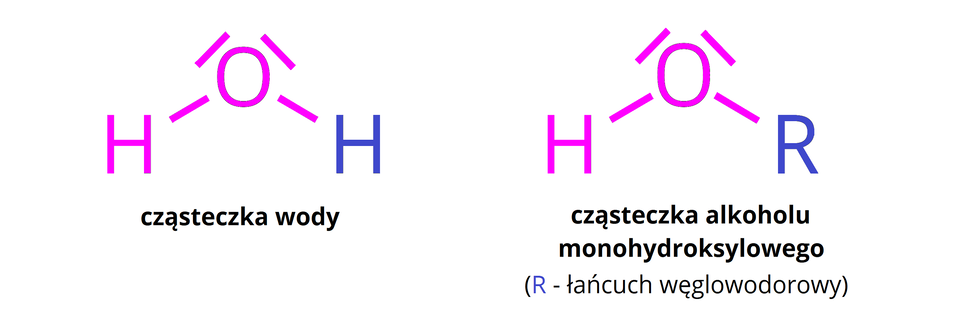
Dlaczego więc nie wszystkie alkohole dobrze rozpuszczają się w wodzie? Przyczyna tkwi głównie w budowie reszty węglowodorowej (), w cząsteczkach poszczególnych alkoholi. Polarną (hydrofilową) budowę w cząsteczce alkoholu ma grupa hydroksylowa (). Łańcuch węglowodorowy jest niepolarny (hydrofobowy).
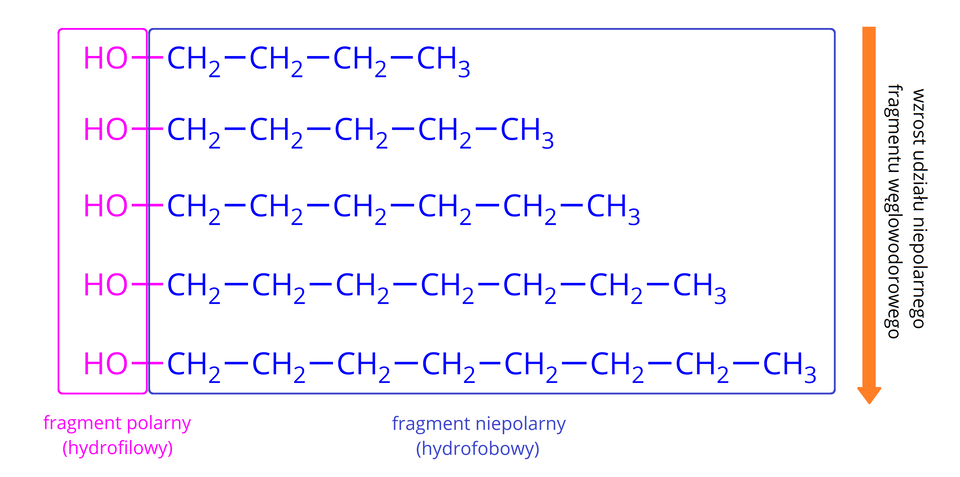
Stąd im większy (dłuższy) jest łańcuch węglowodorowy w cząsteczce alkoholu, tym wpływ polarnej grupy hydroksylowej na jego właściwości jest mniejszy. W związku z tym im więcej atomów węgla znajduje się w cząsteczce alkoholu, tym mniejsza jest rozpuszczalność tego alkoholu w wodzie.
Uczeń badał rozpuszczalność dekan––olu w wodzie w temperaturze pokojowej. W tym celu w probówce umieścił wody destylowanej. Następnie do wody wprowadził dekan––olu i zawartość probówki wymieszał dokładnie bagietką. Spośród podanych poniżej schematów, wybierz i zaznacz ten, który poprawnie odzwierciedla efekt przeprowadzonego przez ucznia doświadczenia. Gęstość dekan––olu w temperaturze pokojowej wynosi .
Uczeń badał rozpuszczalność dekan––olu w wodzie w temperaturze pokojowej. W tym celu w probówce umieścił wody destylowanej. Następnie do wody wprowadził dekan––olu i zawartość probówki wymieszał dokładnie bagietką. Spośród podanych poniżej odpowiedzi, wybierz i zaznacz tę, która poprawnie odzwierciedla efekt przeprowadzonego przez ucznia doświadczenia. Gęstość dekan––olu w temperaturze pokojowej wynosi .
W drugiej połowie kierownik jednej z wielkich wytwórni napojów alkoholowych w Rosji został posądzony o kradzież etanolu. Jeden z członków jego rodziny zwrócił się po pomoc do Dmitrija Mendelejewa, który w tamtym czasie pracował i wykładał chemię w Petersburgu. Pomoc ta okazała się dla oskarżonego zbawienna i pomogła mu uniknąć kary wieloletniego więzienia. Mendelejew wykazał bowiem, że objętość roztworu uzyskanego po zmieszaniu etanolu z wodą jest mniejsza niż suma objętości czystych składników tego roztworu. Innymi słowy, po zmieszaniu litrów wody i litrów etanolu nie otrzymamy litrów roztworu, a jedynie około . Zjawisko to nosi nazwę kontrakcji objętościkontrakcji objętości i należy je uwzględniać w planowaniu i przeprowadzaniu procesów technologicznych związanych z przemysłem alkoholowym.
4. Nasycone alkohole monohydroksylowe – właściwości chemiczne
Związki chemiczne, które należą do tego samego szeregu homologicznego, mają na ogół zbliżone właściwości chemiczne. Nasycone alkohole monohydroksylowe – między innymi metanol i etanol – to związki chemiczne o charakterystycznym zapachu. Są to substancje palne, a produkty ich spalania zależą od dostępności tlenu, niezbędnego do przeprowadzenia tego procesu.
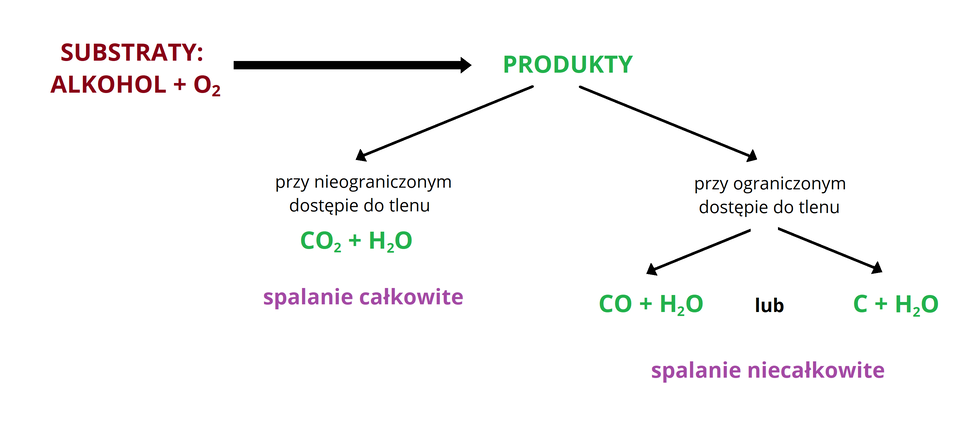
Produktami całkowitego spalania alkoholi, przy nieograniczonym dostępie tlenu, są tlenek węgla() (dwutlenek węgla) oraz woda (w postaci pary). W takich warunkach alkohole spalają się na ogół spokojnie, błękitnym płomieniem. W przypadku ograniczonego dostępu tlenu, alkohole spalają się niecałkowicie. Płomień towarzyszący takiemu spalaniu alkoholi jest mniej lub bardziej kopcący. Produktami spalania alkoholi, oprócz pary wodnej, są wówczas tlenek węgla() (czad) lub węgiel (sadza).
Poniżej zapisano równania reakcji spalania wybranych alkoholi. Dopasuj te równania do odpowiadających im opisów.
Wydawać by się mogło, że grupa hydroksylowa () w cząsteczkach alkoholi ma taki sam skład jak anion wodorotlenkowy (), który wchodzi w skład sieci krystalicznych wodorotlenków. Czy to „podobieństwo” w budowie będzie miało odzwierciedlenie w podobnej reaktywności obydwu wymienionych grup związków chemicznych?
Uczeń badał odczyn wodnych roztworów etanolu oraz wodorotlenku sodu. Wykonując doświadczenie, kilka kropel każdego z przygotowanych roztworów naniósł na uniwersalny papierek wskaźnikowy (każdy z roztworów naniósł na inny uniwersalny papierek wskaźnikowy). Uczeń odnotował następujące obserwacje:
Po naniesieniu kilku kropel wodnego roztworu etanolu na uniwersalny papierek wskaźnikowy, nie zaobserwowano zmiany zabarwienia papierka (pozostał żółty). Po naniesieniu kilku kropel wodnego roztworu wodorotlenku sodu na uniwersalny papierek wskaźnikowy, zaobserwowano zmianę zabarwienia papierka z żółtego na niebieskie.
Zastanów się i odpowiedz na pytanie, o czym świadczą odnotowane przez ucznia obserwacje.
Za zasadowy odczyn wodnych roztworów wodorotlenków odpowiedzialne są obecne w nich (w dużej ilości) aniony wodorotlenkowe (). Aniony te powstają w wyniku procesu dysocjacji elektrolitycznej wodorotlenków rozpuszczalnych w wodzie. Uniwersalny papierek wskaźnikowy, w kontakcie z wodnym roztworem etanolu, nie zmienia swojego zabarwienia. Można więc stwierdzić, że badany roztwór ma odczyn obojętny. Nasuwa się wniosek, że etanol nie uległ w wodzie procesowi dysocjacji elektrolitycznej, w wyniku której powstałyby aniony wodorotlenkowe.
Alkohole nie ulegają w wodzie procesowi dysocjacji elektrolitycznej, tak jak ma to miejsce w przypadku wodorotlenków rozpuszczalnych w wodzie. Ponadto każda z porównywanych grup związków chemicznych ma inną budowę – wodorotlenki mają budowę jonową, a alkohole kowalencyjną. W związku z tym będą miały również inne właściwości (zarówno fizyczne, jak i chemiczne) i nie możemy rozpatrywać reaktywności alkoholi w odniesieniu do reaktywności wodorotlenków.
5. Wirtualne laboratorium
Wykorzystując wirtualne laboratorium zbadaj wskazane właściwości fizykochemiczne wybranych alkoholi. Zbadaj rozpuszczalność w wodzie, ustal temperatury wrzenia i sprawdź palność znajdujących się w laboratorium alkoholi. Sprawdź, jaki jest odczyn wodnych roztworów alkoholi. Zobacz w praktyce, na czym polega zjawisko kontrakcji objętości.
Wykonując doświadczenia, uzupełnij dziennik laboratoryjny. Następnie przejdź do rozwiązywania ćwiczeń.
Słownik
(arab. al‑kuhl „delikatny proszek”) związki organiczne będące pochodnymi węglowodorów, w których przynajmniej jeden atom wodoru został zastąpiony grupą hydroksylową (łac. hydrogenium = wodór, oxygenium = tlen); w cząsteczkach alkoholi grupa hydroksylowa przyłączona jest do atomu węgla, który z innymi atomami w cząsteczce łączy się wyłącznie za pomocą wiązań pojedynczych
zbiór (ciąg) związków organicznych o podobnej budowie, posiadających takie same grupy funkcyjne (w przypadku alkoholi jest to grupa hydroksylowa); kolejne związki chemiczne w szeregu homologicznym różnią się od siebie o taki sam element budowy – grupę metylenową ()
związki chemiczne należące do tego samego szeregu homologicznego
w uproszczeniu – łatwość przechodzenia substancji w stan gazowy
inaczej: budowa dipolowa; charakterystyczna budowa danego indywiduum chemicznego złożonego z atomów pierwiastków o różnej elektroujemności; ponieważ atomy tworzące wiązanie, z różną siłą przyciągają do siebie elektrony wiążące, to dochodzi pomiędzy nimi do rozdzielenie ładunków dodatniego i ujemnego; budowę polarną (dipolową) mają np. cząsteczki, w których można wyróżnić biegun dodatni (na którym zgromadzony jest cząstkowy ładunek dodatni) oraz biegun ujemny (na którym zgromadzony jest cząstkowy ładunek ujemny); przykładem cząsteczki o budowie polarnej jest woda – na atomie tlenu (który ma większą elektroujemność) zgromadzony jest cząstkowy ładunek ujemny, a na atomach wodoru (o mniejszej niż tlen elektroujemności) cząstkowy ładunek dodatni
(łąc. contractio „skurczenie, ściągniecie”) zjawisko fizyczne, które polega na zmniejszaniu objętości podczas mieszania dwóch rozpuszczających się wzajemnie cieczy (suma objętości czystych cieczy jest większa niż objętość roztworu uzyskanego po zmieszaniu tych cieczy); jest wynikiem różnych rozmiarów cząsteczek cieczy i występujących pomiędzy nimi oddziaływań
Ćwiczenia
2. C indeks dolny, dziesięć, koniec indeksu dolnego, H indeks dolny, dwadzieścia jeden, koniec indeksu dolnego, O H, plus, dziesięć O indeks dolny, dwa, koniec indeksu dolnego, strzałka w prawo, dziesięć1. całkowite, 2. C, 3. C O indeks dolny, dwa, koniec indeksu dolnego, 4. H indeks dolny, dwa, koniec indeksu dolnego, O, 5. H indeks dolny, dwa, koniec indeksu dolnego, O, 6. H indeks dolny, dwa, koniec indeksu dolnego, O, 7. C O indeks dolny, dwa, koniec indeksu dolnego, 8. niecałkowite, 9. całkowite, 10. H indeks dolny, dwa, koniec indeksu dolnego, O, 11. C O, 12. niecałkowite plus, jedenaście1. całkowite, 2. C, 3. C O indeks dolny, dwa, koniec indeksu dolnego, 4. H indeks dolny, dwa, koniec indeksu dolnego, O, 5. H indeks dolny, dwa, koniec indeksu dolnego, O, 6. H indeks dolny, dwa, koniec indeksu dolnego, O, 7. C O indeks dolny, dwa, koniec indeksu dolnego, 8. niecałkowite, 9. całkowite, 10. H indeks dolny, dwa, koniec indeksu dolnego, O, 11. C O, 12. niecałkowite
3. dwa C indeks dolny, siedem, koniec indeksu dolnego, H indeks dolny, piętnaście, koniec indeksu dolnego, O H, plus, siedem O indeks dolny, dwa, koniec indeksu dolnego, strzałka w prawo, czternaście1. całkowite, 2. C, 3. C O indeks dolny, dwa, koniec indeksu dolnego, 4. H indeks dolny, dwa, koniec indeksu dolnego, O, 5. H indeks dolny, dwa, koniec indeksu dolnego, O, 6. H indeks dolny, dwa, koniec indeksu dolnego, O, 7. C O indeks dolny, dwa, koniec indeksu dolnego, 8. niecałkowite, 9. całkowite, 10. H indeks dolny, dwa, koniec indeksu dolnego, O, 11. C O, 12. niecałkowite plus, szesnaście1. całkowite, 2. C, 3. C O indeks dolny, dwa, koniec indeksu dolnego, 4. H indeks dolny, dwa, koniec indeksu dolnego, O, 5. H indeks dolny, dwa, koniec indeksu dolnego, O, 6. H indeks dolny, dwa, koniec indeksu dolnego, O, 7. C O indeks dolny, dwa, koniec indeksu dolnego, 8. niecałkowite, 9. całkowite, 10. H indeks dolny, dwa, koniec indeksu dolnego, O, 11. C O, 12. niecałkowite
4. dwa C indeks dolny, dziewięć, koniec indeksu dolnego, H indeks dolny, dziewiętnaście, koniec indeksu dolnego, O H, plus, dwadzieścia siedem O indeks dolny, dwa, koniec indeksu dolnego, strzałka w prawo, osiemnaście1. całkowite, 2. C, 3. C O indeks dolny, dwa, koniec indeksu dolnego, 4. H indeks dolny, dwa, koniec indeksu dolnego, O, 5. H indeks dolny, dwa, koniec indeksu dolnego, O, 6. H indeks dolny, dwa, koniec indeksu dolnego, O, 7. C O indeks dolny, dwa, koniec indeksu dolnego, 8. niecałkowite, 9. całkowite, 10. H indeks dolny, dwa, koniec indeksu dolnego, O, 11. C O, 12. niecałkowite plus, dwadzieścia1. całkowite, 2. C, 3. C O indeks dolny, dwa, koniec indeksu dolnego, 4. H indeks dolny, dwa, koniec indeksu dolnego, O, 5. H indeks dolny, dwa, koniec indeksu dolnego, O, 6. H indeks dolny, dwa, koniec indeksu dolnego, O, 7. C O indeks dolny, dwa, koniec indeksu dolnego, 8. niecałkowite, 9. całkowite, 10. H indeks dolny, dwa, koniec indeksu dolnego, O, 11. C O, 12. niecałkowite
Reakcja numer jeden to spalanie 1. całkowite, 2. C, 3. C O indeks dolny, dwa, koniec indeksu dolnego, 4. H indeks dolny, dwa, koniec indeksu dolnego, O, 5. H indeks dolny, dwa, koniec indeksu dolnego, O, 6. H indeks dolny, dwa, koniec indeksu dolnego, O, 7. C O indeks dolny, dwa, koniec indeksu dolnego, 8. niecałkowite, 9. całkowite, 10. H indeks dolny, dwa, koniec indeksu dolnego, O, 11. C O, 12. niecałkowite.
Reakcja numer dwa to spalanie 1. całkowite, 2. C, 3. C O indeks dolny, dwa, koniec indeksu dolnego, 4. H indeks dolny, dwa, koniec indeksu dolnego, O, 5. H indeks dolny, dwa, koniec indeksu dolnego, O, 6. H indeks dolny, dwa, koniec indeksu dolnego, O, 7. C O indeks dolny, dwa, koniec indeksu dolnego, 8. niecałkowite, 9. całkowite, 10. H indeks dolny, dwa, koniec indeksu dolnego, O, 11. C O, 12. niecałkowite.
Reakcja numer trzy to spalanie 1. całkowite, 2. C, 3. C O indeks dolny, dwa, koniec indeksu dolnego, 4. H indeks dolny, dwa, koniec indeksu dolnego, O, 5. H indeks dolny, dwa, koniec indeksu dolnego, O, 6. H indeks dolny, dwa, koniec indeksu dolnego, O, 7. C O indeks dolny, dwa, koniec indeksu dolnego, 8. niecałkowite, 9. całkowite, 10. H indeks dolny, dwa, koniec indeksu dolnego, O, 11. C O, 12. niecałkowite.
Reakcja numer cztery to spalanie 1. całkowite, 2. C, 3. C O indeks dolny, dwa, koniec indeksu dolnego, 4. H indeks dolny, dwa, koniec indeksu dolnego, O, 5. H indeks dolny, dwa, koniec indeksu dolnego, O, 6. H indeks dolny, dwa, koniec indeksu dolnego, O, 7. C O indeks dolny, dwa, koniec indeksu dolnego, 8. niecałkowite, 9. całkowite, 10. H indeks dolny, dwa, koniec indeksu dolnego, O, 11. C O, 12. niecałkowite.
Poniżej zapisano nazwy pięciu alkoholi:
dekan––ol, pentan––ol, propan––ol, oktan––ol, heksan––ol.
Dokończ poniższe zdanie.
W szeregu homologicznym nasyconych alkoholi monohydroksylowych, o prostych (nierozgałęzionych) łańcuchach węglowych, wraz ze wzrostem liczby atomów węgla w cząsteczce, wzrasta również:
W poniższej tabeli zestawiono nazwy systematyczne oraz gęstość (w temperaturze pokojowej) trzech alkoholi monohydroksylowych.
Nazwa systematyczna alkoholu | Gęstość, |
|---|---|
propan––ol | |
pentan––ol | |
nonan––ol |
Indeks górny Źródło: W. Mizerski, Tablice chemiczne, Warszawa 2004 Indeks górny koniecŹródło: W. Mizerski, Tablice chemiczne, Warszawa 2004
W pewnym laboratorium chemicznym, do rozdzielenia mieszaniny czterech alkoholi – pentan––olu, etanolu, heptan––olu oraz propan––olu – wykorzystano zestaw doświadczalny, którego schemat znajduje się poniżej.
W pewnym laboratorium chemicznym, do rozdzielenia mieszaniny czterech alkoholi – pentan––olu, etanolu, heptan––olu oraz propan––olu – wykorzystano zestaw do destylacji. Uszereguj, w jakiej kolejności powyższe alkohole powinny trafić do odbieralnika.
W laboratorium chemicznym spalono całkowicie (przy nieograniczonym dostępie tlenu) próbkę pentan--olu. Oblicz objętość tlenku węgla(), jaką otrzymano wiedząc, że gęstość tego gazu w warunkach pomiaru wynosiła . Wynik podaj w metrach sześciennych z dokładnością do pierwszego miejsca po przecinku.
Równanie reakcji spalania pewnego alkoholu ma postać:
Równanie reakcji spalania pewnego alkoholu ma postać:
Poniżej znajduje się schematyczny rysunek zestawu doświadczalnego, za pomocą którego można wyznaczyć temperatury wrzenia alkoholi. Do zaznaczonych na zestawie elementów dopasuj odpowiadające im nazwy w języku angielskim.
Bibliografia
Dudek‑Różycki K., Płotek M., Wichur T., Kompendium terminologii oraz nazewnictwa związków organicznych. Poradnik dla nauczycieli i uczniów, Kraków 2020.
Encyklopedia PWN
Krzeczkowska M., Loch J., Mizera A., Repetytorium chemia. Liceum – poziom podstawowy i rozszerzony, Warszawa – Bielsko‑Biała 2010.