Jak powstają wiązania typu pi?
Juz wiesz, że powstawanie wiązań pomiędzy atomami można wyjaśnić zgodnie z zasadami mechaniki kwantowej, a także, że wiązanie kowalencyjne powstaje w wyniku nakładania się . Powstający charakterystyczny rozkład gęstości elektronowej – orbital molekularny – określany jest jako wiązanie sigma (czyt. sigma) lub wiązanie pi (czyt. pi), w zależności od sposobu nakładania się orbitali. Wiązanie sigma zostało już omówione, a teraz pora by przyjrzeć się bliżej wiązaniom typu pi.
Wiązanie pi w cząsteczkach homojądrowych
W cząsteczkach homojądrowych, jak czy , wiązanie chemiczne tworzy się na skutek wzrostu gęstości elektronowej w obszarze międzyjądrowym. Ile i jakiego typu orbitale tworzą wiązania atomowe w wymienionych cząsteczkach?
Zastanów się, czy orbitale cząsteczkowe, które powstają w wyniku czołowego nałożenia orbitali atomowych, mają taki sam kształt jak te, które powstają z nałożenia bocznego?
Prześledźmy na przykładach sposób powstawania orbitali molekularnych typu .


Powstawanie wiązań w cząsteczce
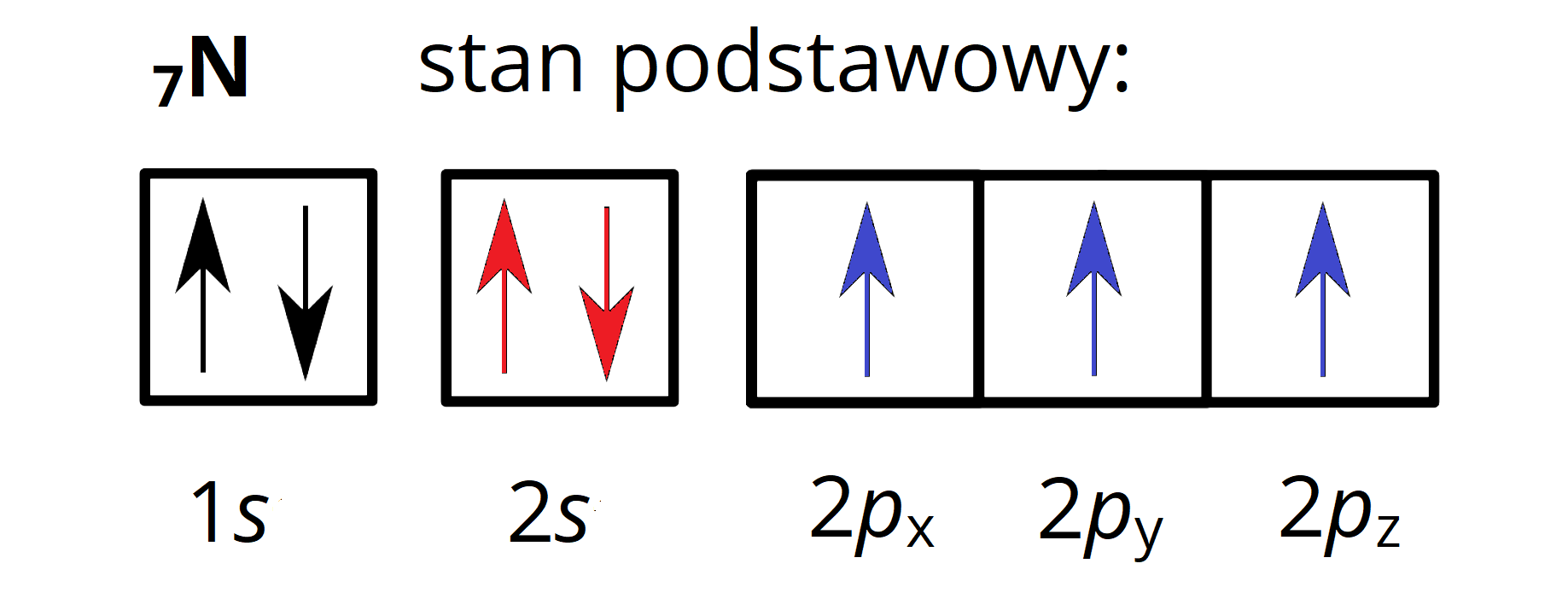
Cząsteczka tlenu () powstaje poprzez nałożenie się chmur elektronowych dwóch atomów tlenu. W stanie podstawowym atom tlenu posiada konfigurację elektronową , z czego dwa niesparowane elektrony znajdują się na orbitalu oraz . Są to elektrony, które tworzą orbitale molekularne w cząsteczce. W wyniku nałożenia się dwóch rodzajów orbitali atomowych ze sobą, pomiędzy atomami tlenu tworzy się wiązanie podwójne ( wiązanie typu oraz jedno wiązanie typu ). W galerii mediów zaprezentowano sposób powstania wiązań w cząsteczce . Zwróć uwagę na kształty utworzonych orbitali molekularnych.


Z zaprezentowanych ilustracji wynika, że w cząsteczce tlenu utworzone wiązanie podwójne składa się z jednego wiązania typu i jednego wiązania typu . Utworzone orbitale molekularne oraz mają odmienny kształt.
Zastanów się, jak powstaje cząsteczka azotu ()? Ile wiązań i jakiego typu powstanie, gdy nałożą się na siebie: po dwa orbitale atomowe typu , oraz ?
Wiązanie w cząsteczkach heteroatomowych
Istotnym przykładem tworzenia wiązań typu jest sytuacja, gdy tylko część z orbitali atomowych ulega hybrydyzacjihybrydyzacji. Pozostałe niehybrydyzowane orbitale mają zdolność do tworzenia wiązań . Poniżej przykład powstawania orbitalu molekularnego w cząsteczce o hybrydyzacji atomu centralnego.
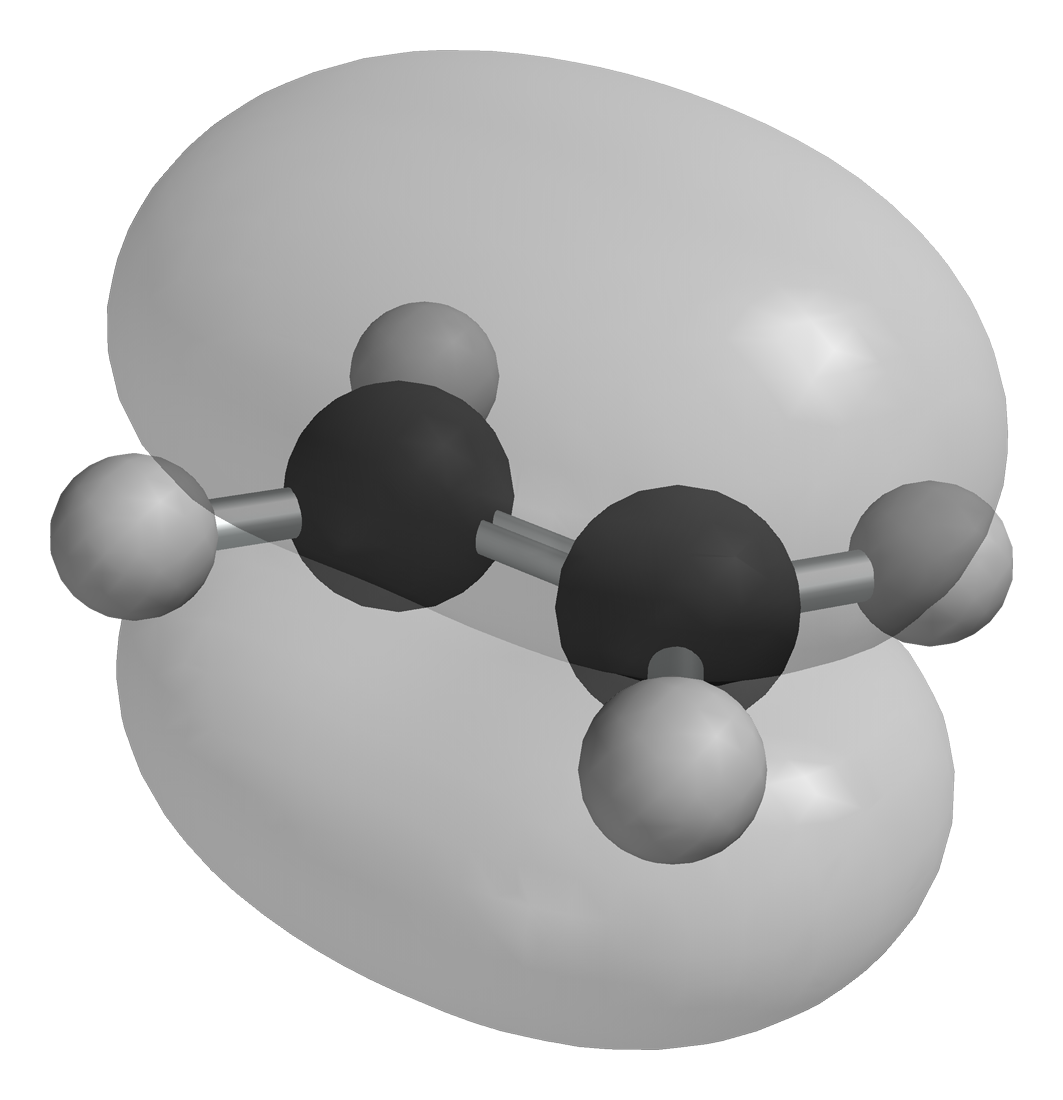

Wiązanie w cząsteczce etenu
Jak powstają wiązania typu w cząsteczce etenu? Jak myślisz, które z zaprezentowanych na poniższym rysunku wiązań jest wiązaniem typu ?
Jak powstają wiązania typu w cząsteczce etenu? Zapoznaj się z opisem rysunku. Jak myślisz, które z wiązań jest wiązaniem typu ?

Wiązanie w wiązaniu podwójnym wynika z nakładania się trzeciego (pozostałego) orbitalu na każdym atomie węgla, który nie uczestniczy w hybrydyzacji. Ten niezhybrydyzowany orbital (płaty pokazane na pomarańczowo) jest prostopadły do płaszczyzny orbitali zhybrydyzowanych . Tak niezhybrydyzowane orbitale zachodzą na siebie, powyżej i poniżej osi między jądrowej, oraz tworzą wiązanie .
Co istotne, wiązanie jest wiązaniem pojedynczym, ponieważ bierze w nim udział jedna para elektronów, wspólna dla dwóch atomów. Natomiast kombinacja jednego wiązania i jednego wiązania odpowiada za występowanie wiązania podwójnego między atomami węgla.
Z kolei wiązania , pomiędzy atomem węgla a atomem wodoru, powstają przez nakładanie się orbitalu typu atomu węgla z orbitalem typu wodoru.

Powstawanie wiązań w cząsteczce

Atom węgla przyjmuje hybrydyzację typu . Jednocześnie dwa orbitale typu ( oraz ) pozostają niezhybrydyzowane i są zdolne do tworzenia wiązań z atomami tlenu. Z kolei atomy tlenu ulegają hybrydyzacji . Każdy atom tlenu posiada zatem po jednym niezhybrydyzowanym orbitalu typu . W wyniku zbliżania się do siebie zhybrydyzowanych orbitali (od atomu węgla) oraz (od atomów tlenu), następuje ich czołowe nakładanie i przenikanie w jedną chmurę, która obejmuje oba atomy. W ten sposób powstaje wiązanie typu . Elektrony orbitali oraz atomu węgla tworzą z orbitalami typu atomów tlenu dwa wiązania typu . Po jednym z każdej strony atomu węgla.

Zapoznaj się z modelami 3D. W jaki sposób zostają utworzone wiązania w cząsteczce azotu oraz benzenu? Rozwiąż poniższe zadania.
Zapoznaj się z opisem modeli 3D. W jaki sposób zostają utworzone wiązania w cząsteczce azotu oraz benzenu? Rozwiąż poniższe zadania.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DB1AQRPN5
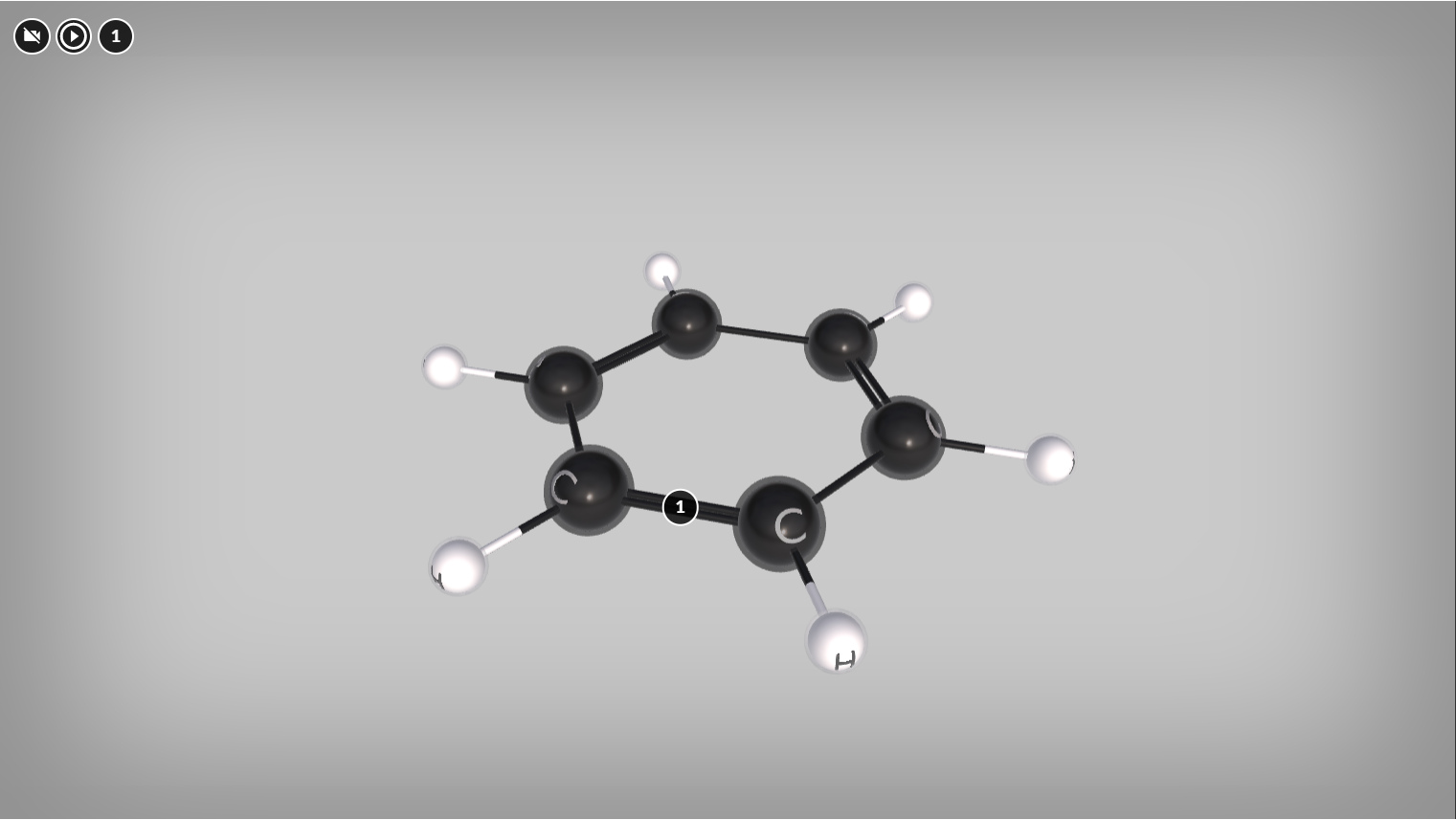
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DB1AQRPN5

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DB1AQRPN5
Wyjaśnij, jak utworzone są wiązania w cząsteczce azotu.
Jak sądzisz, czym będą się różniły między sobą orbitale molekularne, utworzone poprzez nałożenie się orbitali oraz , od tych utworzonych z dwóch orbitali ?