Właściwości fizyczne i chemiczne aldehydów i ketonów
Aldehydy - właściwości fizyczne
Najprostszy aldehydy – metanal (formaldehyd)– w temperaturze pokojowej jest gazem, pozostałe zaś człony szeregu homologicznegoszeregu homologicznego, w zależności od liczby atomów węgla, są cieczami lub ciałami stałymi. Aldehydy zawierające w cząsteczkach do siedmiu atomów węgla, mają charakterystyczną ostrą woń, a zawierające więcej niż siedem atomów węgla w cząsteczce – mają przyjemny zapach.
W szeregu homologicznym nasyconych aldehydów łańcuchowych systematycznie rosną temperatury wrzenia i topnienia oraz gęstość, maleje natomiast rozpuszczalność w wodzie. Temperatury wrzenia nasyconych aldehydów są niższe niż odpowiednich alkoholi, co jest wynikiem braku asocjacji cząsteczek tych związków.
Właściwości fizyczne wybranych n‑aldehydów przedstawia poniższa tabela.
Aldehyd | TIndeks dolny TT [°C] | TIndeks dolny WW [°C] | Właściwości fizyczne w temp. pokojowej | Wzór półstrukturalny |
|---|---|---|---|---|
formaldehyd (metanal) | -90,2 | -19,10 | bezbarwny gaz o charakterystycznym ostrym zapachu drażniącym błony śluzowe, bardzo dobrze rozpuszczalny w wodzie – wodny roztwór to formalina, oraz eterze i etanolu; łatwo polimeryzuje |  Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |
acetaldehyd (etanal) | -123,0 | 20,70 | łatwopalna, bezbarwna ciecz o charakterystycznym zapachu, rozpuszczalna w wodzie, etanolu, eterze i benzynie |  Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |
heksanal | -56,0 | 131,0 | ciecz o nieprzyjemnym zapachu, słabo rozpuszczalna w wodzie, rozpuszczalna w rozpuszczalnikach organicznych | 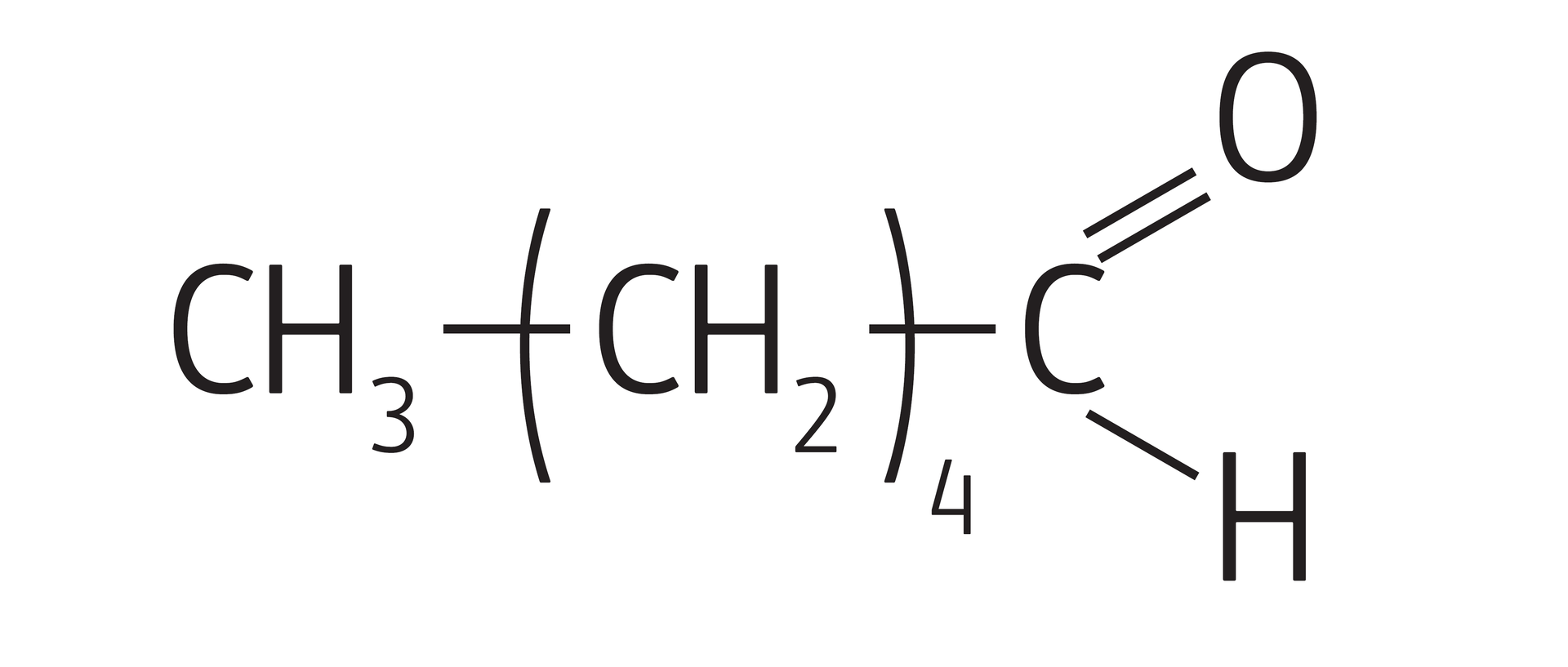 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |
oktanal | -25,4 | 170,0 | nierozpuszczalna w wodzie ciecz o zapachu przypominającym cytrynę lub róże, rozpuszczalna w rozpuszczalnikach organicznych |  Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |
Indeks dolny Źródło: M. Krzeczkowska, J. Loch, A. Mizera, Chemia Repetytorium, Wydawnictwo Szkolne PWN, Warszawa 2010. Indeks dolny koniecŹródło: M. Krzeczkowska, J. Loch, A. Mizera, Chemia Repetytorium, Wydawnictwo Szkolne PWN, Warszawa 2010.
Zmiany właściwości fizycznych aldehydów w szeregu homologicznym

Ketony – właściwości fizyczne
Ketony nasycone, o prostych łańcuchach węglowych, są cieczami o niższych temperaturach wrzenia, niż odpowiadające im alkohole. Podobnie jak w przypadku aldehydów, związane jest to z brakiem asocjacji cząsteczek tych związków. W szeregu homologicznym ketonów, wraz ze wzrostem długości łańcucha, rosną temperatury wrzenia i topnienia.
Właściwości fizyczne wybranych ketonów zestawiono w poniższej tabeli.
Keton | TIndeks dolny TT [°C] | TIndeks dolny WW [°C] | Właściwości fizyczne w temperaturze pokojowej | Wzory półstrukturalne |
|---|---|---|---|---|
propan‑2‑on (aceton) | -94,7 | 56,20 | bezbarwna, lotna ciecz o charakterystycznym zapachu, rozpuszczalna w wodzie, eterze dietylowym i alkoholu metylowym |  Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |
butan‑2‑on | -86,7 | 79,6 | bezbarwna, lotna ciecz o charakterystycznym zapachu, rozpuszczalna w wodzie |  Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |
pentan‑3‑on | -39,0 | 101,7 | bezbarwna, lotna, palna ciecz o charakterystycznym zapachu, z powietrzem tworzy mieszaniny wybuchowe |  Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |
Indeks dolny Źródło: M. Krzeczkowska, J. Loch, A. Mizera, Chemia Repetytorium, Wydawnictwo Szkolne PWN, Warszawa 2010. Indeks dolny koniecŹródło: M. Krzeczkowska, J. Loch, A. Mizera, Chemia Repetytorium, Wydawnictwo Szkolne PWN, Warszawa 2010.
Zmiany właściwości fizycznych ketonów w szeregu homologicznym

Na podstawie powyższych tabel podsumuj zdobyte informacje i sporządź tabelę, w której porównasz właściwości fizyczne ketonów i aldehydów.
Przeprowadź doświadczenie w laboratorium chemicznym. Rozwiąż problem badawczy i zweryfikuj hipotezę. Na podstawie obserwacji tych substancji, sprawdzenia ich rozpuszczalności w wodzie, uzupełnij tabelę (ćwiczenie nr 1.), a następnie sformułuj obserwacje i wnioski.
Problem badawczy:
Rozpuszczalność ketonów w wodzie.
Hipoteza:
Propan‑2-on nie rozpuszcza się w wodzie.
Sprzęt laboratoryjny:
probówki;
pipety.
Odczynniki:
formalina (jest to ok. 30% wodny roztwór metanalu);
propan‑2-on (acetonu);
benzenokarboaldehyd (aldehyd benzoesowy);
woda zabarwiona niebieskim atramentem.
Instrukcja wykonania doświadczenia:
Do trzech probówek wlej wodę zabarwioną atramentem.
Do pierwszej próbówki wlej powoli po ściankach 1 roztworu formaliny.
Do drugiej probówki wlej 1 propan‑2-onu.
Do trzeciej probówki wlej 1 aldehydu benzoesowego.
Zaobserwuj, która ciecz znajduje się w dolnej warstwie mieszaniny.
Wstrząśnij probówkami.
Obserwuj zachodzące zmiany.
Sprawdź samodzielnie właściwości fizyczne aldehydów i ketonów w poniższym laboratorium, a następnie rozwiąż ćwiczenia.
Wykorzystując wirtualne laboratorium, przeanalizuj, jak zmieniają się właściwości fizyczne aldehydów i ketonów. Przeprowadź badanie rozpuszczalności przykładowych substancji w wodzie, oraz oznacz ich temperatury wrzenia, a następnie rozwiąż przedstawione zadania.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DSGLDL48G
Doświadczenie dotyczy badania rozpuszczalności aldehydów i ketonów oraz badanie ich temperatur wrzenia.
Zadanie: Przeprowadź badanie rozpuszczalności przykładowych aldehydów i ketonów w wodzie, oraz oznacz ich temperatury wrzenia.
Odczynniki: etanal, propanal, butanal, pentanal, propan‑2-on, butan‑2-on, pentan‑2-on, heksan‑2-on, woda destylowana
Szkło i sprzęt laboratoryjny: statyw na probówki - prostokątny sprzęt laboratoryjny z rzędami otworów, w których umieszczane są probówki; probówka szklana - podłużne naczynie szklane do przeprowadzania prostych reakcji chemicznych; pipeta szklana 5 centymetrów sześciennych - wąska rurka pobierania i przenoszenia niewielkiej ilości cieczy za pomocą ssawki; tryskawka - plastikowe naczynie zamknięte nakrętką z długą końcówką. Tryskawka wypełniona jest wodą, która pod wpływem nacisku na plastikowe naczynie, uwalnia wodę na zewnątrz przez długą końcówkę; plastikowy korek - niewielki element wykonany z plastiku, służący do szczelnego zamykania probówek; chłodnica - podłużne szkło laboratoryjne, wewnątrz którego znajduje się spiralna rurka przez którą przepływa zimna woda schładzająca powstające podczas reakcji opary. Służy do skraplania gazów powstających podczas ogrzewania substancji; termometr - podłużny sprzęt laboratoryjny zawierający najczęściej skalę w stopniach Celsjusza oraz słup wypełniony rtęcią, który pod wpływem temperatury wskazuje pomiar; kosz grzewczy - sprzęt laboratoryjny umożliwiający podgrzewanie kolb okrągłodennych i ich zawartości. Posiada półokrągłe wgłębienie, w którym umieszcza się kolbę okrągłodenną poddawaną ogrzewaniu; kolba okrągłodenna - szklane naczynie laboratoryjne z zaokrąglonym dnem; kolba stożkowa - szklane naczynie laboratoryjne o kształcie stożka z płaskim dnem i wąską szeroką szyjką; cylinder miarowy - podłużne szklane naczynie laboratoryjne w kształcie walca z umieszczoną na ściance podziałką objętości. Służy do odmierzania cieczy.
Przebieg:
Badanie rozpuszczalności aldehydów i ketonów w wodzie:
Za pomocą szklanej pipety, pobrano 5 cmIndeks górny 33 każdego z przygotowanych aldehydów i ketonów, a następnie próbki umieszczono w szklanych probówkach. Do każdej probówki zawierającej odpowiednią substancję, wprowadzono niewielką ilość wody destylowanej. Probówkę zabezpieczono plastikowym korkiem, a następnie każdą probówkę wstrząśnięto, celem wymieszania wody z substancjami.
Oznaczanie temperatury wrzenia aldehydów i ketonów:
Zmontowano zestaw składający się z kosza grzejnego, termometru, kolby okrągłodennej, chłodnicy (do której podłączona dwa wężyki - jeden doprowadzający wodę do chłodnicy, drugi odprowadzający wodę) oraz kolby stożkowej, połączonej z chłodnicą. Odmierzono pojedynczo 60 cmIndeks górny 33 każdej substancji za pomocą cylindra miarowego, a następnie wprowadzono jego zawartość do kolby okrągłodennej. Kolbę umieszczono w koszu grzejnym w celu ogrzania substancji znajdującej się w kolbie. Podczas ogrzewania następowało pojawienie się oparów substancji, które przechodziły do chłodnicy i ulegały skropleniu. Jednocześnie sprawdzano temperaturę, w celu określenia temperatury wrzenia substancji. Skroploną ciecz zbierano do kolby stożkowej umieszczonej z drugiej strony chłodnicy.
Obserwacje:
Badanie rozpuszczalności aldehydów i ketonów w wodzie:
etanal - rozpuszcza się w wodzie bardzo dobrze, bez ograniczeń
propanal, butanal, pentanal - każdy z kolei rozpuszcza się coraz słabiej (roztwór po wymieszaniu staje się mętny)
propan‑2-on - bardzo dobrze rozpuszczalny, miesza się z wodą tworząc jednolity, bezbarwny roztwór
butan‑2-on, pentan‑2-on, heksan‑2-on - każdy z kolei rozpuszcza się coraz słabiej (roztwór po wymieszaniu staje się mętny)
Oznaczanie temperatury wrzenia aldehydów i ketonów:
etanal: 21°C
propanal: 48°C
butanal: 74,8°C
pentanal: 103°C
propan‑2-on: 56°C
butan‑2-on: 75,6°C
pentan‑2-on: 102°C
heksan‑2-on: 127,6°C
Określ rozpuszczalność w wodzie i temperatury wrzenia podanych poniżej aldehydów i ketonów.
Na podstawie badania rozpuszczalności aldehydów i ketonów w wodzie sformułuj wniosek, który określi zależność pomiędzy rozpuszczalnością tych substancji w wodzie, a wzrostem długości łańcucha węglowego w ich cząsteczce.
Badanie właściwości redukujących formaldehydu (metanalu)
Zapoznaj się z poniższym doświadczeniem dotyczącym badania właściwości redukujących formaldehydu. Uzupełnij puste miejsca w dzienniku laboratoryjnym.
Doświadczenie 1 – badanie właściwości redukujących metanalu
Schemat doświadczenia:


Wnioski:
W wyniku reakcji azotanu(V) srebra(I) z wodorotlenkiem sodu powstaje nierozpuszczalny wodorotlenek miedzi(II):
Tlenek srebra(I) reaguje z wodą amoniakalną, tworząc odczynnik Tollensa – związek kompleksowy o nazwie wodorotlenek diaminasrebra(I). Równanie zostało zapisane w formie jonowej:
Odczynnik Tollensa reaguje z formaldehydem (metanalem) – zapis jonowy skrócony:
W celu uproszczenia przyjmuje się, że formaldehyd reaguje z tlenkiem srebra(I). Wówczas reakcja uproszczona wygląda następująco:
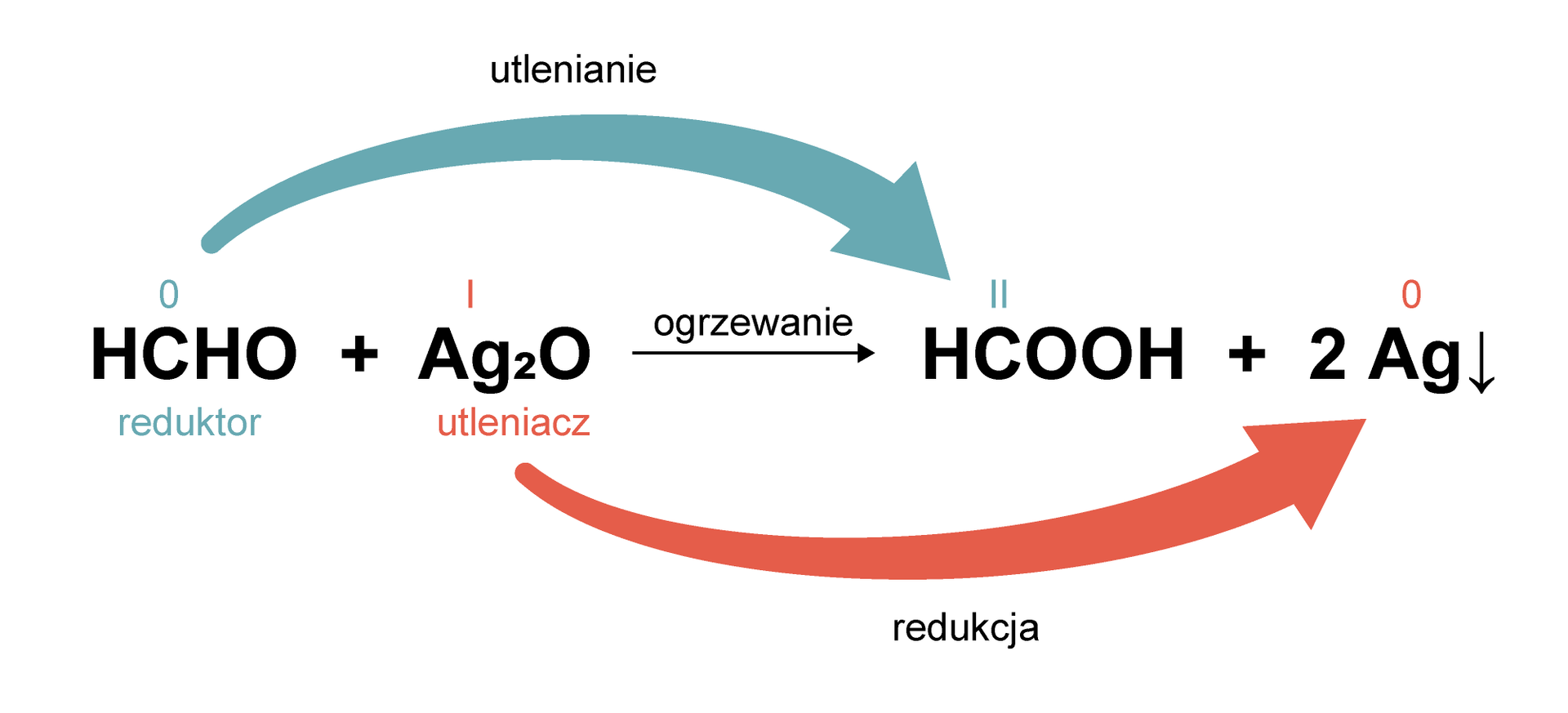
Atom węgla grupy aldehydowej w cząsteczce formaldehydu (metanalu) zwiększa swój stopień utlenienia z 0 na II, czyli ulega reakcji utleniania, będąc reduktorem. Z kolei atom srebra w cząsteczce tlenku srebra(I) zmniejsza swój stopień utlenienia z I na 0, czyli ulega reakcji redukcji, pełniąc rolę utleniacza. Formaldehyd posiada właściwości redukujące, o czym świadczy pozytywny wynik próby Tollensa.
Doświadczenie 2 – badanie właściwości redukujących formaldehydu (metanalu)
Schemat doświadczenia:
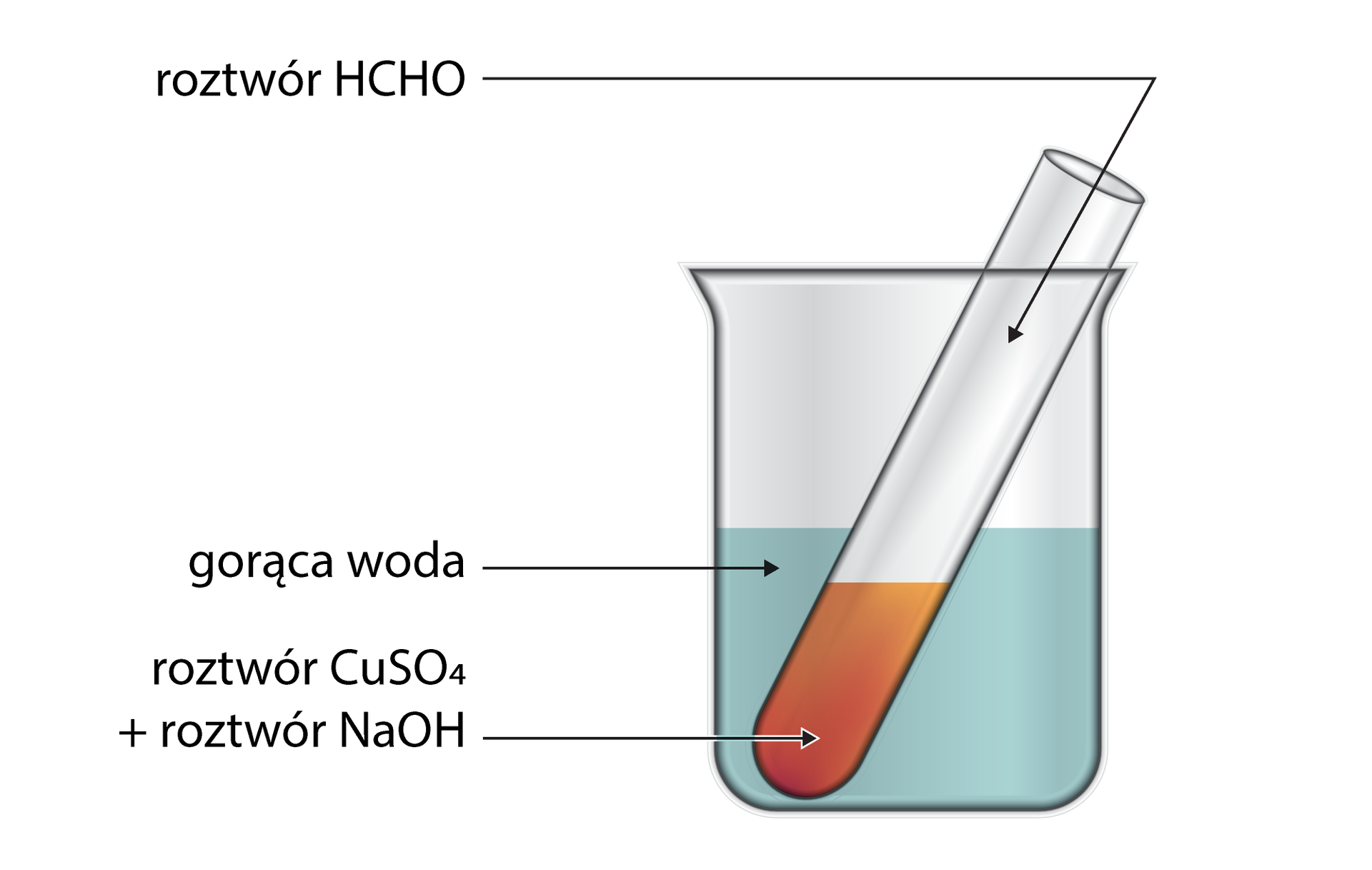

Wnioski:
W wyniku reakcji siarczanu(VI) miedzi(II) z wodorotlenkiem sodu powstaje nierozpuszczalny wodorotlenek miedzi(II):
Nierozpuszczalny w wodzie wodorotlenek miedzi(II) reaguje z formaldehydem (metanalem). W wyniku tej reakcji powstaje kwas mrówkowy (metanowy), woda oraz tlenek miedzi(I), który występuje w postaci ceglastoczerwonego osadu.
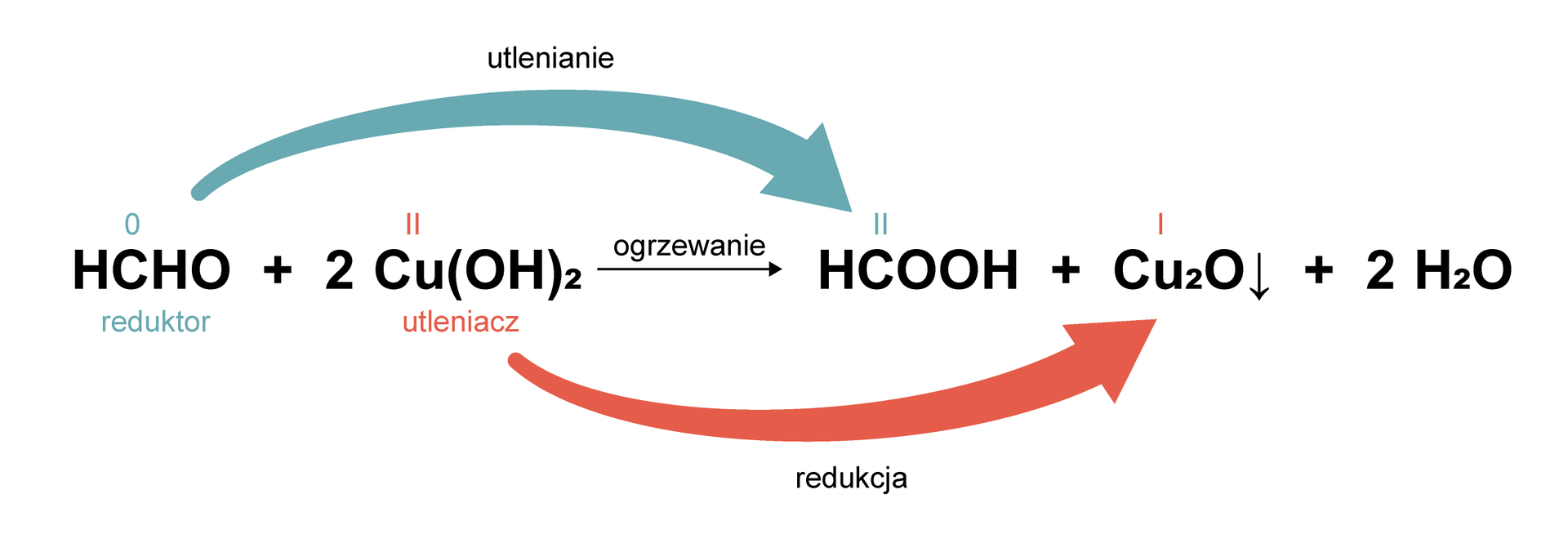
Równanie reakcji utleniania‑redukcji zachodzącej między wodorotlenkiem miedzi(II) a formaldehydem. Atom węgla w cząsteczce formaldehydu zwiększa swój stopień utlenienia z 0 na II, czyli bierze udział w reakcji utleniania, pełniąc rolę reduktora. Z kolei atom wodorotlenku miedzi(II) zmniejsza swój stopień utlenienia z II na I, czyli bierze udział w reakcji redukcji, pełniąc rolę utleniacza.
Formaldehyd posiada właściwości redukujące, o czym świadczy pozytywny wynik próby Trommera.
Poniżej masz możliwość przećwiczyć próbę Trommera i Tollensa w poniższej symulacji. Aby utrwalić zdobytą wiedzę rozwiąż ćwiczenia pod multimedium.
W poniższej symulacji wybierz, jaką reakcję chcesz zobaczyć, następnie połącz ze sobą odpowiednie substraty, a wówczas dowiesz się, jakie produkty powstają. Zwróć uwagę na to, jak przebiega reakcja formaldehydu (metanalu) z amoniakalnym roztworem tlenku srebra(I) i wodorotlenkiem miedzi(II). Na podstawie informacji rozwiąż zebrane zadania.
Zapoznaj się z opisem symulacji dotyczącej reakcji formaldehydu (metanalu) z amoniakalnym roztworem tlenku srebra(I) i wodorotlenkiem miedzi(II) w próbach: Tollensa i Trommera. Na podstawie informacji rozwiąż zebrane zadania.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DSGLDL48G