Budowa i właściwości amin i aminokwasów
Poniższy materiał stanowi uzupełnienie treści zawartych w materiale: https://zpe.gov.pl/a/aminy-i-aminokwasy/DjvV4HEHB
Aminy to organiczne zasady występujące powszechnie w organizmach żywych. Stanowią wiele neuroprzekaźników, takich jak np.: adrenalina, noradrenalina, dopamina, serotonina czy histamina. Aminokwasy z kolei wchodzą w skład białek, które odpowiadają za większość procesów w naszym organizmie. Co łączy te dwie grupy związków organicznych?
budowę i właściwości amoniaku;
budowę i właściwości grup wybranych związków organicznych, takich jak alkohole, kwasy karboksylowe i estry.
wyjaśniać, czym są aminy i aminokwasy;
opisywać budowę i właściwości związków zawierających azot – na przykładzie metanoaminy (aminy) i glicyny (aminokwasu);
zapisywać wzory metanoaminy i glicyny;
wskazywać we wzorach związków organicznych wiązanie peptydowe (tj. wiązanie amidowe łączące w danym związku dwie podjednostki wywodzące się od aminokwasów);
badać podstawowe właściwości fizykochemiczne amin i aminokwasów.
Azot jest jednym z głównych pierwiastków wchodzących w skład wielu związków organicznych. Obok węgla, wodoru i tlenu jest szeroko rozpowszechniony w organizmach roślinnych i zwierzęcych. Zarówno aminy, jak i aminokwasy w swojej strukturze zawierają atom azotu.
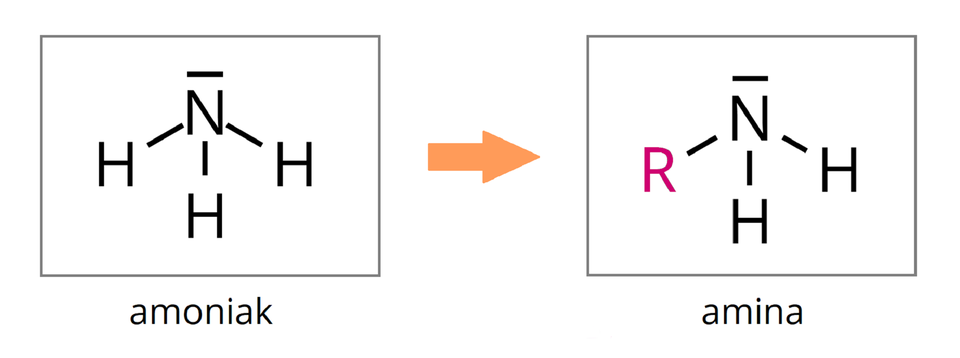
AminyAminy to pochodne amoniaku , w których co najmniej jeden atom wodoru został zastąpiony grupą węglowodorową (oznaczaną literą ).
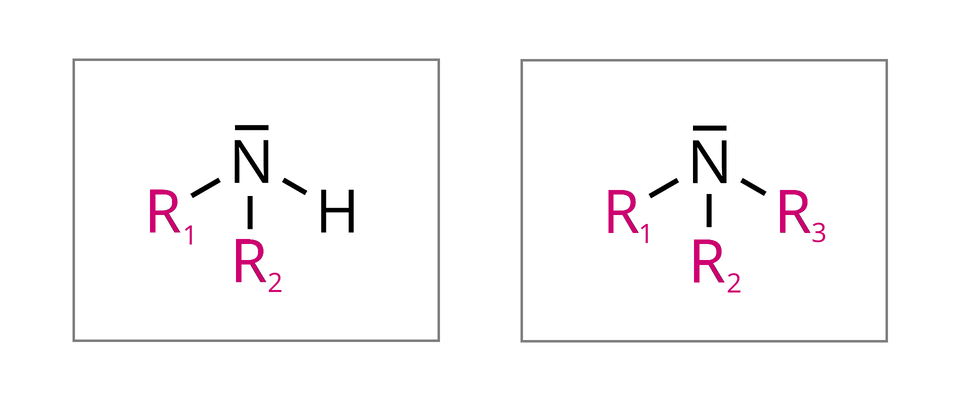
Kiedy zastąpimy kolejne atomy wodoru grupami węglowodorowymi, to również otrzymamy aminy, odpowiednio: drugorzędowe (z dwiema grupami ) oraz trzeciorzędowe (z trzema podstawnikami ).
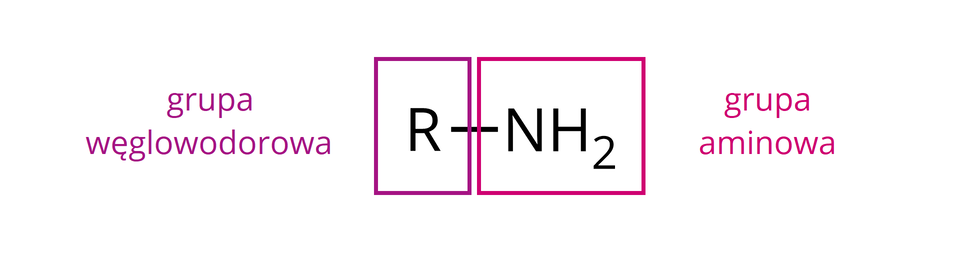
Aminy, oprócz grupy węglowodorowej , którą może stanowić np. grupa metylowa lub etylowa , zawierają grupę aminową (oznaczaną jako , lub , w zależności od rodzaju aminy).
Jednak najprostsze aminy to te zawierające jedną grupę węglowodorową, związaną z grupą .
Do najprostszych amin należą: metanoamina o wzorze oraz etanoamina o wzorze .
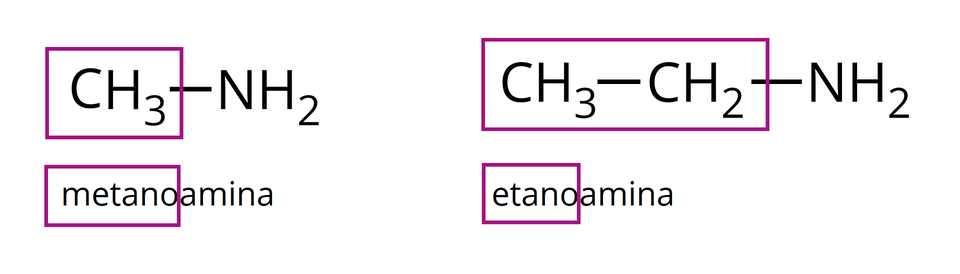
Metanoamina jest trującym, bezbarwnym gazem o charakterystycznym zapachu przypominającym zapach psujących się ryb. Bardzo dobrze rozpuszcza się w wodzie, więc przechowuje się ją jako wodny roztwór (również o nieprzyjemnym zapachu).
W karcie charakterystykikarcie charakterystyki metanoaminy odnajdziemy następujące oznaczenia:

Etanoamina jest z kolei bezbarwną cieczą o temperaturze wrzenia równej , co oznacza, że w temperaturze pokojowej jest gazem. Związek ten charakteryzuje ostry, amoniakalny zapach. Etanoamina bardzo dobrze rozpuszcza się w wodzie.
W karcie charakterystyki etanoaminy odnajdziemy następujące symbole:

Właściwości fizykochemiczne amin można porównać do właściwości chemicznych amoniaku, ze względu na podobieństwo w budowie. Wodne roztwory amin wykazują zatem zasadowy odczyn, ze względu na powstające w wyniku dysocjacji elektrolitycznej aniony wodorotlenkowe .
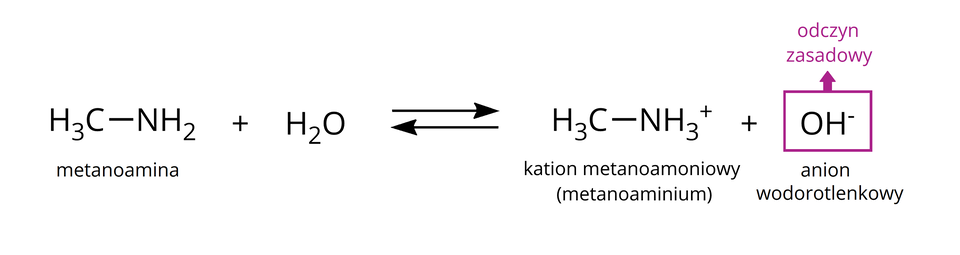
Podwójna strzałka w zapisie dysocjacji elektrolitycznej metanoaminy oznacza, że proces ten jest odwracalny – cząsteczki rozpadają się na jony, które mogą się ponownie łączyć, tworząc cząsteczki. W roztworze wodnym, powstałym poprzez rozpuszczenie w wodzie metanoaminy, występują zatem jony: , oraz niezdysocjowane cząsteczki i .
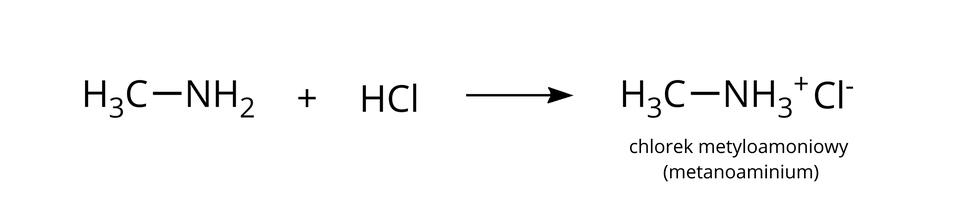
Aminy wykazują zasadowy charakter chemiczny, ponieważ reagują z kwasami.
Metanoamina ulega reakcji z kwasem chlorowodorowym, tworząc sól – chlorek metyloamoniowy.
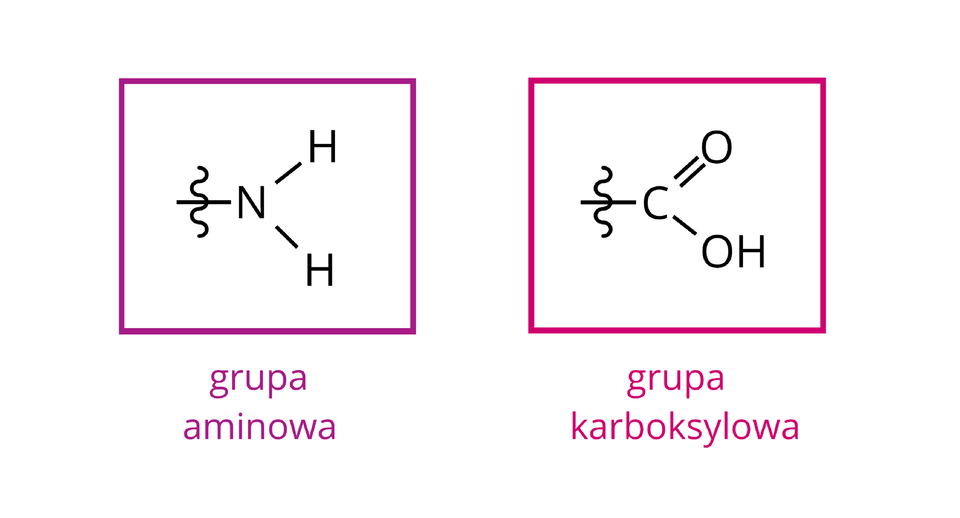
AminokwasyAminokwasy to związki organiczne, zawierające w swojej budowie grupę aminową oraz grupę karboksylową .
Wzór ogólny -aminokwasów (czyli aminokwasów, posiadających grupę aminową przy sąsiednim atomie węgla, względem grupy karboksylowej) można przedstawić następująco:
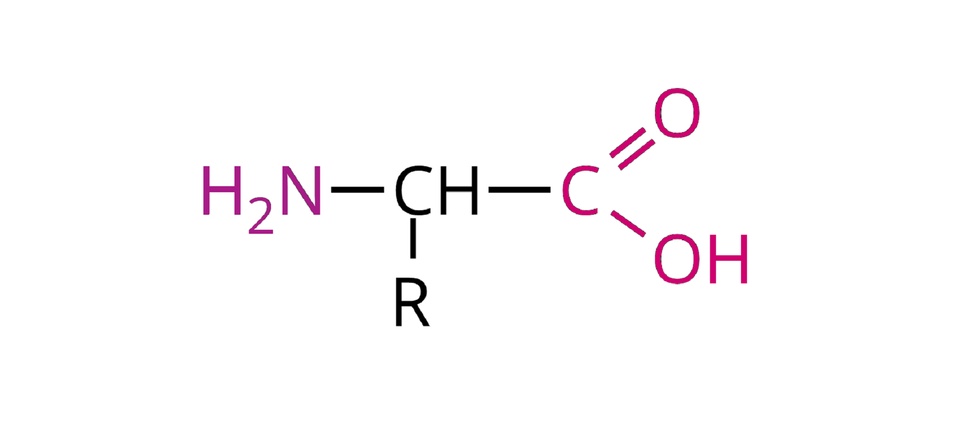
Wszystkie aminokwasy biogenne (białkowe), czyli budujące białka organizmów żywych, są -aminokwasami.
Do najprostszych przedstawicieli aminokwasów należą: glicyna (kwas -aminoetanowy, kwas aminooctowy) oraz alanina (kwas -aminopropanowy).
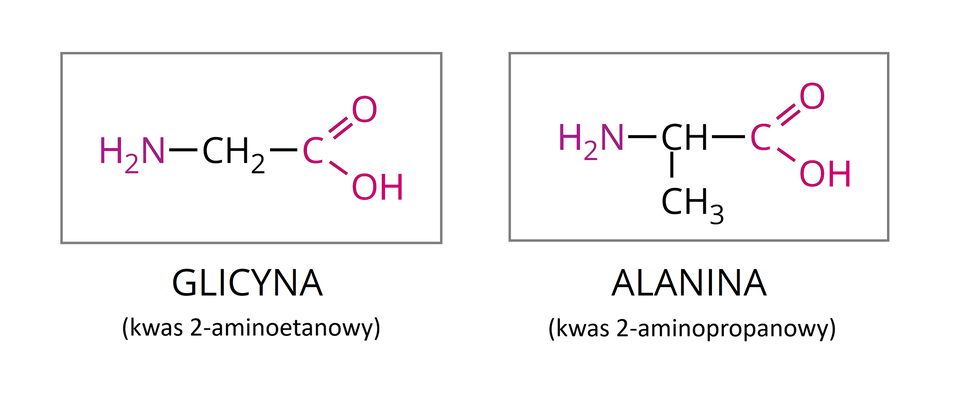
Glicyna i alanina to białe i bezwonne ciała stałe. Bardzo dobrze rozpuszczają się w wodzie. Substancje te są stosunkowo bezpieczne i nie klasyfikuje się ich jako żrące czy drażniące.
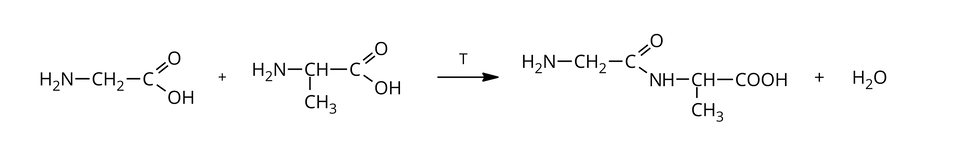
Aminokwasy w swojej budowie posiadają zarówno grupę o właściwościach zasadowych (grupa aminowa ), jak również grupę o właściwościach kwasowych (grupa karboksylowa ). Dlatego w wielu przypadkach odczyn ich wodnych roztworów jest obojętny. Dzięki posiadaniu w swojej strukturze grupy kwasowej i zasadowej, cząsteczki aminokwasów mogą łączyć się w wyniku reakcji kondensacjireakcji kondensacji. Grupa karboksylowa jednej cząsteczki łączy się z grupą aminową drugiej cząsteczki. W ten sposób powstaje wiązanie peptydowewiązanie peptydowe.
Jeżeli kondensacji ulegną dwie cząsteczki glicyny, to wówczas otrzymamy dipeptyddipeptyd – glicyloglicynę. Równanie reakcji zapisujemy następująco:
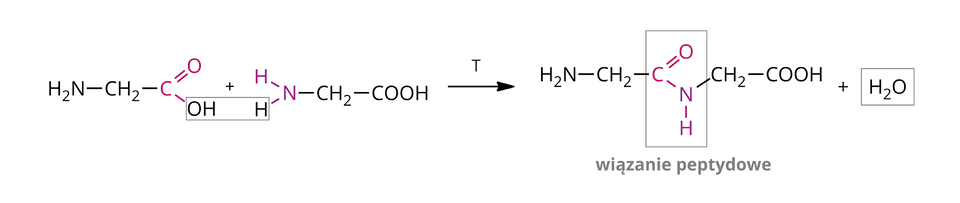
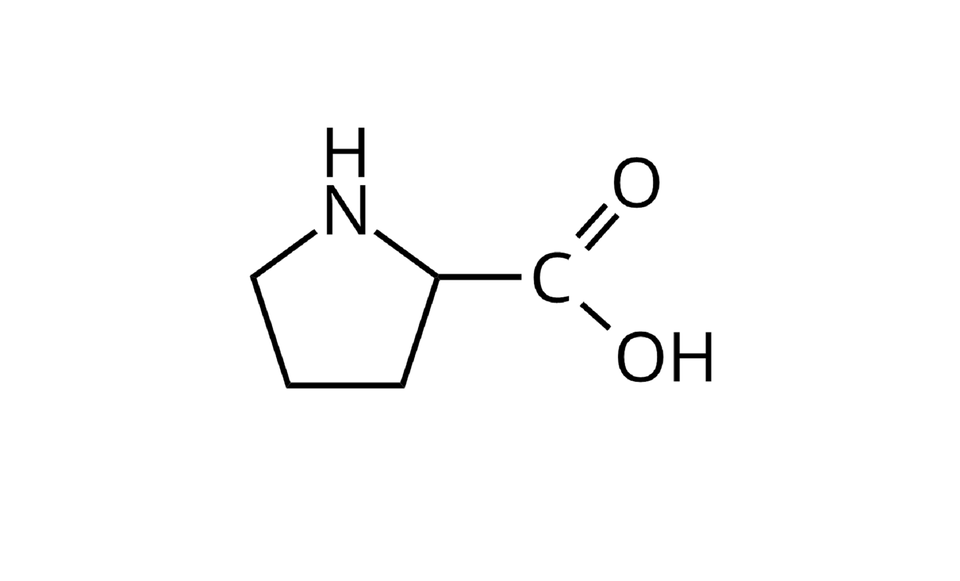
Należy przy tym pamiętać, że istnieją aminokwasy, w których grupa aminowa jest podstawiona. Przykładem takiego aminokwasu jest prolina o następującym wzorze:
Badanie podstawowych właściwości i reaktywności wybranych amin i aminokwasów
Przeprowadź doświadczenia w wirtualnym laboratorium chemicznym, w których zbadasz wybrane właściwości fizykochemicznych amin i aminokwasów. Rozwiąż podane problemy badawcze i zweryfikuj hipotezy. W formularzu zapisz obserwacje, a następnie sformułuj wnioski.
Doświadczenie 1
Doświadczenie 2
Doświadczenie 3
Zapoznaj się z opisem doświadczenia przeprowadzonego w wirtualnym laboratorium chemicznym, polegającym na zbadaniu wybranych właściwości fizykochemicznych amin i aminokwasów. Zapoznaj się z problemem badawczym, hipotezą, obserwacjami oraz wnioskami wyciągniętymi z eksperymentu.
Doświadczenie 1
Temat:
Badanie właściwości fizykochemicznych amin i aminokwasów.
Problem badawczy:
Czym różnią się właściwości fizykochemiczne wodnych roztworów wybranych amin i aminokwasów?
Hipoteza:
Aminy i aminokwasy różnią się właściwościami fizykochemicznymi (takimi jak stan skupienia, barwa i odczyn wodnego roztworu).
Sprzęt laboratoryjny:
probówki – podłużne U‑kształtne naczynie szklane do przeprowadzania prostych reakcji chemicznych;
pipety Pasteura – wąska rurka służąca do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
łyżeczka – długi trzonek wykonany ze szkła, porcelany lub metalu zakończony z jednej strony łyżeczką;
pręcik szklany – pręcik szklany, służący do mieszania cieczy.
Odczynniki chemiczne:
glicyna;
alanina;
propan--amina;
N-propan--ylopropano--amina
woda destylowana;
uniwersalne papierki wskaźnikowe.
Przebieg eksperymentu:
W probówkach umieszczono kolejno próbki badanych aminokwasów. Określono ich stan skupienia, barwę oraz zapach.
Do każdej z probówek za pomocą tryskawki dodano po kilka centymetrów sześciennych wody destylowanej.
Za pomocą bagietek wymieszano zawartości probówek i naniesiono po kilka kropli powstałych roztworów na uniwersalne papierki wskaźnikowe.
Zanotowano wszystkie obserwacje dotyczące właściwości fizykochemicznych badanych związków.
Obserwacje:
Glicyna to białe, krystaliczne ciało stałe bez zapachu. Związek ten dobrze rozpuszcza się w wodzie – powstaje bezbarwny, klarowny roztwór. Wodny roztwór glicyny nie barwi uniwersalnego papierka wskaźnikowego.
Alanina to białe, krystaliczne ciało stałe. Nie ma wyczuwalnego zapachu. Związek ten dobrze rozpuszcza się w wodzie – powstaje bezbarwny, klarowny roztwór. Wodny roztwór alaniny nie barwi uniwersalnego papierka wskaźnikowego.
Propano--amina to bezbarwna, lotna ciecz o charakterystycznym nieprzyjemnym rybim zapachu (nieco amoniakalnym). Związek ten dobrze rozpuszcza się w wodzie (miesza się w dowolnej proporcji, tworząc bezbarwny, klarowny roztwór). Wodny roztwór propan--aminy barwi uniwersalny papierek wskaźnikowy na kolor niebieski, który po przyrównaniu do skali pH wskazuje pH wynoszące około dwanaście trzynaście.
N-prop--ylopropan--amina to bezbarwna ciecz o ostrym, amoniakalnym zapachu. Związek ten dobrze rozpuszcza się w wodzie. Wodny roztwór N-propylo--propan--aminy barwi uniwersalny papierek wskaźnikowy na kolor niebieski, który po przyrównaniu do skali pH wskazuje na pH wynoszące około dwunastu.
Wyniki:
Wybrane aminy i aminokwasy to związki dobrze rozpuszczalne w wodzie. Glicyna i alanina to bezzapachowe, krystaliczne ciała stałe o białym zabarwieniu. Natomiast aminy stanowią przeźroczyste ciecze o nieprzyjemnej woni. Wodne roztwory aminokwasów nie barwią uniwersalnego papierka wskaźnikowego, zatem mają odczyn obojętny. Z kolei zmiana zabarwienia uniwersalnych papierków wskaźnikowych w kontakcie z wodnymi roztworami amin świadczy o ich zasadowym charakterze. W przypadku propano--aminy odczyn jest silniej zasadowy niż dla roztworu N-prop--ylopropan--aminy.
Wnioski:
Hipoteza została potwierdzona.
Doświadczenie 2
Temat:
Badanie reaktywności wybranych amin i aminokwasów wobec kwasów i zasad.
Problem badawczy:
Czym różni się reaktywność amin i aminokwasów względem kwasów i zasad?
Hipoteza:
Aminy i aminokwasy różnią się reaktywnością wobec kwasów i zasad.
Sprzęt laboratoryjny:
probówki – podłużne U‑kształtne naczynie szklane do przeprowadzania prostych reakcji chemicznych;
pipety Pasteura – wąska rurka służąca do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
łyżeczka – długi trzonek wykonany ze szkła, porcelany lub metalu zakończony z jednej strony łyżeczką;
pręcik szklany – pręcik szklany, służący do mieszania cieczy.
Odczynniki chemiczne:
propan--amina;
wodny roztwór alaniny;
L‑arginina (roztwór o stężeniu );
wodny roztwór kwasu chlorowodorowego o stężeniu ;
wodny roztwór wodorotlenku sodu o stężeniu ;
alkoholowy roztwór fenoloftaleiny;
wodny roztwór oranżu metylowego.
Przebieg eksperymentu:
Do trzech probówek dodano po kilka centymetrów sześciennych wodnego roztworu wodorotlenku sodu oraz po kilka kropli alkoholowego roztworu fenoloftaleiny.
Do trzech kolejnych probówek dodano po kilka centymetrów sześciennych kwasu chlorowodorowego oraz po kilka kropli wodnego roztworu oranżu metylowego.
Następnie każdy z badanych związków (w czystej postaci lub w roztworze) dodawano odpowiednio do probówki zawierającej roztwór wodorotlenku i wskaźnika oraz do probówki z roztworem kwasu i indykatora.
Zaobserwowane zmiany zanotowano.
Obserwacje:
Bezbarwny roztwór wodorotlenku sodu po dodaniu alkoholowego roztworu fenoloftaleiny przybrał intensywnie malinowe (różowe) zabarwienie. Po wprowadzeniu do niego roztworu alaniny nastąpiło odbarwienie roztworu. Natomiast zmieszanie roztworu wodorotlenku z propan--aminą nie spowodowało zmian – roztwór pozostał malinowy. Z kolei wprowadzenie do roztworu wodorotlenku sodu wodnego roztworu L‑argininy doprowadziło do zmiany malinowego koloru na bladoróżowy.
Bezbarwny roztwór kwasu chlorowodorowego po dodaniu wodnego roztworu oranżu metylowego o pomarańczowym zabarwieniu przybrał intensywnie czerwony kolor. Wymieszanie go z roztworem alaniny doprowadziło do zmiany zabarwienia na pomarańczowe. Po dodaniu do roztworu kwasu propan--aminy początkowo czerwone zabarwienie, wynikające z obecności wskaźnika, również zmieniło się na pomarańczowe, a wyczuwalny nieprzyjemny rybny zapach został zneutralizowany. Wprowadzenie roztworu L‑argininy do roztworu kwasu chlorowodorowego z oranżem metylowym spowodowało zmianę zabarwienia na pomarańczowe.
Wyniki:
Badana propano--amina ma właściwości zasadowe, o czym świadczy jej reaktywność względem kwasów i jej brak wobec zasad. Wybrane aminokwasy (alanina oraz L‑arginina) reagują zarówno z roztworem wodorotlenku sodu, jak i z roztworem kwasu chlorowodorowego. Świadczy to o obecności w ich strukturach grup odpowiadających za ich właściwości zasadowe (reaktywność względem kwasów), a także za właściwości kwasowe (reaktywność względem zasad). Są to odpowiednio grupa aminowa i grupa karboksylowa. Częściowe odbarwienie roztworu wodorotlenku sodu z fenoloftaleiną wskazuje na obecność w cząsteczce L‑argininy innych grup wykazujących charakter zasadowy – badana L‑arginina jest zaliczana do aminokwasów zasadowych, ponieważ zawiera w swej strukturze grupę guanidynową składającą się z atomu węgla połączonego z trzema atomami azotu, w tym z jednym za pomocą wiązania podwójnego.
Wnioski:
Hipoteza została potwierdzona.
Doświadczenie 3
Temat:
Wykrywanie aminokwasów aromatycznych.
Problem badawczy:
Czy można odróżnić aminokwasy aromatyczne od pozostałych aminokwasów (niezawierających w swoich strukturach grup arylowych)?
Hipoteza:
Aminokwasy aromatyczne można odróżnić od aminokwasów alifatycznych (niezawierających w swoich strukturach grup arylowych, tudzież aromatycznych).
Sprzęt laboratoryjny:
probówki – podłużne U‑kształtne naczynie szklane do przeprowadzania prostych reakcji chemicznych;
pipety Pasteura – wąskie rurki służące do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
łapa laboratoryjna – rodzaj dwuramiennego narzędzia wykonanego przykładowo z drewna oraz wykorzystywanego w laboratorium do trzymania głównie probówek lub małych kolb podczas ogrzewania;
łaźnia wodna (termostat) – urządzenie wyposażone w pojemnik z wodą i w grzałkę, która zapewnia wypełniającemu go medium (tutaj wodzie) zadaną temperaturę.
Odczynniki chemiczne:
wodny roztwór glicyny;
wodny roztwór alaniny;
wodny roztwór tyrozyny;
wodny roztwór tryptofanu;
stężony kwas azotowy.
Przebieg eksperymentu:
W czterech probówkach umieszczono kolejno po kilka centymetrów sześciennych roztworów badanych aminokwasów (glicyny, alaniny, tyrozyny i tryptofanu).
Do wszystkich probówek dodano po kilka centymetrów sześciennych stężonego kwasu azotowego.
Następnie kolejno ogrzewano przez dwie minuty zawartości probówek z wykorzystaniem łaźni wodnej nastawionej na osiemdziesiąt stopni Celsjusza.
Na koniec zanotowano obserwacje.
Obserwacje:
Wszystkie aminokwasy utworzyły z kwasem azotowym bezbarwne roztwory. W wyniku ogrzewania zawartość probówek zawierających tryptofan oraz tyrozynę przybrała żółte zabarwienie. Roztwory sporządzone dla pozostałych aminokwasów pozostały bezbarwne.
Wyniki:
Aminokwasy aromatyczne można odróżnić od alifatycznych w reakcji z kwasem azotowym, prowadzącej do powstawania żółtych roztworów. Zabarwienie wynika z obecności w strukturach wspomnianych związków pierścieni aromatycznych ulegających reakcji nitrowania. Aminokwasy alifatyczne nie reagują z kwasem azotowym.
Wnioski:
Hipoteza została potwierdzona.
Wodny roztwór metanoaminy wykazuje odczyn zbliżony do: Możliwe odpowiedzi: 1. wodnego roztworu glicyny, 2. wodnego roztworu alaniny, 3. kwasu chlorowodorowego, 4. wodnego roztworu amoniaku
Podaj nazwę grupy funkcyjnej charakterystycznej zarówno dla amin, jak i aminokwasów.
Słownik
organiczne pochodne amoniaku, zawierające w swojej budowie atom azotu z wolną parą elektronową
pochodne węglowodorów, posiadające w budowie grupę aminową () oraz grupę karboksylową ()
produkt połączenia (kondensacji) dwóch aminokwasów
dokument zawierający dane dotyczące określonej substancji chemicznej (lub mieszaniny), wśród nich opis zagrożeń związanych z jej użytkowaniem, sposoby bezpiecznego magazynowania oraz utylizacji, schemat działania w razie narażenia na tę substancję (np. poprzez kontakt z oczami, skórą czy drogami oddechowymi), a także informacje dotyczące sposobu postępowania w przypadku przedostania się jej do środowiska, zalecanych środków gaśniczych oraz wskazanych środków ochrony indywidualnej
reakcja, w której pod wpływem temperatury łączą się co najmniej dwie cząsteczki aminokwasów z wydzieleniem cząsteczki wody jako produktu ubocznego
wiązanie tworzące się pomiędzy atomem węgla grupy karboksylowej jednej cząsteczki aminokwasu a atomem azotu grupy aminowej drugiej cząsteczki aminokwasu
Ćwiczenia
Przygotowano wodne roztwory etanoaminy i alaniny. Zanurzono w nich uniwersalne papierki wskaźnikowe. W jednym roztworze zaobserwowano niebieskie zabarwienie uniwersalnego papierka wskaźnikowego, a w drugim nie zaobserwowano zmian barwy. Dopasuj wzór badanej substancji do wyniku doświadczenia przedstawionego na schematycznym rysunku.
Przygotowano wodne roztwory etanoaminy i alaniny. Zanurzono w nich uniwersalne papierki wskaźnikowe. W jednym roztworze zaobserwowano niebieskie zabarwienie uniwersalnego papierka wskaźnikowego, a w drugim nie zaobserwowano zmian barwy. Dopasuj wzór badanej substancji do wyniku doświadczenia.
Poniżej przedstawiono wzór produktu kondensacji cząsteczek aminokwasów.
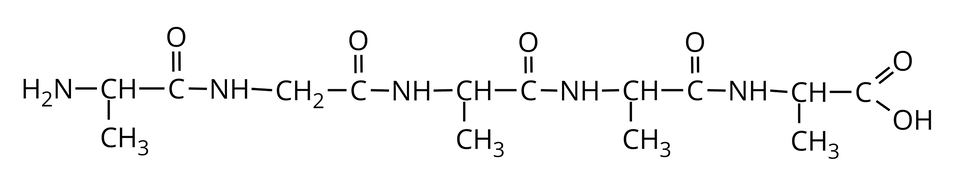
Ile wiązań peptydowych zawiera powyższa cząsteczka peptydu? Ile cząsteczek alaniny i ile cząsteczek glicyny wzięło udział w reakcji kondensacji prowadzącej do powstania tego produktu? Wpisz odpowiednią liczbę.
Wiedząc, że kondensacja aminokwasów to reakcja, w której pod wpływem temperatury łączą się co najmniej dwie cząsteczki aminokwasów z wydzieleniem cząsteczki wody jako produktu ubocznego, zapisz równanie reakcji glicyny z alaniną.
Bibliografia
Kulawik J., Kulawik T., Litwin M.; Podręcznik do chemii dla klasy ósmej szkoły podstawowej; Nowa Era 2020.
Łasiński D., Sporny Ł., Strutyńska D., Wróblewski P., Podręcznik dla klasy ósmej szkoły podstawowej, Mac Edukacja 2020.