Właściwości tlenku węgla(IV)
Co wiemy o gazie będącym składnikiem powietrza, biorącym udział w procesie fotosyntezy, stosowanym do nasycenia napojów gazowanych, a także jako środek gaśniczy? Czy gaz, który wydychamy z płuc, może okazać się zabójczy?

w jaki sposób można dowieść, że powietrze istnieje;
co to jest powietrze i jaki jest jego skład;
w jaki sposób można doświadczalnie potwierdzić, że powietrze jest mieszaniną;
jakie kryteria przyjmuje się do klasyfikacji typów reakcji chemicznych;
jak zapisuje się równania reakcji chemicznych;
co to są tlenki i jak można zaplanować ich otrzymywanie na drodze spalania;
jak domowym sposobem można otrzymać tlenek węgla(IV);
jak rozpoznaje się podstawowy sprzęt laboratoryjny i jak należy się nim posługiwać oraz jakich zasad bezpieczeństwa trzeba przestrzegać w szkolnej pracowni chemicznej.
wymieniać źródła tlenku węgla(IV);
omawiać obieg tlenku węgla(IV) w przyrodzie;
przedstawiać wzór sumaryczny i strukturalny tlenku węgla(IV);
planować i wykonywać doświadczenie pozwalające na otrzymanie i identyfikację tlenku węgla(IV);
projektować i przeprowadzać doświadczenie pozwalające zbadać podstawowe właściwości tlenku węgla(IV);
oceniać znaczenie tlenku węgla(IV) i podawać przykłady jego zastosowania w życiu codziennym;
bezpiecznie posługiwać się sprzętem laboratoryjnym oraz odczynnikami chemicznymi.
1. Jedna z najbardziej tajemniczych katastrof w historii
Rankiem 22 sierpnia 1986 r. w Kamerunie obszar otaczający jezioro Nyos, położone na zboczu nieczynnego wulkanu (900 m n.p.m.), wyglądał na zupełnie wymarły. Z siedmiuset mieszkańców jednej z wiosek, którzy jeszcze dzień wcześniej oddawali się codziennym czynnościom, przeżyło zaledwie sześciu. Ich oczom ukazał się przerażający widok. W obrębie 30 km od jeziora życie straciło 1746 osób i wiele tysięcy sztuk zwierząt. Zagadkowy był brak jakichkolwiek zewnętrznych obrażeń. Osoby przybyłe nad jezioro zdziwiło obniżenie tafli o około metr, zmiana koloru wody z niebieskiej na czerwoną oraz drzewa leżące przy brzegu drzewa jak po przejściu tsunami. Ci, którzy przeżyli, mieli kłopoty ze zdrowiem, mówili, że wszystkiemu winien jest duch jeziora. A jak było naprawdę?

Przyjmuje się, iż nagromadzone pod dnem jeziora potężne ilości gazu wydostały się ponad jego powierzchnię. Dwutlenek węgla ma gęstość ok. 1,5 razy większą od gęstości powietrza. Wypełniając dolinę, wyparł z niej powietrze, zawierające niezbędny do życia tlen. Chociaż nie jest gazem toksycznym, może powodować zgon przez uduszenie. Gdy jego zawartość w powietrzu przekroczy 10%, mogą pojawić się omamy i śpiączka, a przy 20% śmierć następuje w ciągu kilkunastu minut.
2. Obieg dwutlenku węgla w przyrodzie
Dwutlenek węgla jest ważnym składnikiem powietrza atmosferycznego (0,03% objętości). Stanowi niezbędny substrat w procesie fotosyntezy.


Film dostępny na portalu epodreczniki.pl
3_Obieg / Obieg dwutlenku węgla w przyrodzie
3. Otrzymywanie i właściwości tlenku węgla(IV)
Czy dwutlenek węgla otrzymany z sody oczyszczonej i octu podtrzymuje palenie się świeczki?
Wybierz jedną z przedstawionych hipotez, a następnie zweryfikuj ją.
Dwutlenek węgla jest gazem, który podtrzymuje palenie się świeczki.
Dwutlenek węgla jest gazem, który nie podtrzymuje palenia się świeczki.
plastikowa butelka,
soda oczyszczona,
ocet,
balon,
świeczka typu podgrzewacz,
dwie zlewki,
lejek.
Do butelki wlej niewielką ilość octu (maksymalnie 1/3 objętości butelki).
Do balonu za pomocą lejka wsyp 1 łyżeczkę sody oczyszczonej.
Zapal umieszczoną we wnętrzu zlewki świeczkę.
Wylot balonu nałóż na szyjkę butelki, a następnie dodaj do octu sodę.
Zebranym w balonie gazem napełnij drugą zlewkę.
„Przelej” dwutlenek węgla do zlewki z zapaloną świeczką.
Obserwuj zachodzące zmiany.
R1NEmbmG1EvL31 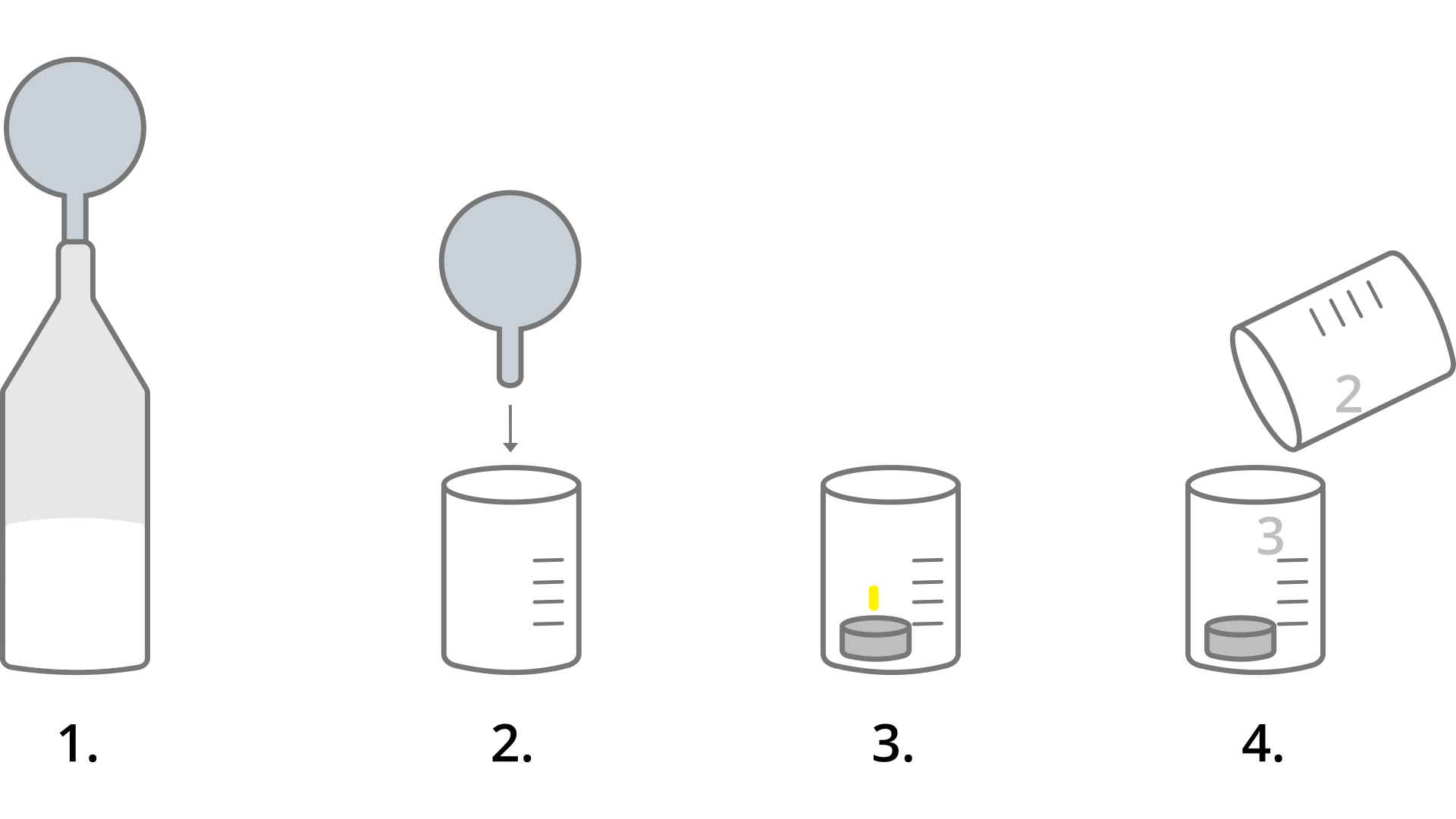 Otrzymywanie dwutlenku węgla i badanie jego właściwości
Otrzymywanie dwutlenku węgla i badanie jego właściwości
W wyniku zmieszania sody z octem wydziela się bezbarwny gaz, który wypełnia balon. Przeniesiony z balonu do zlewki, a następnie przelany do zlewki z palącą się świeczką, gaz powoduje jej zgaśnięcie.
Gazowy produkt reakcji kwasu z sodą to tlenek węgla(IV). Jest to substancja bezbarwna, bezwonna, ma gęstość większą od gęstości powietrza, nie pali się i nie podtrzymuje palenia.
Odszukaj w tablicach chemicznych gęstość dwutlenku węgla i porównaj ją z gęstością powietrza. Zapisz odczytane wartości gęstości w zeszycie.
Określ położenie tlenu i węgla w układzie okresowym oraz ich stan skupienia w temperaturze pokojowej.
Dwutlenek węgla to zwyczajowa nazwa tlenku węgla(IV). Jest on ważnym składnikiem powietrza. Jego zawartość w powietrzu jest zmienna. W odróżnieniu od azotu, tlenu, argonu i pozostałych gazów szlachetnych tlenek węgla(IV) jest związkiem chemicznym. Jego cząsteczka jest zbudowana z atomów dwóch pierwiastków: węgla i tlenu.
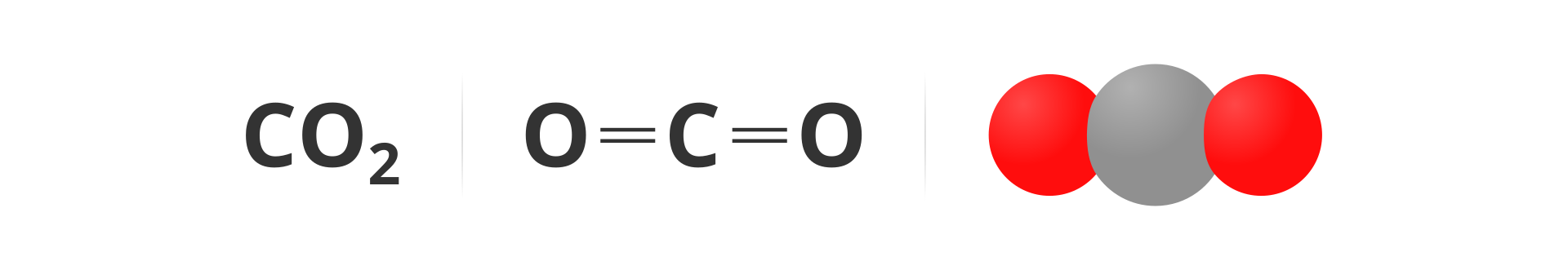
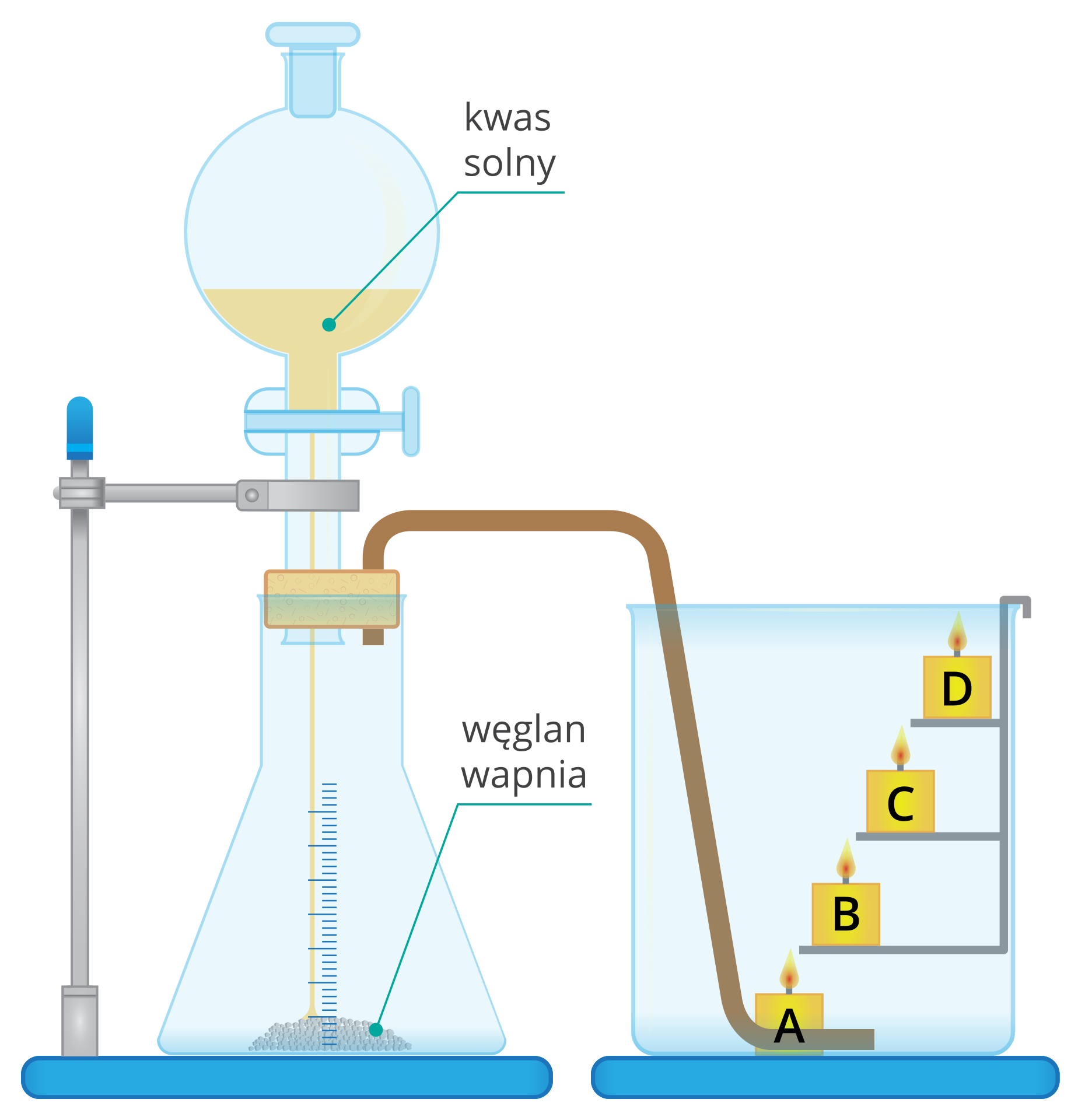
W jakiej kolejności tlenek węgla(IV) będzie gasił świeczki umieszczone w zlewce na różnych wysokościach?
Wybierz jedną z przedstawionych hipotez, a następnie zweryfikuj ją.
Zbierany w zlewce tlenek węgla(IV) wywoła gaśnięcie świeczek, zaczynając od tej znajdującej się najniżej.
Zbierany w zlewce tlenek węgla(IV) wywoła gaśnięcie świeczek, zaczynając od tej znajdującej się najwyżej.
węglan wapnia,
kwas solny,
kolba stożkowa,
zlewka ze świeczkami umieszczonymi na różnych wysokościach,
korek z wkraplaczem i rurką odprowadzającą.
Do kolby z węglanem wapnia wlej rozcieńczony kwas solny.
Zamknij kolbę korkiem z rurką odprowadzającą.
Ostrożnie zapal świeczki, a następnie końcówkę rurki odprowadzającej umieść w zlewce.
Obserwuj zachodzące zmiany.

W wyniku reakcji węglanu wapnia z kwasem solnym wydzielają się pęcherzyki gazu.
Przebieg reakcji opisuje równanie
Zlewka stopniowo wypełnia się gazem, który gromadzi się na jej dnie, powodując gaszenie świeczek. Najpierw gaśnie świeczka znajdująca się najniżej, a na końcu – znajdująca się najwyżej. Wydzielającym się gazem jest tlenek węgla(IV), który nie podtrzymuje palenia i jest cięższy od powietrza.

Film dostępny na portalu epodreczniki.pl
Animacja prezentująca otzynywanie tlenku węgla IV). Demonstrator wsypuje do kolby stożkowej węglan wapnia i zamyka ją korkiem z wkraplaczem i rurką odprowadzającą. W kolejnym kroku Następnie wlewa do wkraplacza rozcieńczonego roztworu kwasu solnego. Koniec rurki umieszcza w zlewce ze świeczkami umieszczonymi na różnych wysokościach oraz otwiera kranik wkraplacza
Zaproponuj sposób wykrywania obecności tlenku węgla(IV).
W jaki sposób można wykryć obecność tlenku węgla(IV)?
Wybierz jedną z przedstawionych hipotez, a następnie zweryfikuj ją.
Tlenek węgla(IV) po wprowadzeniu do wody wapiennej powoduje reakcję barwną.
Tlenek węgla(IV) po wprowadzeniu do wody wapiennej powoduje jej zmętnienie.
dwie probówki lub małe zlewki,
słomka do napojów,
woda wapienna.
Do probówek lub małych zlewek wlej taką samą ilość wody wapiennej.
Do jednej z nich włóż koniec rurki lub słomki i wdmuchuj przez nią powietrze z płuc.
Obserwuj zachodzące zmiany.
RFFr7r3YtEZrg1  Wykrywanie tlenku węgla(IV) – zlewka z wodą wapienną przed doświadczeniem (1) i w trakcie doświadczenia (2)
Wykrywanie tlenku węgla(IV) – zlewka z wodą wapienną przed doświadczeniem (1) i w trakcie doświadczenia (2)
Gaz wydychany z płuc po wprowadzeniu do wody wapiennejwody wapiennej powoduje jej zmętnienie.
Mętnienie wody wapiennej pod wpływem tlenku węgla(IV) jest reakcją charakterystycznąreakcją charakterystyczną, pozwalającą na identyfikację tej substancji. Powietrze wydychane z płuc zawiera dwutlenek węgla.
Czy już wiesz, jaki związek chemiczny wydychamy z płuc oraz jak można go zidentyfikować?
*Metodę wykrywania dwutlenku węgla z użyciem wody wapiennej zaproponował szkocki chemik Joseph Black (1728–1799).
Zaplanuj eksperyment, postaw hipotezę i zbadaj jaki gaz:
znajduje się w wodzie gazowanej,
wydziela się w wyniku rozpuszczania tabletki musującej w wodzie.
Zapisz obserwacje i wnioski.
Wskazówka do eksperymentu 1.

Suchy lódSuchy lód i sublimacjasublimacja
Dwutlenek węgla pod ciśnieniem atmosferycznym w temperaturze –78°C zamienia swój stan skupienia w ciało stałe, tzw. suchy lód. Stały wyglądem przypomina lód, jednak zamiast topić się, sublimuje, tworząc gazowy tlenek węgla(IV), stąd nazwa suchy lód.

Czad to zwyczajowa nazwa tlenku węgla(II), który powstaje przy niecałkowitym spalaniu paliw (drewno, olej, gaz) przy ograniczonym dostępie tlenu. Tlenek węgla(II) jest toksycznym, bezbarwnym, bezwonnym gazem, zwanym cichym zabójcą. Dostaje się do organizmu przez układ oddechowy i jest wchłaniany do krwioobiegu, blokując dopływ tlenu, gdyż tlenek węgla(II) wiąże się z hemoglobiną 210 razy szybciej niż tlen. Stwarza to poważne zagrożenie zdrowia i życia człowieka. Każdego roku blisko dwa tysiące osób ulega zatruciu czadem, a ponad sto z tego powodu umiera.

4. Zastosowanie tlenku węgla(IV)
Tlenek węgla(IV) jest gazem dobrze rozpuszczalnym w wodzie, dlatego znalazł zastosowanie w przemyśle spożywczym do produkcji napojów gazowanych. Dwutlenek węgla nie podtrzymuje palenia i gasi ogień, dlatego wykorzystuje się go w gaśnicach pianowych (jako gaz nośny) oraz w gaśnicach śniegowych (jako środek gaśniczy).
Zestalony tlenek węgla(IV) jest środkiem chłodzącym stosowanym podczas transportu i przechowywania produktów spożywczych, w szczególności owoców i warzyw. Dzięki niskiej temperaturze przyczynia się do zahamowania rozwoju bakterii i grzybów. Suchy lód jest także stosowany w medycynie do przechowywania preparatów i szczepionek oraz w krioterapii (leczeniu zimnem).
Doświadczenie należy przeprowadzać pod nadzorem osób dorosłych, najlepiej na świeżym powietrzu (ze względu na duży strumień piany).
W jakim celu w doświadczeniu używa się płynu do mycia naczyń?
Płyn do mycia naczyń powoduje powstawanie tlenku węgla(IV).
Dodanie płynu do mycia naczyń powoduje powstanie piany.
plastikowa butelka z dozownikiem,
soda oczyszczona,
kwasek cytrynowy,
płyn do mycia naczyń,
zlewka,
świeczka.
Do pustej butelki wlej 200 ml wody.
Dodaj dwie łyżeczki sody oczyszczonej i wstrząśnij.
Dodaj około 30 ml płynu do mycia naczyń i ponownie wstrząśnij.
Przy użyciu lejka szybko dodaj trzy czubate łyżeczki kwasku cytrynowego.
Bardzo szybko zatkaj butelkę.
Na folii, np. malarskiej, ustaw palącą się w zlewce świeczkę, a następnie wstrząśnij zawartością butelki, skieruj wylot domowej gaśnicy nad świeczkę i pociągnij zatyczkę, żeby ją otworzyć.
W wyniku reakcji sody z kwaskiem cytrynowym w zamkniętej butelce powstaje tlenek węgla(IV), który zostaje uwolniony po otwarciu dyfuzora, tworząc w połączeniu z płynem do mycia naczyń fontannę z piany.
Woda nasycona dwutlenkiem węgla – woda sodowa. W 1767 r. John Priestley (czyt. Dżon Pristlej), zawieszając miskę wody nad kadzią piwa, odkrył sposób nasycenia wody dwutlenkiem węgla. Przygotowana w ten sposób woda miała przyjemny smak, a Priestley ogłosił swoje odkrycie w prasie. W artykule opisał produkcję wody gazowanej, polegającą na dodawaniu kwasu do kredy w celu wytworzenia dwutlenku węgla, a następnie nasycania nim wody.
Pod koniec XVIII w. Johann J. Schweppe (czyt. Johan Schłepe)udoskonalił tę technologię i woda gazowana wytwarzana była poprzez nasycenie wody dwutlenkiem węgla pod ciśnieniem. Wyższe ciśnienie zwiększa rozpuszczalność tlenku węgla(IV) w porównaniu z warunkami ciśnienia atmosferycznego. Po otwarciu butelki ciśnienie zostaje wyrównane, co sprawia, że gaz uwalnia się z roztworu, tworząc charakterystyczne pęcherzyki (Pyrmont water).
Podsumowanie
Dwutlenek węgla to zwyczajowa nazwa tlenku węgla(IV). Jest on składnikiem powietrza. Jego zawartość w powietrzu jest zmienna. Powstaje w procesach oddychania, fermentacji i spalania.
Pod wpływem światła słonecznego, w obecności chlorofilu znajdującego się w komórkach, tlenek węgla(IV) z udziałem wody przekształca się w tlen oraz glukozę. Proces ten nazywany jest fotosyntezą.
Tlenek węgla(IV) jest bezbarwnym gazem, dobrze rozpuszczalnym w wodzie, o gęstości około 1,5 razy większej od gęstości powietrza. Nie pali się i nie podtrzymuje palenia.
Tlenek węgla(IV) stosowany jest jako materiał chłodniczy, środek gaśniczy, gaz do napełniania kamizelek i pontonów ratunkowych.
Tlenek węgla(IV) nie jest gazem toksycznym, jednak jego duże stężenie może nawet powodować śmierć.
Człowiek wydycha z płuc około 416 kg dwutlenku węgla rocznie. Oblicz, ile kilogramów wydycha w ciągu tygodnia.
Korzystając z dostępnych źródeł, przygotuj wykres ilustrujący emisję tlenku węgla(IV) w Polsce (w tonach na 1 mieszkańca) dla trzech lub czterech wartości od roku 1990 do dziś. Porównaj i zinterpretuj zebrane dane.
Przygotuj infografikę ilustrującą otrzymywanie i wykrywanie tlenku węgla(IV).
Przygotuj ulotkę ostrzegającą przed niebezpieczeństwem wynikającym z obecności tlenku węgla(II) (czadu) w pomieszczeniach.
Słowniczek
reakcja umożliwiająca wykrycie (identyfikację) danej substancji
przemiana fazowa polegająca na bezpośrednim przejściu substancji z fazy stałej do stanu gazowego z pominięciem fazy ciekłej
zestalony tlenek węgla(IV)
nasycony roztwór wodorotlenku wapnia w wodzie, odczynnik laboratoryjny, który umożliwia identyfikację tlenku węgla(IV)
Zadania
Wykorzystaj przygotowane naczynia laboratoryjne do zbudowania zestawu, w którym można będzie otrzymać tlenek węgla(IV).

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DhbJALC4k
Uczniowie mieli za zadanie podać substraty, z jakich można otrzymać tlenek węgla(IV). Która z osób błędnie wykonała zadanie?
- Maciej – Tlenek węgla(IV) tworzy się w czasie rozkładu wody wapiennej.
- Igor – Tlenek węgla(IV) można otrzymać w wyniku spalania węgla w tlenie.
- Marta – Tlenek węgla(IV) można otrzymać, dodając ocet do sody oczyszczonej.
- Lena – Tlenek węgla(IV) wydziela się, gdy rozpuszczamy tabletkę musującą w ciepłej wodzie.
Oceń czy podane informacje są prawdziwe, czy fałszywe.
| Prawda | Fałsz | |
| Zestalony dwutlenek węgla jest nazywany zimnym lodem. | □ | □ |
| Czad to potoczna nazwa tlenku węgla(II). | □ | □ |
| Tlenek węgla(IV) można wykryć za pomocą wody wapiennej. | □ | □ |
| Oziębiony do temperatury –78°C tlenek węgla(IV) ulega resublimacji. | □ | □ |
Do zlewki z zapalonymi świeczkami powoli wprowadzono tlenek węgla(IV). Wskaż, w jakiej kolejności zgasły świeczki (A, B, C, D).
3, 1, 2, 4
Oceń, czy podane informacje o tleneku węgla(IV) są prawdziwe, czy fałszywe.
| Prawda | Fałsz | |
| W temperaturze pokojowej jest substancją stałą. | □ | □ |
| W temperaturze pokojowej jest gazem. | □ | □ |
| Przewodzi prąd elektryczny. | □ | □ |
| Podtrzymuje palenie. | □ | □ |
| Ma gęstość mniejszą od powietrza. | □ | □ |