Tlen i tlenki (część 1)
Poniższy materiał stanowi uzupełnienie treści znajdujących się w materiale: https://zpe.gov.pl/a/tlen/DmclimloH
Tlen jest jednym z najczęściej występujących pierwiastków chemicznych na Ziemi. Jako cząsteczka dwuatomowa (), znajduje się w niższych warstwach atmosfery i jest jednym z głównych składników powietrza. W tej postaci jest bezbarwnym gazem, niezbędnym do przetrwania wszystkim roślinom i zwierzętom. Ponadto tlen wchodzi w skład wielu związków chemicznych, wśród których znajdują się tlenki.
czym różni się atom od cząsteczki, czym jest wiązanie kowalencyjne niespolaryzowane;
w jaki sposób zapisywać równania reakcji chemicznych w formie cząsteczkowej;
w jaki sposób dobierać współczynniki stechiometryczne w równaniach reakcji chemicznych;
czym jest katalizator i jaki jest jego wpływ na przebieg reakcji chemicznej.
opisywać wybrane właściwości fizyczne i chemiczne tlenu;
zapisywać równania reakcji tlenu z wybranymi metalami i niemetalami;
wskazywać zastosowania tlenu;
projektować i przeprowadzać doświadczenie chemiczne polegające na otrzymywaniu tlenu oraz tlenków;
zapisywać równania reakcji otrzymywania tlenu;
analizować i oceniać czynniki wpływające na obieg tlenu w przyrodzie.
Tlen
TlenTlen to pierwiastek zaliczany do niemetali, położony w okresie, w grupie układu okresowego. W przyrodzie występuje w postaci cząsteczek dwuatomowych, stanowiąc objętościowych powietrza, a także w niewielkim stopniu w postaci trójatomowej jako ozon, czyli jednej z odmian alotropowych tlenu, tworząc warstwę ozonową w ozonosferze, dzięki czemu zapobiega on docieraniu do powierzchni Ziemi szkodliwego promieniowania z zakresu ultrafioletu. Tlen jest w pewnym stopniu rozpuszczalny w wodzie, co umożliwiło ewolucję organizmów, które zaczęły wykorzystywać go w procesie oddychania.
Cząsteczka tlenu składa się zatem z dwóch atomów tlenu połączonych za pomocą dwóch wiązań kowalencyjnych niespolaryzowanych, stanowiących wiązanie podwójne.
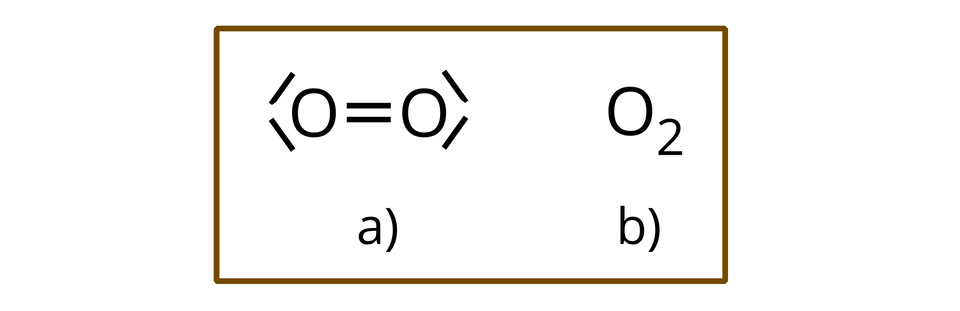
Tlen jest bezbarwnym i bezwonnym gazem o gęstości wynoszącej w temperaturze równej i pod ciśnieniem atmosferycznym (), która to jest większa od gęstości powietrza.
Tlen słabo rozpuszcza się w wodzie, jednak rozpuszczalność ta jest ściśle uzależniona od temperatury. Należy bowiem pamiętać, że wraz ze wzrostem temperatury rozpuszczalność tlenu (oraz innych gazów) w wodzie maleje. Jednak pomimo słabej rozpuszczalności tlenu w wodzie jego ilość jest wystarczająca, aby umożliwić organizmom żywym przetrwanie w zbiornikach wodnych.
Tlen jest gazem niepalnym, ale podtrzymującym spalanie. Dlatego na przykład podczas palenia świecy niezbędny jest stały dostęp do tlenu.
Oprócz tego, że tlen jest niezbędny do życia, to znalazł szereg zastosowań. Wykorzystywany jest między innymi w medycynie, w tak zwanych terapiach tlenowych, stosowanych u osób z chorobami układu oddechowego. Nurkowie, kosmonauci czy wspinacze górscy stosują butle z mieszaniną gazów, w których skład wchodzi tlen, pozwalające im oddychać w skrajnych dla organizmu warunkach. Tlen jest również szeroko wykorzystywany w przemyśle chemicznym i rakietowym.

W Zygmunt Wróblewski oraz Karol Olszewski dokonali pierwszego na świecie skroplenia tlenu ( kwietnia) i azotu ( kwietnia). Stanowiło to ogromne osiągnięcie w ówczesnym świecie naukowym. Do tej pory prace profesorów są najczęściej cytowanymi spośród prac polskich naukowców w tamtych latach. Ciekły tlen charakteryzuje jasnoniebieska barwa i gęstość nieco większa od gęstości wody. Ciecz wrze w temperaturze pod ciśnieniem atmosferycznym. W stanie ciekłym tlen znajduje się w dogodnej formie przeznaczonej zarówno do przechowywania, jak i transportu. Ciekły tlen stanowi powszechnie wykorzystywany czynnik utleniający paliwo rakietowe.

Tlenki
Tlen w połączeniu z innym pierwiastkiem tworzy bardzo dużą grupę związków chemicznych o nazwie tlenki. Tlenki są zbudowane z atomu (lub atomów) tlenu oraz metalu lub niemetalu. Tlen w tlenkach przyjmuje wartościowość równą , zatem wzór ogólny tlenków można zapisać następująco:
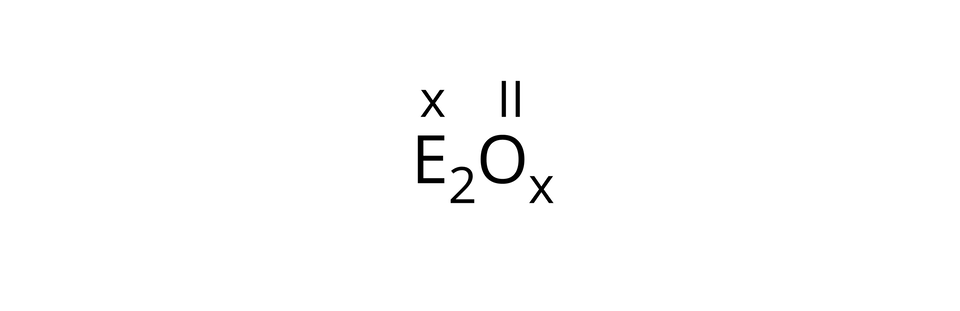
Tlenki możemy otrzymać między innymi poprzez bezpośrednią reakcję tlenu z metalem lub niemetalem. Jest to reakcja spalania.
Słownik
pierwiastek chemiczny o liczbie atomowej , niemetal z grupy tlenowców w układzie okresowym
-procentowy roztwór wodny nadtlenku wodoru ; stosowana do odkażania ran
– nieorganiczny związek chemiczny, nadmanganian potasu
Otrzymywanie tlenu i badanie jego właściwości chemicznych
Przeprowadź doświadczenie w wirtualnym laboratorium chemicznym polegające na otrzymaniu tlenu w wyniku katalitycznego rozkładu wody utlenionejwody utlenionej, czyli wodnego roztworu nadtlenku wodoru o stężeniu . Następnie zbadaj reaktywność tlenu względem wybranych pierwiastków. Rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz obserwacje, a następnie sformułuj wnioski.
Zapoznaj się z opisem doświadczenia w wirtualnym laboratorium chemicznym polegającego na otrzymaniu tlenu w wyniku katalitycznego rozkładu wody utlenionejwody utlenionej, czyli wodnego roztworu nadtlenku wodoru o stężeniu , a następnie z eksperymentami pozwalającymi na zbadanie reaktywności tlenu względem wybranych pierwiastków. Zapoznaj się z problemem badawczym i zweryfikowaną hipotezą, obserwacjami i wnioskami.
Temat:
Otrzymywanie tlenu w wyniku katalitycznego rozkładu wody utlenionej.
Problem badawczy:
Czy podczas działania tlenkiem manganu() na roztwór nadtlenku wodoru otrzymamy tlen?
Hipoteza:
Na przykład: Działając tlenkiem manganu() na roztwór nadtlenku wodoru (dioksydanu), otrzymamy tlen.
Sprzęt laboratoryjny:
statyw z probówką z korkiem i rurką odprowadzającą;
krystalizator;
probówka;
drewniane łuczywo;
zapałki;
pipeta Pasteura;
łyżeczka.
Odczynniki chemiczne:
wodny roztwór nadtlenku wodoru o stężeniu ;
tlenek manganu().
Przebieg eksperymentu
Za pomocą pipety należy wlać do probówki około wody utlenionej.
Następnie należy umieścić probówkę w statywie i dodać za pomocą łyżeczki niewielką ilość tlenku manganu().
Należy szybko zamknąć probówkę korkiem z rurką odprowadzającą, umieszczoną w probówce odwróconej do góry dnem i wypełnionej wodą.
Do probówki z zebranym gazem należy wprowadzić rozżarzone łuczywo drewniane.
Obserwacje:
Po dodaniu do roztworu nadtlenku wodoru niewielkiej ilości tlenku manganu() zawartość probówki zaczyna się intensywnie pienić, co spowodowane jest powstawaniem gazu. Probówka ogrzewa się a nad nią unosi się para. Natomiast w probówce umieszczonej w krystalizatorze zbiera się bezbarwny i bezwonny gaz, który wypiera wodę z probówki. Rozżarzone łuczywo umieszczone w probówce powoduje rozbłysk w jej wnętrzu, przy dnie łuczywo pali się intensywnym płomieniem.
Wyniki:
Otrzymanym gazem jest tlen. Świadczy o tym rozpalenie się łuczywa w probówce wypełnionej gazem. Intensywny płomień na dnie probówki może wskazywać, że otrzymany gaz ma gęstość większą od powietrza i podtrzymuje spalanie (łuczywo wyraźnie płonie).
Woda utleniona rozkłada się do tlenu i wody. Tlenek manganu() nie został zużyty podczas doświadczenia. Jest zatem katalizatorem reakcji rozkładu wody utlenionej, czyli ją przyspiesza. Zaszła reakcja opisana poniższym równaniem:
Wnioski:
Hipoteza została potwierdzona.
lub
Hipoteza nie została potwierdzona.
Następnie zapoznaj się z opisem doświadczenia w wirtualnym laboratorium chemicznym polegającego na badaniu właściwości chemicznych tlenu przez spalanie w tlenie różnych pierwiastków chemicznych. Zapoznaj się z problemem badawczym i zweryfikowaną hipotezą, obserwacjami i wnioskami.
Temat:
Badanie właściwości chemicznych tlenu.
Problem badawczy:
Jak przebiega proces spalania (utleniania) poszczególnych pierwiastków chemicznych?
Hipoteza:
Na przykład: Wynikami spalania magnezu, węgla, siarki i sodu są tlenki tych pierwiastków chemicznych.
Sprzęt laboratoryjny:
palnik;
łyżka laboratoryjna do spalań;
zapałki;
bibuła;
pęseta.
Odczynniki chemiczne:
magnez;
węgiel;
siarka;
sód.
Przebieg eksperymentu:
Za pomocą zapałki należy rozpalić płomień nad palnikiem.
W przypadku sodu należy go najpierw chwycić pęsetą i odsączyć za pomocą bibuły.
Następnie należy nałożyć na łyżeczkę porcję wybranego pierwiastka chemicznego.
Należy umieścić łyżeczkę z odczynnikiem nad płomieniem palnika.
Obserwacje:
Umieszczony na łyżeczce pierwiastek chemiczny spala się, produkując światło oraz ciepło.
Magnez spala się białym, jaskrawym płomieniem, a na łyżce do spaleń pozostaje białawe ciało stałe.
Węgiel spala się, wytwarzając pomarańczowy płomień oraz czarny dym.
Spalaniu siarki towarzyszy niebieski płomień.
Sód pali się jasnym, pomarańczowo‑żółtym płomieniem.
Wyniki:
Zbadane pierwiastki chemiczne podczas spalania w tlenie reagują z nim, tworząc tlenki i generując światło i ciepło.
Spalanie magnezu prowadzi do powstania tlenku magnezu zgodnie z poniższym równaniem:
Spalanie węgla prowadzi do powstania tlenku węgla() zgodnie z poniższym równaniem:
W wyniku spalania siarki powstaje tlenek siarki(), co opisuje poniższe równanie:
Spalanie sodu prowadzi do powstania ditlenku disodu (nadtlenku sodu) oraz tlenku sodu zgodnie z poniższymi równaniami:
Wnioski:
Hipoteza została potwierdzona.
lub
Hipoteza nie została potwierdzona.
Podczas wprowadzania rozżarzonego łuczywa do probówki wypełnionej tlenem wyraźny rozbłysk można było zaobserwować w jej wnętrzu. Odpowiedz, o czym świadczy to zjawisko.
Obieg tlenu w przyrodzie
Obieg tlenu w przyrodzie jest ściśle związany z obiegiem tlenku węgla(), czyli dwutlenku węgla. Równowagę tę znacząco zaburza działalność człowieka. Źródłem tlenu w przyrodzie są organizmy przeprowadzające proces fotosyntezy tlenowej, podczas której pochłaniana jest energia słoneczna wykorzystywana w reakcji tlenku węgla() z wodą. Pozwala to na wytworzenie produktów: glukozy, stanowiącej pokarm dla roślin prowadzących wspomniany proces i zwierząt (dzięki obecności w jej strukturze wysokoenergetycznych wiązań) oraz tlenu, wykorzystywanego w procesie oddychania komórkowego. Dlatego tak ważne jest, aby dbać o środowisko naturalne poprzez stosowanie odnawialnych źródeł energii, poszanowanie lasów, sadzenie nowych drzew i roślinności.
Przeanalizuj poniższą symulację i sprawdź, w jaki sposób człowiek wpływa na obieg tlenu w przyrodzie.
W symulacji przedstawiony jest krajobraz wiejski. Wzdłuż drogi poruszają się dwa samochody. Po obu jej stronach znajdują się domy. Wokół nich rosną drzewa. Przedstawiono również łąki i pastwiska, na których wypasane są krowy. Wzdłuż horyzontu znajduje się las. Nad nim rozpościera się błękitne niebo. Strzałkami zaznaczono wybrane elementy składające się na cykl. powstaje podczas oddychania organizmów żywych (reprezentowanych w symulacji przez krowy. Ponadto tlenek węgla generowany jest podczas spalania paliw kopalnych wykorzystywanych do ogrzewanie domów, jak i w transporcie. Natomiast tlen powstaje w wyniku fotosyntezy prowadzonej przez roślinność. W symulacji zawarta jest informacja dotycząca obiegu tlenu i tlenku węgla w przyrodzie.
Kształtowanie się naszej planety obejmowało liczne, burzliwe wydarzenia, którym towarzyszyły zróżnicowane warunki otoczenia (nie zawsze sprzyjające). Ich wypadkowa pozwoliła na powstanie pierwszych żywych organizmów. Od tego momentu na drodze ewolucji pojawiły się liczne gatunki beztlenowców – w tym cyjanobakterii. Dzięki umiejętności prowadzenia procesu fotosyntezy doprowadziły one do katastrofy tlenowej, w wyniku której gromadzący się w atmosferze ziemskiej tlen spowodował wymarcie wielu organizmów, które nie były w stanie przystosować się do zmieniających się warunków otoczenia. Te, które przetrwały, wykształciły umiejętność wykorzystywania tlenu w procesie oddychania komórkowego. Rośliny oraz cyjanobakterie używają energii słonecznej w procesie fotosyntezy tlenowej. W jej wyniku tlenek węgla oraz woda zostają przekształcone w tlen oraz glukozę. Tlen stanowi substrat w procesach oddychania komórkowego wielu organizmów. Ich głównym produktem jest tlenek węgla, który ponownie może zostać wykorzystany do fotosyntezy. Przedstawione zależności doprowadziły do kształtowania się cyklu tlenowego. Zmiany w składzie oraz strukturze atmosfery ziemskiej pozwoliły na dalszy rozwój organizmów roślinnych i zwierzęcych. Prowadzone przez nie procesy oddychania komórkowego i fotosyntezy przyczyniły się to do ustabilizowania się obiegu tlenu w przyrodzie, czyli cyklu, który obejmuje cyrkulację tlenu na Ziemi – zarówno w formie cząsteczkowej, jak i w postaci związków chemicznych. Do innych naturalnych zjawisk towarzyszących cyklowi tlenowemu należą utlenianie związków nieorganicznych (np. powstawanie tlenków, wybuchy wulkanów) oraz organicznych (np. degradacja materii). Poza tym należy zwrócić uwagę na antropogeniczne (powstałe na skutek działalności człowieka) procesy, którym towarzyszy uwalnianie do atmosfery znacznych ilości tlenku węgla na skutek zużywania tlenu oraz surowców. Wśród procesów tych można wyróżnić spalanie obecne w transporcie, przemyśle (w tym energetycznym) czy też rolnictwie. Wszystkie działania człowieka, które przyczyniają się do zwiększenia udziału tlenku węgla w atmosferze, wpływają również na obieg tlenu w przyrodzie. Zatem powstawanie omawianych gazów jest ze sobą nierozerwalnie powiązane, a ich udział w składzie powietrza nie jest obojętny dla organizmów żywych, w tym ludzi. Z tego względu tak ważne jest, by rozumieć podstawy równowagi dynamicznej (czyli takiej, w wyniku której stężenia tlenku węgla i tlenu w atmosferze pozostają w przybliżeniu niezmienne, tj. reakcje ich tworzenia przebiegają z taką samą szybkością) procesów zachodzących w atmosferze ziemskiej, a także wpływu na nie działań człowieka. Istotna jest również znajomość postaw ora działań, które mogą w pewnym stopniu ograniczyć udział w atmosferze antropogenicznego tlenku węgla.
Po wybraniu danego elementu graficznego w symulacji wyświetlają się informacje.
Hodowla zwierząt
Czy wiesz, że szacowana liczba zwierząt hodowlanych na świecie w roku była około cztery razy większa niż liczba ludzi i wynosiła (nie licząc ryb i innych zwierząt wodnych) miliarda? Szacuje się, że około całej biomasy ssaków na Ziemi to zwierzęta hodowane dla ludzkich potrzeb, a ptaki hodowlane stanowią wszystkich ptaków. Hodowla zwierząt powoduje emisję ogromnych ilości tlenku węgla(), stanowiących nawet około – wszystkich gazów cieplarnianych, za które odpowiada człowiek. Już częściowe jej wyeliminowanie przyczyni się do ochrony środowiska.
Roślinność
Przeciętna roślina doniczkowa wytwarza w ciągu roku około tlenu, podczas gdy wysokie drzewo w tym samym czasie produkuje około tlenu. Rośliny produkują tlen – wzbogacając florę, zwiększasz zatem jego ilość w przyrodzie.
Samochody elektryczne
W samochodach elektrycznych zamiast silnika spalinowego zastosowany jest silnik elektryczny. Do napędu wykorzystywana jest zatem energia elektryczna, czyli prąd. W silniku elektrycznym nie dochodzi do procesu spalania mieszaniny paliwa i powietrza, co z kolei wiążę się z brakiem produkcji zanieczyszczeń. Im więcej samochodów elektrycznych, tym mniejsza emisja tlenku węgla() i innych zanieczyszczeń. Infrastruktura drogowa coraz lepiej przystosowuje się do ładowania silników zasilanych energią elektryczną. Szybkie stacje ładowania umożliwiają uzupełnienie baterii w czasie około minut, co zdecydowanie skraca postój w drodze. Współczesne samochody elektryczne charakteryzują się zasięgiem nawet powyżej .
Samochody napędzane silnikiem spalinowym
Ilość emisji zanieczyszczeń produkowanych przez samochody zależy od ich rodzaju oraz roku produkcji. Jednak samochody osobowe są głównym źródłem zanieczyszczeń i odpowiadają za wszystkich emisji tlenku węgla() z transportu drogowego w Europie, a około w Stanach Zjednoczonych. Samochody napędzane silnikiem spalinowym produkują bardzo duże ilości spalin, w tym tlenku węgla().
Odnawialne źródła energii
Panele fotowoltaiczne przekształcają energię słoneczną na energię elektryczną, dzięki czemu możliwe jest ogrzewanie domu bez konieczności spalania paliw kopalnych i emisji tlenku węgla(). Dziennie jeden panel fotowoltaiczny może wyprodukować około energii*. Przykładowo piekarnik elektryczny zużywa od do w ciągu roku, a zmywarka od do w ciągu roku. Zakładając paneli fotowoltaicznych uzyskujemy w ciągu jednego, słonecznego dnia około energii. Dzięki instalacji fotowoltaicznej zyskujemy ogromne oszczędności i dbamy o środowisko naturalne, wykorzystując jedno z największych źródeł energii odnawialnej na świecie, czyli Słońce.
* kilowatogodzina odpowiada ilości energii, jaką zużywa przez godzinę urządzenie o mocy .
Nieodnawialne źródła energii
Jedną z najistotniejszych przyczyn smogu w Polsce jest ogrzewanie gospodarstw domowych za pomocą paliw kopalnych, często bardzo niskiej jakości. Pomimo tego, że w przeciągu ostatnich kilku lat wyeliminowane zostały piece starego typu (tzw. „kopciuchy”), to jednak piece węglowe są głównym źródłem ogrzewania domów jednorodzinnych niemal połowy Polaków. Ogrzewanie domów za pomocą pieców węglowych prowadzi do emisji dużych ilości zanieczyszczeń, w tym tlenku węgla(). Zwiększając ich ilość przyczyniasz się do powstawania smogu (mieszaniny mgły z dymem i spalinami). Zmniejszając ich ilość przyczyniasz się do redukcji smogu (mieszaniny mgły z dymem i spalinami).
Głównym źródłem energii dla wszystkich organizmów żywych jest: Możliwe odpowiedzi: 1. Ziemia., 2. Księżyc., 3. Słońce., 4. rośliny.
Ćwiczenia
Gazy, które słabo rozpuszczają się w wodzie, zbierają się w probówkach wypełnionych wodą w całości i odwróconych do góry dnem, jak na poniższym rysunku:

Jednak gazy można zbierać również w probówkach odwróconych do góry dnem (a) lub do dołu dnem (b).

Gazy, które słabo rozpuszczają się w wodzie, zbierają się w probówkach wypełnionych wodą w całości i odwróconych do góry dnem. Jednak gazy można zbierać również w probówkach odwróconych do góry dnem (a) lub do dołu dnem (b).
Zaznacz, jaki wniosek dotyczący zależności rozpuszczalności tlenu w wodzie od temperatury można wyciągnąć. Możliwe odpowiedzi: 1. Wraz ze wzrostem temperatury rozpuszczalność tlenu w wodzie wzrasta., 2. Zmiana temperatury nie ma wpływu na rozpuszczalność tlenu w wodzie., 3. Wraz ze wzrostem temperatury rozpuszczalność tlenu w wodzie maleje.
Jedną z reakcji otrzymywania tlenu jest termiczny rozkład manganianu() potasumanganianu() potasu o wzorze sumarycznym . Reakcję tę można przedstawić na schematycznym rysunku.
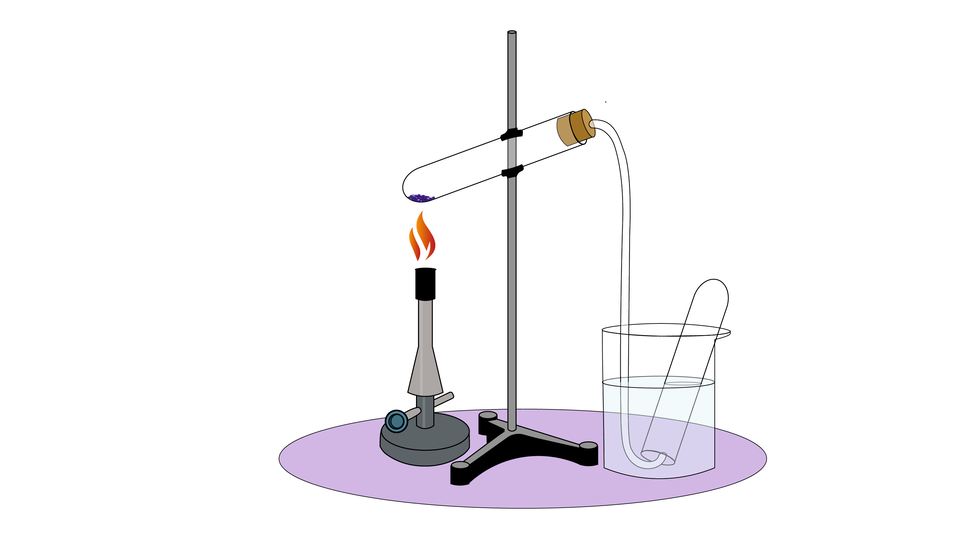
Jedną z reakcji otrzymywania tlenu jest termiczny rozkład manganianu() potasumanganianu() potasu o wzorze sumarycznym .
W jaki sposób doświadczalnie potwierdzisz, że w tej reakcji powstaje tlen? Wpisz odpowiedź w poniższym polu.
luka do uzupełnienia A l, plus luka do uzupełnienia O indeks dolny, dwa, koniec indeksu dolnego, strzałka w prawo luka do uzupełnienia A l indeks dolny, dwa, koniec indeksu dolnego, O indeks dolny, trzy, koniec indeksu dolnego
luka do uzupełnienia H indeks dolny, dwa, koniec indeksu dolnego, plus, O indeks dolny, dwa, koniec indeksu dolnego, strzałka w prawo luka do uzupełnienia H indeks dolny, dwa, koniec indeksu dolnego, O
luka do uzupełnienia N a, plus, O indeks dolny, dwa, koniec indeksu dolnego, strzałka w prawo luka do uzupełnienia N a indeks dolny, dwa, koniec indeksu dolnego, O
Bibliografia
Kulawik J., Kulawik T., Litwin M., Podręcznik do chemii dla klasy siódmej szkoły podstawowej, Warszawa 2020.
Łasiński D., Sporny Ł., Strutyńska D., Wróblewski P., Podręcznik dla klasy siódmej szkoły podstawowej, Mac Edukacja 2020.
Wojtyla Ł., Adamiec M., Co rośliny robią nocą? „Edukacja Biologiczna i Środowiskowa” 2013, nr 3, s. 10‑16.
Przemysłowe hodowle zwierząt - środowiskowa i etyczna katastrofa, „Nauka dla Przyrody”, 05. 04.2021, online: https://naukadlaprzyrody.pl/2021/04/05/przemyslowe-hodowle-zwierzat-srodowiskowa-i-etyczna-katastrofa/, dostęp: 27.04.2022.
Praktyczne spojrzenie na panele fotowoltaiczne, „Teraz Środowisko”, 02.10.2018, online: https://www.teraz-srodowisko.pl/aktualnosci/Praktyczne-spojrzenie-na-panele-fotowoltaiczne-5480.html, dostęp: 29.04.2022.