Symulacja interaktywna
Jakie czynniki wpływają na szybkość dyfuzji?
Poniżej zamieszczono symulację interaktywną, przy pomocy której możesz sprawdzić, jak szybkość dyfuzji zależy od temperatury i od wielkości cząsteczek.
Klikając odpowiednie przyciski na symulacji wybierz temperaturę układu, a następnie usuń przegrodę między pojemnikami wypełnionymi dwoma różnymi rodzajami gazu (helem i neonem). Po usunięciu przegrody atomy obydwu gazów przemieszczają się i zaczynają wypełniać przestrzeń, która była dla nich dotychczas niedostępna. Usunięcie przegrody powoduje automatyczne uruchomienie stopera, który mierzy czas do chwili, gdy po raz pierwszy jeden z atomów neonu uderzy w prawą ściankę połączonego naczynia.
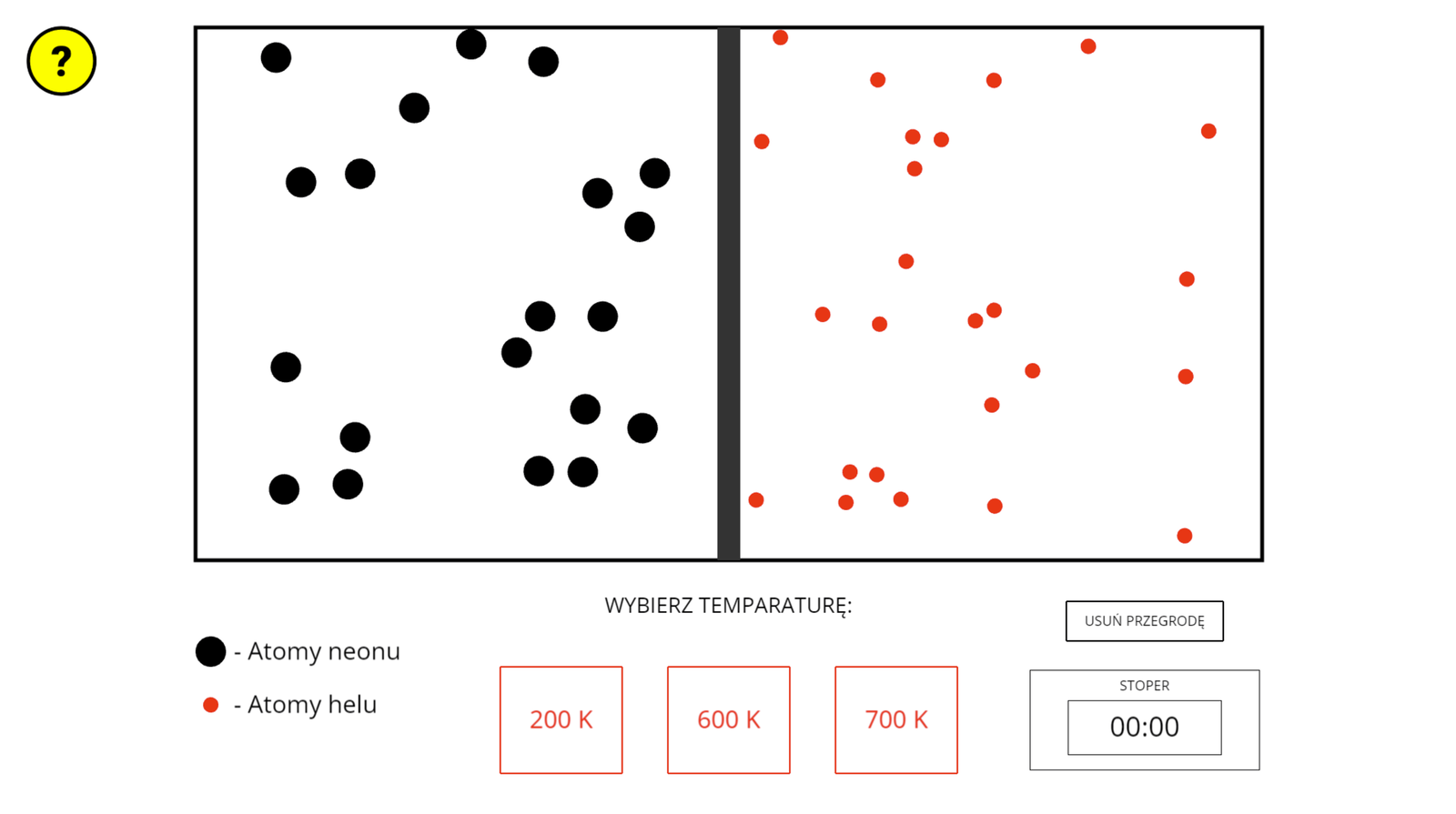
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DqvgWuT7l
Symulacja przedstawia zjawisko dyfuzji atomów neonu i helu. W pojemniki widocznym w postaci poziomego prostokąta o czarnych krawędziach i białym środku znajduje się pionowa przegroda, która dzieli pojemnik na dwie równe części i lewą. W lewej komorze pojemnika znajdują się atomy neonu widoczne w postaci czarnych kulek. W prawej sekcji pojemnika widoczne są atomy helu w postaci mniejszych czerwonych kulek. Pod pojemnikiem widoczne są trzy prostokątne przyciski jeden obok drugiego, których użytkownik może użyć do wyboru temperatury obu gazów w pojemniku. Użytkownik może dokonać wyboru pomiędzy temperaturami dwustu kelvinów, sześciuset kelvinów i siedmiuset kelwinów. Im wyższa temperatura zostanie wybrana tym szybciej poruszają się cząsteczki obu gazów w prawej i lewej części pojemnika. Cząsteczki obu gazów poruszają się w sposób chaotyczny. Obok przycisków temperatury, po prawej stronie widoczny jest przycisk, który służy do usunięcia przegrody w pojemniku. Po usunięciu przegrody cząsteczki neonu i helu zaczynają się mieszać, przemieszczając się po całej objętości naczynia. Odbijają one od ścianek naczynia i od innych cząsteczek. Pod przyciskiem usunięcia przegrody widoczny jest stoper, który odmierza czas potrzebny do całkowitego wymieszania się cząsteczek obu gazów. Czy potrzebne do wymieszania się gazów w zależności od to: dla dwustu kelvinów około czterech sekund, dla sześciuset kelvinów około trzech sekund i dla siedmiuset kelvinów około dwóch sekund. Czasy te przy kilkukrotnym usunięciu przegrody, dla tej samej temperatury różnią się od siebie, ponieważ szybkość dyfuzji zależy od chaotycznego ruchu cząsteczek. Jednak ich średnie wartości są bardzo zbliżone do tych, które podano.
Dla wybranej temperatury, np. T=200 K, wykonaj 10 pomiarów czasu dyfuzji. Wyznacz średnią wykonanych pomiarów tIndeks dolny śr Indeks dolny koniecśr i odchylenie standardowe średniej sIndeks dolny śrśr. Pomiary powtórz dla pozostałych wartości temperatury.
Porównaj uzyskane wyniki. Co na postawie tych wyników możesz powiedzieć o prędkości atomów badanych gazów?
Ustaw w symulacji najniższą temperaturę. Po usunięciu bariery obserwuj ruch atomów helu (tj. czerwonych). Zliczaj, ile razy atomy te uderzają w lewą ścinkę połączonego naczynia zanim symulacja zakończy działanie. Powtórz obserwację kilka razy. Czy na podstawie poczynionych obserwacji możesz wysnuć wniosek o tym, w jaki sposób tempo dyfuzji zależy od masy dyfundujących cząsteczek?
Ustaw w symulacji najniższą temperaturę. Wykonaj 50 pomiarów czasu dyfuzji. Zebrane pomiary przedstaw w postaci histogramu. Zaznacz na nim wartość średnią i odchylenie standardowe od średniej. Czy kształt histogramu coś Ci przypomina?