Charakterystyka i otrzymywanie tlenu
Tlen to pierwiastek, bez którego nie moglibyśmy oddychać – wydaje się więc dobrze znany i oczywisty. Ale to tylko pozory. Jako przedstawiciel tlenowców, tlen odgrywa kluczową rolę nie tylko w procesach życiowych, ale też w niezliczonych reakcjach chemicznych zachodzących na Ziemi i poza nią. To pierwiastek, który łączy świat biologii, chemii i fizyki, będąc jednocześnie cichy uczestnikiem zjawisk codziennych i tych najbardziej niezwykłych – jak spalanie, utlenianie czy oddychanie komórkowe. Zgłębiając właściwości tlenu, zyskujemy nie tylko wiedzę o jednym z podstawowych składników atmosfery, ale też klucz do zrozumienia, jak funkcjonuje życie i materia.
Charakterystyka tlenu
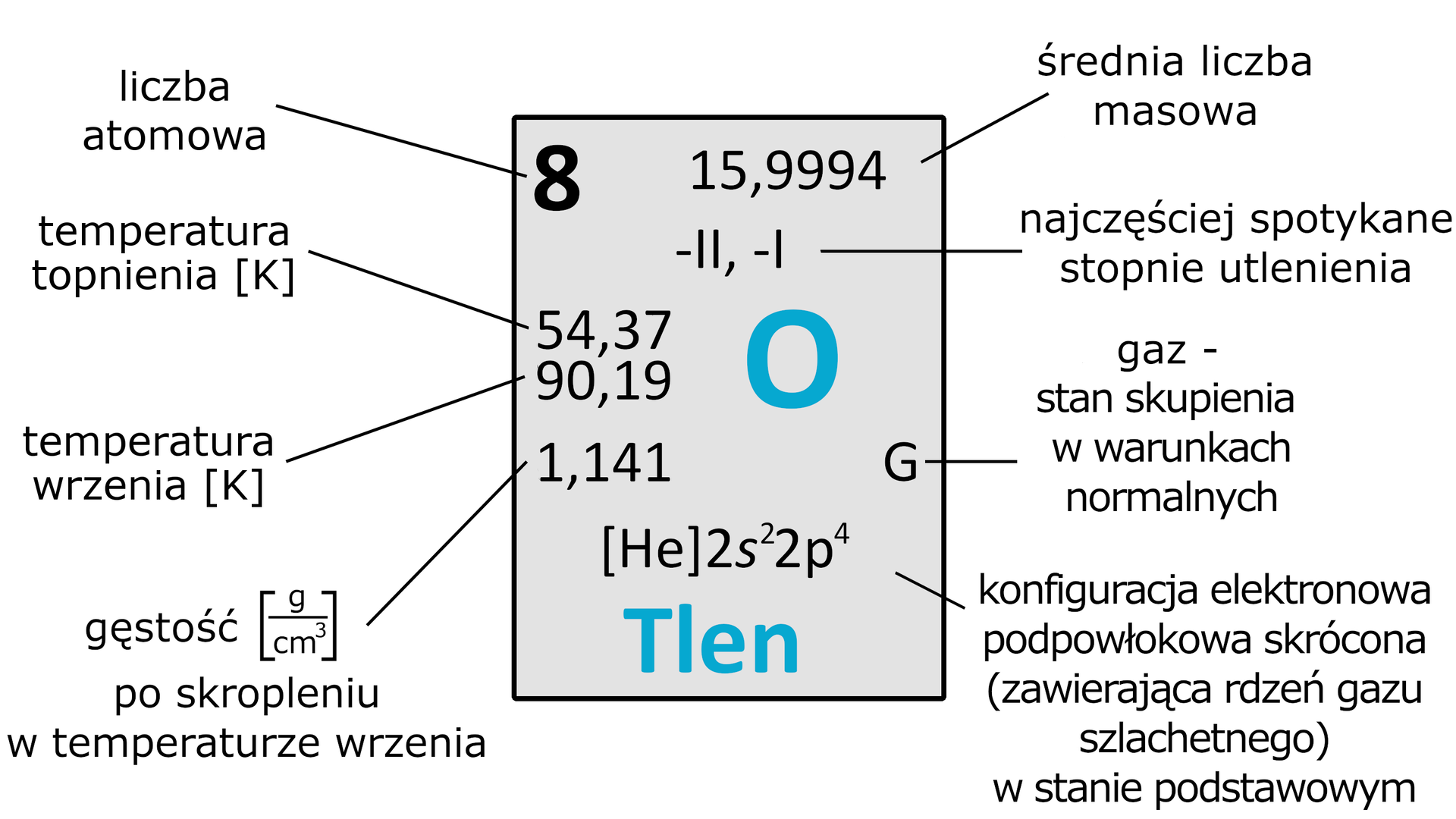
Tlen jest niemetalem, który znajduje się w grupie układu okresowego jako pierwszy przedstawiciel grupy tlenowców. W warunkach standardowych (wg. IUPAC , ) jest bezwonnym i bezbarwnym gazem. Stanowi zwykle ok. objętości powietrza i jest niezbędny do prawidłowego funkcjonowania większości organizmów żywych. Ponadto ma bardzo niską temperaturę topnienia i wrzenia – wynoszą one odpowiednio: i ( i ). To właśnie ze względu na niską temperaturę wrzenia, przez wiele lat tak problematyczne było skroplenie tlenu.
Przyjęto, że tlen został odkryty w roku przez Carla Scheelego, metodą prażenia tlenku rtęci(). Jednak odkrycie to nie zostało opublikowane do roku, dlatego przez dwa lata za odkrywcę uważano Josepha Priestleya, który marca roku ogłosił swoje odkrycie w towarzystwie naukowym Royal Society.
Alotropia tlenu
Tlen występuje w trzech odmianach alotropowych i jest to jedyny przykład alotropii w stanie gazowym.
Ditlen – cząsteczka dwuatomowa. Ditlen jest bezbarwnym i bezwonnym gazem, którego gęstość jest większa od gęstości powietrza.
Ozon – trójatomowa cząsteczka. W stanie gazowym jest bezbarwny lub ma niebieskawą barwę oraz zapach przypominający woń powietrza po burzy. Jest on bardzo silnym utleniaczem i bardzo reaktywnym alotropem tlenu.
Tetratlen – czteroatomowa cząsteczka. Tetratlen jest bardzo nietrwałą cząsteczką – rozpada się, tworząc dwie cząsteczki dwuatomowego tlenu (). Dowód na istnienie tetratlenu zdobyto dopiero poprzez zastosowanie wysokiego ciśnienia rzędu na . Wówczas ditlen ma tendencję do występowania w postaci czteroatomowych cząsteczek. Tetratlen ma jasnoczerwoną barwę.
Ciekły tlen

Ciekły tlen jest cieczą o gęstości (ok. ), o charakterystycznym bladoniebieskim zabarwieniu. Znajduje szereg zastosowań jako utleniacz, np. paliwa rakietowego.
Diagram fazowy tlenu
Poniżej przedstawiono diagram fazowy tlenu – wykres przedstawiający warunki (ciśnienie i temperaturę), w których badana substancja występuje w danym stanie skupienia. Obrazuje także, że temperatura wrzenia cieczy zależy od ciśnienia.
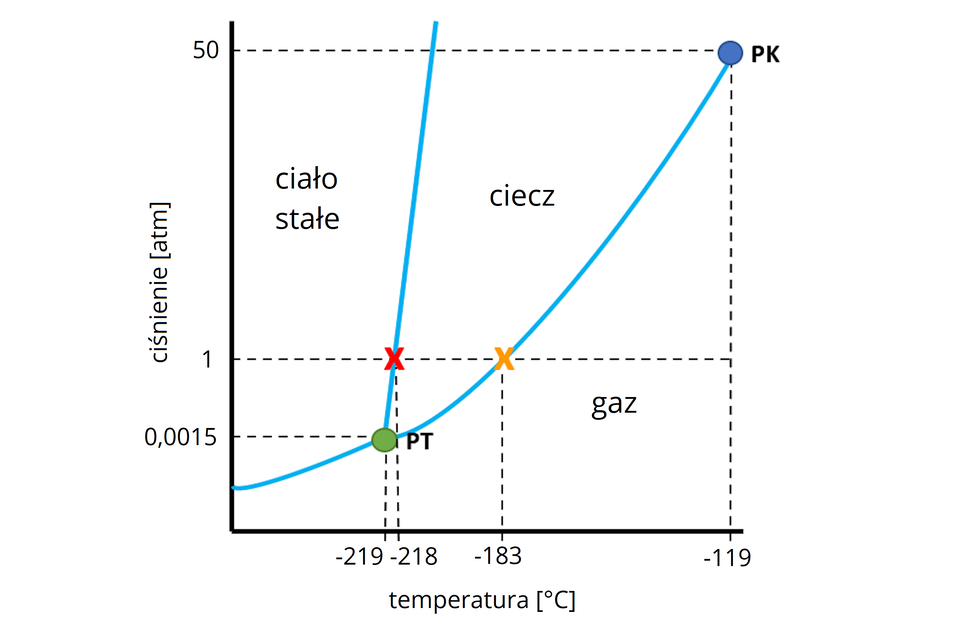
PK to tzw. punkt krytyczny – punkt końcowy krzywej współistnienia cieczy i pary. PT to punkt potrójny, opisuje warunki, w których substancja współistnieje w trzech stanach skupienia (stałym, ciekłym i gazowym).
Otrzymywanie tlenu
Z powietrza
kwietnia roku dwójka polskich uczonych – Karol Olszewski i Zygmunt Wróblewski – jako pierwsi na świecie skraplają tlen. Wykorzystali do tego metodę kaskadową. Polega ona na wykorzystaniu wrzących, pod zmniejszonym ciśnieniem, gazów, które obniżają temperaturę układu, pozwalając przy tym na skroplenie kolejnych substancji w niższych temperaturach.
Olszewski i Wróblewski skonstruowali odpowiednią aparaturę, która pozwoliła na skroplenie tlenu.
a – butla z ciekłym etylenem (etenem), b – zbiornik z mieszaniną Thiloriera, c – termometr wodorowy, d – szklany zbiornik z ciekłym etylenem, e – grubościenna ampuła szklana, w której skrapla się gaz, f – stalowa butla z gazowym tlenem ()
Gazowy tlen, wypuszczany ze stalowej butli (f) pod wysokim ciśnieniem trafia do grubościennej rurki (e). Tam kosztem swojej energii wewnętrznej, rozpręża się, obniżając swoją temperaturę. Kolejnym etapem jest tłoczenie tlenu w dół pod dużym ciśnieniem, w efekcie czego rozpręża się on ponownie do ciśnienia (). Oziębiony gaz zaczyna się skraplać w rurce.
Taka przemiana nazywana jest rozprężaniem adiabatycznym. Korzystając z niej, Olszewskiemu i Wróblewskiemu jako pierwszym na świecie udało się skroplić tlen. Kilka dni później skroplili kolejny składnik powietrza – azot.
W dzisiejszych czasach ciekły tlen pozyskiwany jest z powietrza, którego jest w nim około . Proces ten odbywa się w specjalnych kolumnach.

Opis metody przemysłowego otrzymywania ciekłego tlenu i ciekłego azotu
W pierwszym etapie powietrze jest filtrowane z kurzu oraz innych stałych zanieczyszczeń. Ponadto z powietrza usuwane są inne niepożądane składniki występujące w nim w niewielkich ilościach, takie jak węglowodory czy tlenki azotu.
Następnie powietrze jest sprężane. W tym etapie woda, obecna w powietrzu jako para wodna, jest skraplana w odpowiednich chłodnicach.
Dalej sprężone powietrze jest przepuszczane przez sita molekularne, które wychwytują pozostałości pary wodnej oraz tlenku węgla().
Oczyszczone powietrze zaczyna się skraplać na dno kolumny. Powstała mieszanina charakteryzuje się dużą zawartością ciekłego tlenu (około ). Innymi składnikami mieszaniny jest argon oraz azot. U szczytu kolumny znajduje się mieszanina gazów – głównie azotu, ale także argonu. Mieszanina ta jest następnie destylowana do czystego azotu.
Otrzymane w ten sposób gazy są odpowiednio przechowywane i, w zależności od przeznaczenia, pakowane do butli lub pompowane do cysterny izolowanej termicznie.
Czy znasz sposoby, dzięki którym możliwe jest otrzymanie tlenu z powietrza? W poniższym wirtualnym laboratorium możesz sprawdzić, jak wykonać taki eksperyment. Do metalowego ostrosłupa dodaj ciekły azot, a następnie, kiedy w szklanym naczyniu, znajdującym się pod ostrosłupem, zbierze się ciecz, włóż do niego zapalone łuczywko.
W formularzu zanotuj własną hipotezę, potrzebny sprzęt, odczynniki oraz swoje obserwacje i wyniki, a następnie zapisz wnioski.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DDN32UL5N
Czy znasz sposoby, dzięki którym możliwe jest otrzymanie tlenu z powietrza? Zapoznaj się z opisem poniższego doświadczenia, a następnie wykonaj ćwiczenia sprawdzające.
Analiza eksperymentu:
Jak otrzymać tlen z powietrza?
Problem badawczy:
Czy za pomocą ciekłego azotu można otrzymać tlen z powietrza?
Hipoteza:
Używając ciekłego azotu, można otrzymać tlen z powietrza.
Sprzęt laboratoryjny:
metalowy ostrosłup – naczynie w kształcie ostrosłupa, którego dno stanowi wierzchołek ostrosłupa;
szklane naczynie – na przykład zlewka, to jest naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych;
łuczywo – kawałek smolnego przesyconego żywicą drewna, z reguły z drzewa iglastego.
Odczynniki chemiczne:
ciekły azot.
Przebieg eksperymentu:
Wlanie ciekłego azotu do metalowego ostrosłupa.
Ustawienie pod ostrosłupem szklanego naczynia.
Włożenie do naczynia zapalonego łuczywa po zebraniu cieczy.
Obserwacje:
Po otwarciu naczynia z ciekłym azotem pojawia się dym (para). Po nalaniu do metalowego ostrosłupa, pokrywa się on szronem. Po chwili z ostrosłupa zaczyna się skraplać ciecz. Zapalone łuczywko, włożone do szklanego naczynia, powoduje wyraźny rozbłysk.
Wyniki:
Zebrana ciecz w szklanym naczyniu to skroplony tlen z powietrza.
Wnioski:
Używając ciekłego azotu, można otrzymać tlen z powietrza. Hipoteza została potwierdzona.
Wyjaśnij, dlaczego w powyższym eksperymencie możemy wykorzystać ciekły azot?
Korzystając z tabeli, zastanów się, czy do skroplenia tlenu można wykorzystać ciekły metan. Odpowiedź uzasadnij.
– normalna temperatura wrzenia przy ciśnieniu
ciecz | |
Indeks dolny Źródło: www.hvacr.pl, dostęp: 22.10.2021. Indeks dolny koniecŹródło: www.hvacr.pl, dostęp: 22.10.2021.
Z wody (elektrolityczny rozkład)
Tlen można otrzymać również w wyniku elektrolizy wody.
Równanie reakcji katodowej:
Równanie reakcji anodowej:
Po zsumowaniu:
W związku z tym, że jony i nie mogą być razem po jednej stronie równania, zobojętniają się one tworząc cząsteczki wody.
Równanie reakcji:
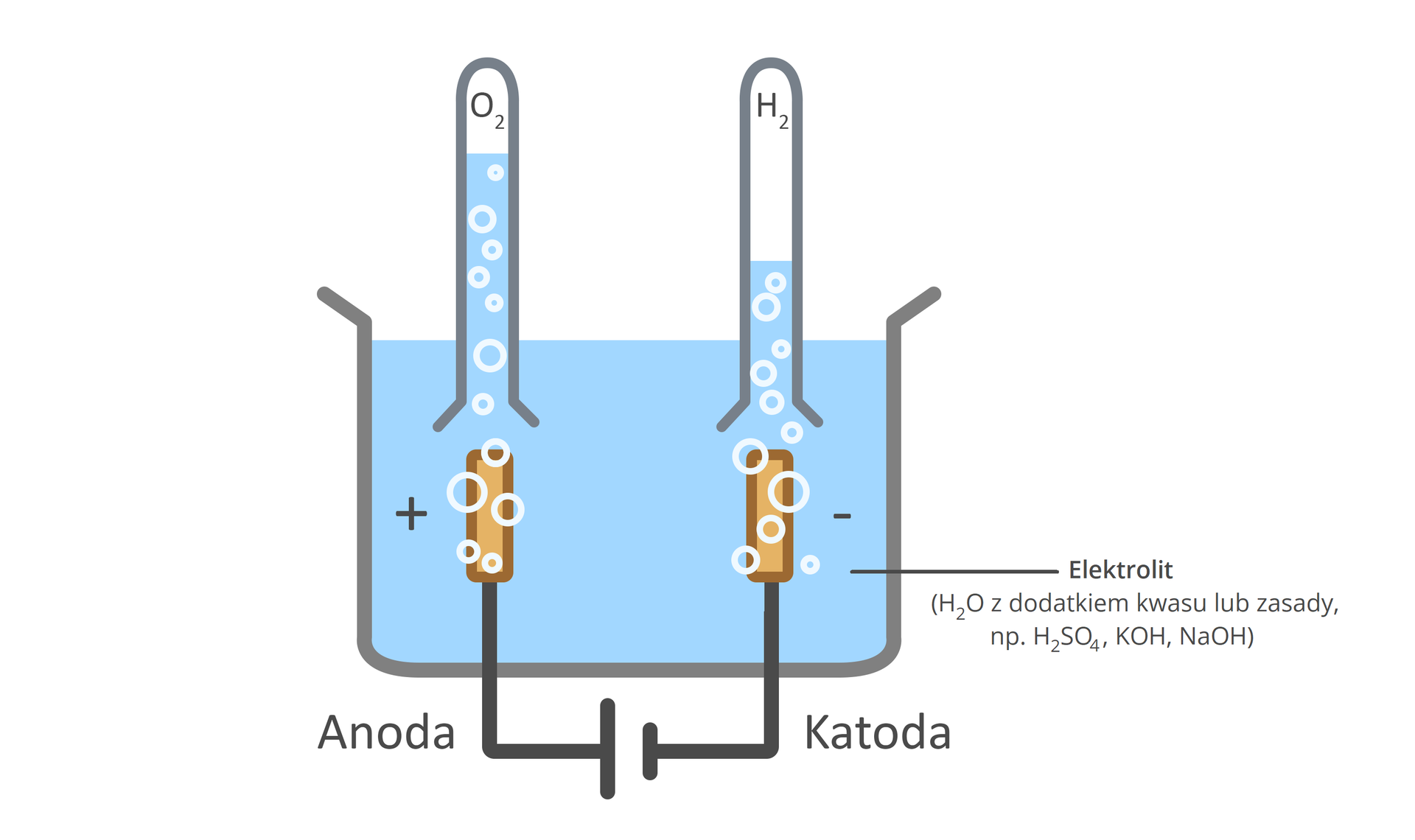
Elektrolityczny rozkład wody
Elektroliza wody to proces rozkładu cząsteczki wody pod wpływem prądu elektrycznego, prowadzący do otrzymania tlenu i wodoru. Proces ten prowadzony jest przez zanurzenie elektrod w roztworze elektrolitu, czyli substancji przewodzącej prąd elektryczny. Elektrolitem mogą być stopione lub rozpuszczone związki, które ulegają dysocjacji elektrolitycznej na jony. Ponieważ nie przewodzi prądu, podczas elektrolizy wykorzystuje się wodne roztwory kwasów lub zasad, np. , lub .
Z nadtlenku wodoru (katalityczny rozkład)
Poniższe doświadczenie należy wykonywać pod sprawnym wyciągiem. Wykonując doświadczenie należy zachować szczególne środki ostrożności i zapoznać się z kartami charakterystyki używanych substancji. Ponadto wykonujący ćwiczenie powinien być zaopatrzony w fartuch, rękawiczki, okulary ochronne lub przyłbicę. Po zakończeniu pracy suche pozostałości należy odpowiednio zutylizować lub przechowywać w przeznaczonych do tego pojemnikach.
Schemat doświadczenia:

Inne metody1
Wykorzystując wirtualne laboratorium, zastanów się, w jaki sposób można otrzymać tlen w warunkach laboratoryjnych. Przeanalizuj przedstawione przykłady rozkładu tlenku rtęci() oraz manganianu() potasu. Rozwiąż problem badawczy, zweryfikuj hipotezę, zapisz obserwacje, wyniki i wnioski.
Spróbuj wykonać doświadczenie samodzielnie. Jeśli jednak będziesz mieć problemy, możesz skorzystać z instrukcji, która znajduje się pod znakiem zapytania w prawym górnym rogu.
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DDN32UL5N
Zastanów się, w jaki sposób można otrzymać tlen w warunkach laboratoryjnych? Przeanalizuj przedstawione przykłady rozkładu tlenku rtęci() oraz manganianu() potasu. Zapoznaj się z poniższym problemem badawczym, hipotezą, obserwacjami, wynikami i wnioskami. Następnie wykonaj ćwiczenia sprawdzające.
Analiza doświadczenia:
Otrzymywanie tlenu w warunkach laboratoryjnych.
Problem badawczy:
W jaki sposób można otrzymać tlen w warunkach laboratoryjnych?
Hipoteza:
Tlen można otrzymać w wyniku rozkładu tlenku rtęci() oraz w wyniku rozkładu manganianu() potasu.
Sprzęt i szkło laboratoryjne:
statyw - pionowy pręt ze stabilną podstawą umożliwiający mocowanie na wybranej wysokości, na przykład szkła laboratoryjnego umieszczonego w łapie;
łapa - rodzaj narzędzia wykorzystywanego w laboratorium do trzymania, na przykład kolb;
zlewka - naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych;
łyżeczka - długi trzonek wykonany ze szkła, porcelany lub metalu zakończony z jednej strony łyżeczką;
probówki - podłużne U‑kształtne naczynia szklane służące do przeprowadzania prostych reakcji chemicznych;
korek gumowy oraz gumowy wężyk;
łuczywo - kawałek smolnego przesyconego żywicą drewna z reguły wykonanego z drzewa iglatego;
palnik - urządzenie techniczne umożliwiające podtrzymywanie płomienia spalanego gazu w kontrolowany sposób.
Odczynniki chemiczne:
tlenek rtęci(); manganian() potasu.
Przebieg doświadczenia:
1. Umieszczenie 0,5 grama tlenku rtęci() w probówce zatkanej korkiem, przez który przechodzi wężyk skierowany do wnętrza drugiej probówki zanurzonej do góry dnem w zlewce z wodą.
2. Ogrzewanie zawartości probówki umieszczonej w łapie statywu w płomieniu palnika.
3. Po wypełnieniu probówki przez wydzielający się gaz wyciągnięcie jej ze zlewki oraz umieszczenie w jej wnętrzu żarzącego się łuczywa.
4. Przeprowadzenie analogicznej procedury w celu otrzymania tlenu z manganianu() potasu.
Obserwacje:
Podczas ogrzewania tlenku rtęci(), zaobserwowano wydzielanie się bezbarwnego gazu, który wypierał wodę z probówki. Po wprowadzeniu żarzącego się łuczywa do probówki wypełnionej otrzymanym gazem - łuczywo zapaliło się.
Podobnych obserwacji dokonano w czasie ogrzewania manganianu() potasu.
Wyniki:
W wyniku termicznego rozkładu tlenku rtęci() lub manganianu() potasu otrzymuje się bezbarwny gaz podtrzymujący spalanie, czyli tlen.
Wnioski:
Hipoteza została potwierdzona — tlen można otrzymać w wyniku rozkładu tlenku rtęci() lub manganianu() potasu.
Równania reakcji chemicznych:
Rozkład termiczny tlenku rtęci(): Rozkład termiczny manganianu() potasu:
Przeprowadź w wirtualnym laboratorium chemicznym doświadczenie na temat otrzymywania tlenu i badania jego właściwości fizycznych. Zapisz swoje obserwacje i wyniki oraz sformułuj wnioski. Spróbuj wykonać doświadczenie samodzielnie. Jeśli jednak będziesz mieć problemy, możesz skorzystać z instrukcji, która znajduje się pod znakiem zapytania w lewym górnym rogu ekranu wirtualnego laboratorium.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DDN32UL5N
W laboratorium chemicznym przeprowadzono doświadczenie na temat otrzymywania tlenu i badania jego właściwości.
Analiza doświadczenia: Sprawdzanie właściwości tlenu cząsteczkowego.
Problem badawczy: Jakie właściwości posiada tlen cząsteczkowy?
Hipoteza: Tlen cząsteczkowy w warunkach standardowych jest bezbarwnym gazem, który podtrzymuje proces spalania.
Odczynniki: manganian() potasu, woda destylowana
Sprzęt laboratoryjny:
palnik – rodzaj sprzętu z regulacją płomienia, umożliwiający podgrzewanie substancji chemicznych;
krystalizator – płaskie naczynie laboratoryjne, które służy do procesu krystalizacji;
probówki – podłużne naczynia szklane do przeprowadzania prostych reakcji chemicznych;
łyżka laboratoryjna – długi trzonek wykonany ze szkła, porcelany lub metalu zakończony z jednej strony łyżeczką; służy do nabierania sypkich substancji chemicznych;
zlewka – naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych;
statyw na probówki – prostokątny sprzęt laboratoryjny z rzędami otworów, w których umieszczane są probówki;
korek z rurką odprowadzającą – niewielki element, służący do szczelnego zamykania probówek wyposażony w rurkę odprowadzającą;
łuczywko – długie drewienko.
Instrukcja wykonania doświadczenia:
Do probówki umieszczonej na statywie wsypano manganianu() potasu.
Krystalizator wypełniono wodą destylowaną, a do środka włożono do góry dnem kolejną probówkę z wprowadzonym do niej gumowym wężem i pozwolono jej napełnić się wodą.
Drugi koniec węża przymocowano do korka pierwszej probówki.
Zapalono palnik i ogrzewano zawartość probówki.
Po zebraniu gazu wyjęto wypełnioną gazem probówkę, zamknięto ją korkiem i umieszczono w statywie.
Zapalono łuczywko.
Otworzono probówkę i wprowadzono łuczywko do środka.
Obserwacje:
W wyniku ogrzewania pierwszej probówki z manganianem() potasu wydziela się bezbarwny gaz, który wypiera wodę z probówki drugiej. Balonik napompowany uzyskanym gazem opada.
Wyniki:
W wyniku termicznego rozkładu manganianu() potasu powstaje tlen.
Wnioski:
Tlen cząsteczkowy w warunkach standardowych jest bezbarwnym, słabo rozpuszczalnym w wodzie gazem, o gęstości większej od gęstości powietrza. Hipoteza została potwierdzona.