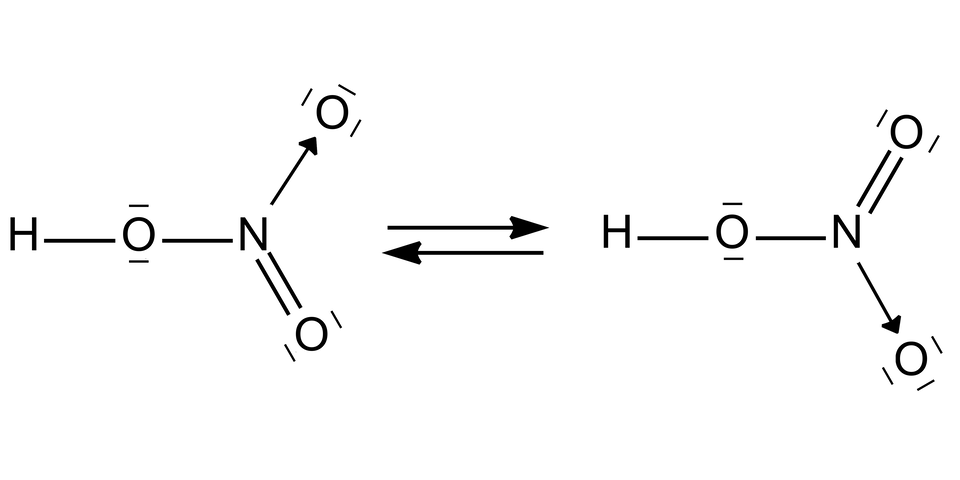
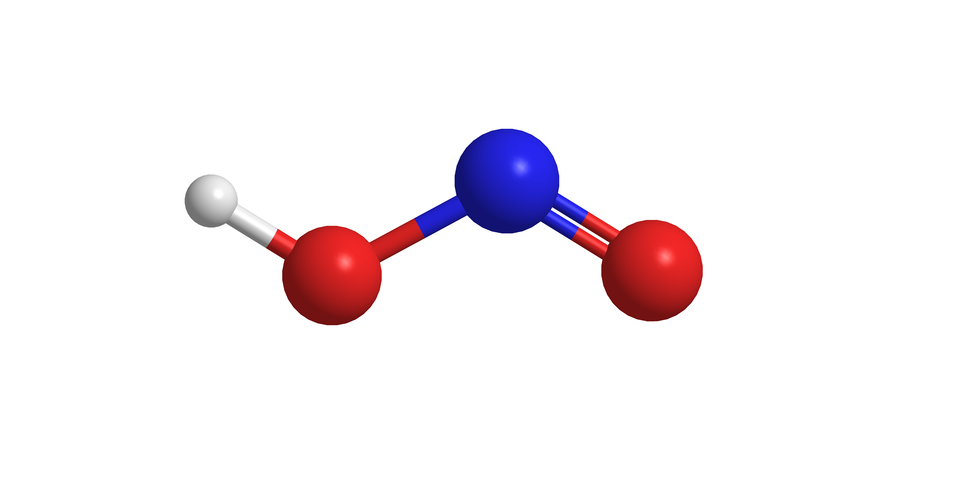
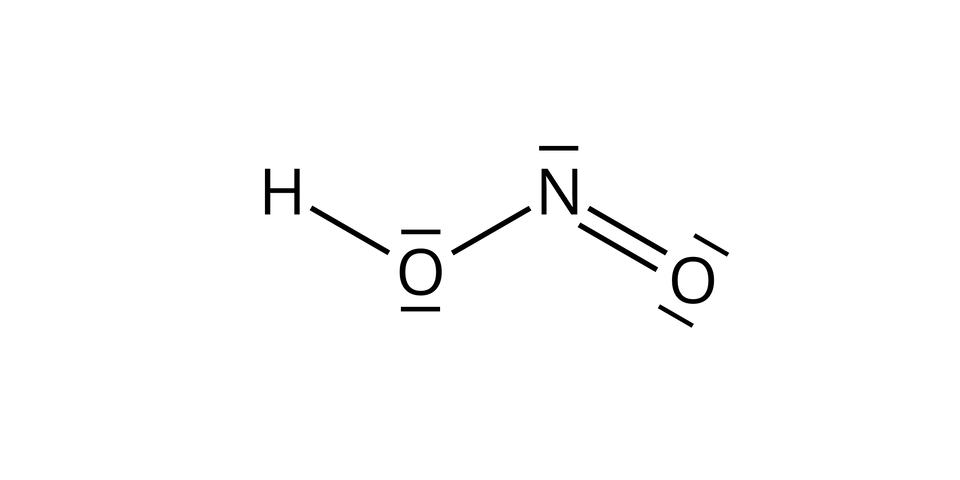
Związki azotu
Tlenki azotu
Azot tworzy z tlenem kilka tlenków, w których występuje na kilku różnych stopniach utlenienia. Tlenki azotu mają charakter kwasowy albo obojętny, w zależności od stopnia utlenienia azotu w związku, co prezentuje poniższy schemat.

Tlenek azotu(I) (tlenek diazotu),
W temperaturze pokojowej jest to bezbarwny gaz o słodkawym zapachu i smaku, kiedyś stosowany jako środek znieczulający (gaz rozweselający) w zabiegach dentystycznych.
Otrzymywany w wyniku łagodnego ogrzewania azotanu(V) amonu ():
Rozkłada się z wydzieleniem tlenu, dzięki czemu podtrzymuje palenie. nie reaguje z wodą, ale się w niej rozpuszcza, tworząc roztwór obojętny. Tlenek diazotu należy do głównych gazów cieplarnianych. Będąc trzecim najważniejszym długotrwałym gazem cieplarnianym przyczynia się do powstawania dziury ozonowej i efektu cieplarnianego.
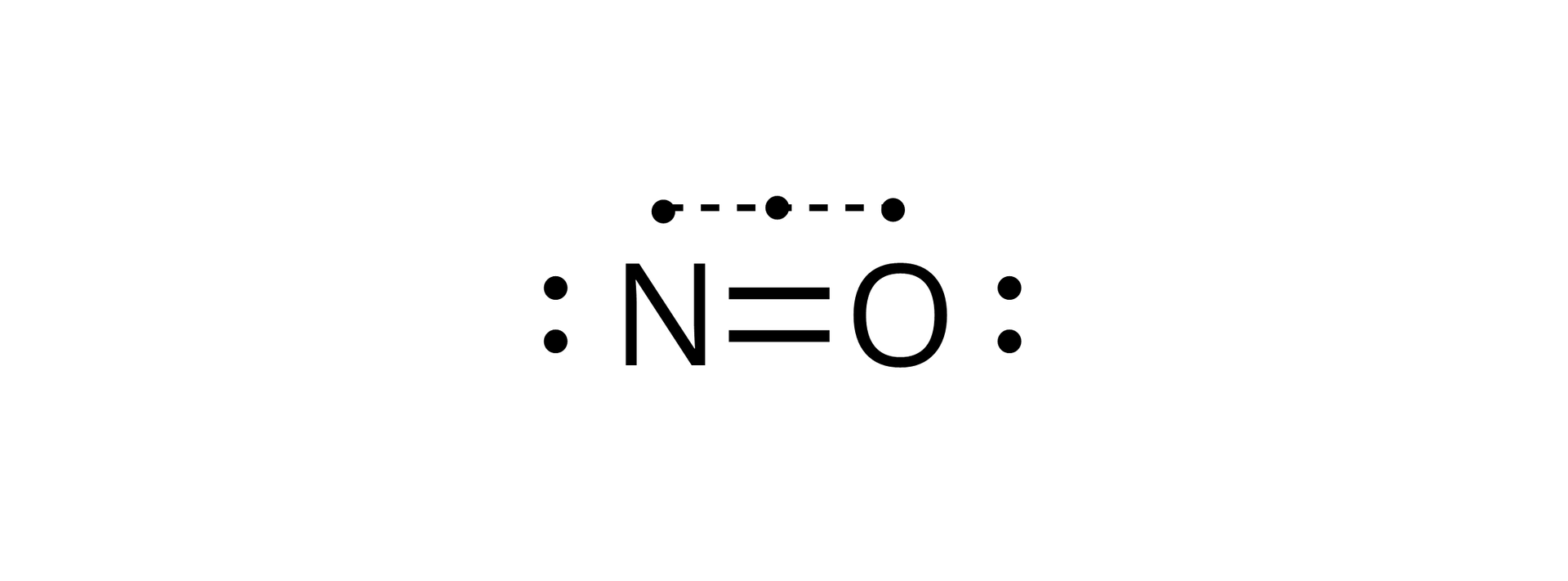
Tlenek azotu(II) (monotlenek azotu),
Jest to bezbarwny gaz, trudny do skroplenia (temperatura wrzenia –151°C). Łatwo utlenia się do , wraz z którym stanowi produkt przejściowy w produkcji kwasu azotowego(V). Z uwagi na jeden niesparowany elektron na atomie azotu jest rodnikiem niestabilnym i bardzo reaktywnym.
W powietrzu samorzutnie reaguje z tlenem, tworząc trujący tlenek azotu(IV).
W stanie ciekłym i stałym tlenek ten tworzy dimery, co zmniejsza jego reaktywność.
Tlenek azotu(II) można otrzymać na drodze bezpośredniej syntezy z pierwiastków w wysokiej temperaturze, możliwej do osiągnięcia podczas wytworzenia łuku elektrycznego.

Na skalę przemysłową można otrzymać metodą katalitycznego spalania amoniaku (tzw. metoda Ostwalda).
W warunkach laboratoryjnych otrzymywany jest z kwasu azotowego(III). Kwas ten jest stabilny w roztworach rozcieńczonych. W miarę wzrostu jego stężenia lub na skutek ogrzewania, rozkłada się na kwas azotowy(V), tlenek azotu(II) oraz wodę.
Tlenek azotu(II) można również otrzymać, działając rozcieńczonym kwasem azotowym(V) na wiórki miedzi.

Tlenek azotu(II) odgrywa ważną rolę w organizmach żywych. Zbadano, że jest produktem przemiany materii w komórkach bakterii. W wyniku jego działania dochodzi do rozkurczu mięśni gładkich naczyń krwionośnych; ponadto hamuje zlepianie się płytek krwi, ma wpływ na funkcje ośrodkowego układu nerwowego (m.in. na procesy uczenia, pamięci, mechanizm drgawek, procesy neurodegeneracyjne). Leki, będące donorami , stosowane w walce z chorobami serca, jak dusznica bolesna, niewydolność mięśnia sercowego, wpływają rozkurczająco na naczynia krwionośne, obniżają ciśnienie tętnicze krwi. Za wyjaśnienie roli w układzie sercowo‑naczyniowym w 1998 r. Nagrodę Nobla otrzymali: R. Furchgott, L.J. Ignarro i F. Murad.
Tlenek azotu(III) (tritlenek diazotu),
Należy do tlenków bardzo nietrwałych, z tego powodu w postaci czystej nie znajduje żadnych praktycznych zastosowań.
Można go otrzymać w postaci intensywnie niebieskiej cieczy, w temperaturze niższej niż -13,5°C, w reakcji:
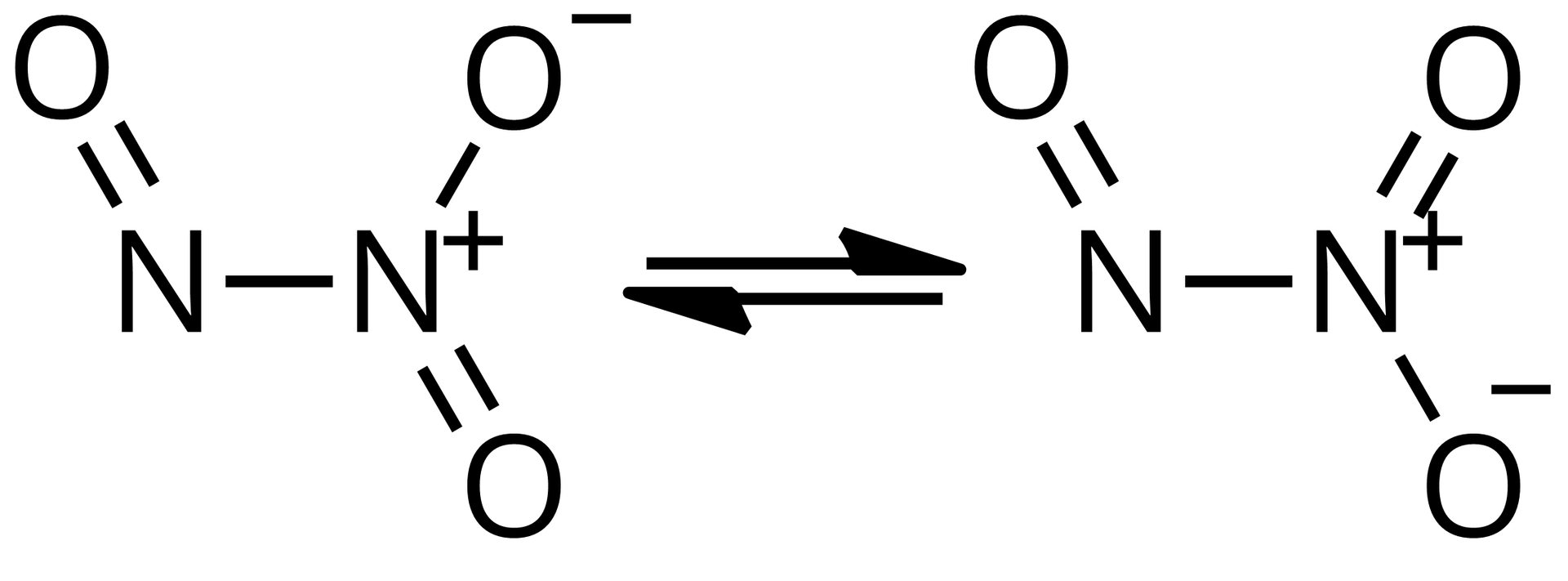
W temperaturze wyższej niż -13,5°C tlenek azotu(III) częściowo się rozkłada na i , przez co barwa zmienia się na jasnożółtą.
Jest bezwodnikiem kwasu azotowego(III).
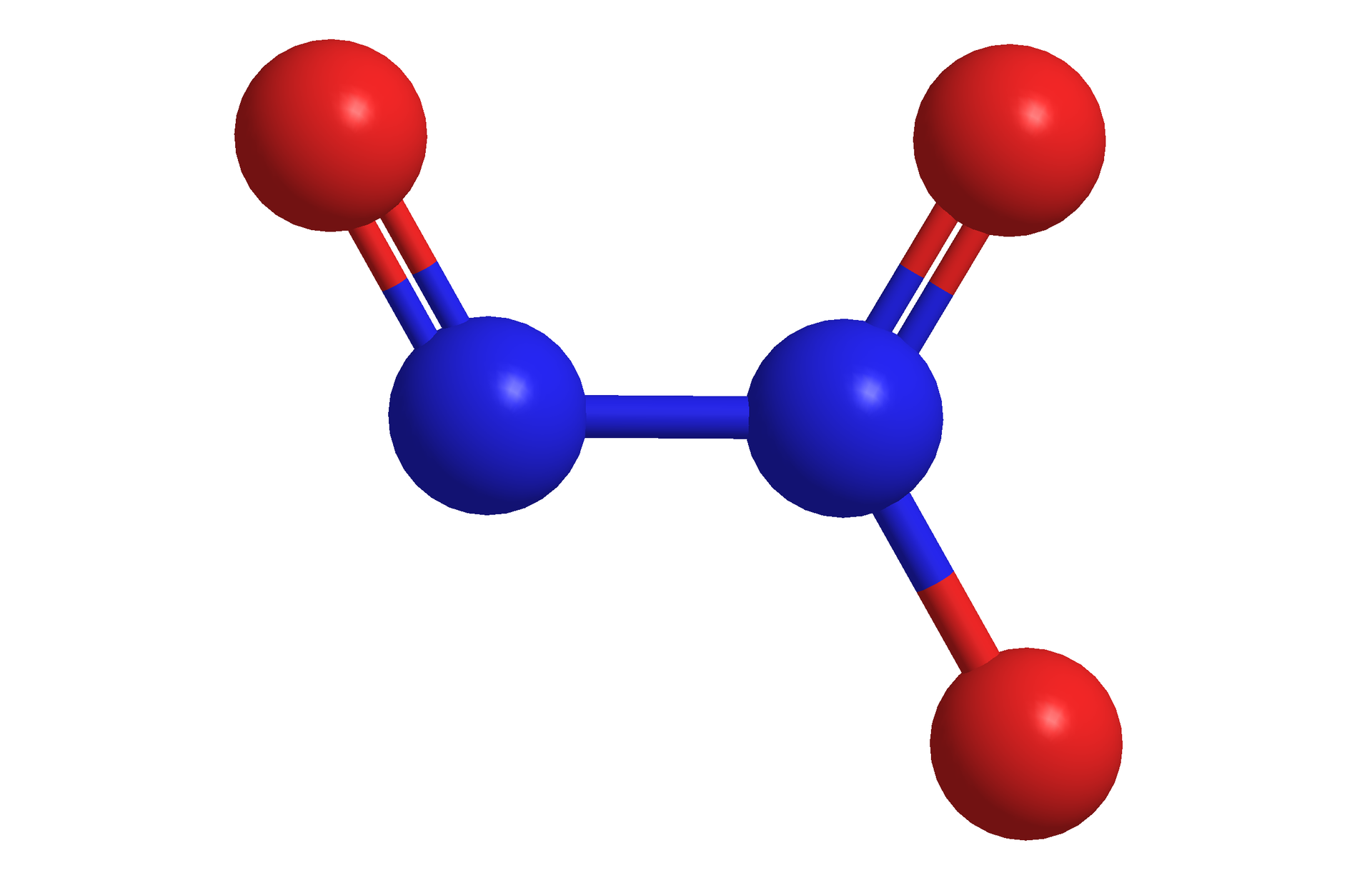
Tlenek azotu(IV) (ditlenek azotu) –
Jest to brunatny gaz o charakterystycznym zapachu. Jest dobrze rozpuszczalny w wodzie.
Na skalę techniczną otrzymuje się go po zmieszaniu tlenku azotu(II) i tlenu, zgodnie z równaniem reakcji:
Innymi sposobami tlenek ten można otrzymać w wyniku rozkładu stężonego kwasu azotowego(V), redukcji miedzi za pomocą stężonego kwasu azotowego(V) albo w wyniku rozkładu termicznego azotanu(V) ołowiu(II), zgodnie z przedstawionymi równaniami reakcji:
Tlenek azotu(IV) jest tlenkiem kwasowym i w reakcji z wodą tworzy równomolową mieszaninę kwasu azotowego(III) i kwasu azotowego(V).
Tlenek azotu(IV) w temperaturze poniżej 147°C spontanicznie dimeryzuje, tworząc dimer – gaz o słomkowej barwie:
Ze spadkiem temperatury stopień dimeryzacji rośnie.

Tlenek azotu(IV) powoduje podrażnienie układu oddechowego, oczu i kaszel. Ze względu na właściwości utleniające, powoduje utlenienie zawartego w hemoglobinie do , w efekcie czego hemoglobina traci zdolność do przenoszenia tlenu. Odpowiada on także za barwę smogu.
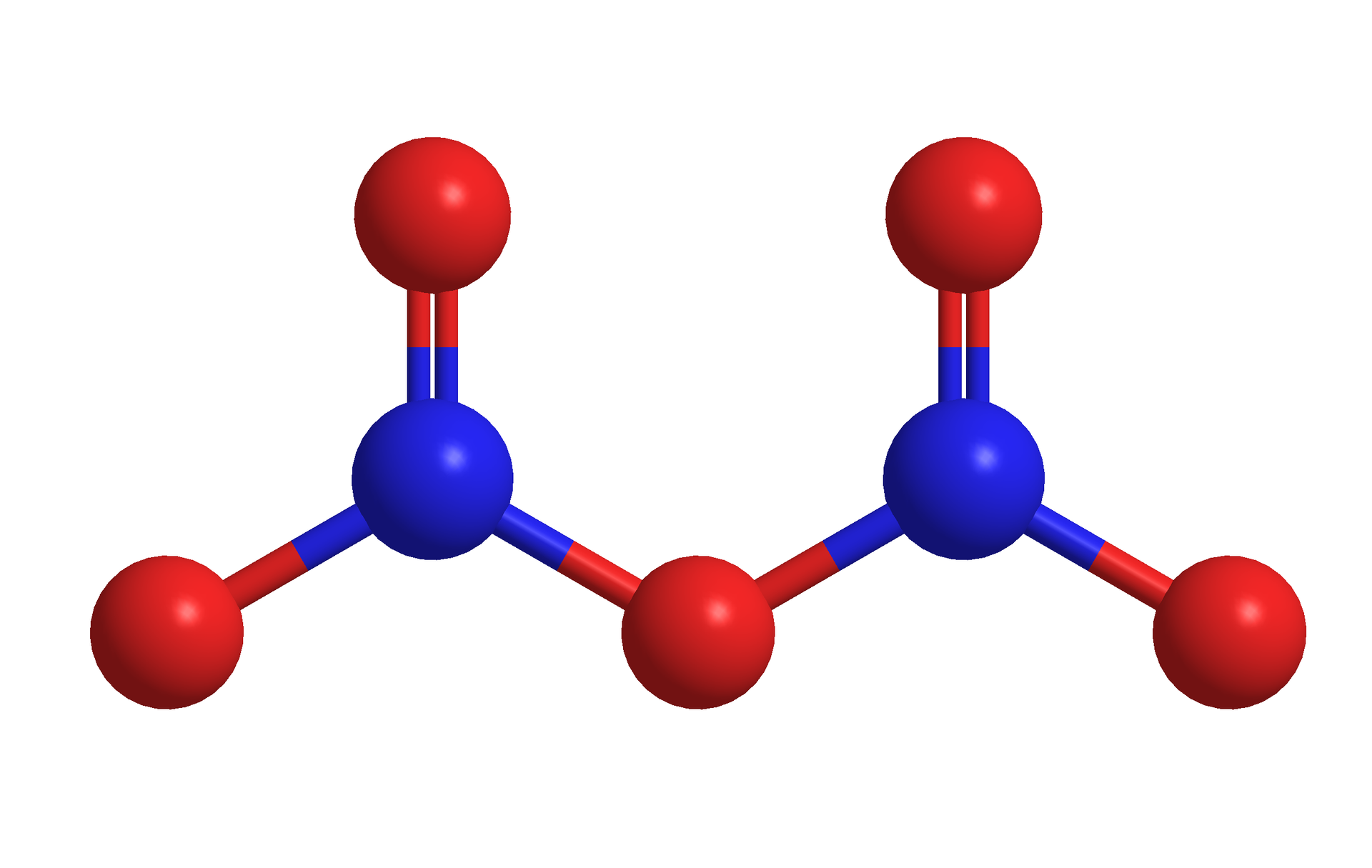
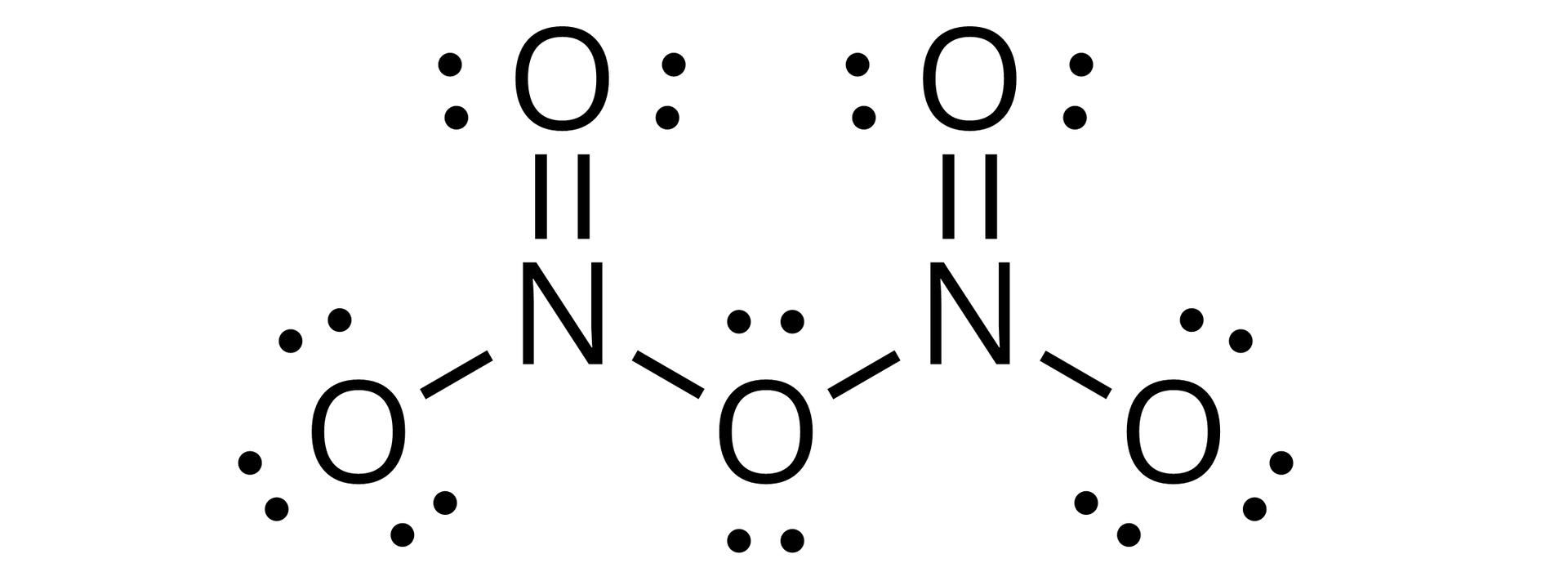
Tlenek azotu(V) (pentatlenek diazotu) –
W temperaturze pokojowej przyjmuje formę białych kryształków rozpuszczalnych w wodzie.
Powstaje przez odwodnienie kwasu azotowego(V) za pomocą tlenku fosforu(V) w temperaturze pokojowej. Równanie reakcji otrzymywania tlenku azotu(V):
Jest związkiem nietrwałym, rozkładającym się spontanicznie w temperaturze pokojowej do dwutlenku azotu i tlenu. Związek ten reaguje gwałtownie z wodą, jest bezwodnikiem kwasu azotowego. Ze względu na jego nietrwałość nie znajduje on w formie czystej praktycznych zastosowań.
Oprócz tlenków, opisanych w tekście, w pewnych warunkach można otrzymać:
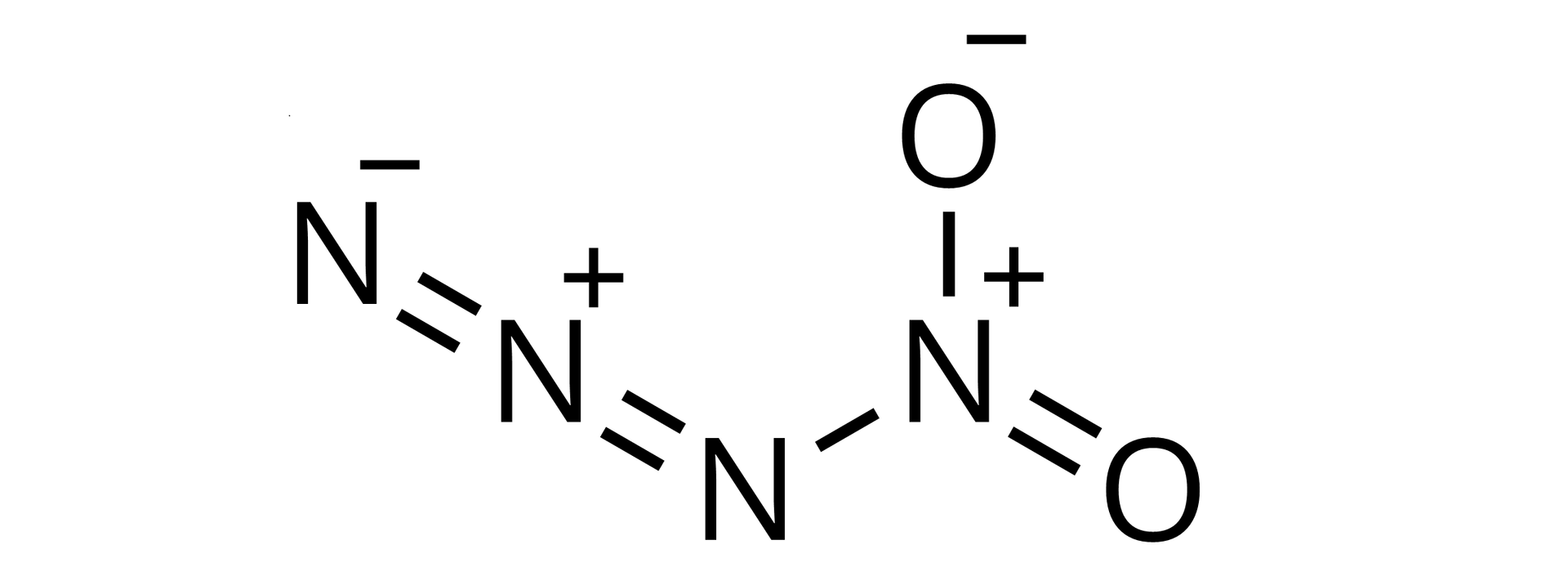
1. Azydek nitrozylu – trwały w temperaturze poniżej -33°C. Po raz pierwszy syntezę nitrozyladyzu opisano w 1958 r. Otrzymano go w reakcji azydku sodu z chlorkiem nitrozylu, w temperaturze poniżej −50°C.
2. Azydek nitroilu - trwały w temperaturze poniżej -10°C.
Kwasy tlenowe azotu
Kwas azotowy()

Kwas azotowy() jest bezbarwną cieczą. Gęstość stężonego kwasu azotowego() jest większa niż gęstość wody w temperaturze pokojowej. W postaci stężonej najczęściej spotyka się go jako roztwór około . Omawiany kwas jest określany również jako „dymiący”, ponieważ po otwarciu butelki wydobywają się obłoki brunatnego gazu. Kwas
azotowy() jest nietrwały i w wyniku dłuższego przechowywania ulega reakcji rozkładu, co przedstawia poniższe równanie reakcji:
Światło i podwyższona temperatura wpływają na przyspieszenie reakcji rozkładu kwasu.
Kwas azotowy() należy do kwasów silnie utleniających oraz jest jednym z najsilniejszych kwasów tlenowych. W temperaturze jego stała dysocjacji wynosi . Równanie dysocjacji kwasu azotowego():
Kwas azotowy() jest substancją żrącą, która powoduje m.in. poparzenia na skórze w postaci żółtych plam. Jest to efekt zajścia reakcji ksantoproteinowej – pod wpływem stężonego zachodzi nitrowanie pierścieni benzenowych białek i powstaje połączenie o barwie żółtej.

- działanie żrące na skórę, kat. zagrożeń , , ; poważne uszkodzenie oczu, kat. zagrożenia ;
- toksyczność ostra, kat. zagrożeń , , ;
- działanie utleniające.

Kwas azotowy() jest jednym z najważniejszych surowców w przemyśle chemicznym. Substancja ta znajduje zastosowanie w produkcji m.in.: nawozów sztucznych, barwników, leków, tworzyw sztucznych oraz materiałów wybuchowych.
Kwas azotowy()
Kwas azotowy() należy do słabych kwasów. Jego stała dysocjacji wynosi . Równanie dysocjacji kwasu azotowego():
Kwas azotowy() jest nietrwałym kwasem tlenowym. W wyniku zatężania ulega reakcji rozkładu, wg poniższego równania reakcji:
Omawiany kwas jest trwały w rozcieńczonym, wodnym roztworze. Zarówno kwas azotowy(), jak i jego sole wpływają negatywnie na organizm człowieka. Kwas działa mutagennie.
Sole
Azotany()
Sole kwasu azotowego(), czyli azotany(), były dawniej określane jako saletry. Wszystkie popularne sole kwasu azotowego() są rozpuszczalne w wodzie.
– azotan() potasu, saletra potasowa lub indyjska.

Saletra potasowa znajduje zastosowanie m.in. jako nawóz mineralny, składnik czarnego prochu strzelniczego czy konserwant w przemyśle spożywczym do konserwacji mięsa.
– azotan() sodu, saletra sodowa lub chilijska.
Saletra sodowa jest białą, krystaliczną substancją stałą. Sól ta znajduje zastosowanie m.in. jako nawóz mineralny w produkcji materiałów wybuchowych, utleniacz stałych paliw rakietowych, a także jako konserwant w przemyśle spożywczym.
– azotan() wapnia, saletra wapniowa lub norweska.
Saletra wapniowa jest białą, krystaliczną substancją stałą. Znajduje zastosowanie m.in. jako nawóz mineralny.
– azotan() amonu, saletra amonowa.
Saletra amonowa to białe lub prawie białe, higroskopijne ciało stałe. Bardzo dobrze rozpuszcza się w wodzie. Azotan amonu ma właściwości utleniające.
Saletry wykazują właściwości utleniające. Tę cechę wykorzystali Chińczycy, którzy mieszali sól kwasu azotowego() z węglem drzewnym i siarką. W ten sposób otrzymali czarny proch strzelniczy.
W wyniku kolizji, poduszki powietrzne w autach są wypełniane azotem, który powstaje dzięki reakcji rozkładu m.in. azydku sodu (). Mieszanina reakcyjna składa się z azydku sodu (), azotanu() potasu oraz tlenku krzemu(). Jeśli będzie miało miejsce zderzenia auta, w ułamku sekundy zajdą reakcje opisane poniższymi równaniami reakcji chemicznych.
Powstały w pierwszej reakcji sód reaguje z azotanem() potasu, przez co tworzy się azot oraz tlenki sodu i potasu, które następnie reagują z tlenkiem krzemu(), tworząc bezpieczne krzemiany.

Jednym z najważniejszych związków azotu i zarazem jednym z najsilniejszych kwasów nieorganicznych jest kwas azotowy(). Znajduje liczne i różnorodne zastosowania. Podobnie jego sole, tzw. saletry, stosowane są na wielu różnych płaszczyznach, głównie jako nawozy azotowe. Innym związkiem jest nietrwały kwas azotowy(). Zarówno on, jak i jego sole działają negatywnie na organizm człowieka.
Związki azotu podsumowanie
Zapoznaj się z poniższym filmem edukacyjnym i odpowiedz na pytanie: jakie ważne związki chemiczne tworzy azot?

Film dostępny pod adresem /preview/resource/RJcTzVj7dnQns
Film opowiadający o tym, jakie ważne związki chemiczne tworzy azot.
Dlaczego występuje tak duża ilość różnych tlenków azotu?
Jakie zagrożenia niosą tlenki azotu?
Stwórz mapę myśli, w której uwzględnisz rodzaje związków azotu.
- Nazwa kategorii: Związki chemiczne azotu
- Nazwa kategorii: tlenki azotu
- Elementy należące do kategorii Związki chemiczne azotu
- Elementy należące do kategorii
- Elementy należące do kategorii tlenki azotuKoniec elementów należących do kategorii tlenki azotu
- Elementy należące do kategorii Koniec elementów należących do kategorii
Obieg azotu w przyrodzie
Czy wiesz, jaki jest obieg azotu w przyrodzie? Jakie związki azotu biorą w nim udział? Gdzie występują tlenki azotu w atmosferze i jak powstają? Zapoznaj się z poniższą grafiką interaktywną przedstawiającą ważną rolę związków azotu w chemii naszej atmosfery, a następnie rozwiąż ćwiczenia.
Czy wiesz, jaki jest obieg azotu w przyrodzie? Jakie związki azotu biorą w nim udział? Gdzie występują tlenki azotu w atmosferze i jak powstają? Zapoznaj się z opisem grafiki interaktywnej przedstawiającej ważną rolę związków azotu w chemii naszej atmosfery, a następnie rozwiąż ćwiczenia.
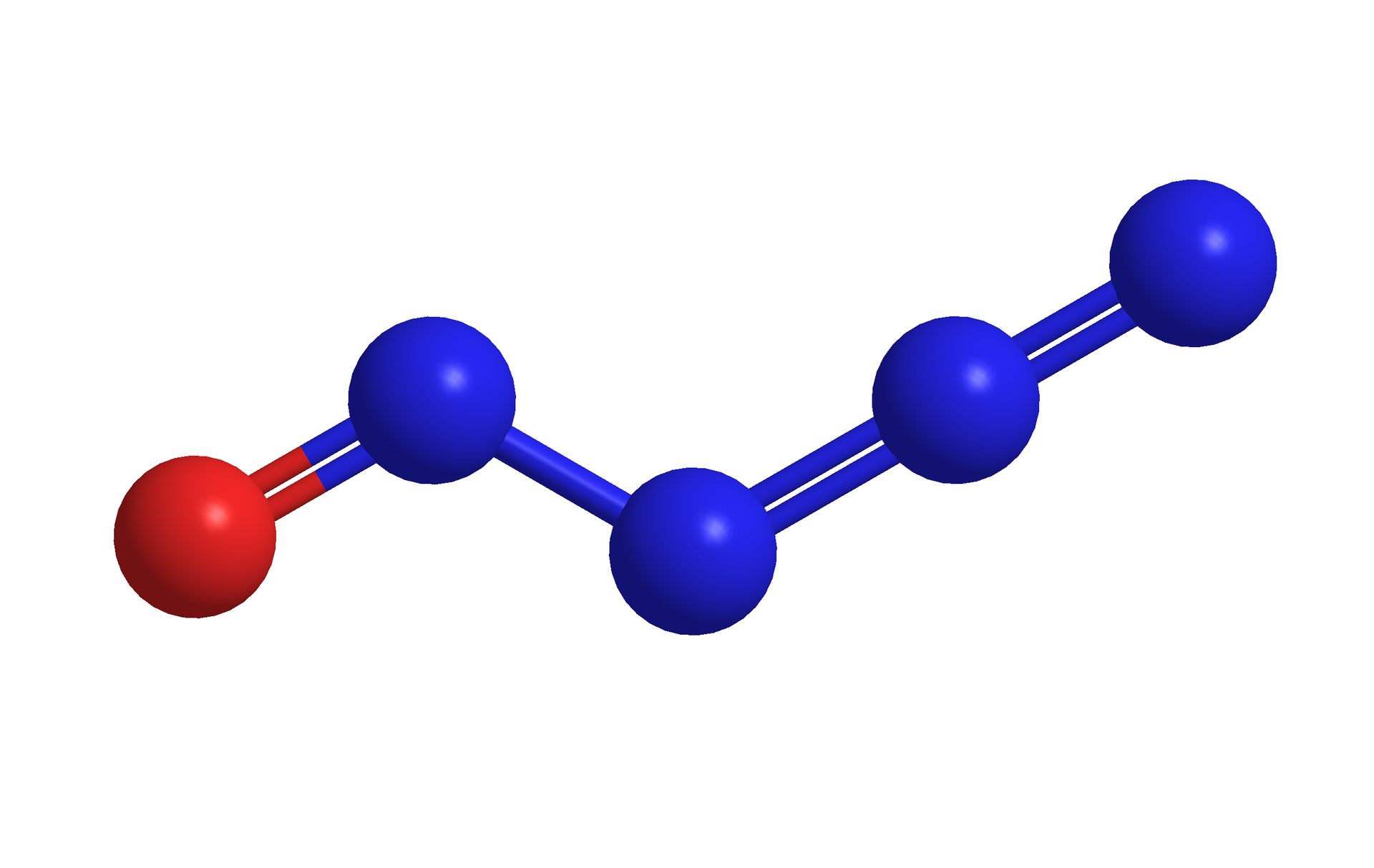
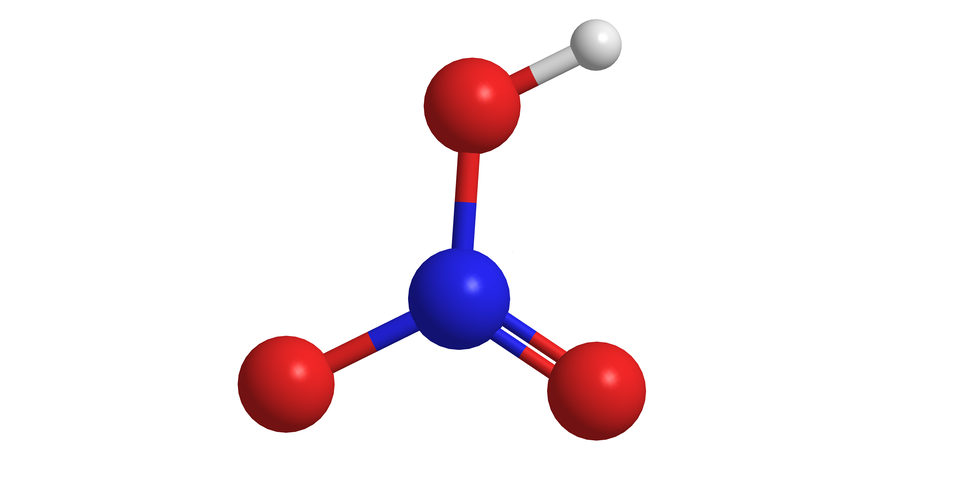
O indeks dolny, dwa, koniec indeksu dolnego, plus, O, razy, strzałka w prawo, O indeks dolny, trzy, koniec indeksu dolnego. Dlatego w ciągu dnia NO, NO2 i ozon istnieją w quasi‑równowadze, która zależy od ilości światła słonecznego., 6. TLENEK AZOTU(II). Tlenek azotu(II) (NO) jest jedną z dwóch najważniejszych form reaktywnego azotu w powietrzu. Na ilustracji jest model 3D tlenku azotu(II) - niebieska kulka łączy się z czerwoną kulką. Opis. W temperaturze pokojowej występuje jako bezbarwny gaz, o temperaturze topnienia −163,6 °C i temperaturze wrzenia −151,7 °C. Posiada on jeden niesparowany elektron (dlatego też występuje jako rodnik), stąd jest niestabilny i bardzo reaktywny., 7. TLENEK AZOTU(IV). OTRZYMYWANIE. Tlenek azotu(II) (NO) przy zetknięciu z tlenem (O2) reaguje z wytworzeniem brunatnych par tlenku azotu(IV) (N O indeks dolny 2) według równania reakcji chemicznej: dwa N O, plus, O indeks dolny, dwa, koniec indeksu dolnego, strzałka w prawo, dwa N O indeks dolny, dwa, koniec indeksu dolnego, 8. TLENEK AZOTU(IV). OTRZYMYWANIE. NO jest utleniany przez ozon w atmosferze w skali czasu wynoszącej dziesiątki minut, prowadząc do otrzymania NO2 zgodnie z poniższym schematem reakcji chemicznej: N O, plus, O indeks dolny, trzy, koniec indeksu dolnego, strzałka w prawo, N O indeks dolny, dwa, koniec indeksu dolnego, plus, O indeks dolny, dwa, koniec indeksu dolnego, 9. RODNIKI. Organiczne rodniki nadtlenowe (nietrwałe związki utlenione) mogą być zaangażowane w ten cykl azotowy. Wszystkie formy nadtlenowe, pochodzące z reakcji, ulegają następnie w atmosferze dość skomplikowanym i licznym procesom prowadzącym do otrzymania alkoholi, aldehydów, azotanów(V), kwasów karboksylowych., 10. AZOT. Cząsteczki azotu (N indeks dolny 2) w powietrzu są bardzo stabilne i z tego też powodu nie łatwe do utlenienia. Kilka rodzajów bakterii rozwinęło specjalne mechanizmy pękania potrójnego wiązania w cząsteczce azotu i tworzenia jego utlenionych związków. Na ilustracji są połączone ze sobą wiązaniem potrójnym dwa atomy azotu. Każdy z nich ma po jednej czarnej pionowej kresce z boku. Podpis pod zdjęciem: Wzór strukturalny N indeks dolny 2. Ale o wiele bardziej istotne są procesy, w których potrójne wiązanie pęka, takie jak wysoka temperatura. Przykładem może być spalanie paliwa w silniku samochodowym. Większość antropogenicznych (wytworzonych przez człowieka) N O indeks dolny x pochodzi właśnie z tego źródła. Na zdjęciu są samochody na ulicy. Z rury wydechowej jednego z nich wydobywa się ciemny dym. Podpis pod zdjęciem: Spaliny. Opis. Pękanie wiązania ma miejsce również podczas innych reakcji, w których występuje wysoka temperatura, tj. w najgorętszych miejscach płomieni spalających biomasę np. podczas procesów spalania, erupcji wulkanicznych, czy procesów przemysłowych. Głównym źródłem pękania wiązania w cząsteczce azotu jest błyskawica (gdzie temperatury dochodzą do 30 000 stopni Celsjusza)., 11. TLENEK AZOTU(IV). Druga najważniejsza reaktywna forma azotu w powietrzu to tlenek azotu(IV) (N O indeks dolny 2). Tlenek azotu(IV) jest rozkładany przez światło słoneczne, tworząc tlenek azotu(II) (NO). Na ilustracji jest model czaszowy cząsteczki - do niebieskiej kulki przylegają z dwóch stron czerwone kulki. Podpis pod zdjęciem: Model 3D tlenku azotu(IV). Opis. Podstawowy stan elektronowy tlenku azotu(IV) jest stanem dubletowym, ponieważ azot posiada jeden niesparowany elektron. Samotny elektron w cząsteczce związku azotu oznacza również, że ten związek jest wolnym rodnikiem, dlatego też jest on często zapisywany jako ·N O indeks dolny 2., 12. Na ilustracji jest strzałka od tlenku azotu do kwasu azotowego. Opis. KWAS AZOTOWY(V). Kwas azotowy(V) może powstawać zarówno w ciągu dnia, jak i w nocy. W świetle dziennym wytwarzany jest w wyniku utleniania N O indeks dolny 2, co stanowi główny sposób usuwania tlenku azotu(IV) z atmosfery. trzy N O indeks dolny, dwa, koniec indeksu dolnego, plus, H indeks dolny, dwa, koniec indeksu dolnego, O, strzałka w prawo, dwa H N O indeks dolny, trzy, koniec indeksu dolnego, plus, N O, 13. KWAS AZOTOWY(V). Na ilustracji jest model kulkowo‑pręcikowy. Niebieska kulka łączy się u góry i na dole po lewej stronie z czerwoną kulką - jedno wiązanie zaznaczono linią przerywaną - oraz na dole po prawej stronie z czerwoną kulką połączoną z małą, białą kulką. Podpis pod ilustracją: Model 3D kwasu azotowego(V). Kwas azotowy(V) jest częścią polarnych chmur stratosferycznych. Trihydrat kwasu azotowego(V) (HNO3·3 H2O) tworzy cząsteczki, na których rozwija się dziura ozonowa., 14. KWAS AZOTOWY(V). Kwas azotowy(V) (para) jest wchłaniany bezpośrednio przez ziemię i przekształcany w jony azotanowe(V)., 15. KWAŚNE DESZCZE. H N O indeks dolny 3 może rozpuścić się w kropelkach chmur i spowodować powstawanie kwaśnego deszczu. Na zdjęciu jest las. Na pierwszym planie stoją suche pnie drzew. Podpis pod zdjęciem: Uszkodzenia drzewostanu wywołane kwaśnymi deszczami w Czechach., 16. ASYMILACJA AZOTU. Asymilacja azotu ma na celu generowanie organicznych pochodnych azotowych, takich jak aminokwasy, z nieorganicznych form azotu dostępnych w środowisku naturalnym. Rośliny, grzyby i niektóre bakterie nie potrafiące wiązać azotu (N indeks dolny 2), zależą od właściwości absorbowania azotanów(V) lub amoniaku do własnych potrzeb. Natomiast zwierzęta, są uzależnione od azotu organicznego pochodzącego z pożywienia. Rośliny czerpią azot z gleby w formie anionów azotanowych(V) (N O indeks dolny 3 indeks górny -) i kationów amonowych (N H indeks dolny 4 indeks górny +). Dominującą postacią przyswajalnego azotu w glebach tlenowych, gdzie może mieć miejsce nitryfikacja, są aniony azotanowe(V). Jednak ze względu na fakt, iż występowanie amoniaku może przeważać na łąkach oraz w zalanych glebach beztlenowych (np. pola ryżowe), nie zawsze tak jest. Na liczebność różnych postaci azotu mogą wpływać same korzenie roślin, poprzez zmianę pH i dostarczanie związków organicznych lub tlenu. Ma to wpływ na aktywność drobnoustrojów, taką jak: wzajemna przemiana różnych gatunków azotu, uwalnianie amoniaku z materii organicznej w glebie, wiązanie azotu przez bakterie. Rośliny pobierają jony amonowe poprzez transportery amoniaku, które znajdują się w błonie komórkowej. Aniony azotanowe(V) przenoszone są przez różne białka transportowe, które wykorzystują gradient protonów do napędzania ich transportu. Azot cząsteczkowy przenoszony jest z korzenia do pędu przez ksylem w postaci azotanów(V), rozpuszczonego amoniaku i aminokwasów. Na ilustracji są trzy spiralne wstążki w różnych kolorach. Podpis pod zdjęciem: Glikoproteina Rhesus C PDN 3hd6., 17. TLENEK AZOTU(I). Tlenek azotu(I) (N indeks dolny 2 O) powstaje podczas procesów degradacji mikrobiologicznej. Jest to ważny gaz cieplarniany, ale nie reaguje w troposferze. W stratosferze niszczy ozon. Koncentracja N indeks dolny 2 O w atmosferze zwiększyła się z ok. 270 ppb do 322 ppb do 2008 r., a do wzrostu rozwoju tlenku azotu(I) w atmosferze niewątpliwie przyczynia się jego emisja z terenów rolniczych. Powodem jest prawie dziesięciokrotne zwiększenie zużycia nawozów azotowych w ostatnim czasie. Głównym źródłem emisji tego gazu jest gleba (za 2/3 emisji). Emisja tlenku azotu(I) z gleby jest zależna od ilości wprowadzonego nawozu azotowego do gleby oraz od intensywności nitryfikacji i denitryfikacji, które zależą od wielu innych czynników, takich jak: klimat, ocena gleby, czy też zabiegów agrotechnicznych. Emisja tego tlenku jest zależna również od ilości azotu wymywanego z gleb, co prowadzi do ich zubożenia w azot. Na ilustracji jest model cząsteczki: dwie niebieskie kulki są ze sobą połączone wiązaniem o długości 112,6 pikometrów. Kulka leżąca po prawej stronie łączy się z czerwoną kulką wiązaniem o długości 118,6 pikometra. Podpis pod zdjęciem: Model 3D tlenku azotu(I)., 18. RODNIK razy N O indeks dolny 3. Kolejna forma tlenku azotu to bardzo reaktywny rodnik azotanowy (razy N O indeks dolny 3), który powstaje w ciemności, co kontroluje chemię nocnej atmosfery. Rodniki azotanowe razy N O indeks dolny 3 są najbardziej aktywnymi utleniaczami. Rodniki to związki chemiczne, które są bardzo nietrwałe i zwykle reagują niezwykle szybko.
Reakcja tlenku azotu(IV) z ozonem prowadzi do powstania rodnika razy N O indeks dolny 3 o stosunkowo długim czasie życia: N O indeks dolny, dwa, koniec indeksu dolnego, plus, O indeks dolny, trzy, koniec indeksu dolnego, strzałka w prawo, razy, N O indeks dolny, trzy, koniec indeksu dolnego, plus, O indeks dolny, dwa, koniec indeksu dolnego. Rodniki ·NO3 absorbują promieniowanie widzialne (570‑670 nm). Pod wpływem tego promieniowania rozkładają się bezpośrednio na N O indeks dolny 2 i razy O (częściowo powstaje NO i O indeks dolny 2). Funkcją rodników razy N O indeks dolny 3 jest udział w procesach atmosferycznego utleniania aldehydów, alkanów i węglowodorów aromatycznych. Poza tym uczestniczą one w analogicznych procesach w hydrosferze., 19. TLENEK AZOTU(V). Reakcja między razy N O indeks dolny 3 i razy N O indeks dolny 2 jest jedynym sposobem powstawania N indeks dolny 2 O indeks dolny 5 w atmosferze. Na ilustracji jest model cząsteczki. Są dwie niebieskie kulki. Każda z nich łączy się na górze z czerwoną kulką oraz na dole z czerwoną kulką. Niebieskie kulki łączą się za pośrednictwem jednej wspólnej czerwonej kulki. Po zewnętrznych stronach modeli zaznaczono wiązania linią przerywaną. Podpis pod zdjęciem: Model 3D tlenku azotu(V). razy, N O indeks dolny, trzy, koniec indeksu dolnego, plus, razy, N O indeks dolny, dwa, koniec indeksu dolnego, strzałka z dwoma grotami N indeks dolny, dwa, koniec indeksu dolnego, O indeks dolny, pięć, koniec indeksu dolnego. Tlenek azotu(V) jest nietrwały i może rozpaść się z powrotem na ·N O indeks dolny 3 i ·N O indeks dolny 2., 20. RODNIK razy N O indeks dolny 3 razy N O indeks dolny 3 tworzy się również w reakcji dysproporcjonowania tlenku azotu(V): N indeks dolny, dwa, koniec indeksu dolnego, O indeks dolny, pięć, koniec indeksu dolnego, strzałka w prawo, razy, N O indeks dolny, trzy, koniec indeksu dolnego, plus, razy, N O indeks dolny, dwa, koniec indeksu dolnego, 21. TLENEK AZOTU(V). N indeks dolny 2 O indeks dolny 5 utworzony w zanieczyszczonych obszarach może reagować z kroplami wody lub mokrymi powierzchniami z wytworzeniem kwasu azotowego(V) (H N O indeks dolny 3): N indeks dolny, dwa, koniec indeksu dolnego, O indeks dolny, pięć, koniec indeksu dolnego, plus, H indeks dolny, dwa, koniec indeksu dolnego, O, strzałka w prawo, dwa H N O indeks dolny, trzy, koniec indeksu dolnego, 22. KWAS AZOTOWY(V). Kwas azotowy(V) może powstać również w reakcji rodnika azotanowego z wodą, zgodnie ze schematem: razy, N O indeks dolny, trzy, koniec indeksu dolnego, plus, H indeks dolny, dwa, koniec indeksu dolnego, O, strzałka w prawo, H N O indeks dolny, trzy, koniec indeksu dolnego, plus, razy, O H, 23. DENITRYFIKACJA. Denitryfikację stanowi redukcja jonów azotanowych (N O indeks dolny 3 indeks górny -) do wolnego azotu (N indeks dolny 2). Powstały azot zostaje uwolniony do atmosfery w postaci gazowej. Proces ten ma miejsce dzięki bakteriom denitryfikacyjnym (anaeroby, beztlenowce). Bakterie beztlenowe żyją w miejscach niedostępnych dla wolnego tlenu np. w głębokich warstwach gleby bądź w wodach gruntowych. Proces anammox to analogiczny proces przeprowadzany przez bakterie, który prowadzi do bezpośredniego utleniania nadmiernych jonów amonowych do azotu gazowego.