Film edukacyjny
Wyobraź sobie, że pracujesz w laboratorium syntezy organicznej. Realizujesz projekt, który zakłada otrzymanie pewnego związku organicznego o ciekawych właściwościach spektroskopowych. Jednym z etapów syntezy jest oczyszczanie produktu organicznego i wykonanie ekstrakcji. Procedura ekstrakcji zakłada przemycie fazy organicznej przy pomocy roztworu kwasu octowego (etanowego) o stężeniu .
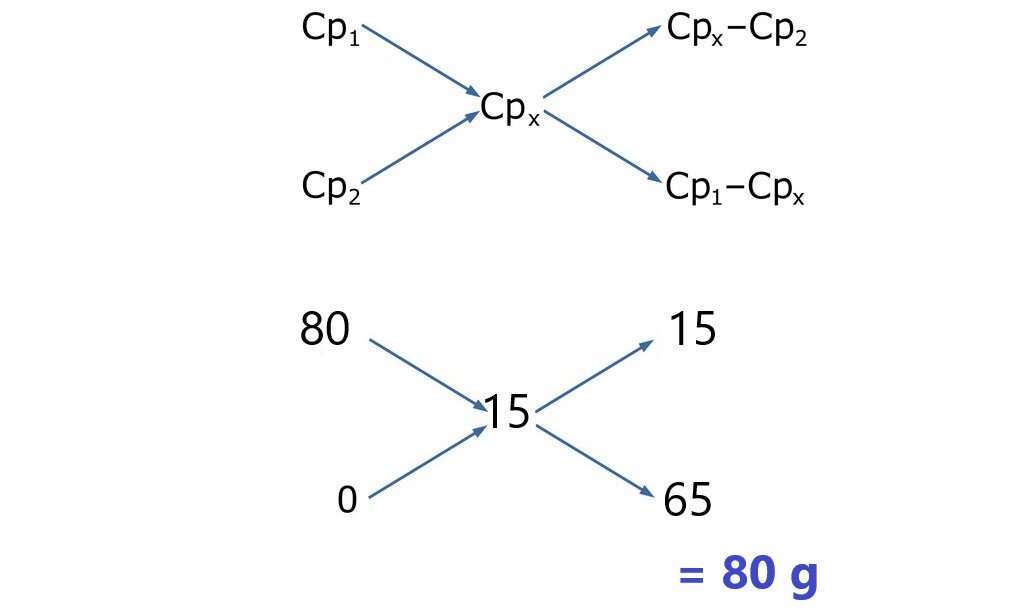
W jaki sposób przygotujesz (około ) roztworu o stężeniu , jeżeli w laboratorium znajduje się wyłącznie kwas octowy o stężeniu ? Na etykiecie butelki ze stężonym kwasem widnieją również, takie informacje jak: , .
Zapoznaj się z filmem edukacyjnym i spróbuj rozwiązać ten problem. W trakcie oglądania filmu zastanów się, dlaczego w życiu codziennym znajomość stężenia procentowego roztworu jest tak bardzo ważna. Następnie rozwiąż ćwiczenia sprawdzające.

Film dostępny pod adresem /preview/resource/R1Ou2wONlUdHr
Film nawiązujący do treści materiału dotyczącej sporządzania roztworów o określonym stężeniu procentowym.