Grafika interaktywna
Polecenie 1
Przeanalizuj cyklizacje glukozy z projekcji chemicznej Fischera we wzór w projekcji chemicznej Hawortha. Następnie wykonaj ćwiczenie 1.
Zapoznaj się z opisem cyklizacji glukozy w projekcji chemicznej Fischera we wzór w projekcji chemicznej Hawortha. Następnie wykonaj ćwiczenie 1.Przeanalizuj cyklizacje glukozy z projekcji chemicznej
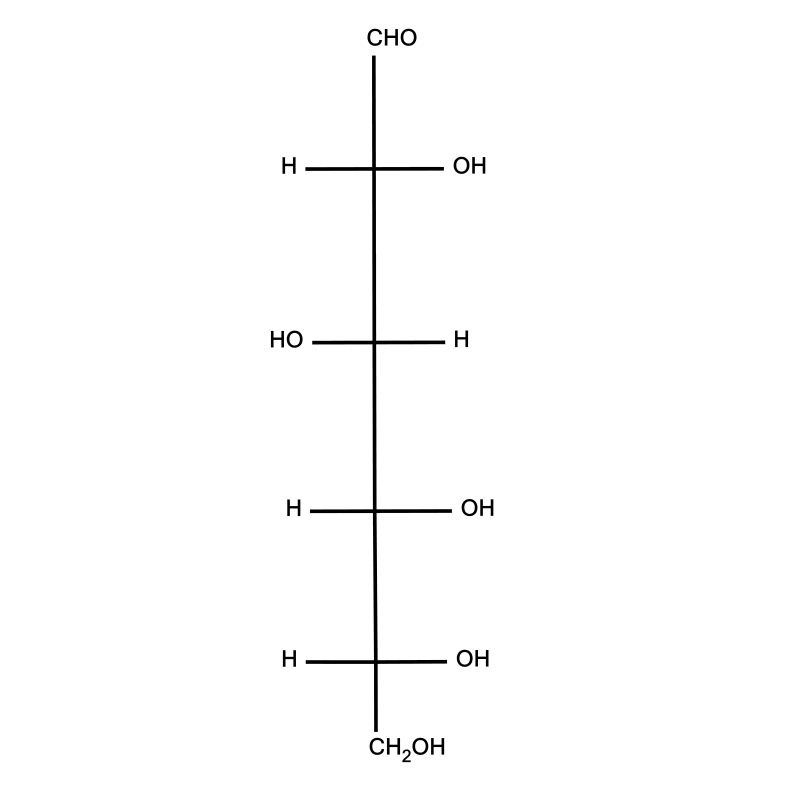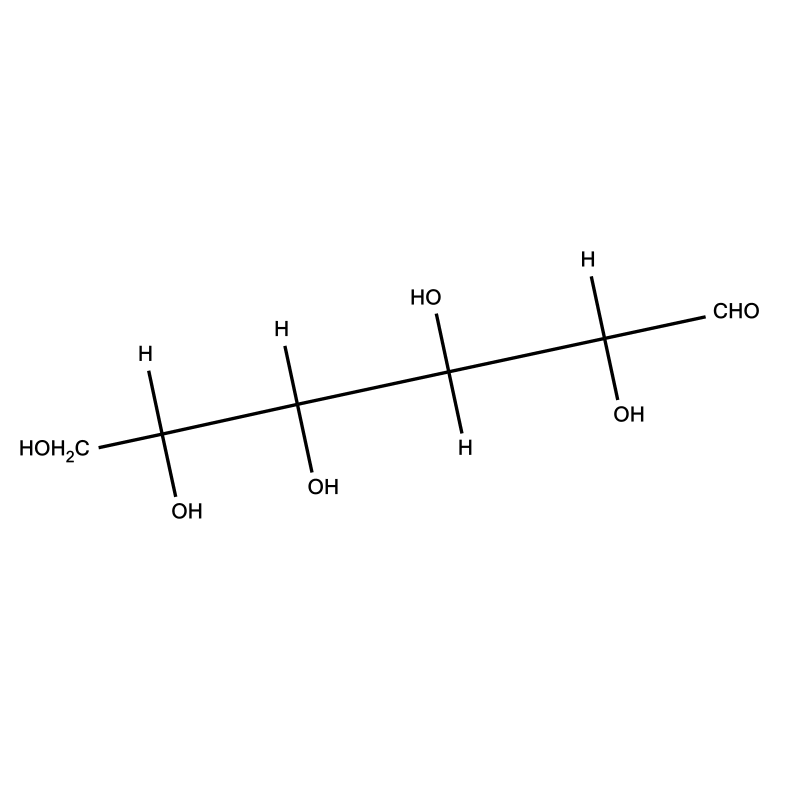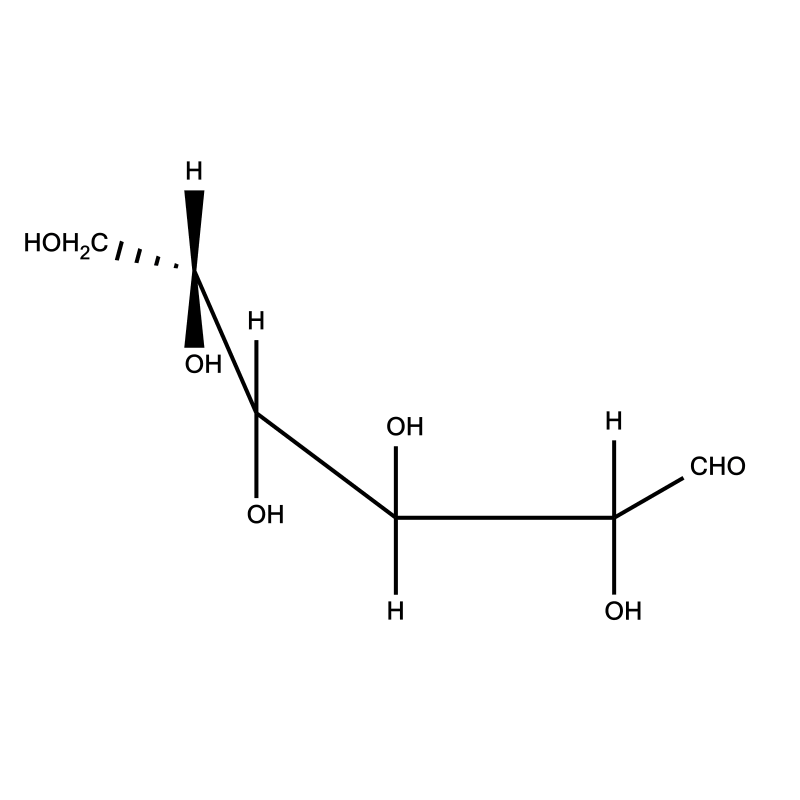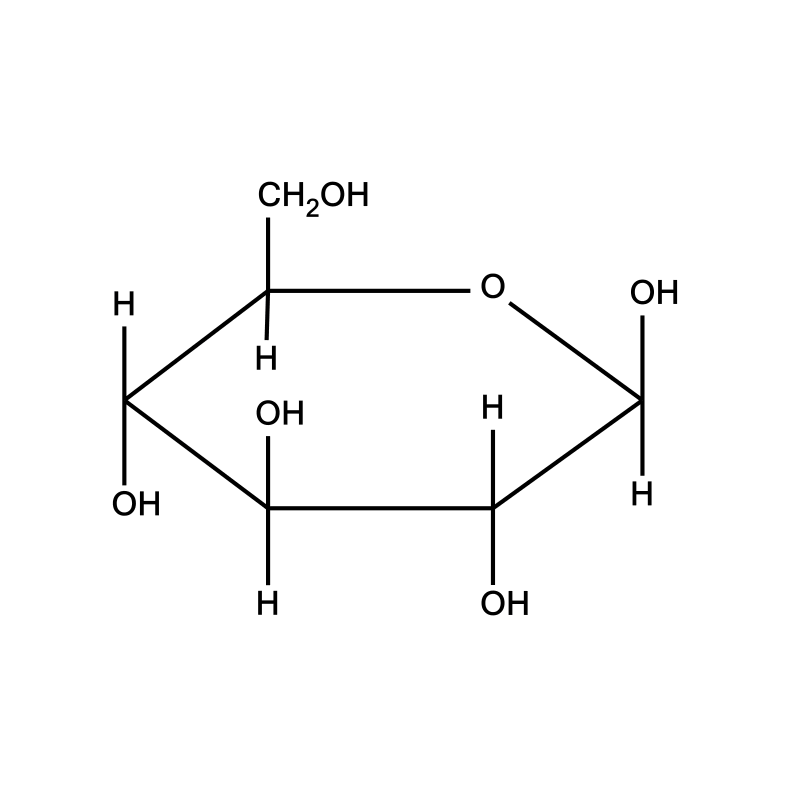
Cyklizacja glukozy
Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0.
Źródło: GroMar Sp. z o.o., J. McMurry, „Chemia organiczna”, Wydawnictwo naukowe PWN, Warszawa 2003., licencja: CC BY-SA 3.0.
Ćwiczenie 1
Wyjaśnij, jak powstaje sześcioczłonowy pierścień glukozy.
Polecenie 2
Ile form anomerycznych ma D‑fruktoza i w jakich formach występuje w roztworach wodnych? Zapoznaj się z grafiką, a następnie wykonaj ćwiczenia znajdujące się pod grafiką.
Ile form anomerycznych ma D‑fruktoza i w jakich formach występuje w roztworach wodnych? Zapoznaj się z opisem grafiki, a następnie wykonaj ćwiczenia znajdujące się pod grafiką.
Formy anomeryczne fruktozy
Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0.
Mutarotacja fruktozy.
Źródło: GroMar Sp. z o.o., Materiał opracowany na podstawie informacji znajdujących się pod adresem: http://www.e-biotechnologia.pl/Artykuly/cukry, licencja: CC BY-SA 3.0.
Ćwiczenie 2
Źródło: dostępny w internecie: commons.wikimedia.org, domena publiczna.
Ćwiczenie 3