Izomeria konstytucyjna i cis/trans w alkenach
Izomeria w alkenach
Izomeria to zjawisko, w którym związki chemiczne mają taki sam wzór sumaryczny, ale inną budowę cząsteczki. Takie związki nazywamy izomerami.
Rodzaje izomerii w węglowodorach:
1. Izomeria szkieletowa
Dotyczy budowy łańcucha węglowego. Atomy węgla mogą być ułożone w łańcuch prosty lub rozgałęziony.
Przykład: butan i izobutan mają ten sam wzór sumaryczny (C₄H₁₀), ale inną budowę.
Jak utworzyć wzory wszystkich możliwych izomerycznych alkenów, które zawierają pięć atomów węgla w cząsteczce?
Najpierw narysujmy wszystkie możliwe szkielety węglowe:
2. Izomeria położenia wiązania wielokrotnego
Występuje w alkenach i alkinach. Wiązanie podwójne (lub potrójne) może znajdować się w różnym miejscu łańcucha.
Przykład: but‑1-en i but‑2-en różnią się tylko pozycją wiązania podwójnego.
Jakie znasz izomery położenia wiązania podwójnego butenu? Sprawdź na poniższej grafice, jakie są możliwe położenia wiązania podwójnego w cząsteczce butenu.

Podaj nazwę systematyczną alkenu, który nie posiada w łańcuchu głównym wiązania podwójnego o wzorze sumarycznym .
Zaproponuj wzór półstrukturalny alkenu o pięciu atomach węgla, który w wyniku reakcji z utworzy trzeciorzędowy bromek alkilu.
3. Izomeria cis/trans i E/Z
Ta izomeria występuje w alkenach, czyli związkach z wiązaniem podwójnym między atomami węgla. Wiązanie podwójne blokuje obrót wokół osi, dlatego grupy przy tych atomach mogą się ustawić w różny sposób w przestrzeni — i właśnie stąd biorą się izomery geometryczne.
Jednym z rodzajów stereoizomerii jest tzw. diastereoizomeria. Diastereoizomery różnią się konfiguracją (w uproszczeniu – rozmieszczeniem atomów w przestrzeni) przy przynajmniej jednym i jednocześnie nie przy wszystkich atomach węgla w cząsteczkach.
Do diastereoizomerów zaliczamy m.in. izomery typu /, których szczególnym przypadkiem są izomery typu cis-trans.
Jednym z warunków występowania zjawiska izomerii typu E/Z (w tym również izomerii typu cis-trans) jest ograniczona rotacja atomów bądź grup atomów wokół wiązania węgiel‑węgiel w cząsteczce.
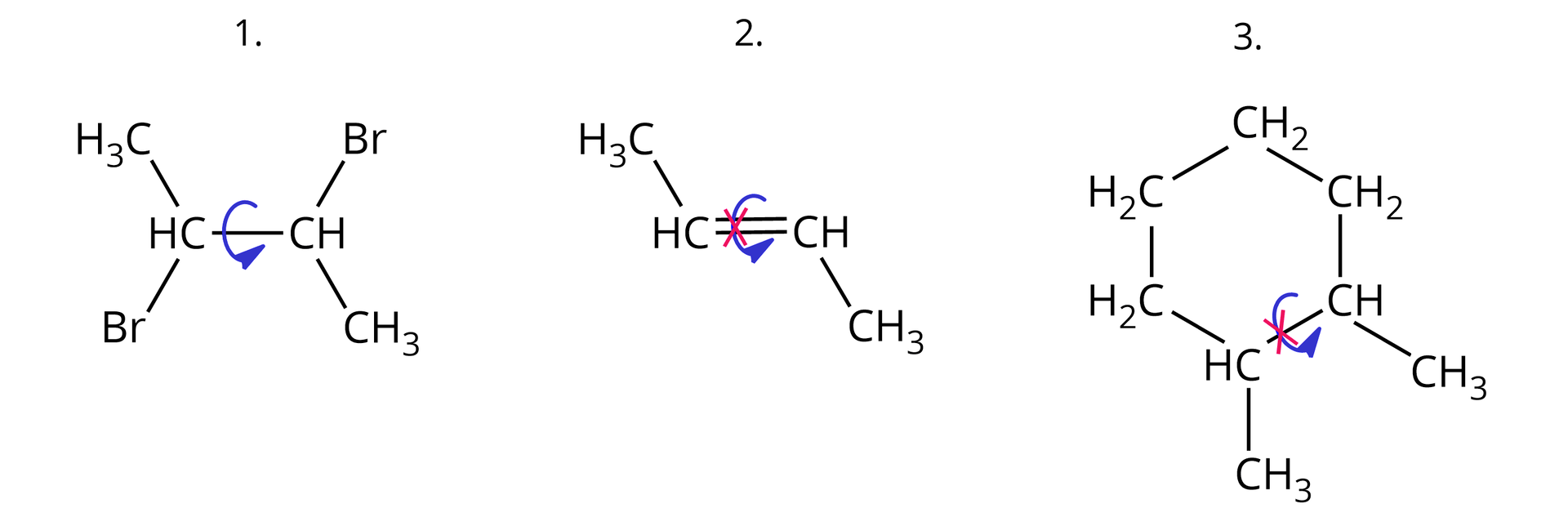
Z izomerią typu / mamy do czynienia wówczas, gdy rozpatrywane cząsteczki różnią się położeniem atomów lub grup atomów w stosunku do płaszczyzny odniesienia. W przypadku alkenów, płaszczyzną odniesienia jest płaszczyzna wiązania podwójnego.
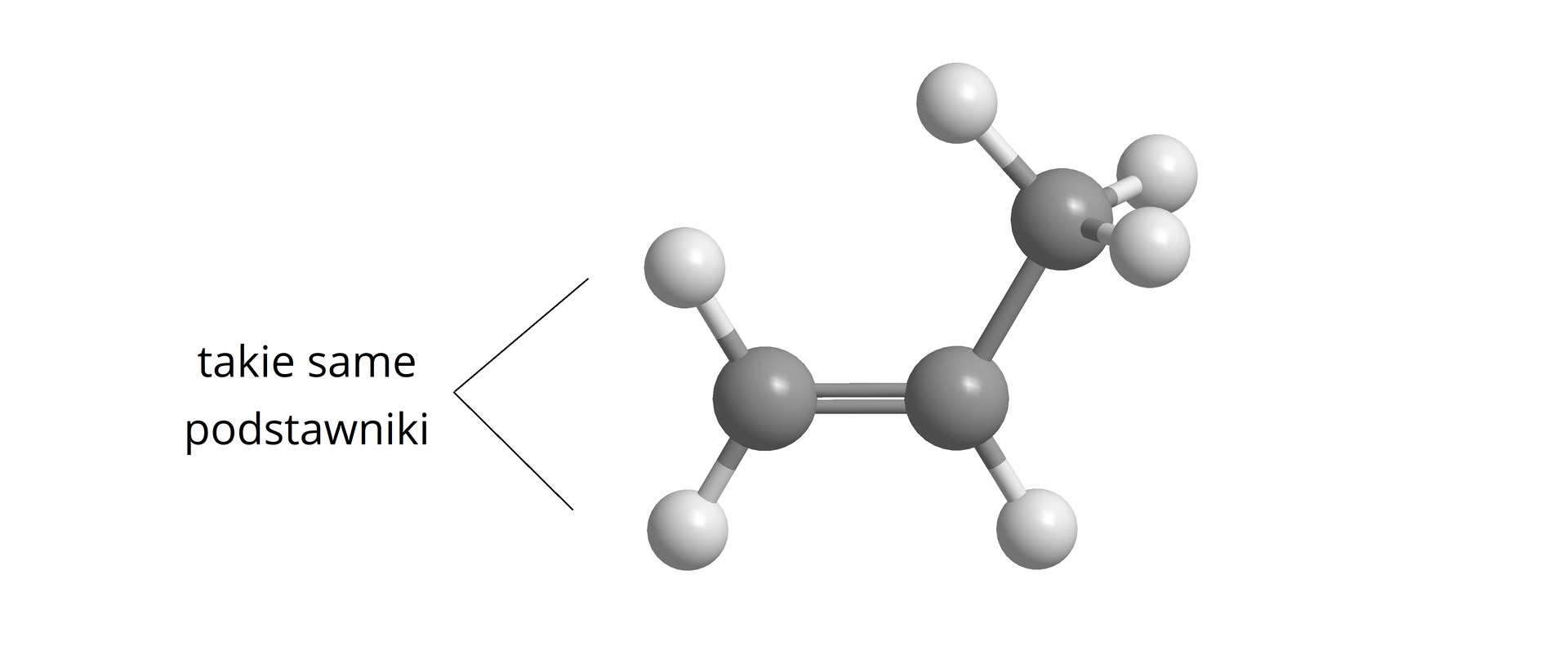
Jednak nie wszystkie alkeny, pomimo obecności wiązania podwójnego w cząsteczkach, mogą tworzyć izomery typu /. Kolejnym warunkiem do występowania izomerii typu / w alkenach jest bowiem obecność w ich cząsteczkach, przy atomach węgla połączonych wiązaniem podwójnym, podstawników parami nieidentycznych. Warunek ten zilustrowano na poniższej grafice.
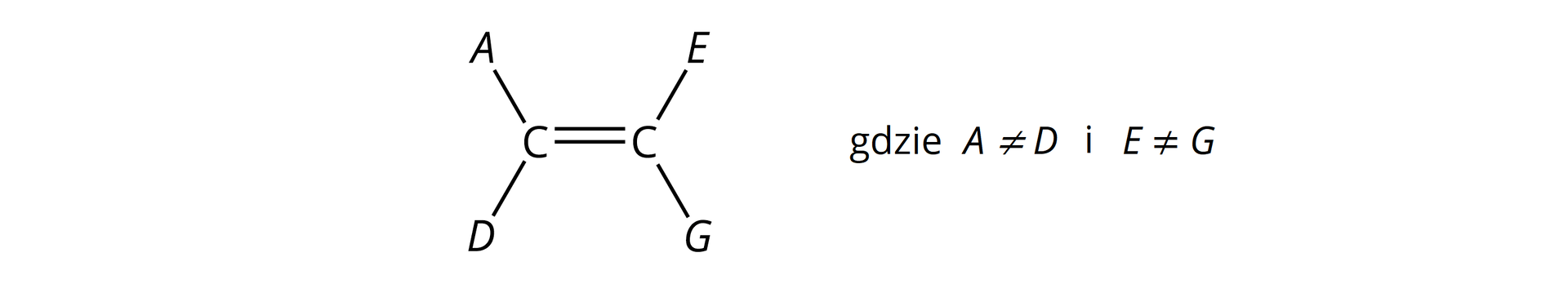
Zastanów się i odpowiedz na pytanie, czy propen może tworzyć izomery typu /. Odpowiedź krótko uzasadnij.
Jak już wspomniano, izomeria typu cis-trans jest szczególnym przypadkiem izomerii typu /. Z izomerami typu cis-trans, w przypadku alkenów, mamy do czynienia wówczas, gdy przy każdym z atomów węgla, połączonych wiązaniem podwójnym, znajduje się jeden atom wodoru i podstawnik identyczny dla obydwu atomów węgla.

Rozpatrując izomerię typu / i cis-trans dla alkenów, często posługujemy się sformułowaniami, takimi jak: alken jednopodstawiony, dwupodstawiony, trójpodstawiony lub czteropodstawiony. Z alkenem czteropodstawionym mamy do czynienia wówczas, gdy w jego cząsteczce, do atomów węgla połączonych wiązaniem podwójnym, nie jest przyłączony żaden atom wodoru. W przypadku cząsteczki alkenu trójpodstawionego, do atomów węgla, uczestniczących w tworzeniu wiązania podwójnego, przyłączone są trzy podstawniki inne niż atom wodoru, w cząsteczce alkenu dwupodstawionego – do wspomnianych atomów węgla przyłączone są dwa podstawniki inne niż atomy wodoru, a w cząsteczce alkenu jednopodstawowego – jeden podstawnik inny niż atom wodoru.
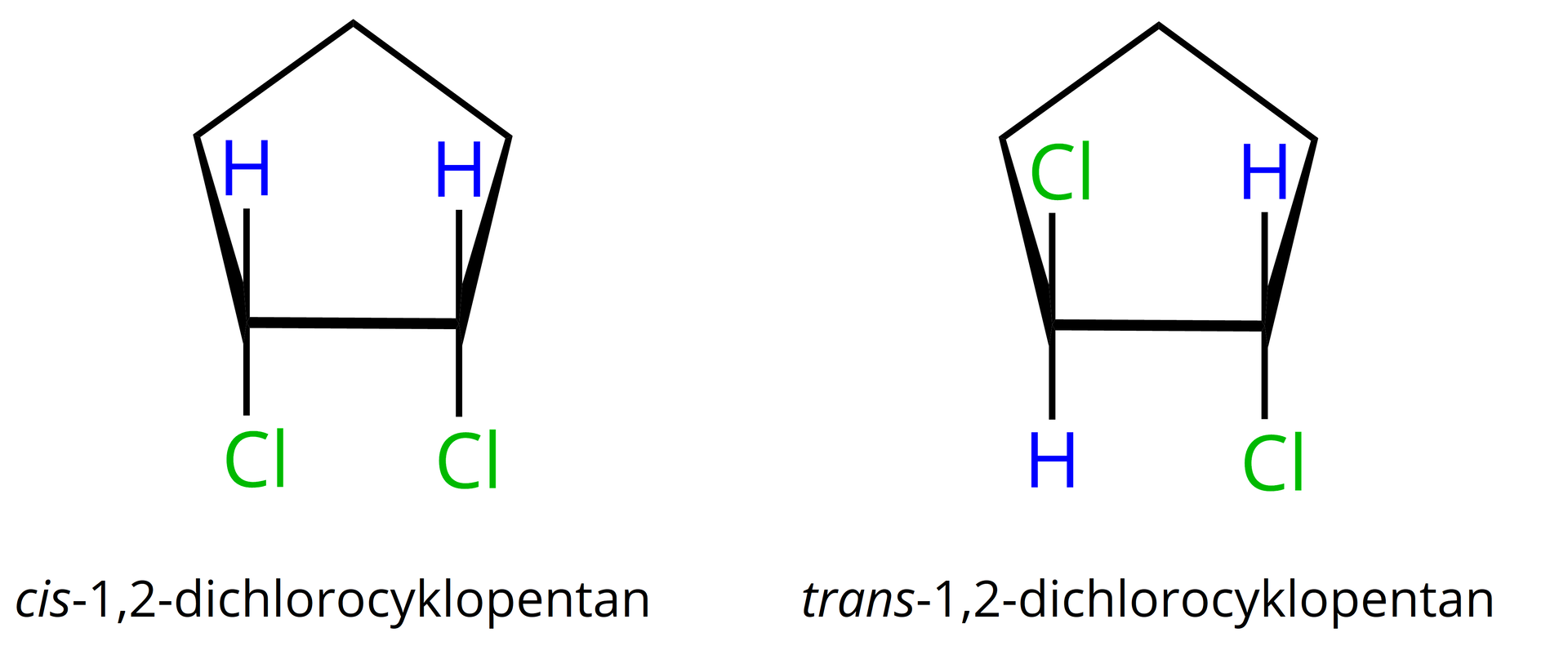
Zjawisko diastereoizomerii cis-trans dotyczy nie tylko alkenów, ale również cykloalkanów, w których cząsteczkach rotacja wokół pojedynczych wiązań węgiel‑węgiel w pierścieniu jest utrudniona. Dany cykloalkan (lub jego pochodna) może występować w postaci izomerów cis-trans wówczas, gdy w jego cząsteczce, do sąsiednich atomów węgla w pierścieniu, przyłączone są po dwa parami nieidentyczne podstawniki, przy czym jednym z nich w każdym przypadku jest atom wodoru.
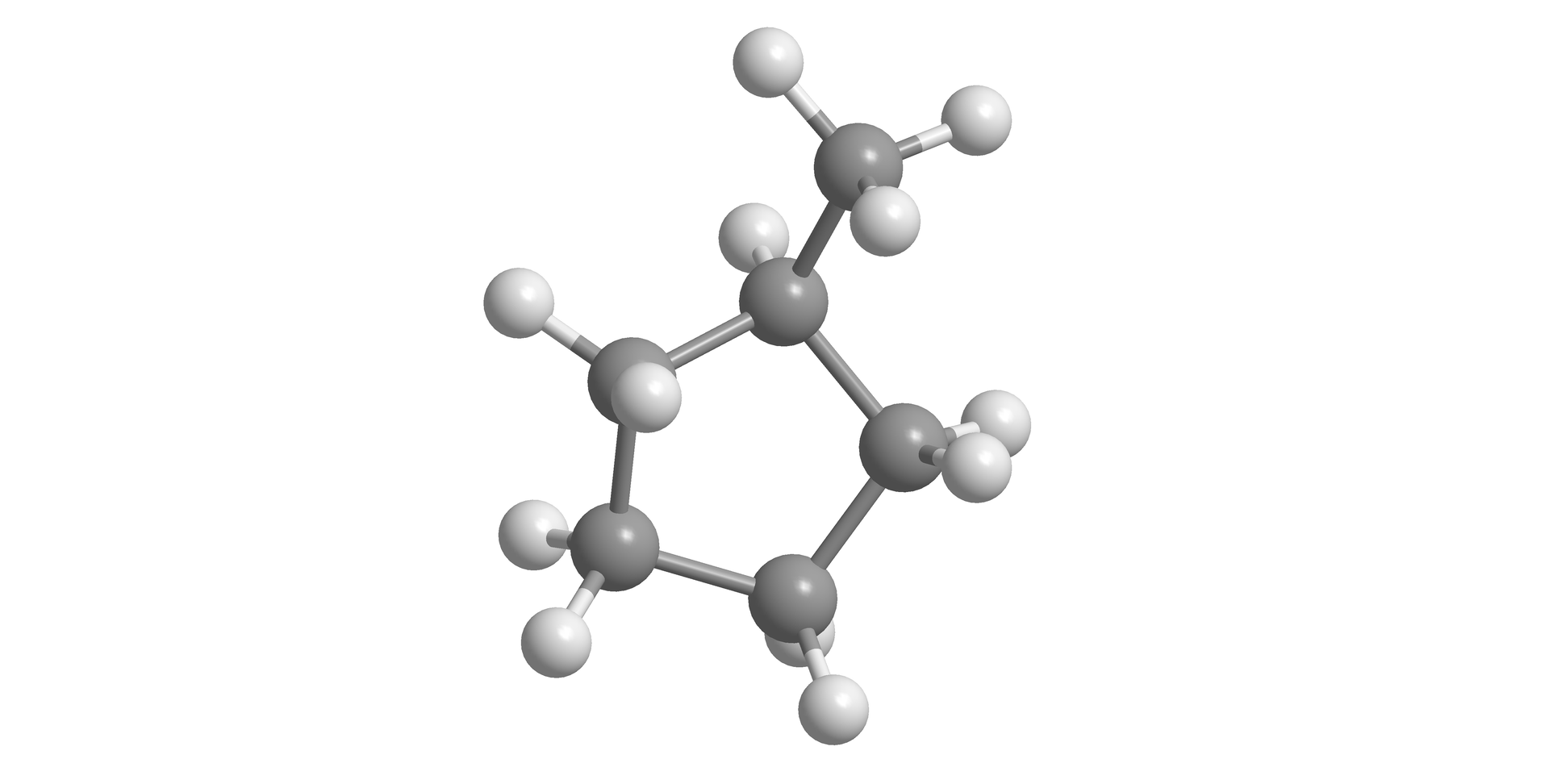
Zastanów się i odpowiedz na pytanie, czy metylocyklopentan może tworzyć izomery typu cis-trans. Odpowiedź krótko uzasadnij.
Reguły pierwszeństwa podstawników
Atom o większej liczbie atomowej jest ważniejszy niż atom o mniejszej liczbie atomowej, np. .
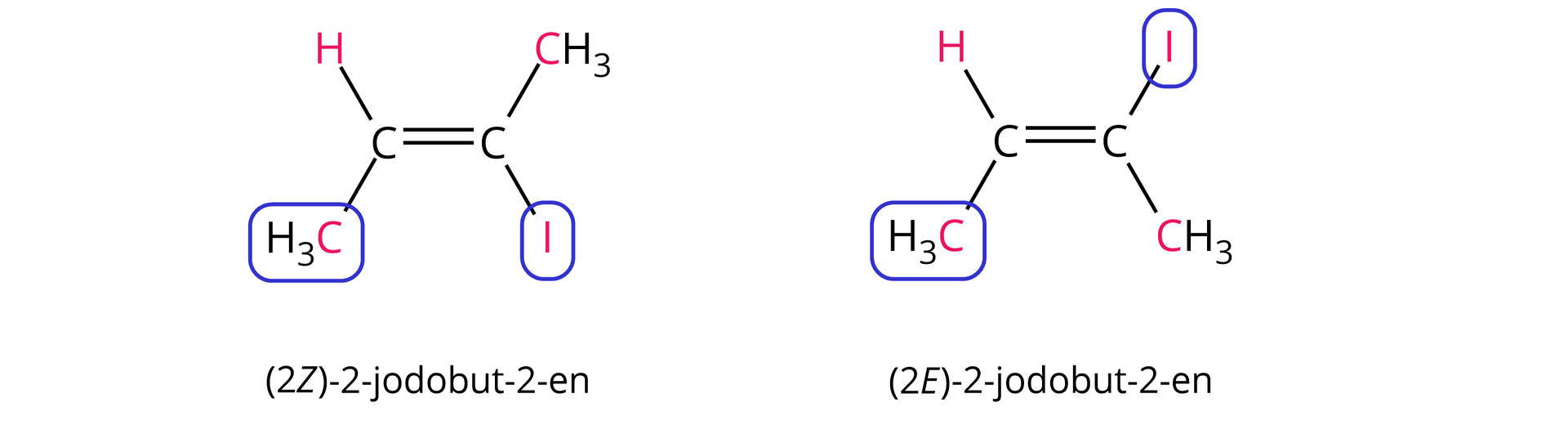
Zwróć uwagę, że podając nazwę odpowiedniego izomeru typu /, przed nazwą związku umieszczamy zapisany w nawiasie deskryptor stereochemiczny ( lub ) z odpowiadającym mu lokantem (numerem atomu węgla, którego deskryptor ten dotyczy).
2. W przypadku gdy atomy bezpośrednio przyłączone do atomów węgla połączonych wiązaniem podwójnym nie różnią się liczbą atomową, należy porównać liczby atomowe kolejnych atomów (aż do rozstrzygnięcia).
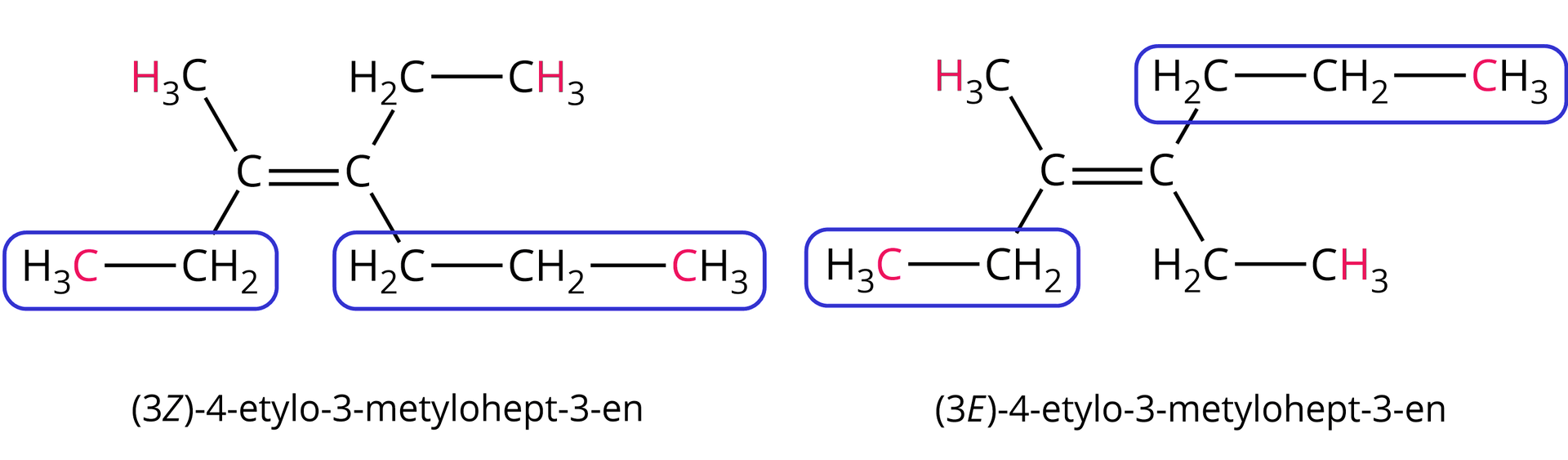
3. W przypadku gdy atomy podstawnika połączone są wiązaniem wielokrotnym, należy rozpisać je na odpowiednią liczbę wiązań pojedynczych.
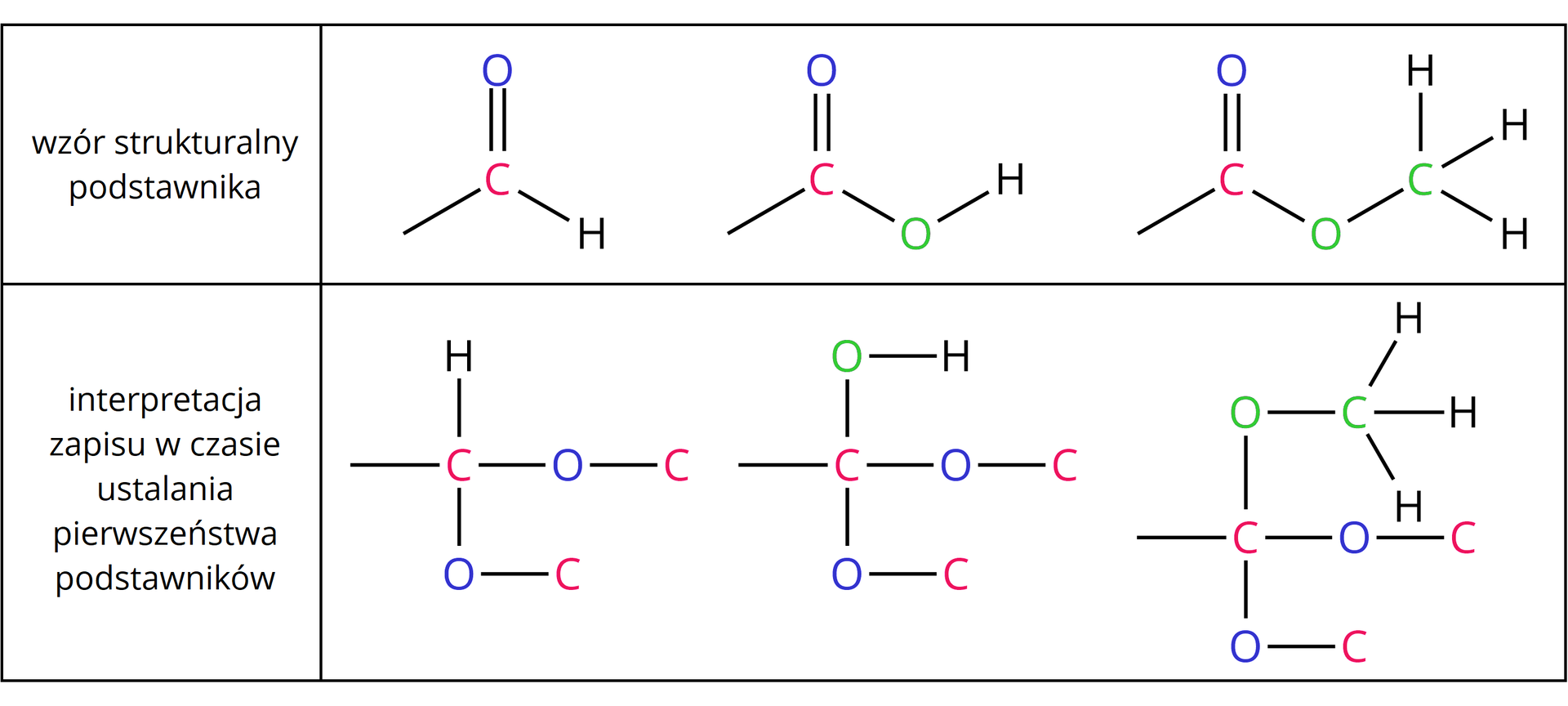
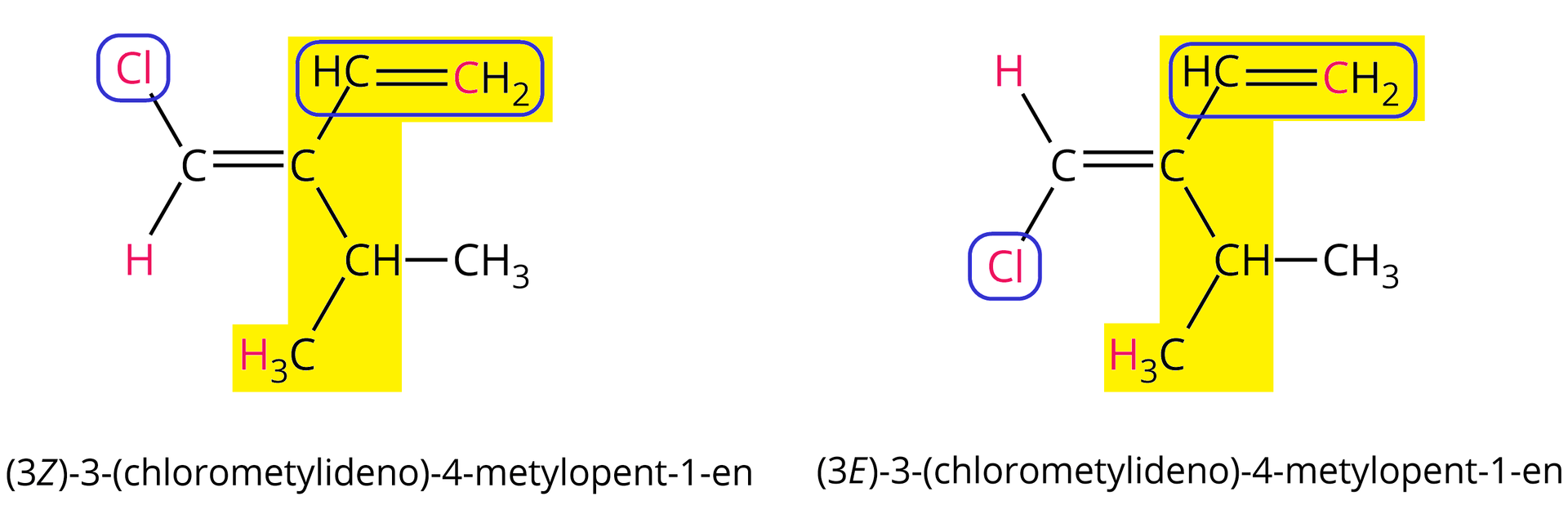
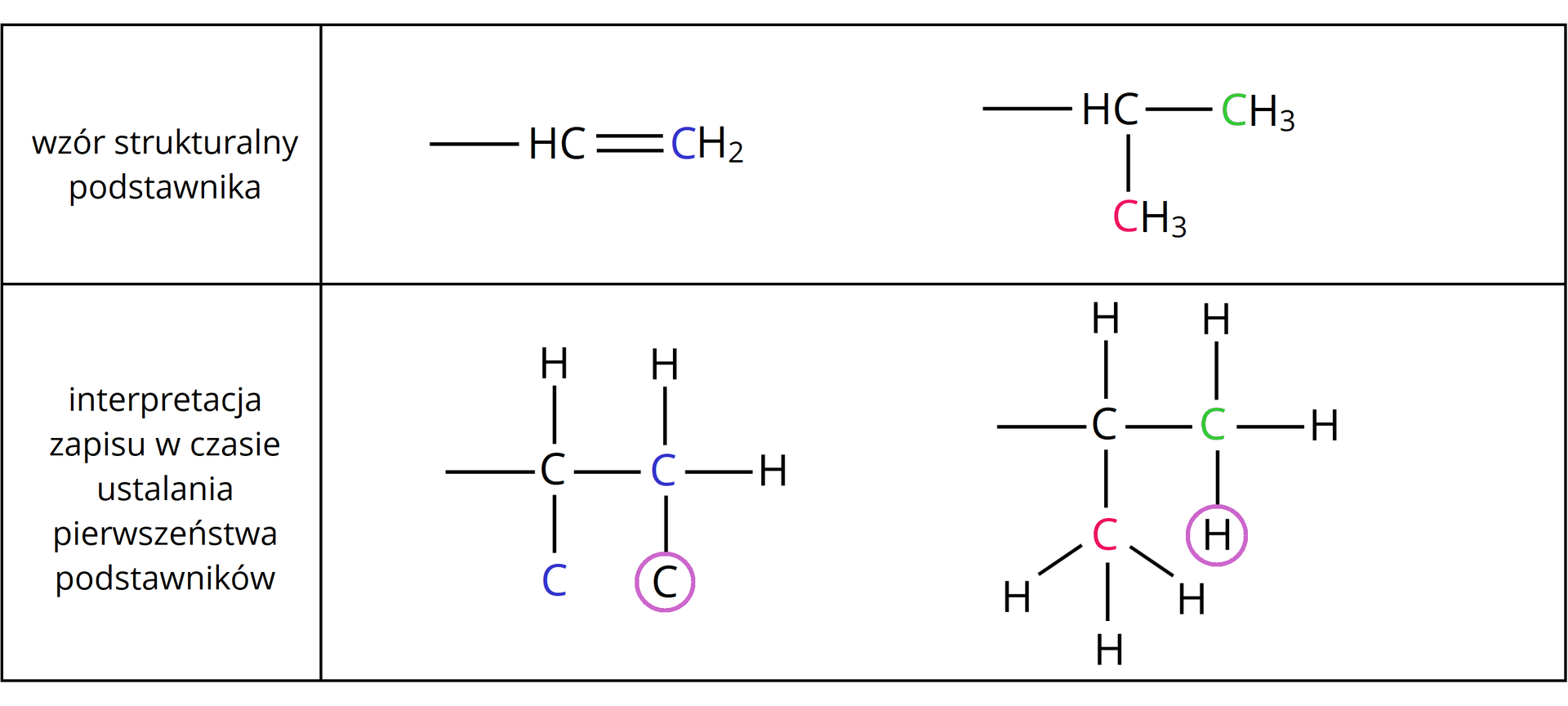
Stosując reguły pierwszeństwa podstawników, należy rozpisać atomy w rozpatrywanych powyżej wzorach podstawników w następujący sposób:
Pamiętaj, że formalnie każdy izomer typu cis jest jest jednocześnie izomerem typu , a każdy izomer typu trans – izomerem typu . Relacja ta nie jest jednak spełniona w drugą stronę – nie każdy izomer typu jest jednocześnie izomerem typu cis i nie każdy izomer typu jest izomerem typu trans.
Zapoznaj się z poniższym filmem dotyczącym izomerii geometrycznej w cząsteczkach alkenów, a następnie rozwiąż zadania.
Film dostępny pod adresem /preview/resource/R1PI8xqZ1IO38
Film nawiązujący do treści materiału dotyczącej izomerii geometrycznej w cząsteczkach alkenów.
Nazwij poniższe związki, uwzględniając izomerię geometryczną.
Nazwij opisane związki, uwzględniając izomerię geometryczną.

Narysuj wzory półstrukturalne związków odpowiadających podanym nazwom.
a) cis-3‑metyloheks‑3-en
b) trans-1,6‑dijodoheks‑3-en
c) cis-4,4,-dimetylopent‑2-en