Przeczytaj
Estry kwasów organicznych
EstryEstry pochodzące od kwasów organicznych to związki chemiczne, które posiadają następujący wzór ogólny:
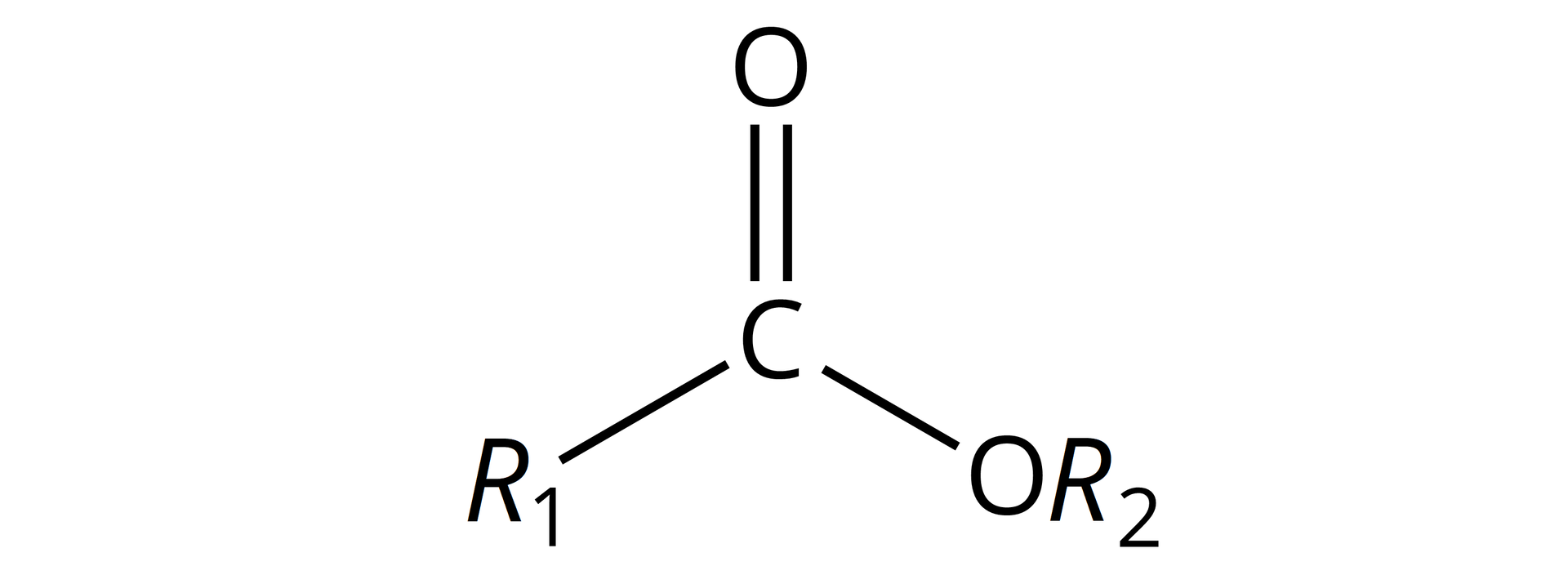
W związkach chemicznych, zaliczanych do estrów pochodzących od kwasów organicznych, występuje grupa funkcyjnagrupa funkcyjna zwana grupą estrowągrupą estrową .

Najprostszym przykładem estru jest mrówczan metylu lub systematycznie – metanian metylu.
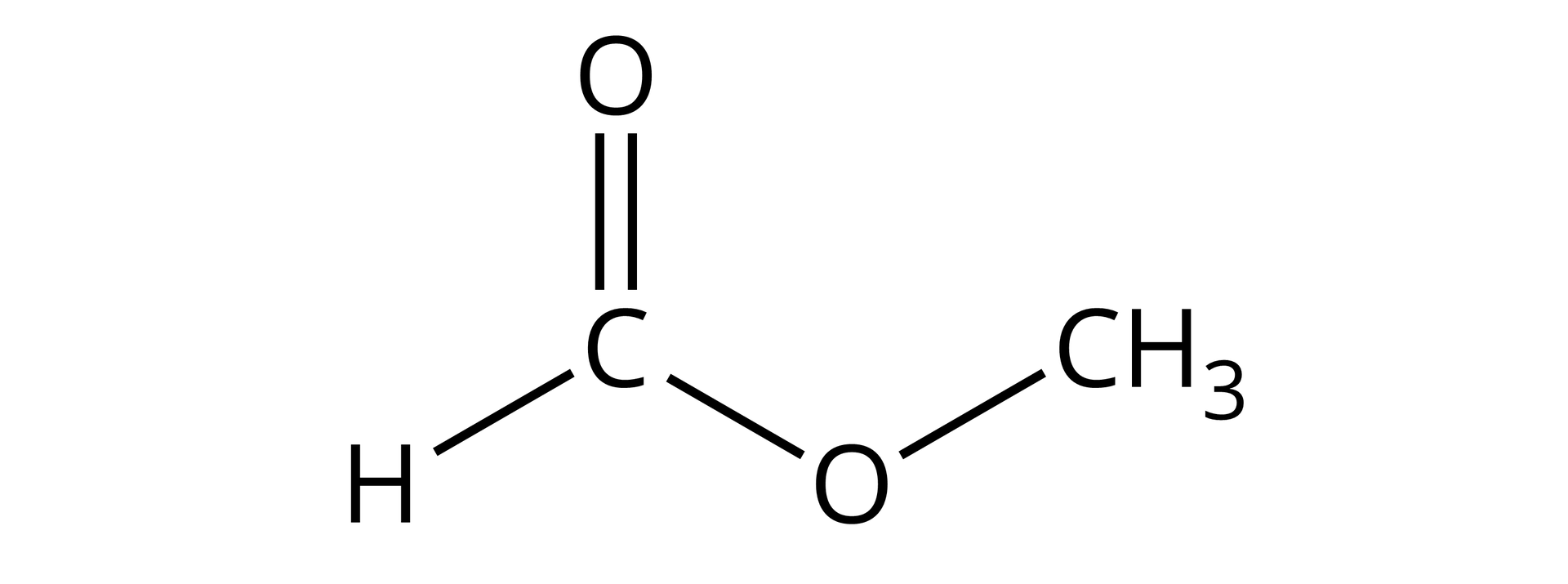
Estry kwasów nieorganicznych
Estry pochodzące od kwasów nieorganicznych powstają w reakcji alkoholi z kwasami nieorganicznymi – takimi jak kwas borowy, który daje estry boranowe, kwas siarkowy(), dzięki któremu otrzymujemy estry siarczanowe, kwas fosforowy(), dający estry fosforanowe, czy też kwas azotowy(), zapewniający estry azotanowe.

Przykłady reakcji estryfikacji
Estry to związki chemiczne, które powstają w reakcji chemicznej estryfikacjiestryfikacji. Może ona przebiegać na kilka sposobów.
Mechanizm estryfikacji Fischera
W celu ustalenia mechanizmu estryfikacji, należy wiedzieć, który atom tlenu (pochodzący z kwasu czy alkoholualkoholu lub fenolufenolu) pozostaje w estrze, a który ulega odczepieniu w postaci cząsteczki tlenku wodoru (wody).
Estryfikacja metodą Fischera polega na substytucjisubstytucji grupy
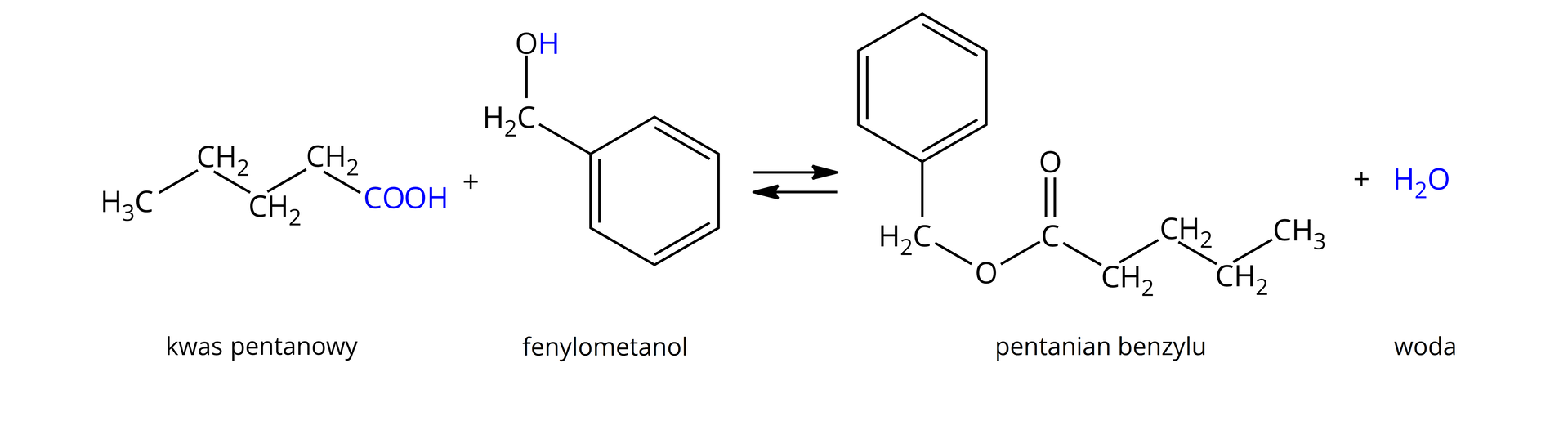
Bardziej szczegółowy mechanizm reakcji estryfikacji został przedstawiony poniżej:
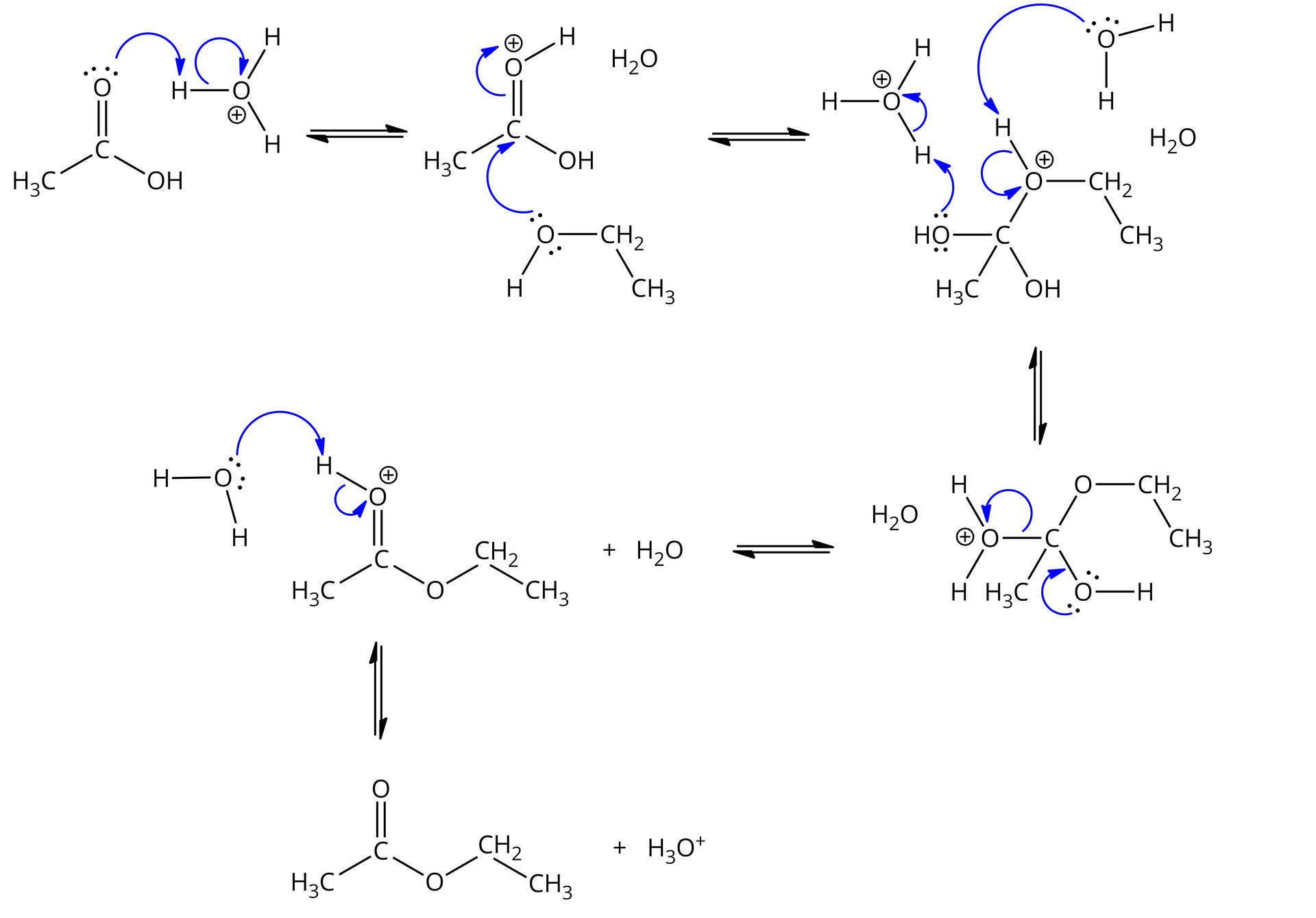
Synteza poprzez acylowanie alkoholi lub fenoli bezwodnikami kwasowymi
Tego typu reakcja acylowania przebiega z udziałem katalitycznych ilości zasad, takich jak NaOH czy pirydyna. Jest to metoda otrzymywania estrów trudnych do otrzymania metodą Fischera (np. fenylowych). W wyniku reakcji otrzymujemy ester oraz sól kwasu karboksylowego, np. octan sodu.
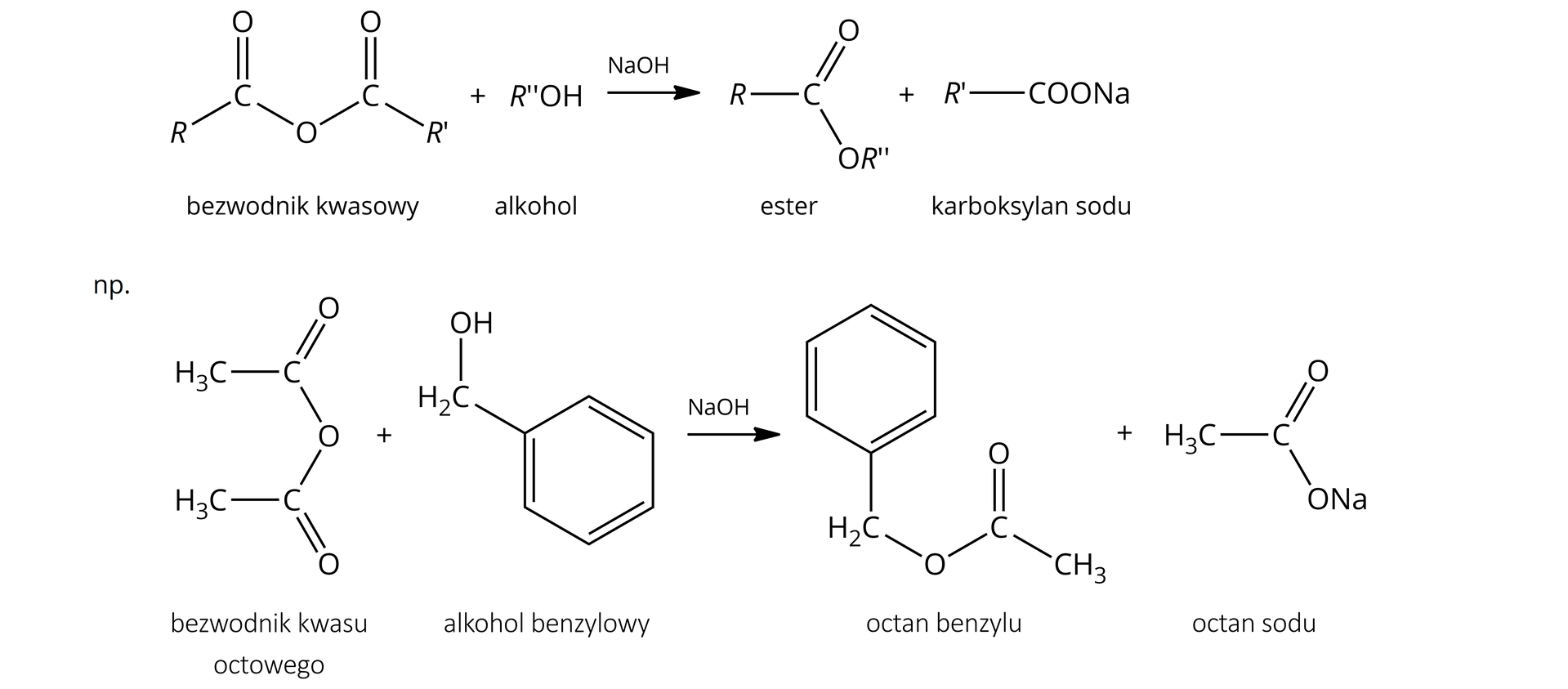
Synteza poprzez acylowanie alkoholi lub fenoli chlorkami kwasowymi
Podobnie do reakcji wykorzystującej bezwodniki kwasowe, reakcja z chlorkami kwasowymichlorkami kwasowymi wymaga zastosowania katalitycznych ilości zasady, jak NaOH lub pirydyna. Jako produkt uboczny takiej reakcji, w zależności od rodzaju zastosowanej zasady, powstają sole – np. chlorek sodu lub chlorek pirydynium.

Estryfikacja wybranych kwasów nieorganicznych (tlenowych)
Estryfikacja kwasu azotowego(
V
Estryfikacja kwasu siarkowego(
VI
Estryfikacja kwasu fosforowego(
V
Reakcja transestryfikacji estrów – alkoholiza i acydoliza
Alkoholiza
Alkoholiza to reakcja, w której jeden alkohol wypiera drugi z estru, podstawiając się tym samym na jego miejsce. W wyniku takiej reakcji otrzymujemy nowy ester oraz alkohol. Bardzo popularną reakcją tego typu jest transestryfikacja triacylogliceroli.

Acydoliza
To reakcja, w której jeden kwas wypiera drugi z estru, podstawiając się tym samym na jego miejsce. W wyniku takiej reakcji otrzymujemy nowy ester oraz kwas.

Słownik
(niem. essigäther „octan etylu” essig „ocet” i Äther „eter”) związek organiczny, powstający w wyniku działania kwasów na alkohole lub fenole
atom lub grupa atomów, która powoduje pojawienie się charakterystycznych cech w danym związku chemicznym
grupa funkcyjna
(gr. katálysis „rozłożenie”) zjawisko polegające na tym, że obecność stosunkowo niewielkiej ilości obcej substancji, zwanej katalizatorem, przyspiesza reakcję chemiczną
substancja, która zwiększa szybkość reakcji chemicznej, nie naruszając stanu końcowej równowagi i właściwości termodynamicznych układu, i pozostaje w stanie niezmienionym po zakończeniu reakcji
(arab. al‑kuhl „delikatny proszek”) związki organiczne, pochodne węglowodorów, których cząsteczki zawierają grupę hydroksylową (wodorotlenową)
związki organiczne, mono-, di- i polihydroksylowe, pochodne benzenu oraz alkilobenzenów, których cząsteczki zawierają grupy hydroksylowe (
związki organiczne, których cząsteczki zawierają grupę karboksylową (
związki chemiczne odznaczające się charakterystycznymi właściwościami, m.in. kwaśnym smakiem, zdolnością wywoływania reakcji barwnych ze wskaźnikami (np. barwią lakmus na czerwono), roztwarzaniem wielu substancji, np. kwas
fosforowy(
związki chemiczne będące pochodnymi kwasów karboksylowych, w których grupa
reakcja chemiczna między alkoholem (lub fenolem) i kwasem, w wyniku której powstaje ester i woda
przeestryfikowanie; reakcja chemiczna prowadząca do otrzymania estrów m.in. przez reakcję estrów z alkoholami (alkoholiza)
związki nieorganiczne, tlenki pierwiastków niemetalicznych dające w reakcji z wodą odpowiednie kwasy
suma wykładników potęg, w których występują stężenia reagentów w równaniu kinetycznym opisującym szybkość reakcji chemicznej
(łac. substitutio „podstawianie”) reakcja podstawiania, podstawienie, chem. reakcja chem., w której atom lub grupa atomów w cząsteczce związku org. zostaje podstawiona innym atomem lub grupą atomów
atom bogaty w elektrony (mający nadmiar elektronów), dzięki czemu może utworzyć wiązanie poprzez dostarczenie pary elektronowej atomowi ubogiemu w elektrony (mającemu niedomiar elektronów)
Bibliografia
Dudek‑Różycki K., Płotek M., Wichur T., Węglowodory. Repetytorium i zadania, Kraków 2020.
Dudek‑Różycki K., Płotek M., Wichur T., Związki organiczne zawierające azot oraz wielofunkcyjne pochodne węglowodorów. Repetytorium i zadania, Kraków 2021.
Dudek‑Różycki K., Płotek M., Wichur T., Kompendium terminologii oraz nazewnictwa związków organicznych. Poradnik dla nauczycieli i uczniów, Kraków 2020.
Mastalerz P., Podręcznik chemii organicznej, Wrocław 1998.
McMurry J., Chemia organiczna, tom 1 i 2, Warszawa 2000.
Morrison R. T., Boyd R. N., Chemia organiczna, tom 1 i 2, Warszawa 1997.
Oleksik. J.,Krasodomski. W., Zastosowanie cieczy jonowych i katalizatorów stałych w syntezie biokomponentów paliwowych, „Nafta‑Gaz” 2015, 4, s. 256–265.