Przeczytaj
Fluor w stanie wolnym jest żółtozielonym gazem i występuje w postaci dwuatomowej cząsteczki . Ten niemetal, ze względu na swoją dużą reaktywność, nie występuje w środowisku naturalnym w stanie wolnym. Jest pierwiastkiem należącym do grupy fluorowców, zlokalizowanych w 17. grupie układu okresowego. Cechuje go największa elektroujemnośćelektroujemność spośród wszystkich znanych pierwiastków. Naturalnie występuje w postaci jednego, stabilnego izotopuizotopu , w takich minerałach jak:
fluoryt :
R1OYoHugLNyGF  Kryształ fluorytuŹródło: CarlesMillan, dostępny w internecie: commons.wikimedia.org, licencja: CC BY-SA 3.0.
Kryształ fluorytuŹródło: CarlesMillan, dostępny w internecie: commons.wikimedia.org, licencja: CC BY-SA 3.0.
kriolit :
R1JIF38Ealr0X  Kryształ kriolituŹródło: Didier Descouens, dostępny w internecie: commons.wikimedia.org, licencja: CC BY-SA 3.0.
Kryształ kriolituŹródło: Didier Descouens, dostępny w internecie: commons.wikimedia.org, licencja: CC BY-SA 3.0.
Znaczenie biologiczne fluoru
Fluor występuje w wodzie pitnej w postaci jonów fluorkowych (). Według listy naturalnych składników, obecnych w wodach mineralnych, opublikowanej w 2003 r. przez Komisję Europejską, maks. zawartość fluoru wynosi 5 . W Polsce stężenie fluoru w wodzie przeznaczonej do spożycia i celów gospodarczych nie może przekraczać 1,5. Źródłem tego pierwiastka w pokarmach i napojach są herbata czy ryby. Fluorki charakteryzują się dużą przyswajalnością – między 80% a 90%. Pełnią istotną rolę we wchłanianiu wapnia do kości, powodując tym samym tworzenie nowej tkanki kostnej, tak ważnej podczas leczenia złamań.
Średnia zawartość fluoru w organizmie człowieka wacha się w zależności od wieku. Zostało przyjęte, że optymalna ilość fluorków to 0,05 mg na 1 kg masy ciała. Jednak nadmierne spożycie fluoru wraz z wodą pitną może powodować fluorozę – chorobę, która objawia się białymi plamami na zębach, ale także pogrubieniem warstwy korowej kości i zwiększeniem gęstości istoty gąbczastej. Plamy występujące na szkliwie spowodowane są demineralizacją szkliwa, co wpływa na zwiększenie jego kruchości i twardości.
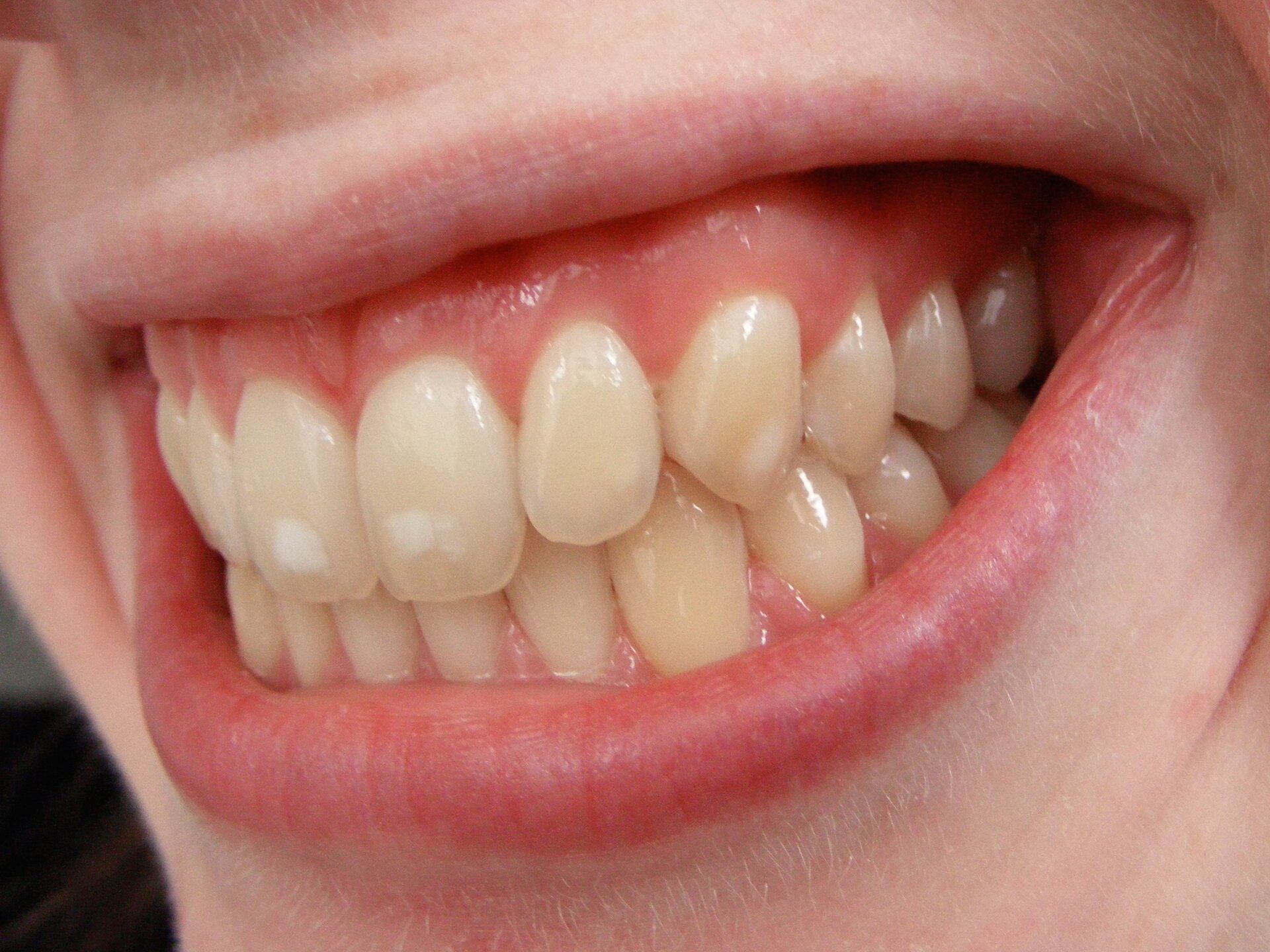
Jednym z dodatków umieszczanych w paście do zębów, zawierających jony fluorkowe, jest monofluorofosforan sodu, który zapobiega próchnicy.
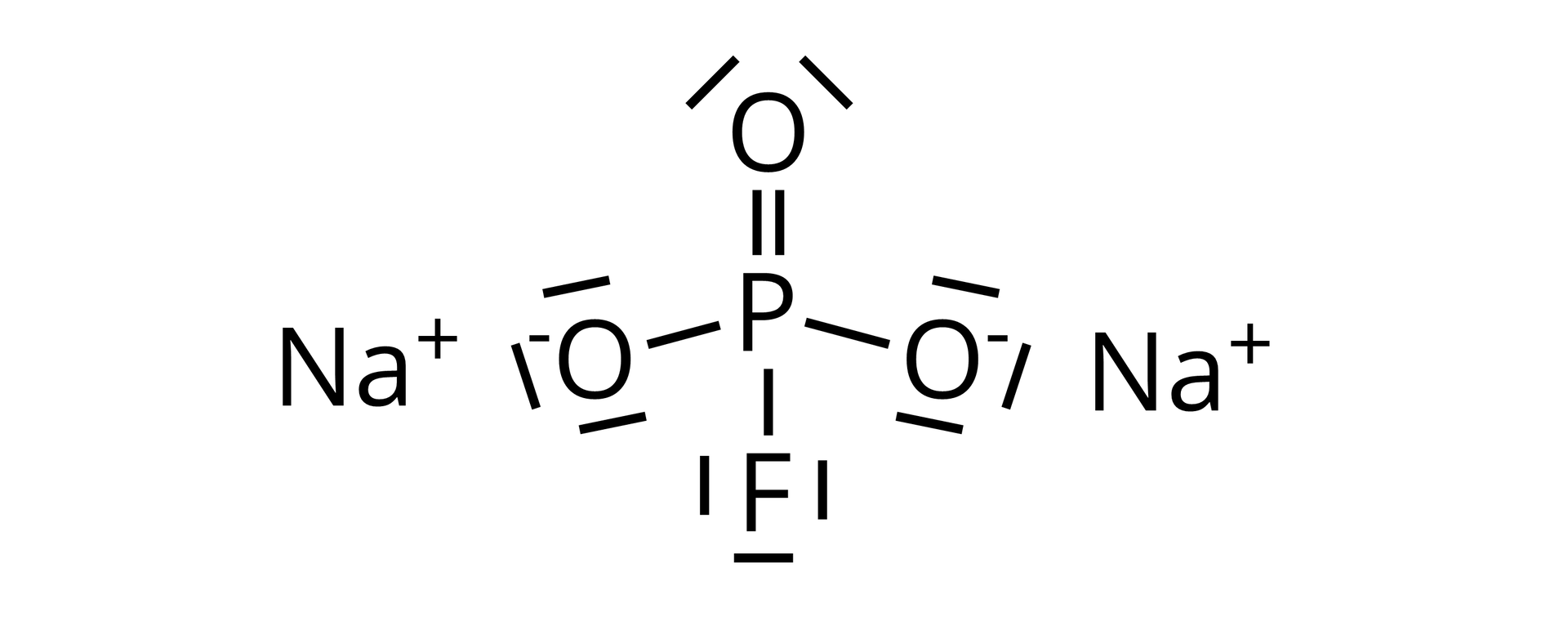
Zazwyczaj na opakowaniu pasty jest podane stężenie fluoru, np. 1450 ppm . Co to właściwie jest ppmppm? Inaczej sposób zapisu, który oznacza stosunek danej liczby do
1 000 000. Liczby te muszą być wyrażone w tych samych jednostkach (z ang. ppm to part per milion). Dla pasty do zębów wartość 1450 ppm oznacza tyle, że: w 1 000 000 g pasty znajduje się 1450 g jonów fluorkowych albo w 1 000 000 mg pasty do zębów znajduje się 1450 mg jonów fluorkowych. Dzięki umiejętności odczytu ppm możemy policzyć, że w 100 g pasty znajduje się 145 mg jonów fluorkowych.
Pasta do zębów zawiera średnio 1450 ppmppm jonów fluorkowych. Do mycia zębów średnio używamy 0,3 g. Oblicz masę jonów fluorkowych w 0,3 g pasty do zębów.
Fluor obecny jest także w medycynie, m.in. w środkach anestetycznychśrodkach anestetycznych stosowanych podczas operacji do znieczulenia ogólnego. W medycynie znajduje zastosowanie promieniotwórczy izotop fluoru . Powstaje on w wyniku bombardowania izotopu tlenu protonami. Powstały w tej reakcji fluor rozpada się z emisją pozytonu (promieniowania betaIndeks górny ++) z powrotem do izotopu tlenu .
Związki, które zawierają izotop fluoru , są stosowane w diagnostyce medycznej. Jednym z nich jest 2‑deoksy‑2-fluoro‑D-glukoza.
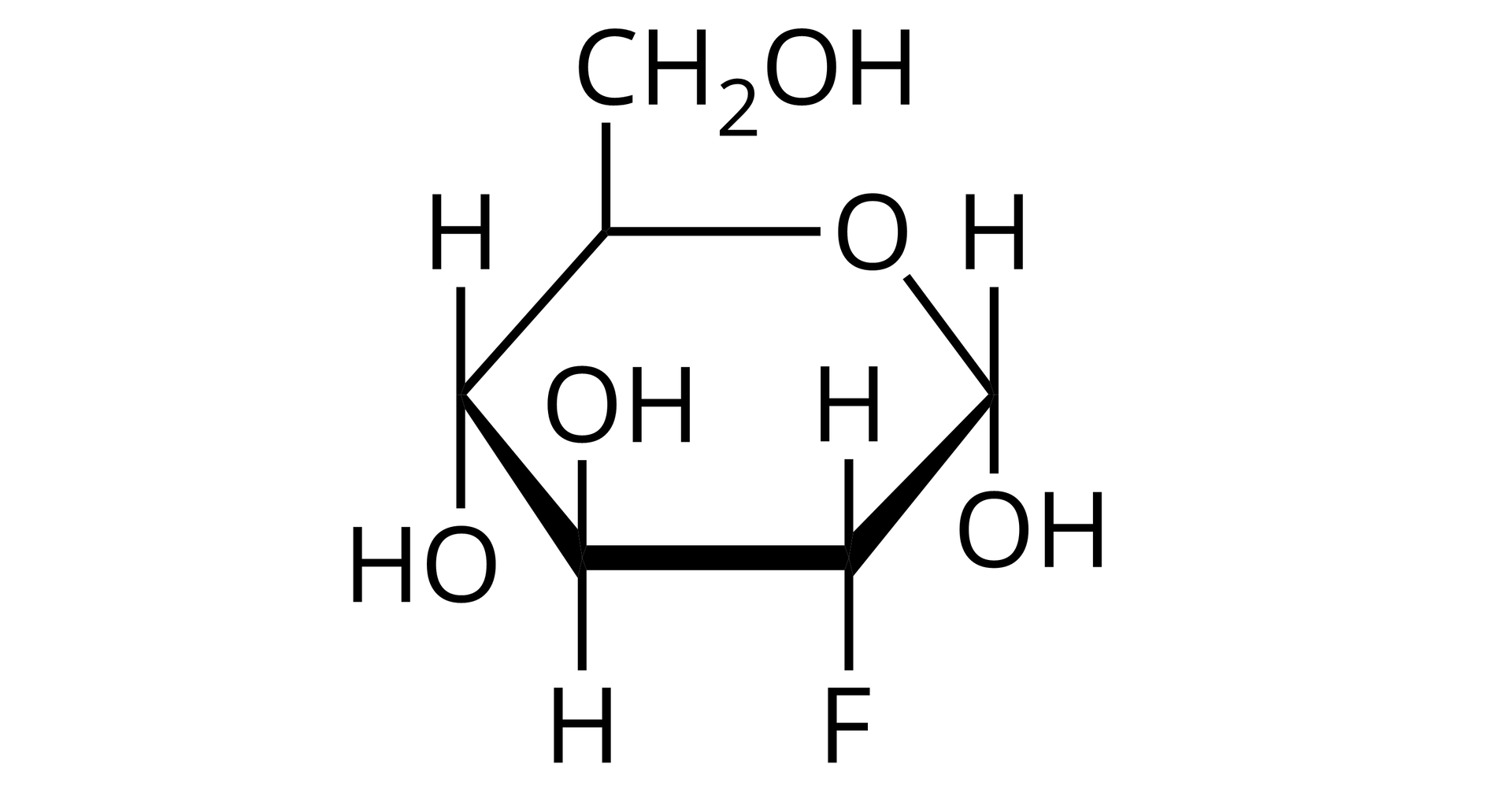
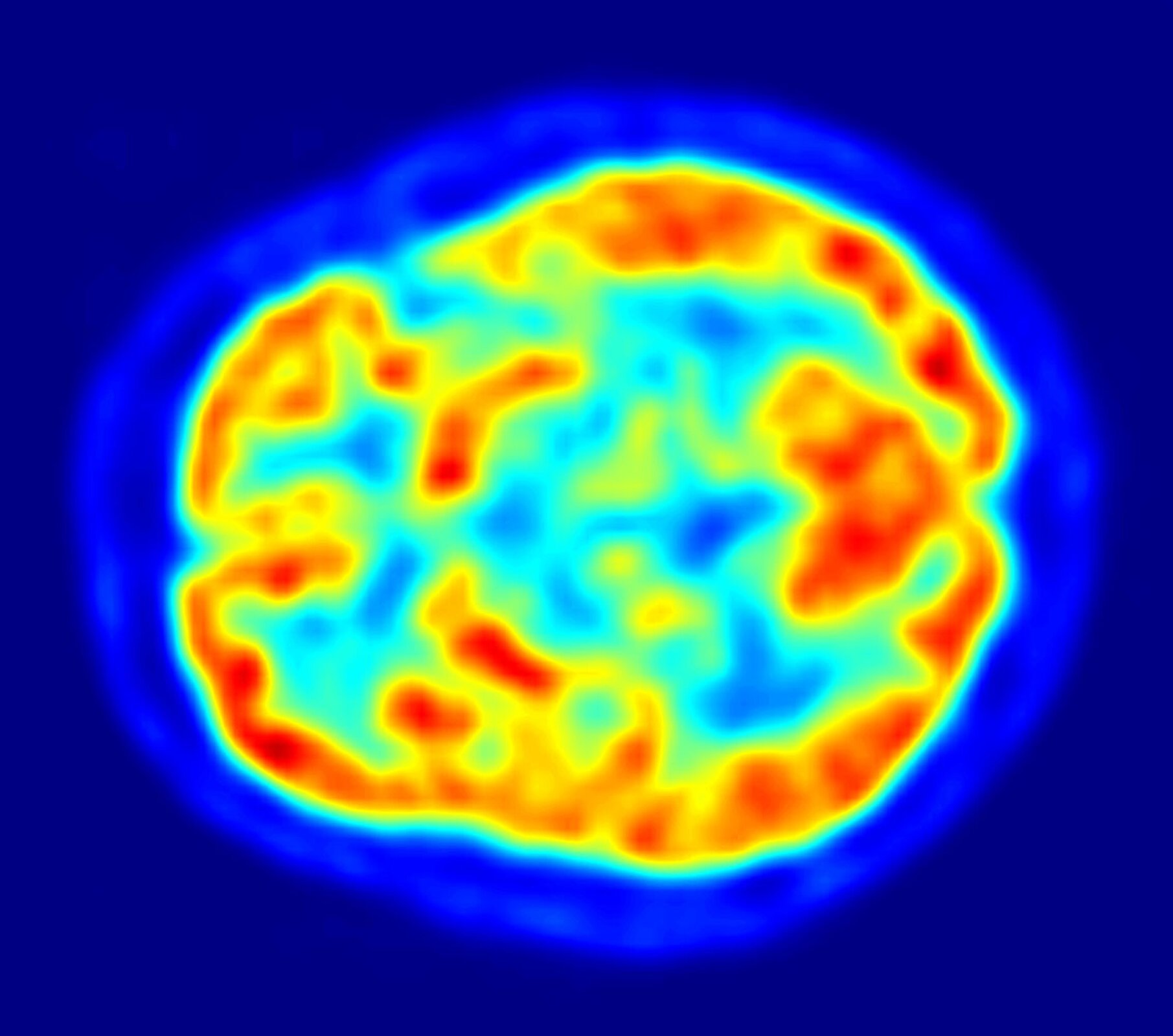
Związek ten jest pochodną glukozy, w której jedna grupa hydroksylowa została zastąpiona izotopem fluoru‑18. Ze względu na to, że obie cząsteczki są do siebie bardzo podobne, zmodyfikowana cząsteczka cukru może bez problemu wnikać do wnętrza komórek. Ma to ogromne znaczenie w wykrywaniu nowotworów. Komórki nowotworowe namnażają się niezwykle intensywnie, w wyniku czego potrzebują dużo energii, która jest dostarczana przez cząsteczki cukru. Emitowane przez cząsteczki zmodyfikowanego cukru promieniowanie pozytonowe jest wykorzystywane w technice diagnostycznej PETPET (pozytonowa tomografia emisyjna) do obrazowania czy badania funkcjonowania tkanek.
Fluor w nadmiernym stężeniu działa toksycznie na organizm ludzki. Wskaźnik LDIndeks dolny 5050 jest wskaźnikiem dawki śmiertelnej, która dla fluorku sodu wynosi 52 mg na 1 kg masy ciała.
Podsumowując, fluor jest potrzebny do funkcjonowania naszemu organizmowi. Należy do mikroelementów, jednak – jak w przypadku większości substancji – jego nadmiar może okazać się śmiertelny.
Słownik
środki stosowane w celu wywołania narkozy, tzn. przejściowego stanu zahamowania czynności kory mózgowej, ośrodków podkorowych i rdzeniowych, w celu przeprowadzenia bezbolesnego zabiegu chirurgicznego
miara zdolności atomów w cząsteczkach związków chemicznych do przyciągania elektronów
(gr. ísos „równy”, tópos „miejsce”) nuklidy o tej samej liczbie atomowej Z i różnych liczbach masowych A (tj. o tej samej liczbie protonów i różnych liczbach neutronów)
(ang. Positon Emission Tomography) tomografia emisyjna pozytonowa; metoda pozwalająca uzyskać dwuwymiarowy obraz przekroju obiektu trójwymiarowego z zastosowaniem emisji pozytonów
(ang. parts per million „części na milion”) oznaczenie stosunku wartości tej samej wielkości (masy, objętości) do 1 000 000
Bibliografia
Atkins P., Jones L., Chemia ogólna. Cząstki, materia, reakcje, Warszawa 2004, s. 951‑968.
Encyklopedia PWN