Przeczytaj
Budowa estrów
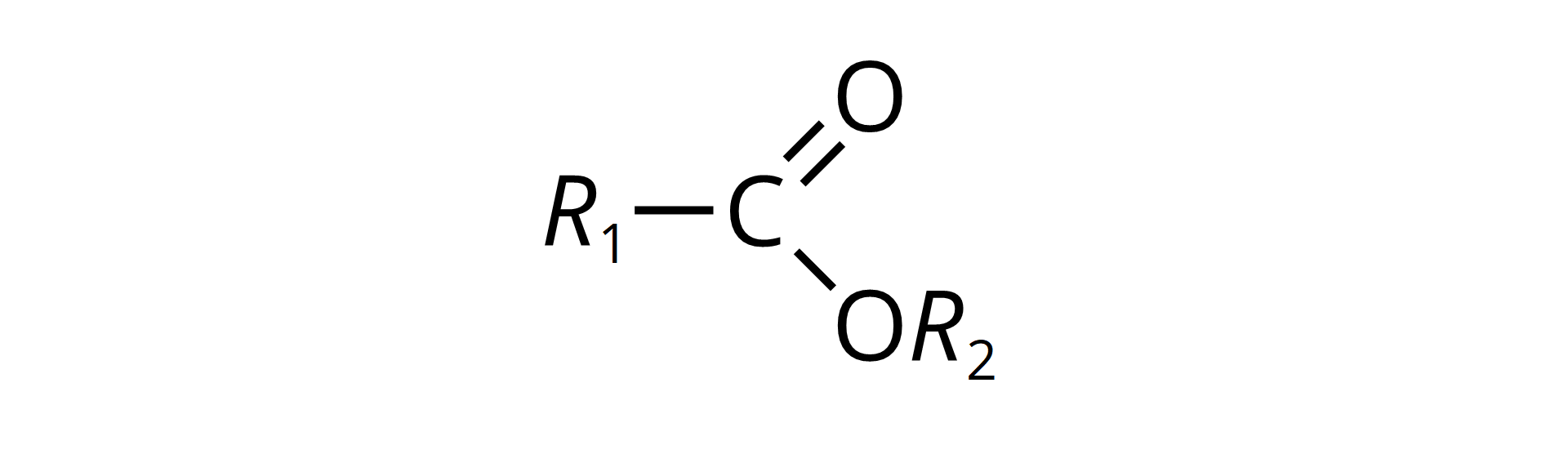
EstryEstry należą do grupy związków organicznych. Powstają w wyniku reakcji kondensacjireakcji kondensacji kwasów z alkoholami lub fenolami. Ich wzór ogólny to .
Estryfikacja
Reakcję chemiczną, podczas której powstają estry, nazywamy estryfikacjąestryfikacją. Substratami są kwas i alkohol (lub fenol), a produktami ester i woda. Reakcja przebiega w obecności stężonego kwasu siarkowego(), umożliwiającego przebieg reakcji.
Równowaga chemiczna
W układzie chemicznym nie zachodzą makroskopowo żadne zmiany. Jest to stan, w którym prędkość estryfikacji jest równa prędkości reakcji do niej odwrotnej – hydroliziehydrolizie estrów. Produkty i substraty są wtedy w równowadze.
Stała równowagi K dla estryfikacji
Jeśli ogólne równanie reakcji estryfikacji zapisuje się:
to stała równowagi wynika wówczas ze stężenia reagentów w stanie równowagi. W przypadku estryfikacji stała równowagi ma postać:
Jakie czynniki wpływają na stan równowagi estryfikacji?
, środowisko reakcji Ogrzewanie mikrofalowe, użyte w estryfikacji skrobi kwasami tłuszczowymi, pozwala na znaczne skrócenia czasu reakcji.
Sposoby przesuwania równowagi w kierunku produktów
Estryfikacja jest bardziej efektywna, jeśli:
zastosuje się nadmiar jednego z substratów;
odbiera się ze środowiska reakcji tworzący się ester;
odbiera się ze środowiska reakcji tworzącą się wodę.

Zastosowanie powyższych metod pozwala zwiększyć ilość otrzymywanego estru. W innym przypadku skuteczność procesu będzie na poziomie około .
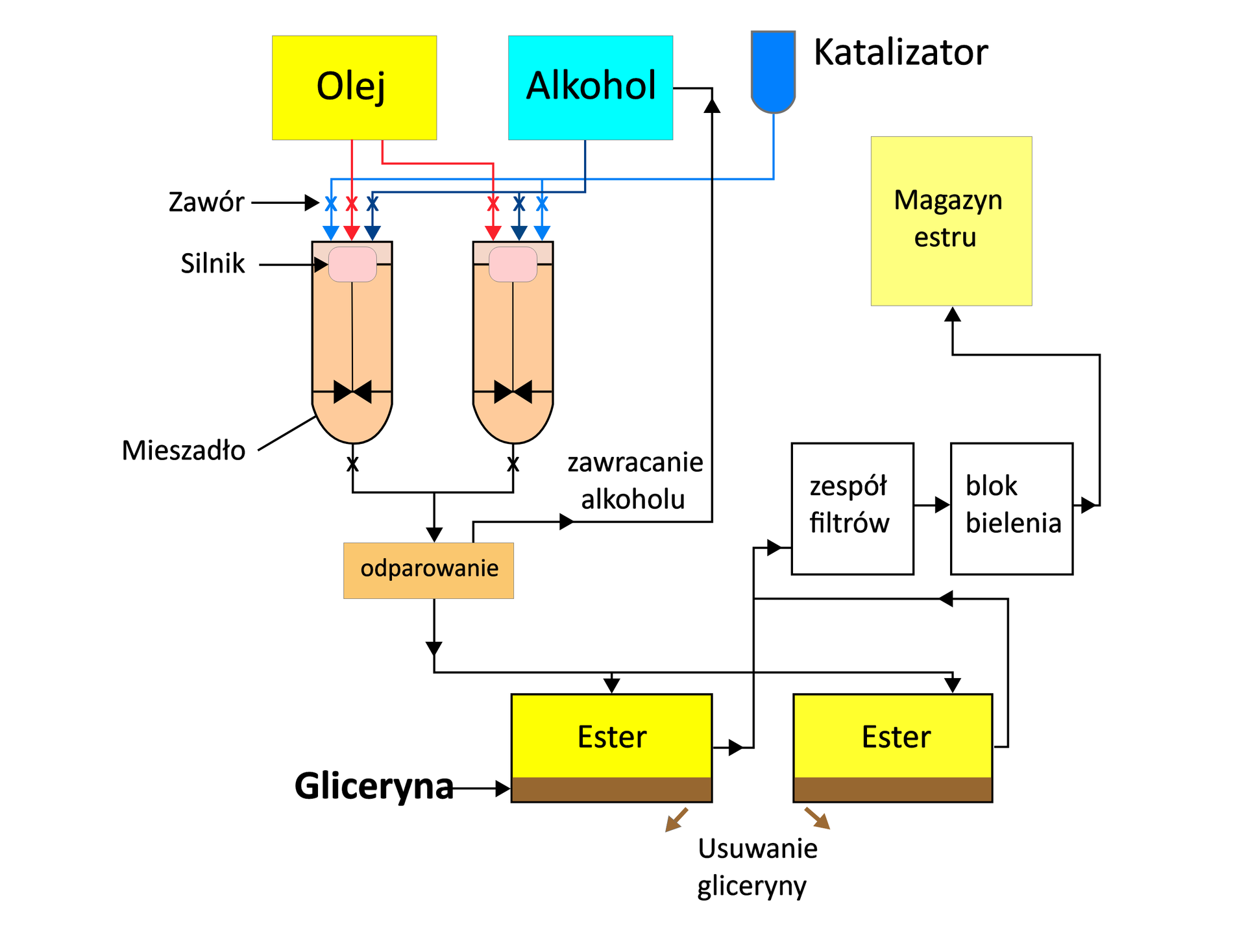
Słownik
(niem. Essigäther „octan etylu’’; Essig „ocet’’; Äther „eter’’) grupa organicznych związków chemicznych; powstają w wyniku estryfikacji; powstają z kwasów (kwasy karboksylowe lub kwasy nieorganiczne) i alkoholi lub fenoli
reakcja chemiczna, w której powstają estry; przykłady niektórych sposobów otrzymywania estrów:
przez substytucję nukleofilową chlorków lub bezwodników kwasowych alkoholami;
przez substytucję nukleofilową kwasów karboksylowych alkoholami (katalizator kwas nieorganiczny)
(gr. hýdōr „woda”; lýsis „rozłożenie”) reakcja zachodząca pomiędzy substancją rozpuszczoną a rozpuszczalnikiem (w tym przypadku wodą); ulegają jej związki organiczne i nieorganiczne
w technologii chemicznej jest to określenie procesów, które mają na celu zmianę właściwości przekształcanych materiałów w wyniku różnych reakcji chemicznych; jest prowadzona w specjalnych aparatach (zwykle w wysokiej temperaturze, pod wysokim ciśnieniem lub z użyciem katalizatorów)
w chemii – rodzaj reakcji; dochodzi w niej do połączenia substratów w większą cząsteczkę. Powstaje tzw. produkt główny. Wynikiem reakcji mogą być również małe cząsteczki produktu/produktów o drugorzędnym znaczeniu
(czyt. lö szatöljẹ) po wprowadzeniu zmiany do układu w stanie równowagi, następuje przesunięcie położenia równowagi w kierunku przeciwdziałającym tej zmianie
stosunek iloczynu równowagowych stężeń (lub ułamków molowych, albo ciśnień cząstkowych) produktów reakcji chemicznej, podniesionych do potęg równych ich współczynnikom stechiometrycznym do iloczynu równowagowych stężeń (lub ułamków molowych, albo ciśnień cząstkowych) substratów w odpowiednich potęgach
gdzie: , , , – stężenia molowe substancji , , , w stanie równowagi chemicznej
otrzymywanie nowego estru w wyniku reakcji chemicznej innych estrów z alkoholami (alkoholiza), kwasami (acydoliza) lub innymi estrami

Bibliografia
Bose K. S., Roy S., Principles of Metallurgical ermodynamics, 2014.
Grabowska B., Wykład 3. Termodynamika a kinetyka chemiczna, Katedra Inżynierii Procesów Odlewniczych, WO AGH.
Liu Y., Lotero E., Goodwin J., Effect of water on sulfuric acid catalyzed esterification. „Journal of Molecular Catalysis A”, 245, pp. 132–140.
Pigoń K., Ruziewi Z., Chemia Fizyna, Warszawa 2014.
Smith E. B, Basic chemical thermodynamics, Londyn 2014.
Pisarek S., Praca doktorska. Nowe pochodne i analogi protoporfiny IX, Instytut Chemii Organicznej, Polska Akademia Nauk, Warszawa 2013.
Materiały do ćwiczeń laboratoryjnych z chemii organicznej dla studentów biologii. Wydanie II poprawione i uzupełnione, pod red. A. Jarczewskiego, Zakład Chemii Ogólnej Wydziału Chemii, Uniwersytet im. Adama Mickiewicza w Poznaniu, Poznań 2007.
Ptak S., Roczkowska M., Żarski A., Kapuśniak J., Esterification of starch with fatty acids. New opportunities and challenges. Estryfikacja skrobi kwasami tłuszczowymi. Nowe możliwości i wyzwania, Akademia im. Jana Długosza, Częstochowa; Politechnika Łódzka, DOI: dx.medra.org
Preparatyka organiczna. Skrypt dla studentów Farmacji Uniwersytetu Medycznego we Wrocławiu, Uniwersytet Medyczny im. Piastów Śląskich we Wrocławiu, Wydział Farmaceutyczny z Oddziałem Analityki Medycznej, Katedra i Zakład Chemii Organicznej, Wrocław 2014.