Przeczytaj
Manganian() potasu
To jeden z najpopularniejszych manganianów(). Stosuje się go zarówno w chemii nieorganicznej, jak i organicznej, ponieważ jest bardzo silnym utleniaczem.
Odróżnienie alkanu od alkenów i alkinów umożliwiają m.in. reakcje z bromem i manganianem() potasu.
Jak można odróżnić alkany od alkenów i alkinów?
Związki nienasycone reagują z w środowisku słabo alkalicznym lub obojętnym, utleniając się do glikoli. Przy tym jednak warto zaznaczyć, że mangan przechodzi z siódmego na czwarty stopień utlenienia, zgodnie z równaniem:
Potwierdzeniem charakteru nienasyconego związku jest pozytywny wynik w reakcjach z roztworem manganianu() potasu (wytrącenie brunatnego osadu w przypadku reakcji zachodzącej w środowisku obojętnym) lub z roztworem bromu w (odbarwienie roztworu).
Alkany
Alkany reagują z bromem pod wpływem światła, ale nie reagują z .
Alkeny
Utlenianie alkenów manganianem() potasu prowadzi do otrzymania różnych produktów organicznych, co jest zdeterminowane środowiskiem i temperaturą, w której prowadzi się reakcję. Alkeny ulegają reakcji z w środowisku kwasowym lub obojętnym.
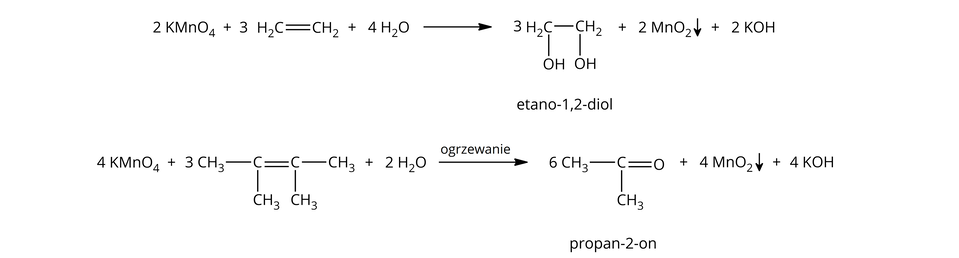
Jeżeli reakcja zachodzi w środowisku obojętnym w temperaturze pokojowej, następuje pęknięcie wiązania piwiązania pi. W wyniku tego powstają diole (układ ) oraz m.in. brunatny osad .
W podwyższonej temperaturze cząsteczki ulegają rozerwaniu w miejscu wiązania podwójnego. W efekcie powstaje mieszanina kwasów lub kwas i keton, albo mieszanina ketonów oraz m.in. brunatny osad . W przypadku alkenów terminalnych, powstaje odpowiedni kwas i .
Opisane powyżej reakcje przedstawiają następujące równania:
Z kolei utlenienie w środowisku kwasowym, podczas którego zaobserwowano odbarwienie roztworu, można zapisać w następujący sposób:
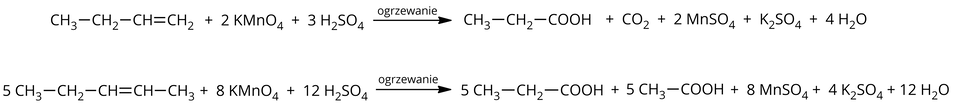
Alkiny
Alkiny, podobnie jak alkeny, można utlenić manganianem() potasu. Uzyskany produkt organiczny zależy od rodzaju użytego w reakcji alkinu. Reakcja zachodzi w środowisku kwasowym.
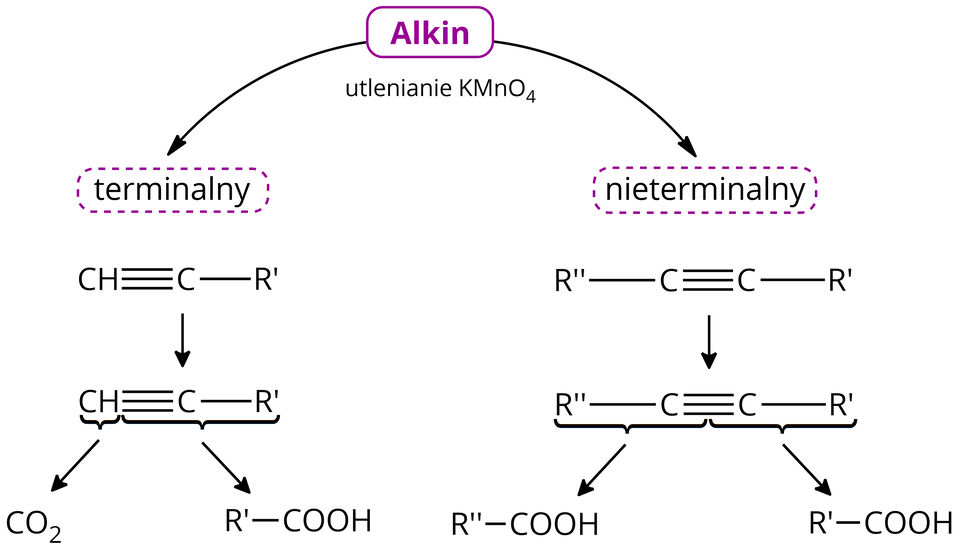
dla alkinu terminalnegoalkinu terminalnego, np.:

dla alkinu nieterminalnegoalkinu nieterminalnego, np.:
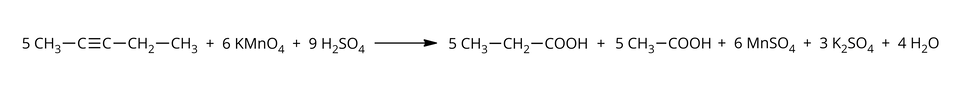
Jaki charakter – nasycony czy nienasycony – wykazuje benzen?
Benzen nie wykazuje ani charakteru nienasyconego, ani nasyconego. Ze względu na obecność wiązań zdelokalizowanych i trwałość cząsteczki, nie odbarwia wody bromowej ani zakwaszonego roztworu manganianu() potasu. Reaguje z bromem w obecności katalizatora lub pod wpływem światła.
Słownik
wiązanie chemiczne utworzone przez elektrony, opisane orbitalem molekularnym antysymetrycznym, względem odbicia w płaszczyźnie, która przechodzi przez oś wiązania
alkin, który posiada wiązanie potrójne na końcu łańcucha węglowego
alkin, który posiada wiązanie potrójne wewnątrz łańcucha węglowego
Bibliografia
Dudek‑Różycki K., Płotek M., Wichur T., Węglowodory. Repetytorium i zadania, Kraków 2020.
Dudek‑Różycki K., Płotek M., Wichur T., Kompendium terminologii oraz nazewnictwa związków organicznych. Poradnik dla nauczycieli i uczniów, Kraków 2020.
Krzeczkowska M., Loch J., Mizera A., Chemia. Repetytorium. Liceum – poziom podstawowy i rozszerzony, Warszawa – Bielsko‑Biała 2010.