Przeczytaj
Fermentacja alkoholowa – istota reakcji
Fermentacja alkoholowa to proces rozkładu cukrów prostych do alkoholu etylowego (etanolu) i tlenku węgla() . Fermentacja alkoholowa jest procesem oddychania beztlenowego. W reakcji tej substrat oddechowy ulega rozbiciu i przekształceniu. Jest to przykład reakcji dysproporcjonowania, ponieważ otrzymuje się z niej zarówno bardziej utlenione produkty, jak i bardziej zredukowane.


Przebieg reakcji fermentacji alkoholowej
Ogólne równanie fermentacji alkoholowej można zapisać:
W czasie fermentacji alkoholowej powstaje również wiele produktów ubocznych, np. gliceryna, kwas bursztynowy i kwas octowy. Inne produkty uboczne, takie jak wyższe alkohole i estry odpowiadają za bukiet smakowo–zapachowy produktu.
Glikoliza
Fermentacja alkoholowa rozpoczyna się od fosforylacjifosforylacji glukozy do glukozo–6–fosforan z wykorzystaniem enzymu heksokinazy.


Przekształcenie glukozo–6–fosforanu we fruktozo–6–fosforan następuje przy udziale izomerazy glukozo–6–fosforanowej. Jest to reakcja odwracalna.

Fosforylację fruktozo–6–fosforanu przy użyciu przeprowadza enzym fosfofruktokinaza. Powstaje fruktozo–1,6‑bisfosforanu oraz .

Kolejny etap stanowi reakcja, która polega na rozszczepieniu fruktozo–1,6–bisfosforanu na aldehyd 3–fosfoglicerynowy oraz fosfodihydroksyaceton. Enzym przeprowadzający tę reakcję to aldolaza. Jest to reakcja odwracalna.
Przekształcenie fosfodihydroksyacetonu w aldehyd 3–fosfoglicerynowy jest katalizowane przez izomerazę triozofosforanową. Dzięki izomerazie triozofosforanowej możliwe jest szybkie wytworzenie aldehydu 3–fosfoglicerynowego, niezbędnego do dalszego zachodzenia glikolizy. Jest to reakcja odwracalna.

Pi – fosforan nieorganiczny
Reakcja ta przebiega w dwóch etapach. W pierwszym z nich aldehyd 3–fosfoglicerynowy łączy się z grupą tiolową –, tworząc tym samym hemitioacetal. W drugim etapie jon wodorkowy przenoszony jest na , połączonym z enzymem w pobliżu reszty cysteiny. Powstaje 1,3–bisfosfoglicerynian. Reakcja jest odwracalna.
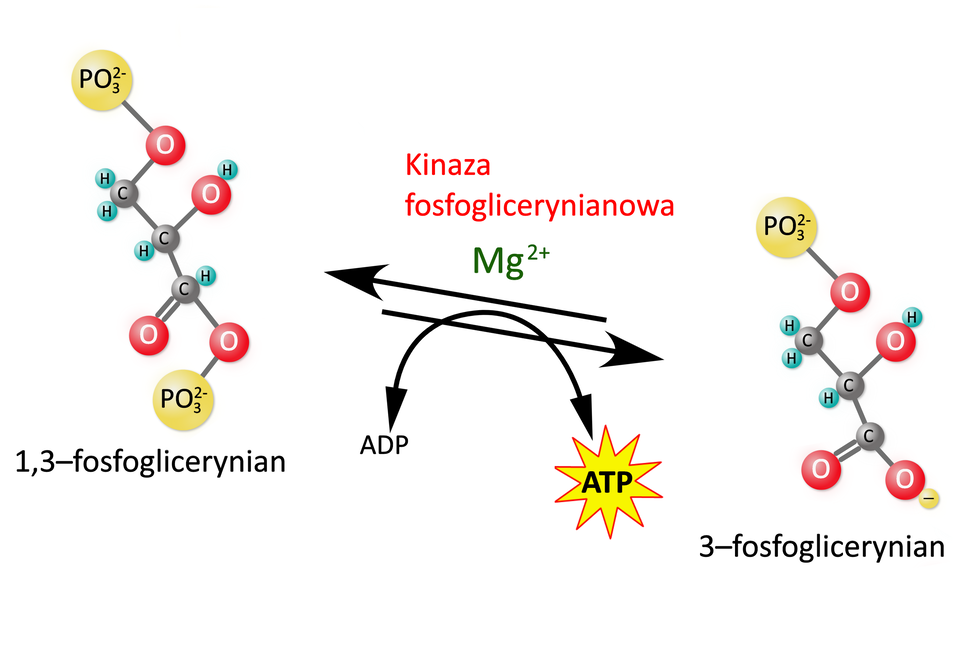
Przeniesienie grupy fosforanowej z 1,3– na i utworzenie (fosforylacja substratowa) oraz 3–fosfoglicerynianu – reakcja katalizowana przez kinazę fosfoglicerynianową.
Przekształcenie 3–fosfoglicerynianu w 2–fosfoglicerynian przez fosfogliceromutazę.

Odwodnienie 2–fosfoglicerynianu i powstanie fosfoenolopirogronianu () katalizowane jest przez enolazę.

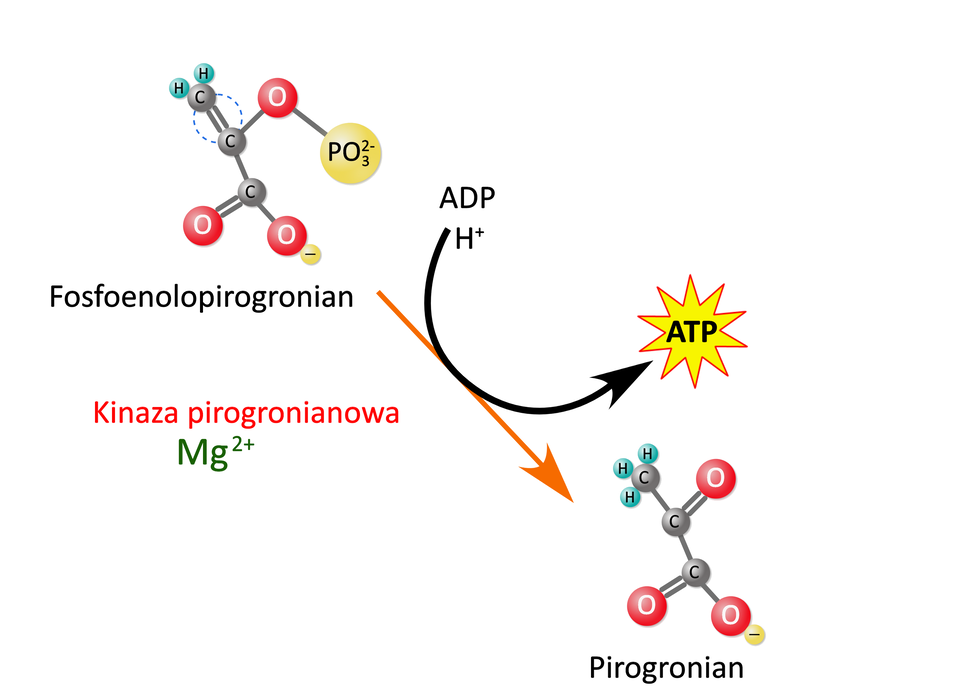
Przeniesienie grupy fosforanowej z na i powstanie oraz pirogronianu katalizowane jest przez kinazę pirogronianową.

Pi – fosforan nieorganiczny
Powstawanie alkoholu etylowego – fermentacja alkoholowa
Zachodzi dekarboksylacjadekarboksylacja kwasu pirogronowego. Produktem jest aldehyd octowy i tlenek węgla().


Później następuje zredukowanie aldehydu octowego (etanalu) do etanolu pod wpływem zredukowanego (dinukleotyddinukleotyd nikotynoamidoadeninowy) i enzymuenzymu dehydrogenazy alkoholowej.

Ciekawostka
Czym jest „kac”?
„Kac” to nic innego jak nieprzyjemne samopoczucie pojawiające się dnia następnego po spożyciu zbyt dużej ilości alkoholu etylowego.
Tylko niewielka część alkoholu etylowego jest usuwana z naszego organizmu z moczem lub za pomocą dróg oddechowych. Druga część tego związku ulega przemianie w hepatocytach wątroby, gdzie następuje jego transformacja w etanal w obecności enzymu dehydrogenazy alkoholowej, kolejno w kwas octowy za pomocą dehydrogenazy acetaldehydowej. A to nie alkohol etylowy tylko etanal jest bardziej toksyczny dla naszego organizmu.
Zespół autobrowaru
Pacjenci, u których zdiagnozowano zespół auto‑browaru, po spożyciu pokarmów o wysokiej zawartości węglowodanów wchodzą w stan nietrzeźwości. Przyczyną tego jest obecność w ich organizmie drożdży, np. Candida albicans, Candida krusei, Candida glabrata i Saccharomyces cerevisiae. Nie jest zaskakującym fakt wytwarzania alkoholu z węglowodanów dzięki drożdżom, ponieważ to normalna i powszechna reakcja we florze układu pokarmowego człowieka, lecz ilość tego wyprodukowanego alkoholu. Kolejnym elementem oddziałującym jest nieprawidłowy enzym wątrobowy (dehydrogenaza alkoholowa). Organizm nie jest w stanie szybko przetworzyć alkoholu, w skutek czego dochodzi do stanu upojenia bez wypicia grama alkoholu.
Fermentacja alkoholowa jest więc reakcją wieloetapową, zachodzącą w żywych organizmach. W ogromnym uproszczeniu, biorąc pod uwagę jedynie główny substrat i ostateczne produkty, równanie reakcji chemicznej można skrótowo opisać:
Fermentację alkoholową drożdży wykorzystuje się w:
piwowarstwie;
winiarstwie;
gorzelnictwie;
spulchnianiu pieczywa – przemysł piekarniczy;
spulchnianiu ciast – przemysł cukierniczy.
Fermentacja jest sposobem uzyskiwania energii przez organizmy żyjące w środowisku beztlenowym. Jest procesem mniej wydajnym niż oddychanie tlenowe. Brakuje w nim końcowego akceptora elektronów, którym jest tlen.
Słownik
organiczny związek chemiczny; nukleotyd adeninowy zbudowany z adenozyny z przyłączonym wiązaniem estrowym w pozycji grupą trifosforanową; ma istotną rolę w biologii komórki, jest wielofunkcyjnym koenzymem i molekularną jednostką w wewnątrzkomórkowym transporcie energii; nośnik energii chemicznej, który jest niezbędny w metabolizmie komórki; jest syntetyzowany w procesach fotosyntezy i oddychania komórkowego; stanowi magazyn energii
reakcja chemiczna, polegająca na usunięciu grupy karboksylowej z kwasów karboksylowych, ich soli i estrów; wynikiem reakcji jest najczęściej wydzielanie tlenku węgla(); w organizmach katalizowana przez enzymy
związek chemiczny będący nukleotydem, ma istotne znaczenie biologiczne; szczególnie ważny jest w procesach oddychania komórkowego; pochodne tego związku są akceptorami elektronów i protonów w procesach utleniania komórkowego:
– forma utleniona dinukleotydu
– ester fosforanowy dinukleotydu
– forma zredukowana
– forma zredukowana
(z gr. ἔnuzetaupsilonmuomicronnu, od ἔnu en ‘w’ i zetaύmueta dzýmē „zaczyn”, „(za)kwas”) wielkocząsteczkowe związki chemiczne; katalizatory przyspieszające specyficzne reakcje chemiczne; ich działanie polega na obniżeniu energii aktywacji katalizowanej reakcji chemicznej
reakcja chemiczna, polegająca na przyłączeniu reszty fosforanowej do nukleofilowego atomu dowolnego związku chemicznego; przeciwieństwem fosforylacji jest defosforylacja
gęsty, ciemnobrązowy syrop, powstajacy w czasie produkcji cukru spożywczego; zawiera około sacharozy, ale dalsze jej pozyskiwanie jest nieopłacalne; produkt wykorzystywany m.in. do produkcji alkoholu
Bibliografia
Bednarski W., Reps A., Adamczak M., Biotechnologia żywności: praca zbiorowa, Warszawa 2003.
Berg J. M., Tymoczko J. L., Stryer L., Clarke N. D., Biochemia: Glikoliza i glukoneogeneza, Warszawa 2007, s. 425–464.
Bortel E., Zarys technologii chemicznej, Warszawa 1992.
Cordell B., McCarthy J., A Case Study of Gut Fermentation Syndrome (Auto‑Brewery) with Saccharomyces cerevisiae as the Causative Organism, „International Journal of Clinical Medicine” 2013, t. 4, nr 7.
Fayemiwo S. A., Adgeboro B., Gut Fermentation Syndrome, „Afr. J. Cln. Exper. Microbiol.” 2014, t. 15, nr 1, s. 48‑50.
Gabryś H., Fizjologia roślin: Procesy oddechowe, pod. red. J. Kopcewicza, S. Lewaka, Warszawa 2002, s. 387–420.
Hames B. D., Hooper N. M., Krótkie wykłady. Biochemia: Metabolizm węglowodanów. Warszawa 2005, s. 305–354.
Haynes W. M., CRC Handbook of Chemistry and Physics, USA 2016, s. 3‑10, wyd. 97.
Kuczyński W., Podręcznik do ćwiczeń z technologii chemicznej, Warszawa 1974.
Logan B. K., Jones A. W., ,Endogenous Ethanol „Auto‑Brewery Syndrome” as a DrunkDriving Defence Challenge, „Med Sci Law. Jul.„ 2020, t. 40, nr 3, s. 206‑2015.
Mayes P. A., Murray R. K., Granner D. K., Rodwell V. W., Harper H. A., Biochemia Harpera: Glikoliza i utlenianie pirogronianu, Warszawa 1995, s. 207–216.
McMurry J., Chemia organiczna: Podstawowe pojęcia dotyczące metabolizmu i energii biochemicznej, t. 5, Warszawa 2005, s. 1096–1097.
Molenda J., Technologia chemiczna, Warszawa 1997.
Ronimus R.S., Morgan H.W., Distribution and phylogenies of enzymes of the Embden‑Meyerhof‑Parnas pathway from archaea and hyperthermophilic bacteria support a gluconeogenic origin of metabolism, ”Archaea” 2003, t. 1, nr 31, s. 199–221.
Duszyński J., Kozłowska‑Rajewicz A., Krenz‑Niedbała, Biologia Jedność i różnorodność, Warszawa 2008.
Dinukleotyd nikotynoamidoadeninowy (nr N8285) – karta charakterystyki produktu Sigma‑Aldrich (Merck KGaA) na obszar Polski.
Dinukleotyd nikotynoamidoadeninowy (DB01907) – informacje o substancji aktywnej (ang.). DrugBank.