Przeczytaj
Budowa aminokwasów białkowych
Aminokwasy to związki dwufunkcyjne, które zawierają w swych cząsteczkach grupę karboksylową -COOH oraz grupę aminową -NHIndeks dolny 22. Często są uznawane za pochodne kwasów karboksylowych, w których atom wodoru w grupie węglowodorowej został podstawiony przez grupę aminową. Do aminokwasów zalicza się związki, które zawierają także inne grupy funkcyjne, np. dodatkową grupę aminową lub karboksylową, grupę tiolową lub hydroksylową, układy heterocykliczne czy pierścienie aromatyczne.

R – alifatyczna grupa boczna aminokwasu
Ar – aromatyczna grupa boczna aminokwasu
Występująca w cząsteczce aminokwasu grupa –R, może reprezentować grupę zróżnicowaną pod względem:
kształtu;
wielkości;
ładunku elektrycznego;
reaktywności;
zdolności do tworzenia wiązań wodorowychwiązań wodorowych i oddziaływań hydrofobowych.
Często stosowaną zasadą, określającą wzajemne położenie grupy aminowej i karboksylowej, jest oznaczenie atomów węgla w łańcuchu węglowodorowym kolejnymi literami greckimi: alfa, beta, gamma i delta:
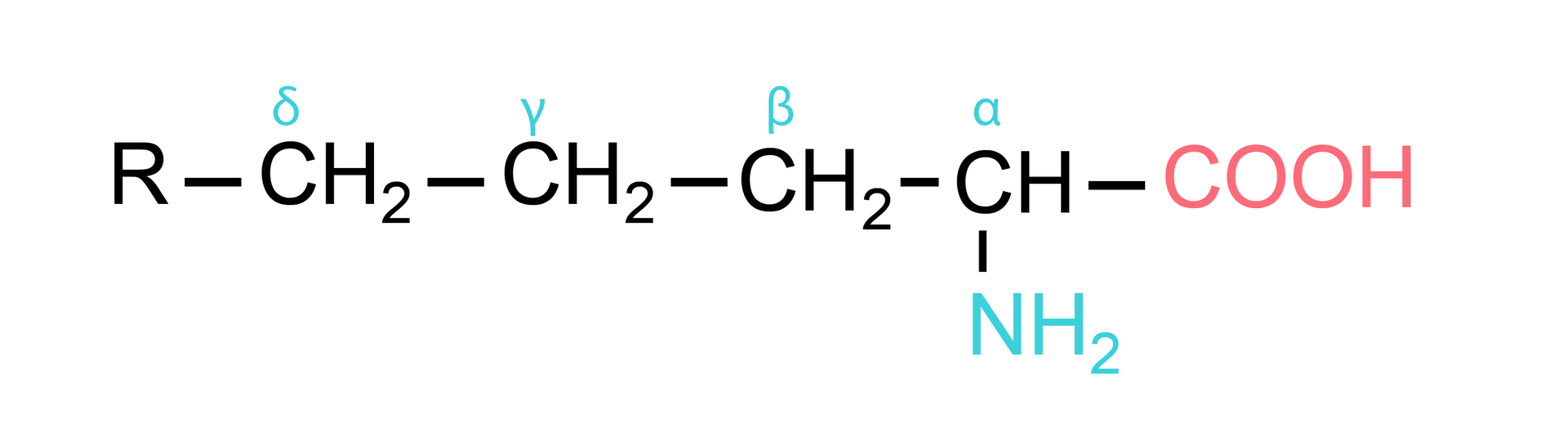
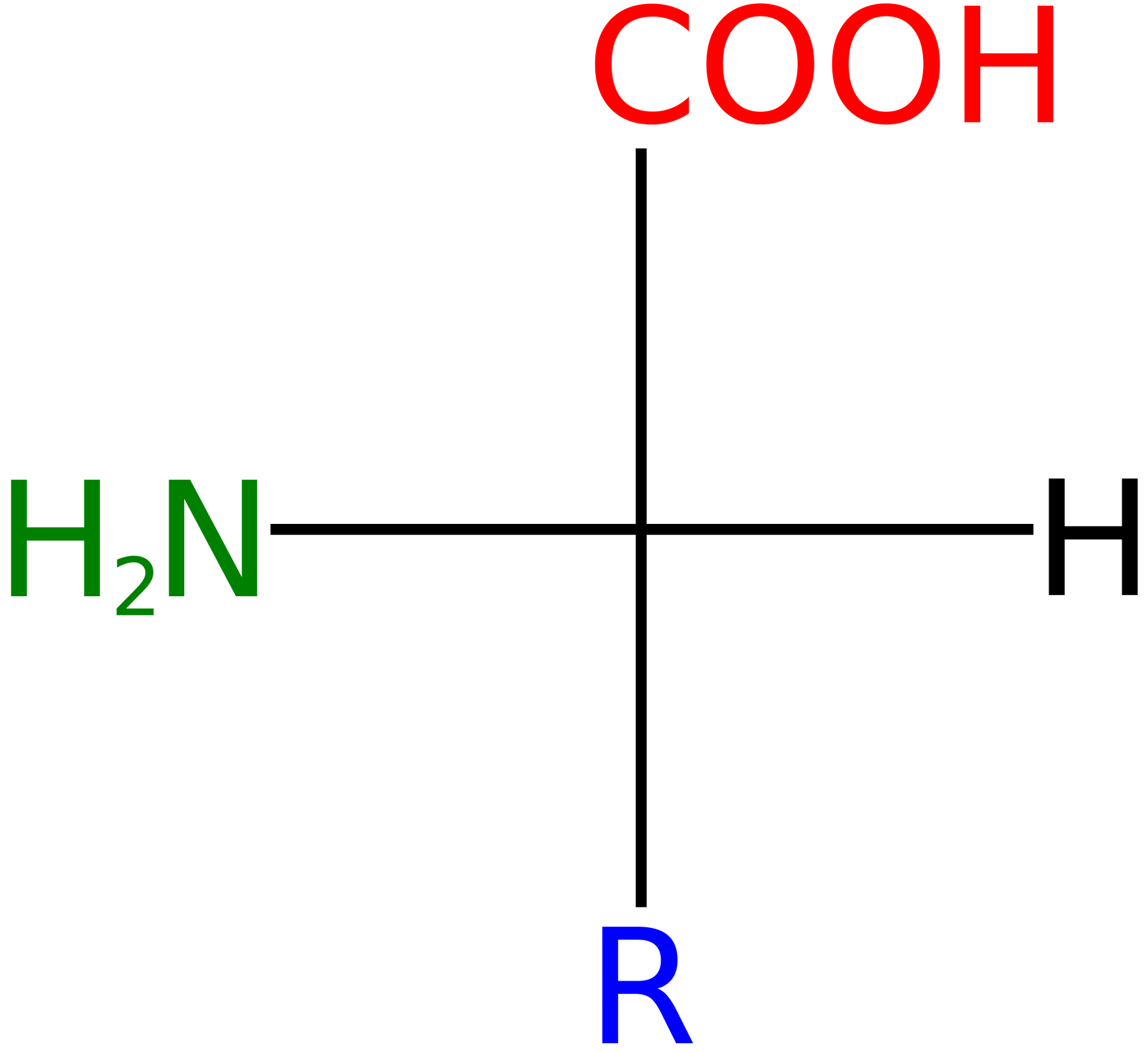
Wszystkie aminokwasy białkowe w organizmie ludzkim (z wyjątkiem glicyny) wykazują czynność optycznączynność optyczną i są alfa‑L-aminokwasami. Oznacza to, że posiadają centrum asymetrii na węglu i należą do szeregu stereochemicznego L, czyli mają grupę aminową po lewej stronie łańcucha głównego w projekcji Fischera. Do ustalenia ich przynależności do szeregu L, jako wzór wybrano L‑serynę.
Słownik
właściwość ośrodka (substancji); przejawia się skręcaniem płaszczyzny polaryzacji światła spolaryzowanego liniowo, które przechodzi przez ten ośrodek (skręcalność optyczna) lub też przejawia się zmianą stanu polaryzacji z liniowej na eliptyczną (eliptyzacja światła)
rodzaj oddziaływania międzycząsteczkowego lub wewnątrzcząsteczkowego między atomem wodoru a atomem elektroujemnym, który posiada wolne pary elektronowe
Bibliografia
Encyklopedia PWN
Krzeczkowska M., Loch J., Mizera A., Chemia. Repetytorium. Liceum - poziom podstawowy i rozszerzony, Warszawa – Bielsko‑Biała 2010.