Przeczytaj
Fenole
Fenole charakteryzują się znacznie większą kwasowością od alkoholi. Dla większości prostych fenoli ich znajduje się w przedziale od do . Różnica ta wynika m.in. z tego, że:
cząsteczki fenoli charakteryzują się większą polaryzacją wiązania , która spowodowana jest deficytem elektronów na atomie tlenu;
fenole posiadają lepszą stabilizację anionu fenolanowego (w porównaniu z jonem alkoholanowym), która to wynika z możliwości delokalizacji ładunku ujemnego na pierścień aromatyczny.
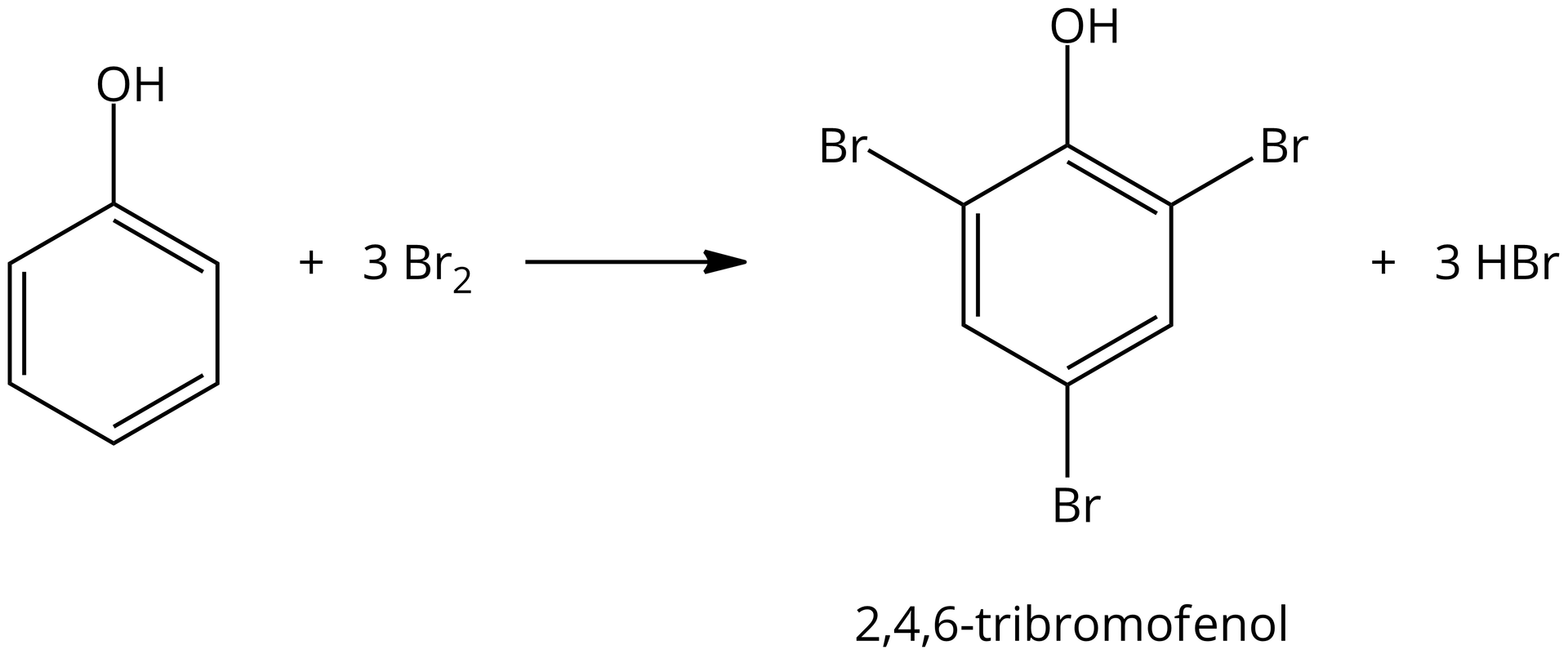
Reakcja fenolu z bromem
FenolFenol jest związkiem aromatycznym, dlatego ulega reakcjom charakterystycznym dla tych związków, np. bromowaniu i nitrowaniunitrowaniu. Reakcje te zachodzą dużo łatwiej niż w przypadku benzenu.
Obecność grupy hydroksylowej, aktywującej pierścień, powoduje, że fenole reagują z bromem w temperaturze pokojowej bez użycia katalizatora. Wykorzystanie wody bromowej lub 2% roztworu bromu w do bromowania, powoduje powstanie trudno rozpuszczalnego w wodzie produktu, który wytrąca się z roztworu w formie osadu. Osad ten ma barwę białą lub lekko żółtą. Reakcja z bromem wykorzystywana jest do wykrywania fenoli oraz do ilościowego oznaczania ich zawartości (np. w ściekach).
Doświadczenie
Do nasyconego wodnego roztworu rezorcyny (dla fenoli trudno rozpuszczalnych używa się około etanolu) dodaje się kroplami wodę bromową, aż do pojawienia się jasnożółtej barwy roztworu.
Reakcje z wodorotlenkiem sodu
Ze względu na większą kwasowość od alkoholi, fenole ulegają wszystkim reakcjom charakterystycznym dla kwasów, którym na ogół nie ulegają alkohole, czyli m.in. reagują z wodorotlenkiem sodu z wydzieleniem wody.
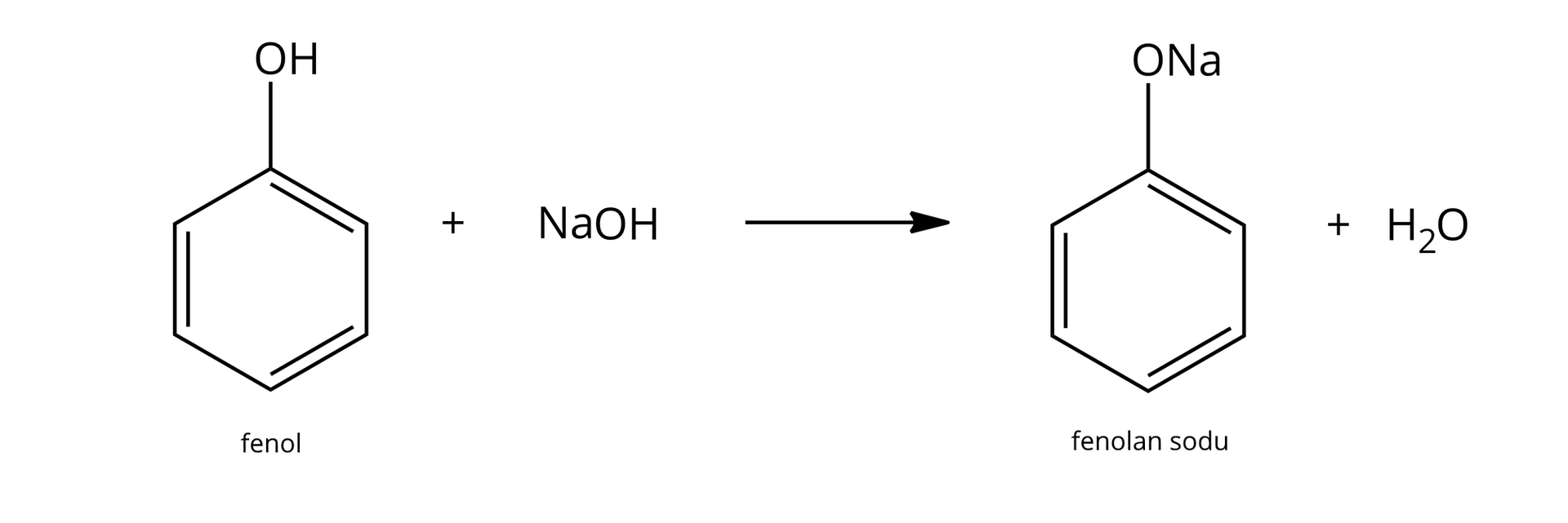
Zachowanie wobec wodnego roztworu NaOH
Fenole są kwasami mocniejszymi od alkoholi, dlatego też mogą wypierać alkohole z roztworów alkoholanów. Alkohole, jako kwasy słabsze od fenoli, nie wypierają ich z roztworów fenolanów.
Reakcję tę przeprowadza się w skali probówkowej. W chemii analitycznej wykorzystuje się ją do szybkiego odróżniania alkoholi od fenoli. Fenol reaguje z wodorotlenkiem sodu obecnym w roztworze wodnym, podczas gdy alkohol takiej reakcji nie ulega.
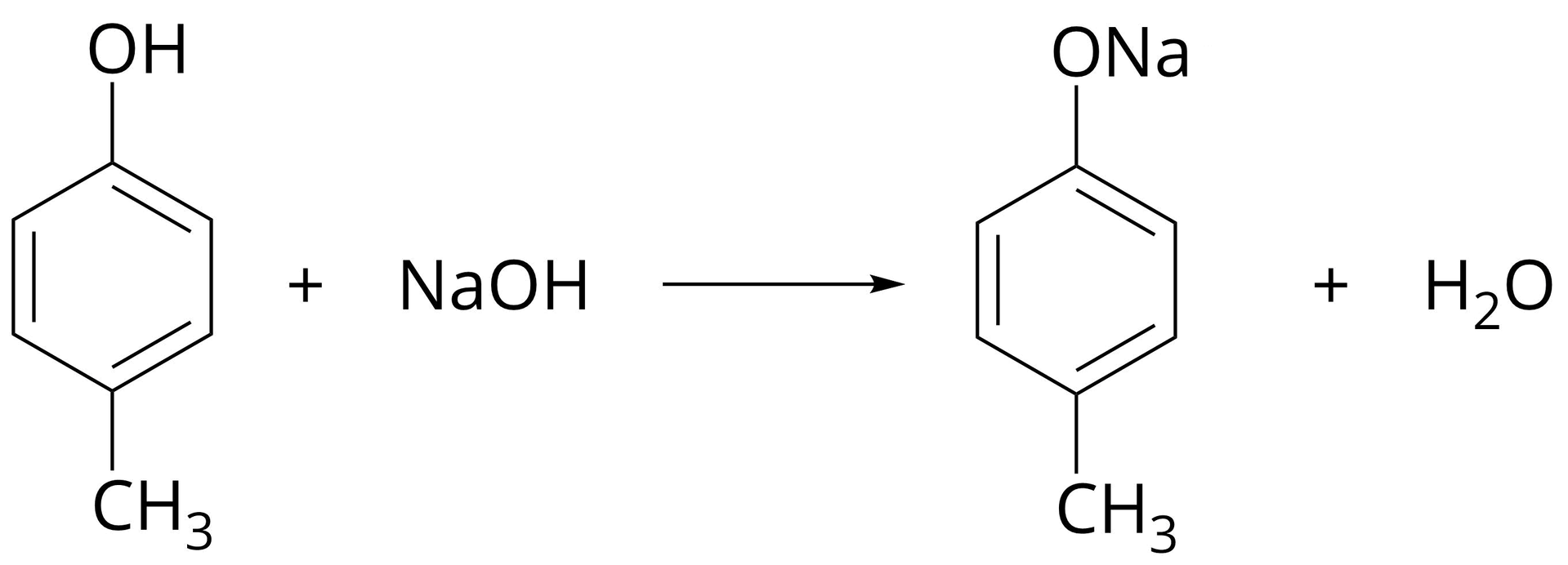
Poniżej przedstawiono wzory półstrukturalne dwóch związków chemicznych: fenylometanolu (alkoholu benzylowego) i -metylofenolu.
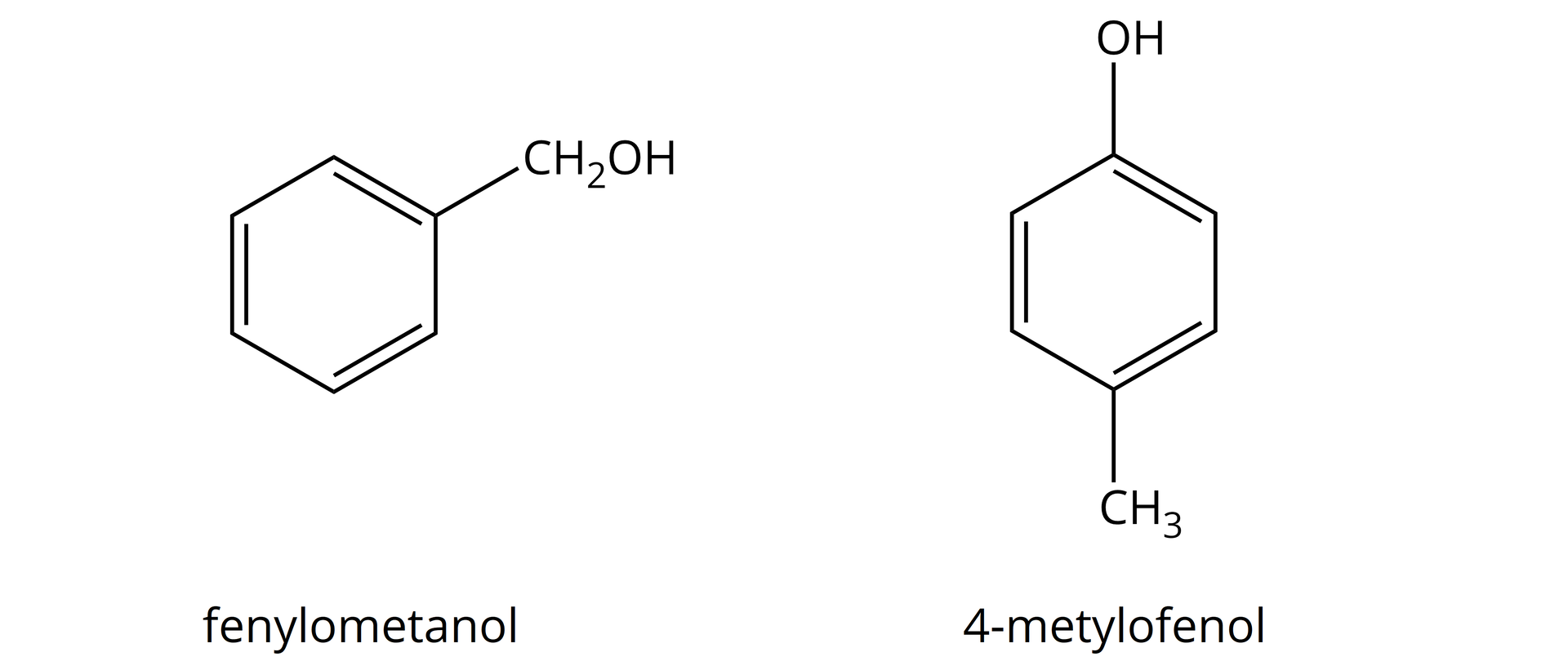
Wskaż, który z powyższych związków reaguje z wodnym roztworem wodorotlenku sodu i stosując zapis cząsteczkowy, napisz równanie odpowiedniej reakcji chemicznej.
Reakcja nitrowania
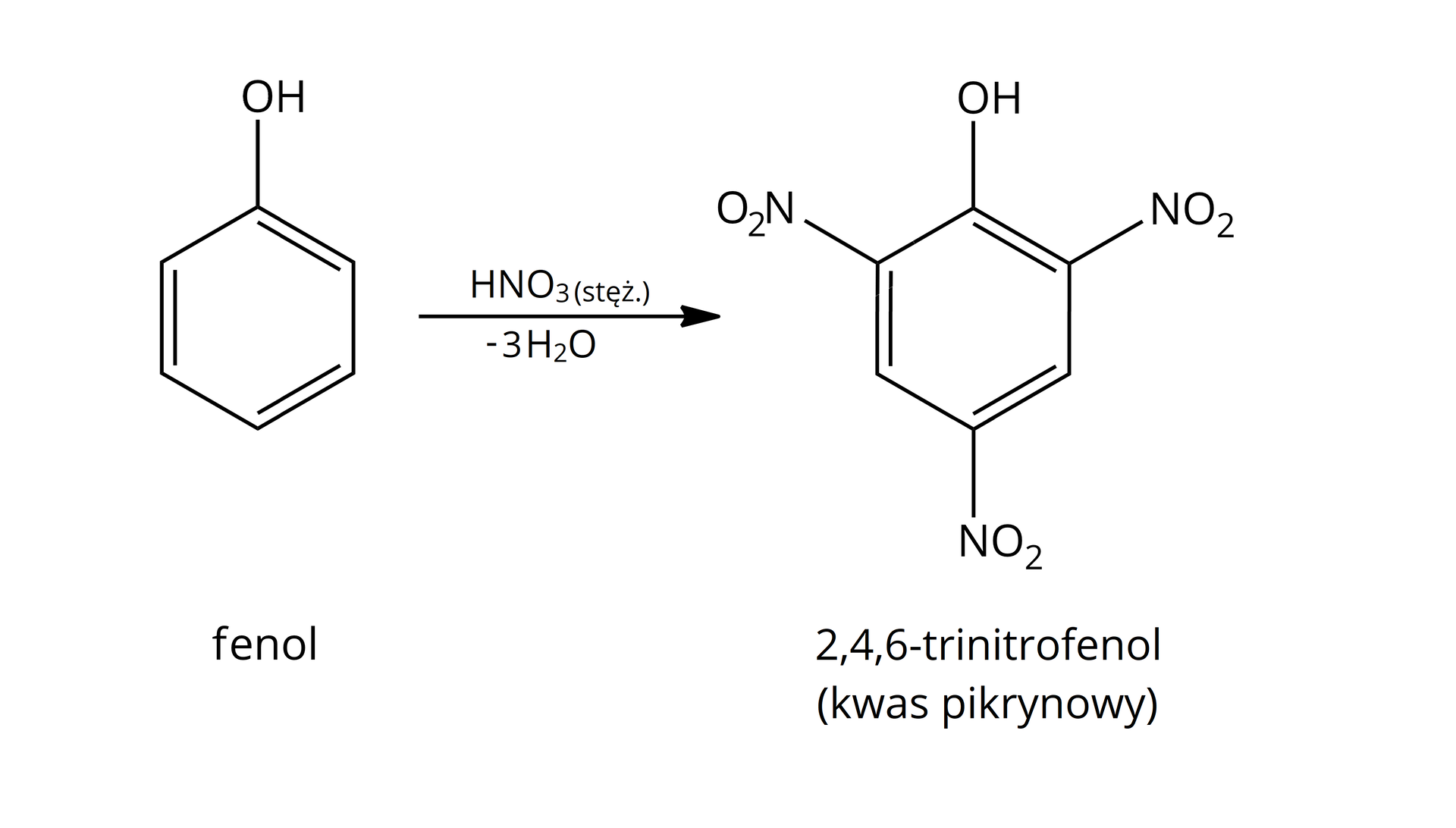
W reakcji nitrowania wykorzystuje się tzw. mieszaninę nitrującą – mieszankę stężonego kwasu azotowego i stężonego kwasu siarkowego. Składy mieszanin nitrujących mogą różnić się proporcjami użytych kwasów. Są one dobierane zależnie od reaktywności nitrowanego związku. Do nitrowania związków bardzo reaktywnych, do których należą m.in. fenole, można użyć tylko kwasu azotowego. Fenole są bardzo podatne na utlenianie, dlatego do ich nitrowania nie jest konieczne zastosowanie stężonego kwasu siarkowego.
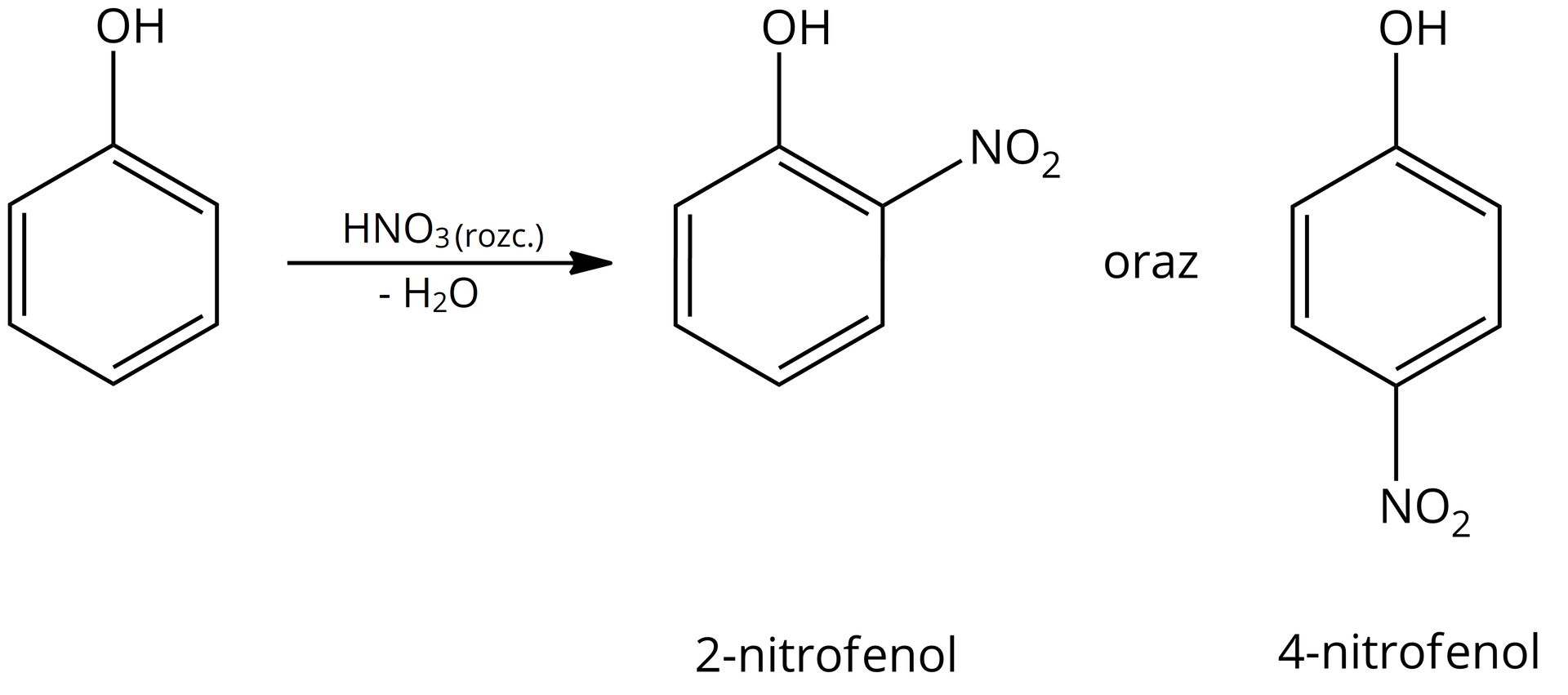
Podczas reakcji przeprowadzonej z rozcieńczonym kwasem azotowym(V) (np. czy ) tworzą się dwa produkty. Reakcja przebiega z małą wydajnością ze względu na uboczny proces utleniania fenolu przez kwas azotowy.
Reakcja fenolu z chlorkiem żelaza
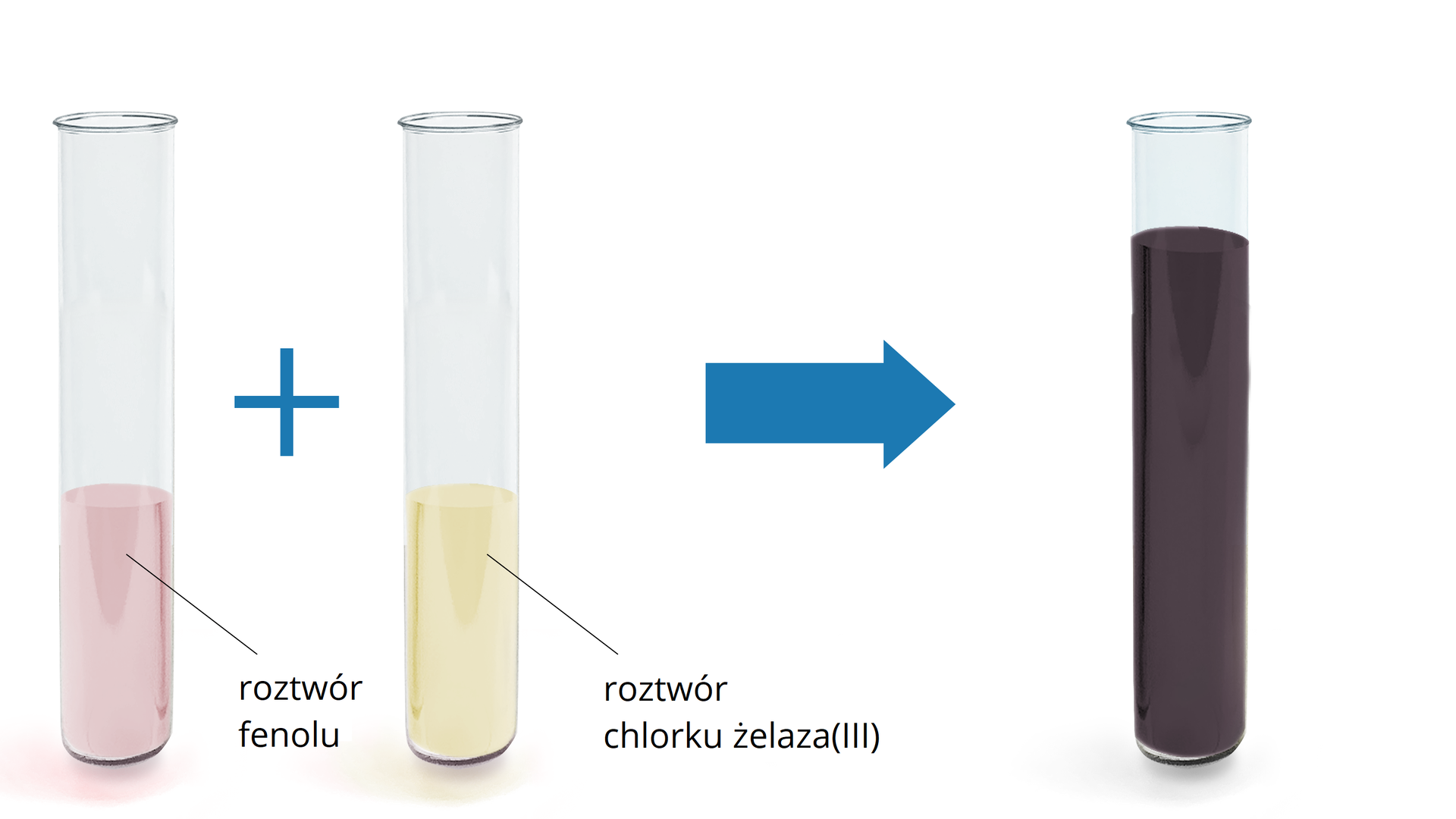
Reakcja z wodnym roztworem umożliwia wykrycie ugrupowania fenolowego w związku chemicznym. Związki aromatyczne zawierające grupę hydroksylową połączoną z pierścieniem, w reakcji z chlorkiem żelaza tworzą związki koordynacyjnej o charakterystycznej ciemnofioletowej barwie. Na barwę otrzymanego roztworu wpływa jednak stężenie .
Słownik
reakcja chem. polegająca na wprowadzeniu grupy nitrowej do cząsteczki związku org. w wyniku podstawienia atomu wodoru
związki organiczne, mono-, di- i polihydroksylowe pochodne benzenu oraz alkilobenzenów, których cząsteczki zawierają grupy hydroksylowe () związane z atomem węgla pierścienia benzenowego
Bibliografia
Dudek‑Różycki K., Płotek M., Wichur T., Węglowodory. Repetytorium i zadania, Kraków 2020.
Dudek‑Różycki K., Płotek M., Wichur T., Kompendium terminologii oraz nazewnictwa związków organicznych. Poradnik dla nauczycieli i uczniów, Kraków 2020.
encyklopedia PWN