Wirtualne laboratorium – I
Przeprowadź w wirtualnym laboratorium chemicznym doświadczenie na temat reaktywności fenoli. Zapisz swoje obserwacje i wyniki oraz sformułuj wnioski.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DhaNSv1eb
Przeprowadzono doświadczenie w laboratorium chemicznym. Zapoznaj się z opisem doświadczenia, a następnie wykonaj polecenia.
Analiza doświadczenia: Badanie reaktywności fenoli.
Problem badawczy: Czy fenol reaguje z wodorotlenkami, kwasami oraz metalami?
Hipoteza: Fenol reaguje z metalami aktywnymi i wodnymi roztworami ich wodorotlenków, z wodą bromową, kwasem azotowym oraz z chlorkiem żelaza.
Odczynniki:
fenol,
sód,
wodorotlenek sodu,
fenoloftaleina,
woda bromowa,
kwas azotowy roztwór jedno molowy,
kwas azotowy ,
chlorek żelaza.
Sprzęt laboratoryjny:
pręciki szklane – służą do mieszania cieczy;
łyżki laboratoryjne- długi trzonek wykonany ze szkła, porcelany lub metalu zakończony z jednej strony łyżeczką. Służy do nabierania sypkich substancji chemicznych;
pipety – wąskie rurki do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
palnik – rodzaj sprzętu z regulacją płomienia, umożliwiający podgrzewanie substancji chemicznych;
trójnóg laboratoryjny – urządzenie w kształcie pierścienia, zaopatrzone w trzy wkręcane nogi, mocowane prostopadle do jego powierzchni, służące do ustawiania nad palnikiem naczyń laboratoryjnych, przeznaczonych do podgrzania;
pęseta – narzędzie o sprężystych ramionach używane do chwytania przedmiotów, których mały rozmiar utrudnia lub uniemożliwia manipulację za pomocą rąk;
zlewka – naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych;
tryskawka z wodą destylowaną- plastikowe naczynie zamknięte nakrętką z długą końcówką. Tryskawka wypełniona jest wodą, która pod wpływem nacisku na plastikowe naczynie, uwalnia wodę na zewnątrz przez długą końcówkę.
Przebieg doświadczenia:
Do zlewki dodano około stu centymetrów sześciennych wody destylowanej oraz łyżeczkę fenolu, zamieszano szklanym pręcikiem i obserwowano rozpuszczanie w zimnej wodzie. Następnie delikatnie ogrzano zlewkę aż do rozpuszczenia fenolu.
Do pierwszej probówki wprowadzono roztwór fenolu oraz odrobinę sodu,
Do drugiej probówki dodano wodorotlenek sodu, kilka kropli fenoloftaleiny, do trzeciej wodę bromową, do czwartej rozcieńczony roztwór kwasu azotowego, do piątej stężony roztwór kwasu azotowego i do szóstej – wodny roztwór chlorku żelaza. Następnie do wszystkich probówek wprowadzono roztwór fenolu w wodzie.
Do wylotu probówki trzeciej zbliżono zwilżony papierek uniwersalny.
Obserwacje:
W zimnej wodzie fenol nie rozpuszcza się, a jego rozpuszczalność wzrasta ze wzrostem temperatury.
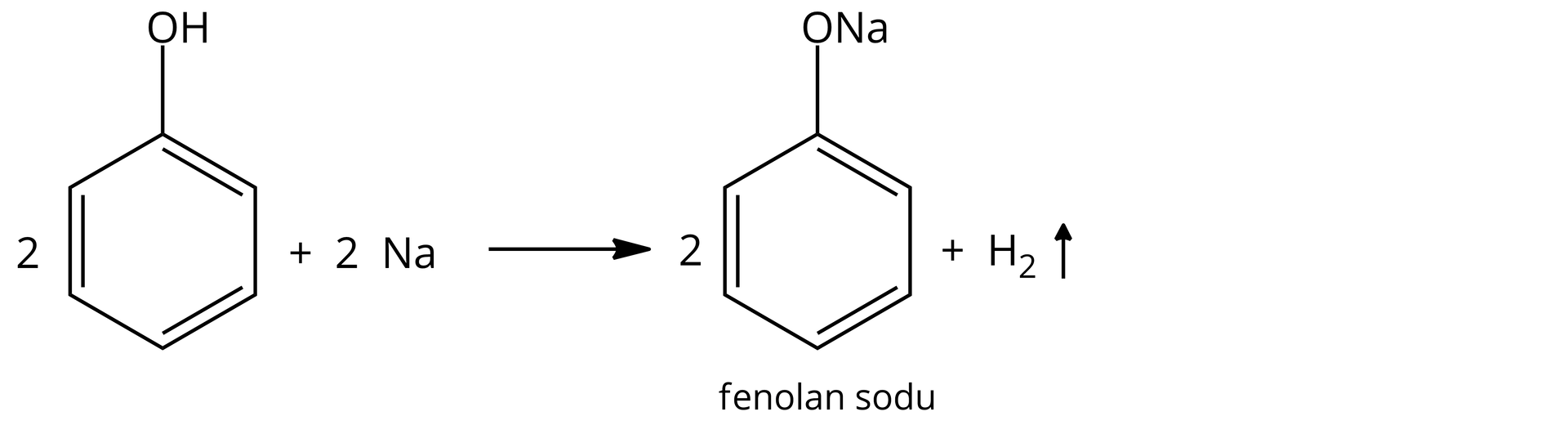
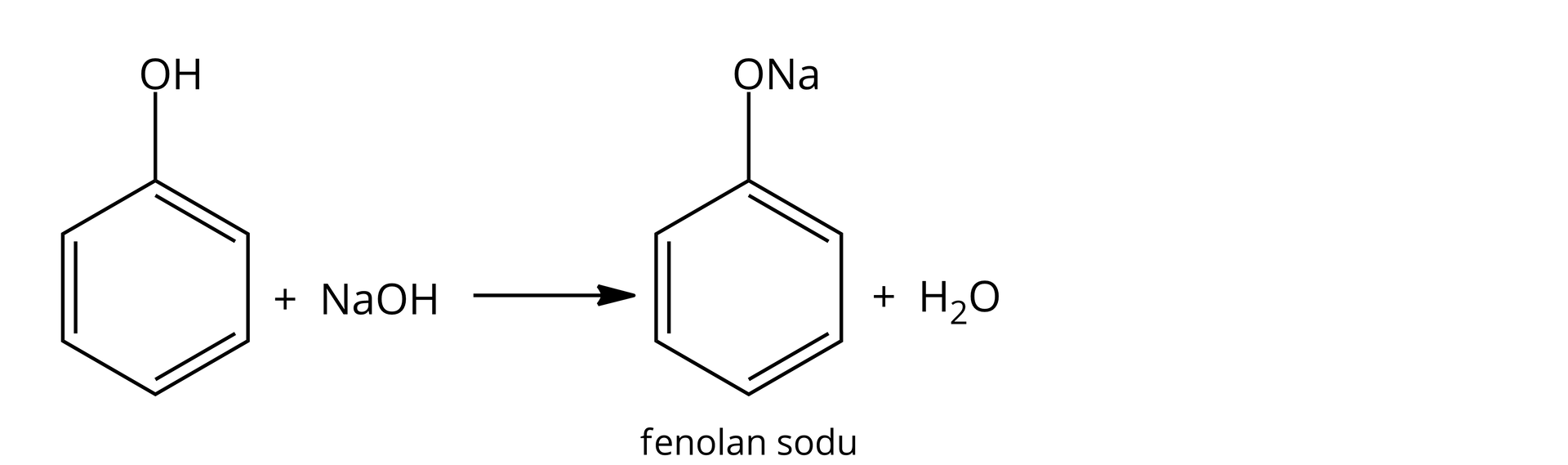
W probówce z sodem widoczne jest wydzielanie się bezbarwnego gazu oraz roztwarzanie metalu. Natomiast w probówce, w której do wody dodano stałą próbkę fenolu powstał mętny roztwór, który następnie po dodaniu wodnego roztworu wodorotlenku sodu stał się klarowny.
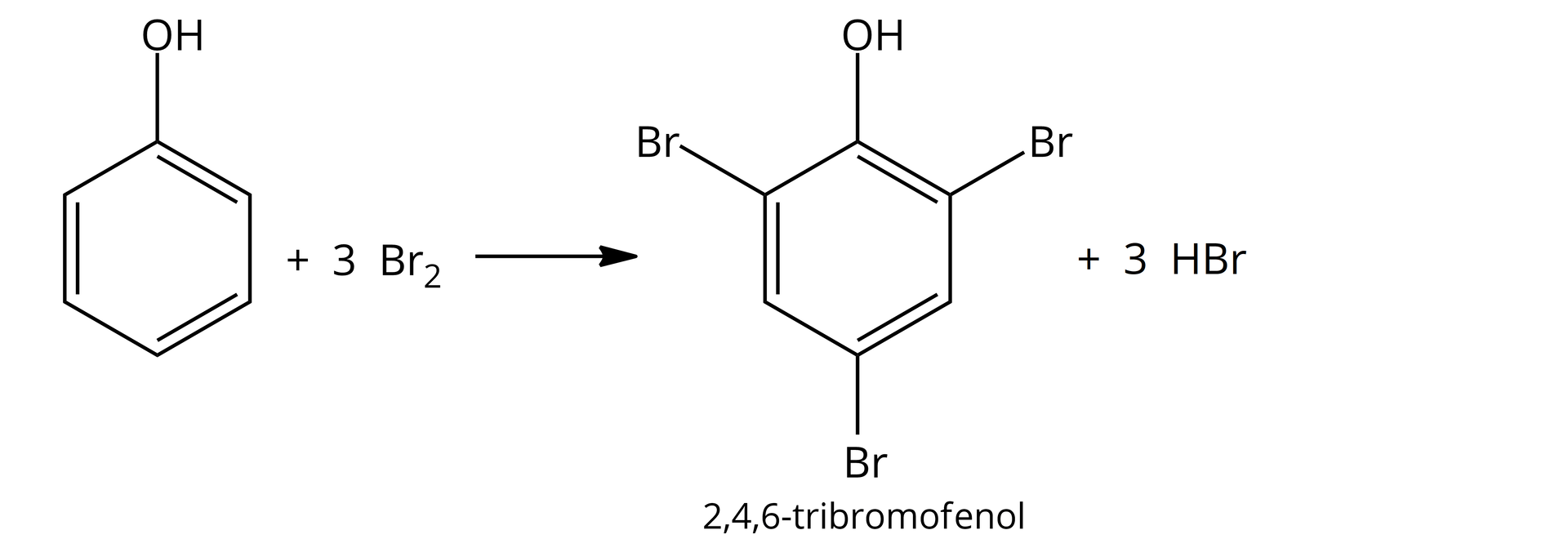
W trzeciej probówce nastąpiło odbarwienie wody bromowej i wytrącenie żółtego osadu. Po przyłożeniu zwilżonego wodą uniwersalnego papierka wskaźnikowego do wylotu probówki, papierek zabarwił się na czerwono.
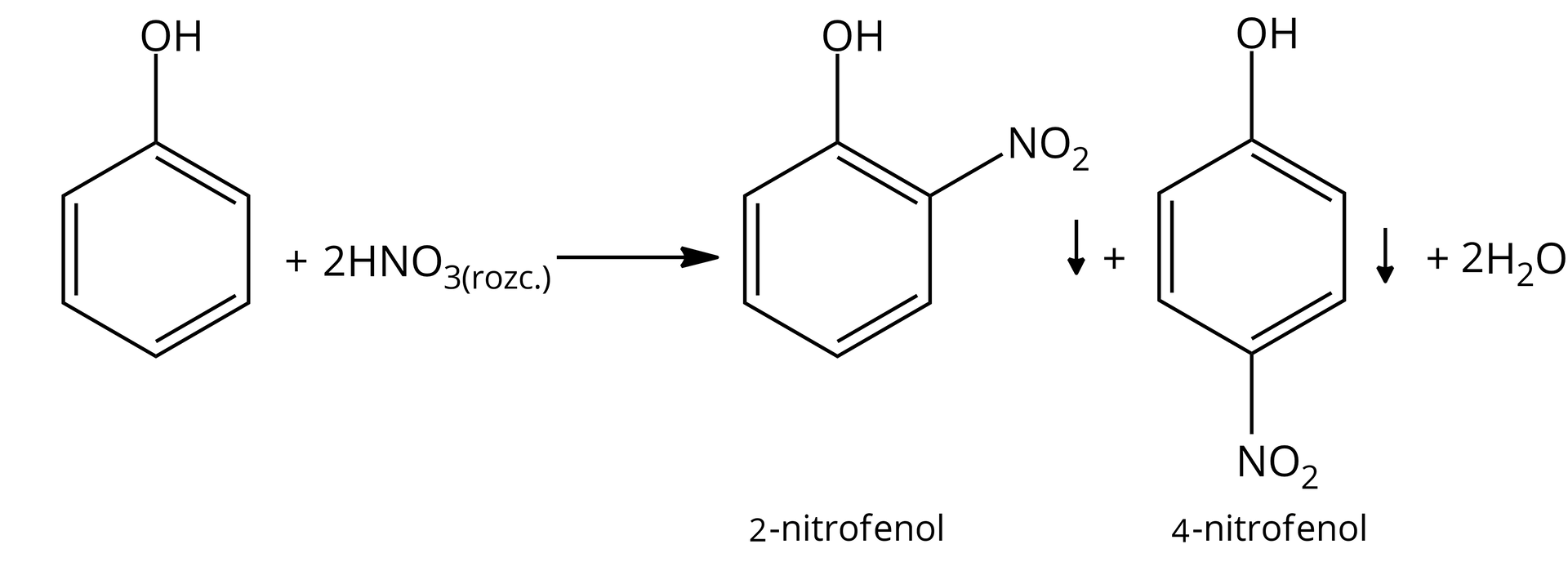
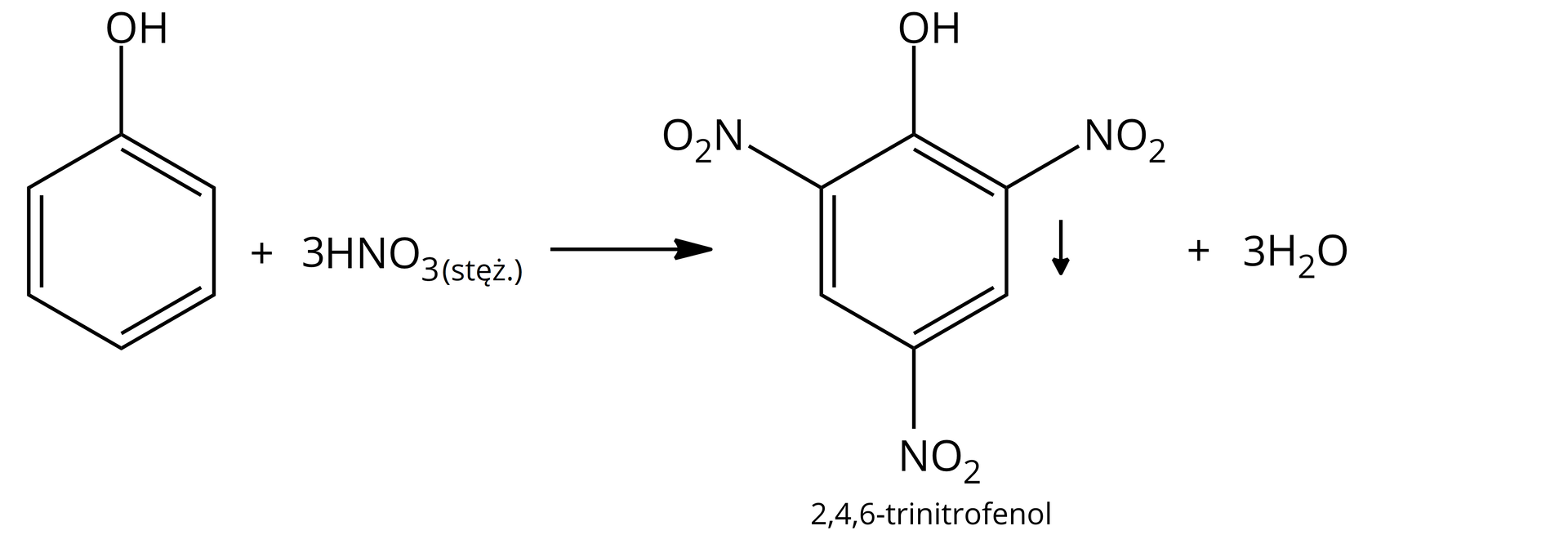
W probówce czwartej po dodaniu fenolu do rozcieńczonego kwasu azotowego powstał żółty osad w kształcie igieł, w piątej, po dodaniu fenolu do stężonego kwasu azotowego, powstał żółty osad w kształcie płatków. W probówce szóstej po dodaniu fenolu żółtopomarańczowy roztwór zmienił zabarwienia na cimnofioletowe. W zimnej wodzie fenol nie rozpuszcza się, a jego rozpuszczalność wzrasta ze wzrostem temperatury.
Wyniki:
Wykazano charakter kwasowy fenolu, przeprowadzając reakcje z sodem (podstawienie wodoru jonami metalu) oraz z wodorotlenkiem sodu. Fenol reaguje z rozcieńczonym i stężonym kwasem azotowym, wodą bromową, wchodząc w reakcje substytucji elektrofilowej oraz z solą żelaza z wytworzeniem barwnego kompleksu.
Wnioski:
Reakcja fenolu z wodą bromową i roztworami kwasu azotowego (rozcieńczonym i stężonym) jest reakcją substytucji elektrofilowej. W wyniku reakcji fenolu z wodnym roztworem chlorku żelaza tworzy się barwny związek kompleksowy. Fenol słabo rozpuszcza się w wodzie na zimno. Rozpuszczalność fenolu w wodzie rośnie wraz ze wzrostem temperatury. Fenol ulega reakcji z sodem, a wydzielającym się w reakcji gazem jest wodór. Fenol reaguje również z wodnym roztworem wodorotlenku sodu.