Przeczytaj
W jaki sposób roztworzyć miedź, srebro i złoto?
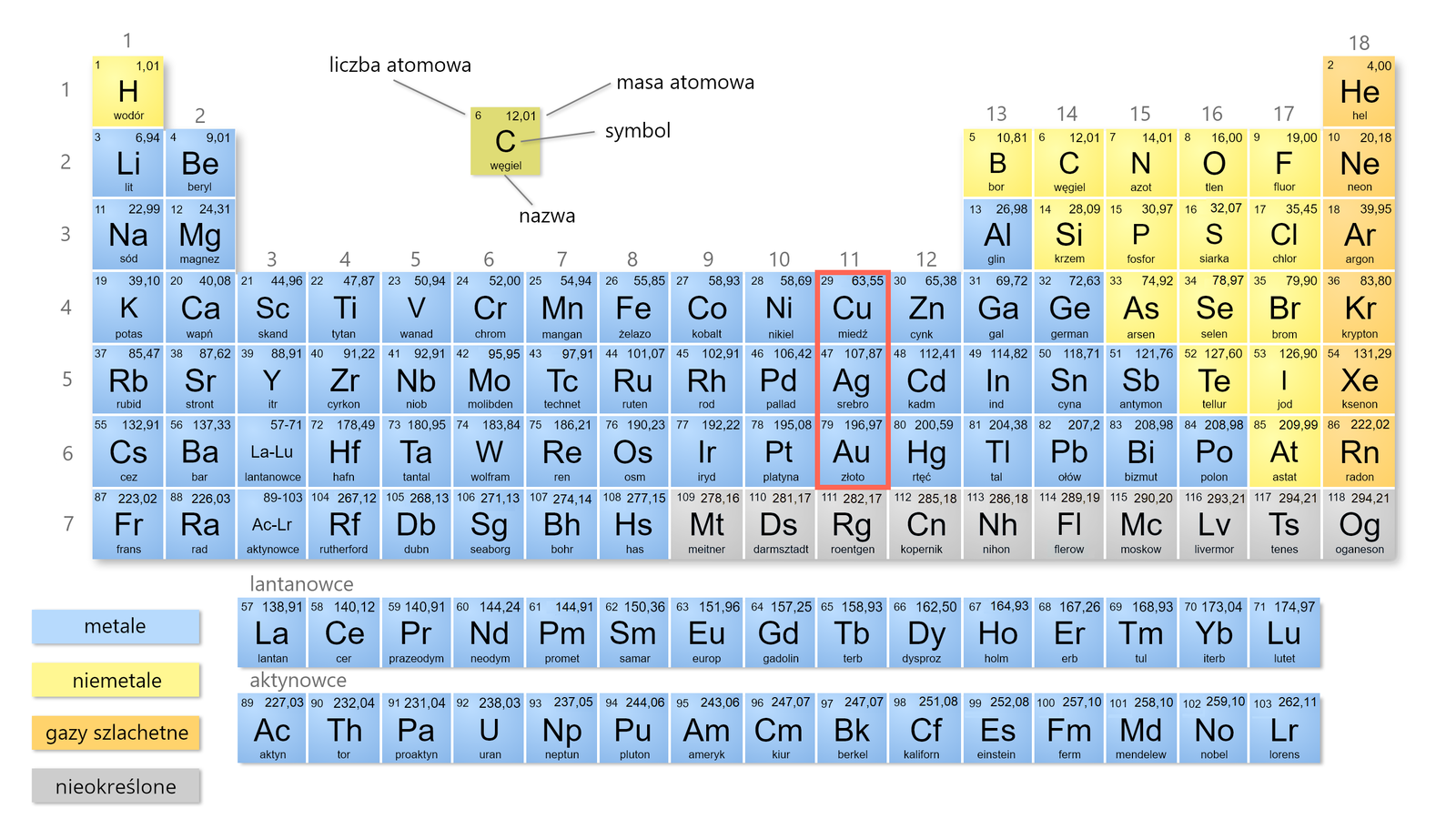
Miedź, srebro i złoto znajdują się w grupie układu okresowego. Miedź zaliczana jest do metali półszlachetnychmetali półszlachetnych, natomiast srebro i złoto do metali szlachetnychmetali szlachetnych. Pierwiastki te wykazują dodatnie potencjały standardowepotencjały standardowe, przez co nie reagują z kwasami, które nie wykazują silnych właściwości utleniających.
Reakcja połówkowa | Potencjał standardowy () |
Reakcje metali z kwasami nieutleniającymi zachodzą tylko wtedy, gdy ich potencjały standardowe są ujemne. W wyniku reakcji metalu o potencjale standardowym ujemnym z kwasem nieutleniającym wydziela się wodór, którego potencjał standardowy z zasady równy jest . Przykładem może być reakcja cynku z kwasem solnym.
Metale o dodatnich potencjałach standardowych mogą natomiast reagować tylko z kwasami utleniającymi. W wyniku reakcji metalu, o dodatnim potencjale standardowym z kwasem utleniającym, metal utlenia się, natomiast reszta kwasowa redukuje się do odpowiednich tlenków.
Porównując potencjały standardowe, możemy zauważyć, że reaktywność miedziowców maleje w dół grupy. Tłumaczy to również zaliczenie miedzi do grupy metali półszlachetnych.
Jednym z najsilniejszych nieorganicznych kwasów utleniających jest kwas azotowy() –
W wyniku reakcji rozcieńczonego z metalami zachodzi następująca reakcja chemiczna:
Reakcja połówkowa | Potencjał standardowy () |
W przypadku zastosowania stężonego kwasu azotowego(), jako produkt redukcji powstawałby tlenek azotu(). Potencjał standardowy takiej reakcji wynosi . Redukcja atomu azotu może również prowadzić do powstania azotu cząsteczkowego lub jonów amonowych.
Jak łatwo zauważyć, potencjał standardowy powyższej reakcji jest równy , więc jest on wyższy niż potencjał standardowy dla miedzi czy srebra. Dlatego też kwas azotowy() może reagować z metaliczną miedzią (), jak i metalicznym srebrem (). Potencjał standardowy złota jest zdecydowanie wyższy
(), przez co złoto nie będzie reagowało z kwasem azotowym(). Należy jednak pamiętać, że potencjały standardowe zależą od stężeń reagentów i mogą się wraz z nimi zmieniać.
Rozpatrzmy to na przykładzie:
Zapisz w formie cząsteczkowej równanie reakcji srebra z rozcieńczonym kwasem azotowym().
Co to jest woda królewska?
Złoto można roztworzyćroztworzyć w tzw. wodzie królewskiej. Woda królewska (z łaciny „aqua regia” – oznacza dosłownie wodę królewską. Woda królewska wywodzi swoją nazwę od alchemików, którzy opracowali roztwór, będący w stanie roztworzyć metale szlachetne. Jest to mieszanina stężonych kwasów – solnego (chlorowodorowego) i azotowego() w stosunku , a więc objętości stężonego kwasu chlorowodorowego i objętość stężonego kwasu solnego. Woda królewska wykazuje silne właściwości utleniające, przez co może roztwarzać większość metali w układzie okresowym już w warunkach temperatury pokojowej.

Reakcja chemiczna pomiędzy złotem a wodą królewską, w zależności od źródła, może zachodzić na różne sposoby. Poniżej przedstawiono dwa z nich:
lub:
Reakcja połówkowa | Potencjał standardowy () |
Porównując potencjały standardowe, możemy zauważyć, że roztwarzanie złota w wodzie królewskiej jest termodynamicznie preferowane. W wyniku tej reakcji chemicznej powstaje anion kwasu tetrachlorozłotowego() – , tlenek azotu() oraz woda.
Dlatego też, wracając do pytania zawartego we wstępie, złoto jest wysoce stabilnym i niskoreaktywnym metalem. Roztwarza się w wodzie królewskiej. Złoto na skórze mogłoby ulegać reakcji utleniania tylko wtedy, gdyby nasze komórki potowe wytwarzałyby właśnie wodę królewską. Starszy jubiler wiedział, że najprawdopodobniej biżuteria podarowana kobiecie nie była do końca czystym złotem. Podobnie do złota, dopiero z wodą królewską reaguje inny metal szlachetny – platyna.
Słownik
przechodzenie substancji stałej do roztworu w wyniku zachodzącej reakcji chemicznej
siła elektromotoryczna, wytworzona przez metal zanurzony w roztworze swojej soli względem elektrody wodorowej, której potencjał standardowy równy jest ; potencjał można określić standardowym, jeżeli stężenie jonu wynosi
zwyczajowa nazwa metali będących wysoce odpornych chemicznie; zalicza się do nich: ruten, rod, pallad, platynę, osm, iryd, srebro i złoto; są to metale, które mają dodatni potencjał standardowy
metale o niskiej reaktywności, jednakże wyższej niż metale szlachetne; są to metale, które mają dodatni potencjał standardowy
Bibliografia
Bielański A., Podstawy chemii nieorganicznej, t. 2, Warszawa 2012.
Encyklopedia PWN
Harris H. H., Is it real gold?, „Journal of Chemical Education”, t. 76, nr 2, 1999.