Przeczytaj
Estry kwasów nieorganicznych
Estrami kwasów nieorganicznych nazywamy związki powstające w wyniku reakcji alkoholi i kwasów nieorganicznych. Przykładami kwasów, które wchodzą w skład estrów, są:
kwas siarkowy(),
kwas azotowy(),
kwas ortofosforowy(),
kwas borowy.
W zależności od ilości atomów wodoru, wchodzących w skład cząsteczki kwasu, kwas może reagować z jedną, dwoma lub trzema cząsteczkami alkoholu.
Estry kwasu siarkowego()
Wzór ogólny estrów kwasu siarkowego():

Przykładowa reakcja otrzymywania estru kwasu siarkowego():

Wodorosiarczany() i siarczany() alkilowe (metylowy i etylowy) są silnymi truciznami.
Estry kwasu azotowego()
Wzór ogólny estrów kwasu azotowego():

Przykładowa reakcja otrzymywania estru kwasu azotowego():

Opary azotanu() metylu są skrajnie łatwopalne i silnie wybuchowe. Opary lub kontakt cieczy ze skórą skutkuje szybkim spadkiem ciśnienia krwi i dotkliwym bólem głowy.
Estry kwasu ortofosforowego()
Wzór ogólny estrów kwasu fosforowego():

Przykładowa reakcja otrzymywania estru kwasu ortofosforowego():

Proste fosforany organiczne wykazują często silne właściwości toksyczne.
Estry kwasu ortofosforowego() to jednocześnie istotne związki biologiczne. Przykładem jest kwas deoksyrybonukleinowy DNA. W jego nukleotydzie wiązanie estrowe znajduje się pomiędzy resztą kwasu ortofosforowego() a cukrem, zwanym -deoksyrybozą. Natomiast w kwasie rybonukleinowym RNA wiązanie estrowe jest pomiędzy resztą kwasu ortofosforowego() a cukrem, zwanym rybozą.

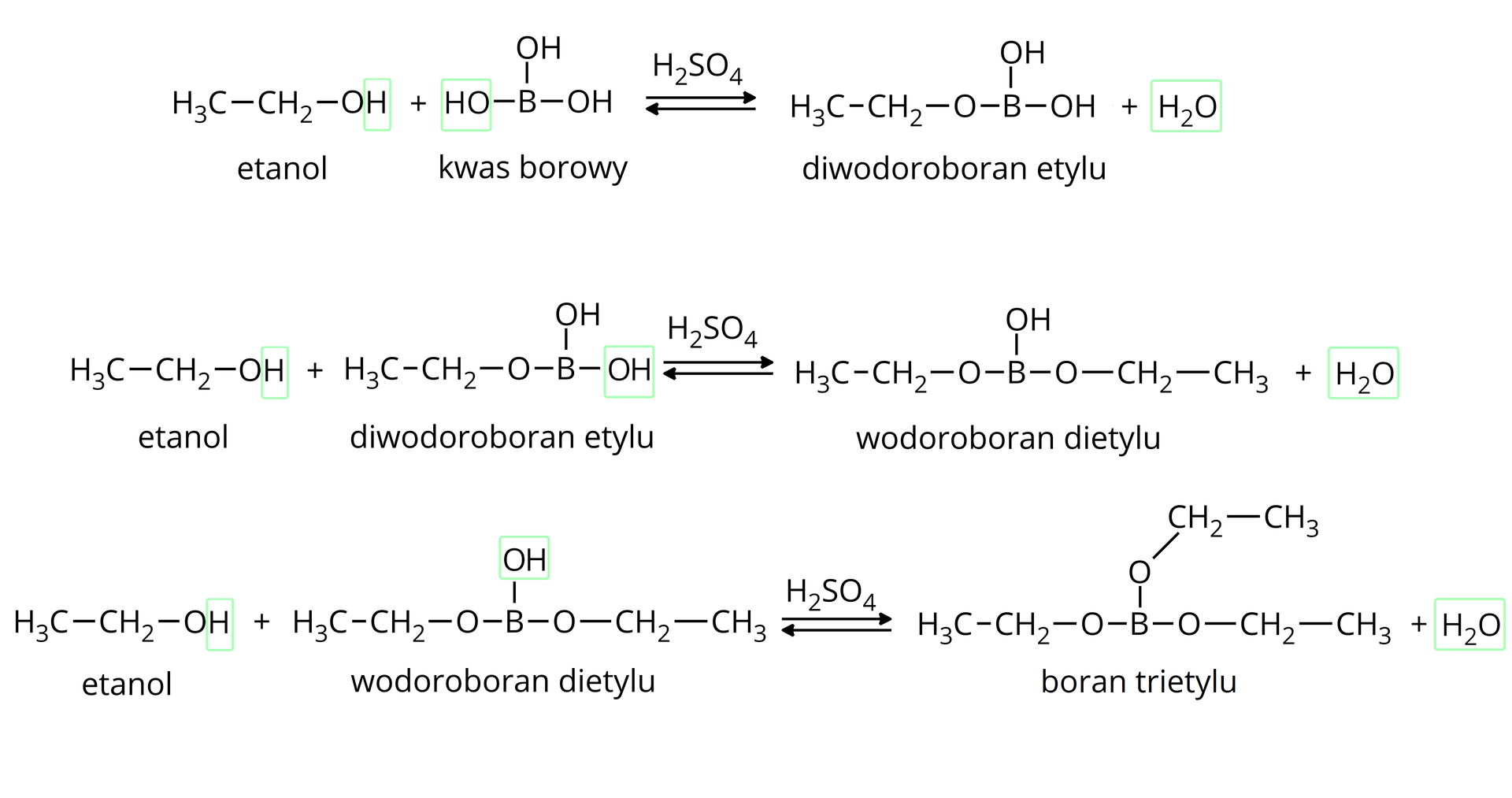
Estry kwasu borowego
Wzór ogólny estrów kwasu borowego:

Przykładowa reakcja otrzymywania estru kwasu borowego:
Boran trietylu barwi płomień palnika na kolor zielony.
Triazotan()-propano‑,,‑triolu, triazotan() glicerolu, TNG, nitrogliceryna
Jest to oleista ciecz, która charakteryzuje się słodkawym, piekącym smakiem. Nie występuje naturalnie w środowisku. Stosowana jest jako materiał wybuchowy. Związek ten jest bardzo wrażliwy na uderzenia i wstrząsy. Ulega hydroliziehydrolizie i rozkładowi termicznemu. Wykorzystywany jest do leczenia napadów bólu w chorobie wieńcowej, a jego działanie polega na rozszerzeniu światła naczyń krwionośnych.

EstryEstry kwasów nieorganicznych występują w organizmach żywych. Znalazły również zastosowanie w przemyśle. Ten najbardziej znany jest wykorzystywany do produkcji dynamitudynamitu – mowa tu o triazotan()-propano-,,-triolu, potocznie nazywanym nitrogliceryną. Z jednej strony może uratować komuś życie, a z drugiej je odebrać. Ważna jest nasza świadomość dotycząca właściwości poszczególnych związków chemicznych i ich mądrego wykorzystania.
Słownik
rodzaj materiału wybuchowego, wynaleziony przez Alfreda Nobla; zgłoszony do urzędu patentowego i opatentowany w roku; w wersji opatentowanej zawierał triazotanu()-propano-,,-triolu oraz ziemi okrzemkowej
grupa organicznych związków chemicznych, będących produktami kondensacji kwasów (karboksylowych lub nieorganicznych) i alkoholi lub fenoli; charakteryzują się występowaniem grupy estrowej
reakcja chemiczna, w której powstają estry; przykłady niektórych sposobów otrzymywania estrów:
przez substytucję nukleofilową chlorków lub bezwodników kwasowych alkoholami
przez substytucję nukleofilową kwasów karboksylowych alkoholami (katalizator kwas nieorganiczny)
grupa funkcyjna, charakterystyczna dla organicznych związków chemicznych, zwanych estrami

reakcja zachodząca pomiędzy substancją rozpuszczoną a rozpuszczalnikiem (w tym przypadku wodą); ulegają jej związki organiczne i nieorganiczne
Bibliografia
Berg J., Stryer L., Tymoczko J. L., Biochemia, Warszawa 2005.
Ćwiczenia z biochemii, praca zbiorowa pod red. L. Kłyszejko‑Stefanowicz, Warszawa 2003.
Driver P. S., Jarvi E. J., Grater P. L., Stability of nitroglycerin as nitroglycerin concentrate for injection :d in plastic syringes, „Am. J. Health Syst. Pharm.” 1993, s. 50‑2563.
EPA Method 8330B (SW‑846): Nitroaromathics, Nitramines, and Nitrate Estersby High Performance Liquid Chromatography (HPLC) [w:] United States Environmental Protection Agency 2006.
Maranda A., i in., Podstawy chemii materiałów wybuchowych, Warszawa 1997.
Korzun M., 1000 słów o materiałach wybuchowych i wybuchu, Warszawa 1986, s. 73.
Kowalska J., Triazotan()-propano-,,-triylu. Zastosowanie chromatografii gazowej z detektorem wychwytu elektronów w analizie próbek powietrza, „Podstawy i Metody Oceny Środowiska Pracy”, 2013, t. 78, nr 4, s. 135‑148.
Kączkowski J, Podstawy biochemii, Warszawa 2005.
Praktikum z biochemii, praca zbiorowa pod red. A. Dubina i B. Turyny, Kraków 1999.
Biochemia. Kwasy nukleinowe. Izolacja oraz badanie właściwości fizycznych i chemicznych. Ćwiczenie 10. Kwas deoksyrybonukleinowy (DNA). Ćwiczenie 11. Kwas rubonukleinowy (RNA), online: https://cbimo.zut.edu.pl/fileadmin/pliki/cbimo/grafika/Kwasy_nukleinowe.pdf, dostęp: 05.07.2021.