Przeczytaj
Czy amidy ulegają hydrolizie?
AmidyAmidy to organiczne związki chemiczne, będące pochodnymi kwasów karboksylowych, w których grupa hydroksylowa () została zastąpiona grupą , przy czym to atomy wodoru, grupy węglowodorowe lub inne dowolne grupy organiczne.
Wzór ogólny | Rzędowość | Grupa funkcyjna |
|---|---|---|
 | Pierwszorzędowe (‑rzędowe, ). Mające jedną grupę acylową przy atomie azotu. 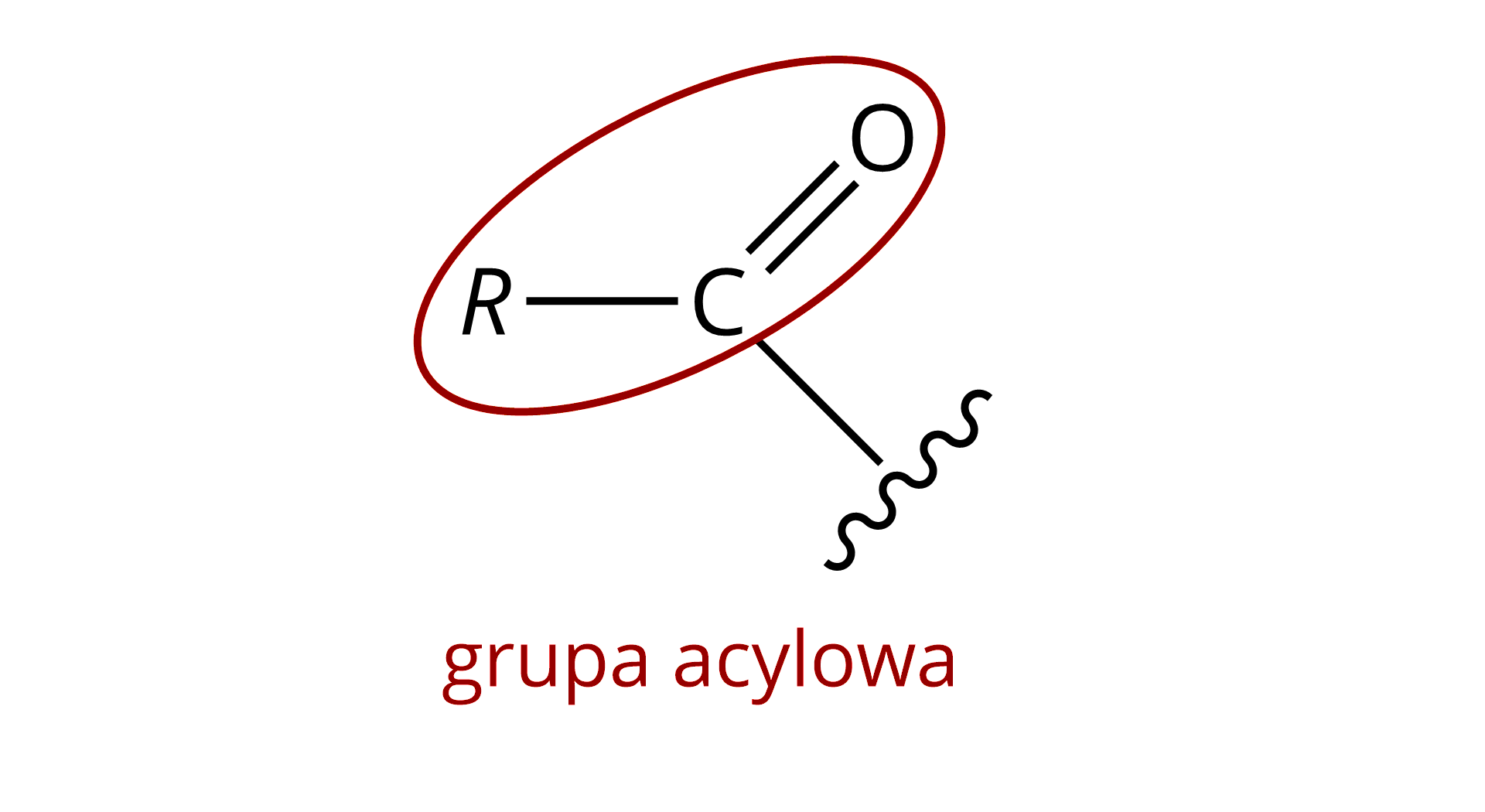 |  |
 | Drugorzędowe (‑rzędowe, ). Mające dwie grupy acylowe przy atomie azotu. Są to inaczej imidy.  |  |
 | Trzeciorzędowe (‑rzędowe, ). Mające trzy grupy acylowe przy atomie azotu. Są to inaczej triacyloiminy.  |  |
Tabela rzędowości amidów
Indeks dolny Źródło: GroMar Sp. z o.o., licencja: CC BY‑SA 3.0. Indeks dolny koniecŹródło: GroMar Sp. z o.o., licencja: CC BY‑SA 3.0.
Grupa acylowa w amidach wywiera silny efekt indukcyjny, dlatego gęstość elektronowa na atomie azotu jest niższa niż w pozornie podobnych aminach. Amidy nie są zdolne do przyłączenia protonu (kationu wodoru), z czym wiąże się ich odczyn obojętny oraz stosunkowo niska reaktywność.


Film dostępny pod adresem /preview/resource/RmrAkzQ5UT1lf
Film przedstawia wizualizację efektu indukcyjnego w cząsteczce metanoamidu.
Amidy ulegają reakcjom hydrolizy w wyniku ogrzewania w wodnym roztworze kwasu lub zasady. Poniżej zapisano równania reakcji chemicznych hydrolizy amidów na przykładzie etanoamidu (acetamidu).
Hydroliza kwasowa etanoamidu
Jest to reakcja, w której powstaje kwas karboksylowy oraz sól amonowa. Mechanizm tej reakcji polega na addycjiaddycji cząsteczki wody do protonowanego amidu. W wyniku reakcji następuje odszczepienie kationu amonowego.

W pierwszym etapie cząsteczka amidu zostaje aktywowana przez protonowanie karbonylowego atomu tlenu, dzięki czemu w drugim etapie następuje addycja nukleofilowaaddycja nukleofilowa cząsteczki wody. Wówczas tworzy się tetraedryczny produkt pośredni, a w trzecim etapie następuje przeniesienie kationu wodoru od przyłączonej cząsteczki wody na atom azotu. Eliminacja kationu amonu w czwartym etapie prowadzi do otrzymania produktu końcowego, czyli kwasu karboksylowego.

Hydroliza zasadowa etanoamidu
Jest to reakcja, w której powstaje amoniak oraz sól kwasu karboksylowego, od którego pochodzi amid.

Mechanizm tej reakcji polega na addycji nukleofilowej grupy hydroksylowej do karbonylowego atomu węgla grupy amidowej, co ma miejsce w pierwszym etapie reakcji. W drugim zaś następuje przegrupowanie wiązań i eliminacja anionu amidkowego () oraz utworzenie kwasu karboksylowego, który ulega deprotonacji w trzecim etapie. Powstający proton łączy się z jonem amidkowym, tworząc cząsteczkę amoniaku.

Hydroliza mocznika (karbamidu, diamidu kwasu węglowego)
Analizując reakcje hydrolizy kwasowej i zasadowej amidów, należy pamiętać o szczególnym przedstawicielu amidów, czyli mocznikumoczniku. Ponieważ jest to diamid kwasu węglowego, to w reakcji hydrolizy kwasowej powstaje tlenek węgla() pochodzący z nietrwałego kwasu węglowego.
Z kolei w reakcji hydrolizy zasadowej powstaje sól kwasu węglowego – węglan.


Inne reakcje amidów
Hydroliza amidów, w których atomy wodoru grupy aminowej zostały zastąpione grupami węglowodorowymi zachodzi równie łatwo pod wpływem kwasów jak i zasad, prowadząc do otrzymania m.in. amin - i -rzędowych.
Hydroliza N‑metyloetanoamidu
W wyniku hydrolizy kwasowej powstaje kwas etanowy (octowy) oraz chlorek metyloamoniowy, a w wyniku hydrolizy zasadowej powstaje etanian sodu (octan sodu) oraz metyloamina.

Hydroliza N,N‑dimetyloetanoamidu
W wyniku hydrolizy kwasowej powstaje kwas octowy oraz chlorek dimetyloamoniowy, natomiast w wyniku hydrolizy zasadowej powstaje etanian sodu oraz dimetyloamina.

Hydroliza amidów kwasem azotowym()
Ta reakcja nie jest często realizowana. Dzięki niej powstaje kwas karboksylowy, woda oraz wydziela się azot.

Przegrupowanie Hoffmana
Do przegrupowania Hoffmana dochodzi, gdy do amidu i zasadę. Końcowym etapem reakcji jest dekarboksylacja, a schematycznie można tę reakcję przedstawić na przykładzie acetamidu.

W wyniku reakcji powstają aminy I‑rzędowe.
Słownik
pochodne kwasów organicznych, w których cząsteczkach grupa hydroksylowa została zastąpiona (podstawiona) grupą aminową
grupa funkcyjna, powstająca przez oderwanie grupy hydroksylowej, zazwyczaj od cząsteczki kwasu karboksylowego

pochodne amidów, w których jedną z grup funkcyjnych przy atomie azotu grupy jest grupa acylowagrupa acylowa
pochodne amidów, w których przy atomie azotu występują trzy grupy acylowegrupy acylowe
reakcja chemiczna, polegająca na przyłączeniu jednej cząsteczki do drugiej, w wyniku czego powstaje tylko jeden produkt, bez żadnych produktów ubocznych
reakcja chemiczna typu addycji, polegająca na przyłączeniu reagenta nukleofilowego (drobina o nadmiarze elektronów) do wiązania wielokrotnego substratu.
związek organiczny o wzorze , diamid kwasu węglowego
Bibliografia
R. T. Morrison, R. N. Boyd, Chemia organiczna, Warszawa 1985.
J. McMurry, Chemia organiczna, Warszawa 2000.
J. McMurry, Chemia organiczna, Warszawa 2016.
W. Danikiewicz, Chemia organiczna, t. 3, Warszawa 2009.