Przeczytaj
AminokwasyAminokwasy, ze względu na obecność w cząsteczkach grupy karboksylowej i grupy aminowej, mogą się ze sobą łączyć w tzw. reakcji kondensacji aminokwasów. PolipeptydyPolipeptydy oraz białkabiałka są polimerami zbudowanymi ze skondensowanych reszt aminokwasowych.
Jeśli poddamy aminokwasy z dwoma reaktywnymi grupami funkcyjnymi (aminową i karboksylową) reakcji kondensacji, możemy otrzymać różne polipeptydy o tym samym składzie aminokwasowym, ale różnej ich kolejności. Na przykład poddając kondensacji sześć różnych aminokwasów, możemy otrzymać różnych heksapeptydów ().
Wykrywanie białek
Reakcja biuretowa

Polega na reakcji jonów w środowisku zasadowym z roztworem białkabiałka, w wyniku czego tworzą się związki, które barwią roztwór na kolor fioletowy.
Pozytywny wynik reakcji biuretowej świadczy o obecności w badanej próbce co najmniej dwóch wiązań peptydowych, które występują bezpośrednio obok siebie lub przedzielonych maksymalnie jednym atomem węgla.
Nazwa testu pochodzi od najprostszego związku, który ulega reakcji – biuretu. Alternatywna nazwa – reakcja Piotrowskiego lub odczyn Piotrowskiego – pochodzi od nazwiska polskiego fizjologa Gustawa Piotrowskiego, który opisał ją w roku.
Reakcja ksantoproteinowa
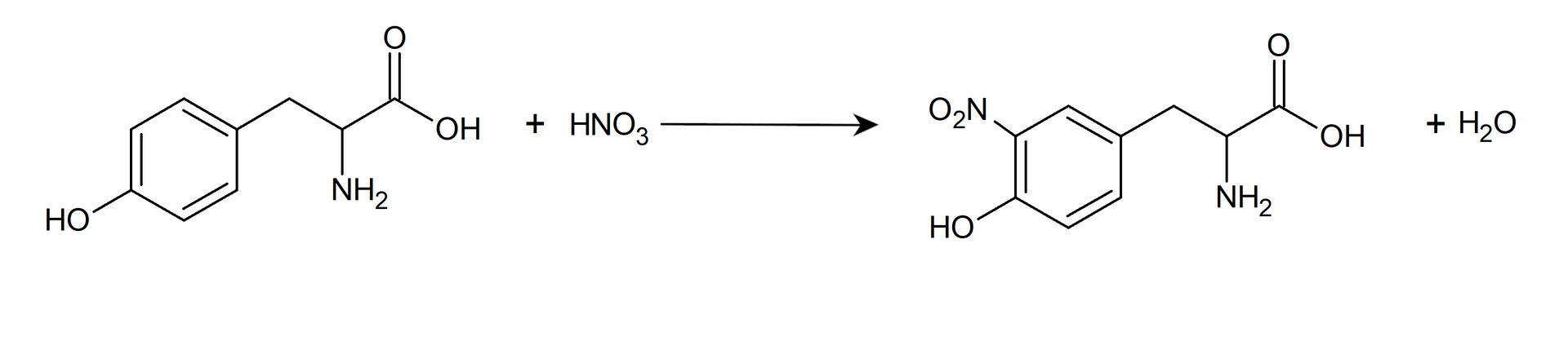
Polega na działaniu stężonym na białko. Pod wpływem tego kwasu tworzą się pochodne, które mają żółte zabarwienie.

Pozytywny wynik reakcji ksantoproteinowej dają białka, które posiadają w swojej cząsteczce reszty aminokwasów aromatycznych (fenyloalaniny, tryptofanu, tyrozyny). Podczas reakcji dochodzi do nitrowania aromatycznych reszt aminokwasowych, co prowadzi z kolei do powstania żółtego zabarwienia.
Reakcja cystynowa
Test ten polega na wykrywaniu w białkach reszt aminokwasowych, które zawierają siarkę (reszt cystyny i cysteiny), w reakcji z azotanem() ołowiu() lub etanianem (octanem) ołowiu(), po wcześniejszym przeprowadzeniu siarki z grupy tiolowej .

W wyniku powyższej reakcji otrzymujemy siarczek sodu, który reaguje z jonami ołowiu(), powodując wytrącenie się czarnego osadu siarczku ołowiu().


Reakcja ninhydrynowa
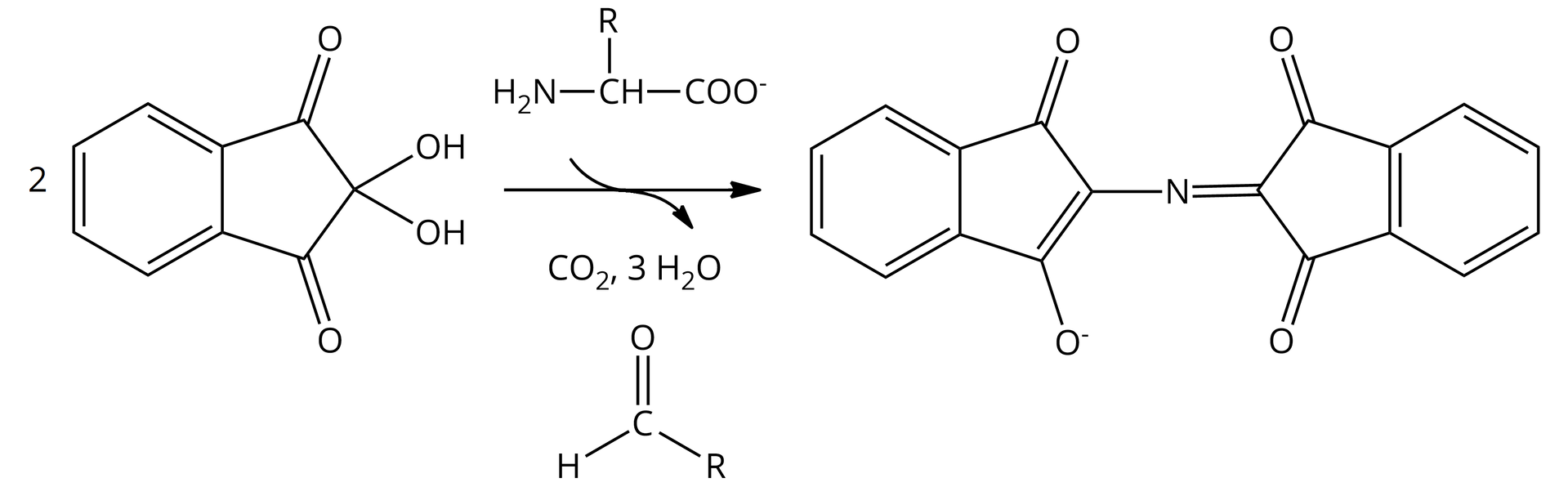
Próba ninhydrynowa polega na wykrywaniu wolnych grup aminowych w aminokwasach, ale także peptydach i białkach w reakcji z ninhydryną. W efekcie otrzymujemy roztwór o barwie niebieskofioletowej. Związek odpowiedzialny za tę barwę nazywamy „purpurą Ruhemanna”. Pozytywny wynik tego testu można otrzymać, badając również sole amonowe, aminocukry i amoniak.
Zobacz, jak wykryć obecność białka w produktach spożywczych
Zapoznaj się z poniższym filmem, a następnie wypełnij dokumentację doświadczenia.

Film dostępny pod adresem /preview/resource/R1KqvLWhsTUkA
Film dotyczy wykrywania obecności białka w produktach spożywczych. Na szalkach Petriego znajdują się: jogurt, kawałek chleba, banana, jabłka, plasterek szynki, białko jaja kurzego, twaróg, plasterek ziemniaka. Na każdy produkt osoba wykonująca doświadczenie daje kilka kropli kwasu azotowego. Na żółto zabarwiły się wszystkie produkty.
Słownik
związki chemiczne często obecne w organizmach żywych; zbudowane z co najmniej jednej grupy karboksylowej () oraz grupy aminowej ()
znane również pod nazwą: proteiny; są to wielkocząsteczkowe związki chemiczne, w których skład wchodzą reszty aminokwasowe (aminokwasy), powiązane za pomocą wiązania peptydowego
peptydy, w których skład wchodzą od do reszt aminokwasowych; peptydy zawierające ilość reszt aminokwasowych, znajdujące się w górnej granicy tego przedziału (czysto umownej i nieostrej), określa się jako białka
typ wiązania amidowego obecnego w białkach i peptydach, powstaje pomiędzy dwoma aminokwasami, z których jeden wykorzystuje do jego tworzenia grupę -karboksylową, a drugi -aminową
Bibliografia
M. Krzeczkowska, J. Loch, A. Mizera, Repetytorium chemia. Liceum – poziom podstawowy i rozszerzony, Warszawa – Bielsko‑Biała 2010.
encyklopedia.pwn.pl