Przeczytaj
Czy znasz przebieg doświadczenia, które pozwala zbadań chromatografię bibułową barwnika pisaka? Na bibule filtracyjnej zaznaczono kreskę mazakiem, a następnie zanurzono ją w zlewce z octem. Poziom cieczy podnosił się i zaczynała ona pochłaniać za sobą wchodzące w skład tuszu pisaka barwniki, które podczas rozdzielania wędrowały z różnymi prędkościami. Wniosek brzmiał następująco: w skład tuszu pisaka określonego koloru wchodzi więcej niż jeden barwnik.
Czy wiesz, kto odkrył chromatografię i w jakich okolicznościach?
Chromatografia
Chromatografia jest zaliczana do jednej z metod analitycznych i preparatywnych. Technika ta pozwala na rozkładanie mieszaniny na oddzielne składniki lub ich grupy (frakcjefrakcje), a także ich identyfikację. Procedura ta korzysta z różnic w zachowaniu poszczególnych związków chemicznych w układzie dwufazowym – czyli działa na zasadzie oddziaływań międzycząsteczkowych, powstających pomiędzy związkami chemicznymi, z których składa się mieszanina, a złożem. Wówczas pewne związki chemiczne przechodzą przez złoże szybciej, a inne wolniej.
Jedna z faz pozostaje w tym samym miejscu, nie ulega zmianie jej położenie (faza stacjonarna, faza nieruchomafaza nieruchoma, złoże, adsorbent). Druga natomiast przemieszcza się w stosunku do pierwszej w określonym kierunku (roztwór rozwijający, eluent, faza ruchomafaza ruchoma, faza nośna).
Chromatografię można podzielić, w zależności od stanu skupienia fazy ruchomej, na:
gazową – fazę ruchomą stanowi gaz (zazwyczaj hel, argon, wodór);
cieczową – fazę ruchomą stanowi ciecz;
nadkrytyczną – fazą ruchomą jest substancja (najczęściej tlenek węgla()) w stanie nadkrytycznym.
Możliwe zależności pomiędzy fazą ruchomą i fazą stacjonarną:
Faza ruchoma | Faza nieruchoma |
|---|---|
gaz | ciecz |
gaz | ciało stałe |
ciecz | ciecz |
ciecz | ciało stałe |
Chromatografia kolumnowa
Chromatografia kolumnowa jest reprezentantem chromatografii cieczowej. Jest dobrą i wydajną techniką, służącą do rozdzielania mieszanin i oczyszczania produktów naturalnych i syntetycznych.
W mechanizmie rozdzielania wykorzystuje się istnienie różnic w sile oddziaływań międzycząsteczkowych dla różnych związków, pomiędzy składnikami mieszaniny a fazą ruchomą oraz składnikami mieszaniny a fazą stacjonarną. W roli fazy stacjonarnej można używać rozmaitych adsorbentów, którymi są ciała stałe, porowate, o silnie rozwiniętej powierzchni, nierozpuszczalne w wodzie i rozpuszczalnikach organicznych.
Najczęściej stosowanymi adsorbentami (faza stacjonarna) są:
żel krzemionkowy – (silnie polarny);
tlenek glinu() – ;
węgiel aktywny;
poliamid;
glinokrzemiany.
Z kolei fazę ruchomą stanowią woda lub organiczne rozpuszczalniki, takie jak: metanol, acetonitryl, propanol lub heksan.
Związki polarne adsorbują się silniej na polarnych cząsteczkach silikażelu, dlatego są wymywane z kolumny później niż składniki mniej polarne, które poruszają się szybciej przy zastosowaniu rozpuszczalnika mniej polarnego.
Etapy analizy metodą chromatografii kolumnowej:
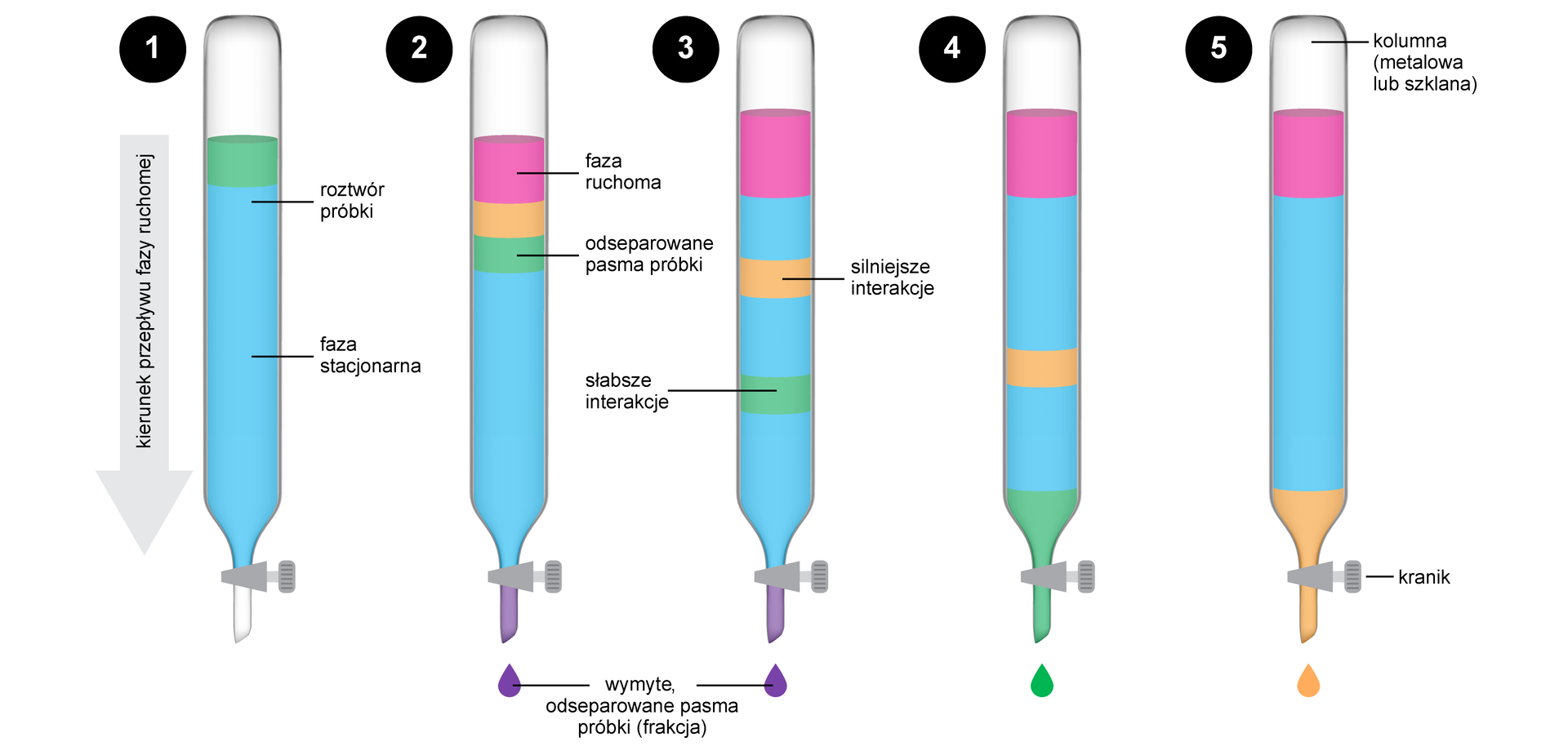
Chromatografia cienkowarstwowa (TLC)
Chromatografia cienkowarstwowa (TLC, ang. Thin Layer Chromatography) stanowi powszechną technikę sprawnego kontrolowania postępu reakcji chemicznych i czystości produktów. Za pomocą tej metody można zidentyfikować związki zarówno organiczne, jak i nieorganiczne.
W technice TLC, fazę stacjonarną nakłada się w formie cienkiej, równomiernej warstewki na płytkę szklaną, arkusz folii aluminiowej lub na tworzywo sztuczne. Mieszaninę substancji do rozdzielenia lub po rozdziale nanosi się punktowo przy dolnej krawędzi płytki. Następnie płytkę chromatograficzną umieszcza się w komorze chromatograficznej. Jeden koniec płytki zanurzony jest w zlewce z fazą ruchomą, która – dzięki siłom kapilarnym – porusza się przez złoże prostopadle do powierzchni fazy ruchomej. Taki ruch kapilarny jest porównywany do dyfuzji substancji rozpuszczonej w fazie ruchomej pod kątem prostym w stosunku do drogi migracji, więc substancja rozpuszczona ograniczona jest do wąskiej dróżki.
Składniki rozdzielanej mieszaniny chemicznej wiążą się z różną siłą z polarnym adsorbentem. Następnie są wymywane za pomocą rozpuszczalnika, który pełni funkcje fazy ruchomej.
Wraz z polarnością badanej substancji, wzrasta wiązanie się ich z fazą stałą, czego efektem jest trudniejsze wymywanie substancji chemicznych przez eluent. Natomiast wraz ze wzrostem polarności fazy ruchomej następuje wzrost blokowania przez niego polarnych centrów aktywnych fazy stałej, co zmniejsza „opory” przesuwania się wymywanych substancji.
Rozpuszczalniki dobiera się na zasadzie „podobne rozpuszcza się w podobnym „. Wówczas wykonuje się kilka prób (modyfikując polarność fazy ruchomej) i stara się otrzymać jak najmniejszą wartość tzw. współczynnika opóźnienia (ang. retardation factor). Współczynnik ten przedstawia ułamek czasu spędzonego przez substancję w fazie ruchomej i powinien być wyższy od i niższy od .
Gdzie to długość drogi, którą przebył nałożony analit, a to długość drogi, którą przebył eluent.
Jeżeli wartość współczynnika jest równa lub bliska zeru, oznacza to, że substancja adsorbujeadsorbuje się bardzo silnie, przez co w tym samym czasie, co w przypadku substancji o wysokich wartościach współczynnika (-) przebywa krótszą drogę. W uproszczeniu, współczynnik pokazuje stosunek prędkości próbki do prędkości eluentu.
Technika TLC jest wykorzystywana w celu znalezienia optymalnych warunków dla chromatografii kolumnowej oraz analizy frakcji uzyskanych techniką chromatografii kolumnowej.
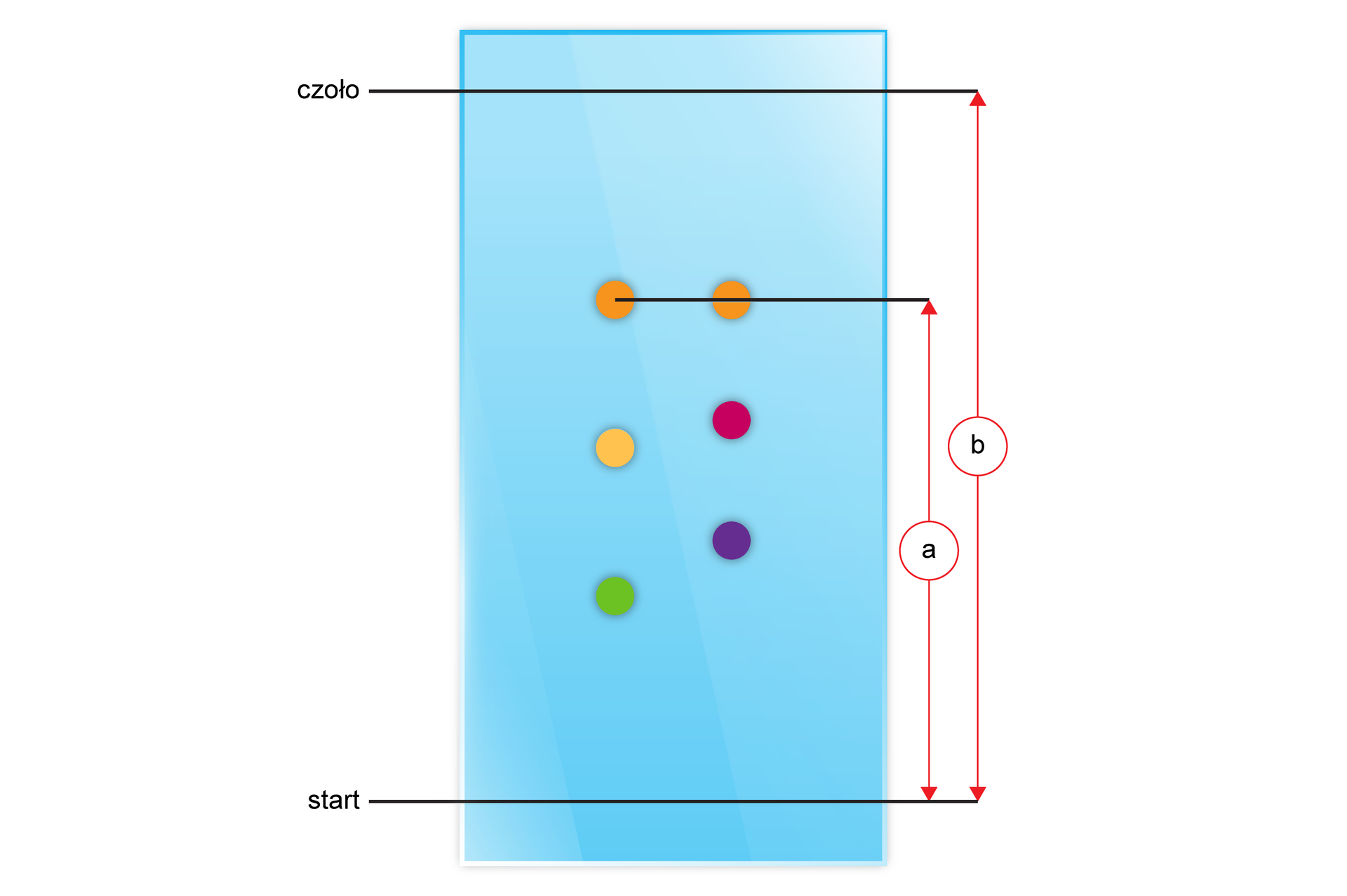
- start to linia, na którą punktowo nanosimy analit (mieszaninę substancji) za pomocą kapilary;
- a to punkt, do którego dotarł nałożony analit;
- b to poziom, do którego dotarło czoło eluentu;
- czoło to linia pomocnicza, która przedstawia moment wyciągnięcia płytki z komory rozwijającej (eluent dotarł do tej linii).
Metoda liniowa to najpopularniejsza technika rozwijania płytek chromatograficznych. Wymagany jest kontakt jednego końca płytki (warstwy chromatograficznej) z rozpuszczalnikiem (faza ruchoma). Potem płytkę chromatograficzną ustawia się w pozycji pionowej lub pod kątem, zanurzając ją w kilku mililitrach rozpuszczalnika, który znajduje się w odpowiednim pojemniku zwanym komorą chromatograficzną. Rozwijanie liniowe może być jednokierunkowe lub dwukierunkowe.
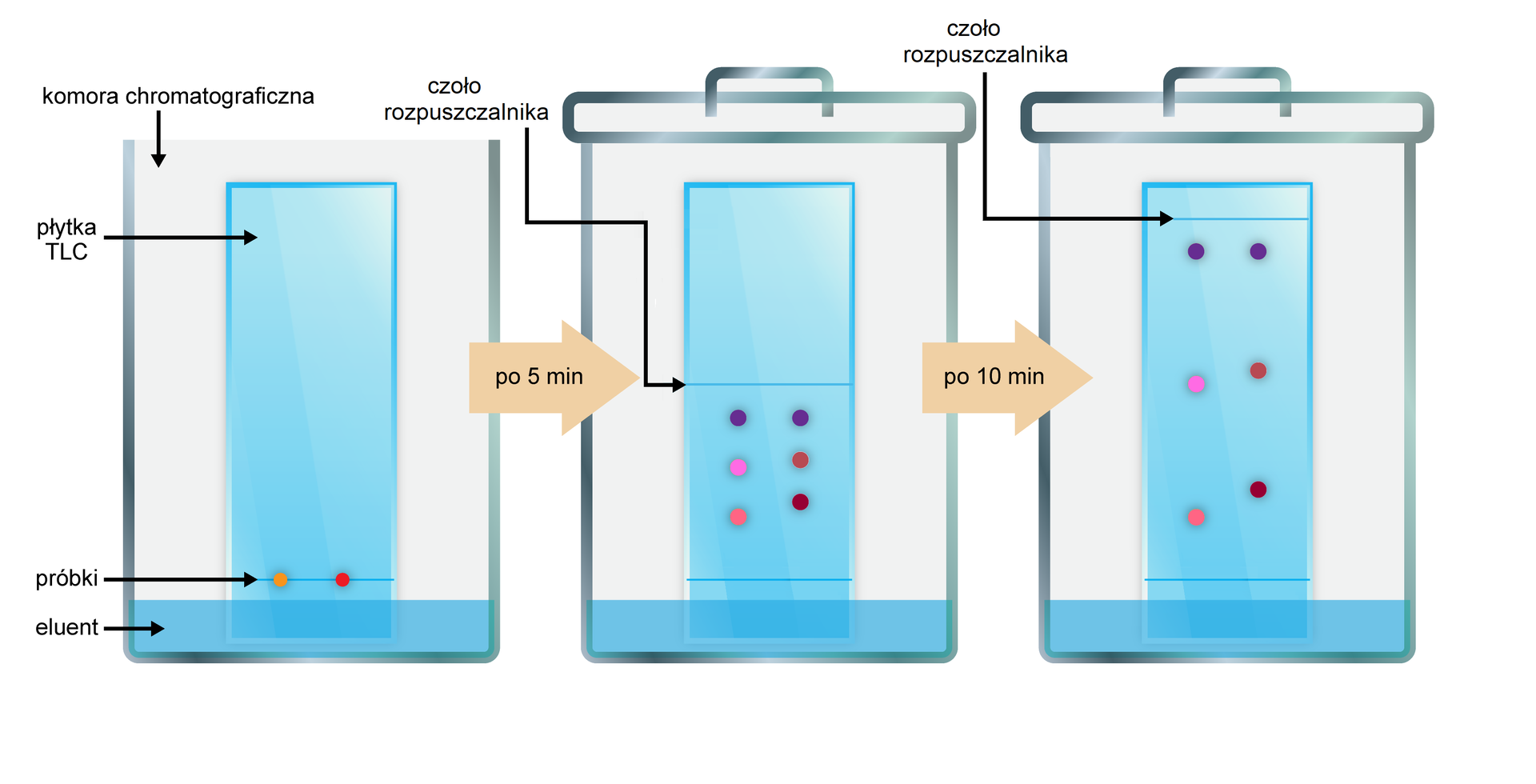
Płytkę chromatograficzną można rozwijać:
pojedynczo;
W rozwijaniu jednokierunkowym, faza ruchoma przemieszcza się od dołu płytki chromatograficznej ku górze. Spotykane jest również rozwijanie dwukierunkowe. W tym przypadku, po pierwszym rozwinięciu należy płytkę wysuszyć w celu usunięcia rozpuszczalnika, a następnie ponownie ją zanurzyć w tym samym lub innym rozpuszczalniku. Konieczne jest jednak obrócenie płytki o stopni.
wielokrotnie.
W rozwijaniu wielokrotnym, po każdej analizie, płytkę chromatograficzną należy wysuszyć i ponownie rozwinąć. W tym celu można zastosować taką samą lub inną fazę ruchomą. Technika wielokrotnego rozwijania ma na celu zwężenie pasma stężeniowego substancji, czego efektem jest zwiększenie sprawności układu i czułości metody.

Zalety TLC
Stosowana jest do wstępnego doboru faz dla układów kolumnowych, ponieważ zużycie rozpuszczalników, w porównaniu z chromatografią kolumnową, jest znacznie mniejsze.
Możliwość przechowywania płytek z rozdzielonymi substancjami.
Na jednej warstwie chromatograficznej można równocześnie rozdzielać kilka różnych próbek.
Pozwala określić stopień rozdzielenia substancji na każdym etapie rozwijania chromatogramu i przerwać ten proces w dowolnym momencie.
W przypadku kolumny chromatograficznej, zarówno detekcja składników, jak i ocena stopnia ich rozdzielenia możliwe są dopiero, gdy związki te opuszczą kolumnę.
Zastosowania chromatografii w życiu codziennym
Słownik
faza nieruchoma jest umieszczona w specjalnej kolumnie, przez którą przepuszcza się roztwór badanej mieszaniny, po czym wymywa składniki mieszaniny, stosując eluent
substancja umieszczona w kolumnie chromatograficznej (chromatografia kolumnowa) lub na płaszczyźnie (chromatografia cienkowarstwowa), która ma budowę porowatą i spełnia rolę sorbentu, tzn. działa na zasadzie zatrzymywania składników rozdzielanej mieszaniny na powierzchni (adsorpcja) lub w masie (absorpcja)
eluent lub inaczej czynnik wymywający; w przypadku chromatografii cieczowej jest nim ciekły rozpuszczalnik, który przenosi analizowaną substancję przez złoże, a w przypadku chromatografii gazowej gaz – mówimy wtedy o gazie nośnym
proces wymywania składników
efekt powierzchniowy; wynika z oddziaływań elektrostatycznych (wiązania wodorowe, oddz. dipol‑dipol, dipol‑dipol indukowany) pomiędzy substancją rozdzielaną i miejscami polarnymi (polarne grupy funkcyjne np. , lub ) fazy stacjonarnej
układ dwóch lub więcej związków chemicznych, zmieszanych ze sobą w dowolnym stosunku oraz podlegających rozdzielaniu
składnik wykrywany lub/i oznaczany w badanej próbce
, iloraz odległości przebytej przez substancję rozdzielaną przez odległość przebytą przez czoło eluentu w tym samym czasie
części mieszaniny, wyodrębnione w procesie rozdzielania
Bibliografia
Szczepaniak W., Metody instrumentalne w analizie chemicznej<c/ite>, Warszawa 1996.
Witkiewicz Z., Podstawy chromatografii, Warszawa 1995.
Zniszczoł, A., Budniok S., Laboratorium z chemii organicznej. Chromatografia Cienkowarstwowa (TLC)<c/ite>, Gliwice 2010.