Przeczytaj
Aminokwasy aromatyczne
Próba ksantoproteinowaproteinowa nie wykrywa wszystkich istniejących białek. Jest to reakcja charakterystyczna dla białek zawierające w swoich cząsteczkach pierścienie aromatycznepierścienie aromatyczne, które znajdują się w aminokwasach. Aminokwasy, zawierające pierścień aromatyczny, to np. fenyloalanina, tyrozyna i tryptofan. Ich wzory strukturalne zostały zaprezentowane poniżej.
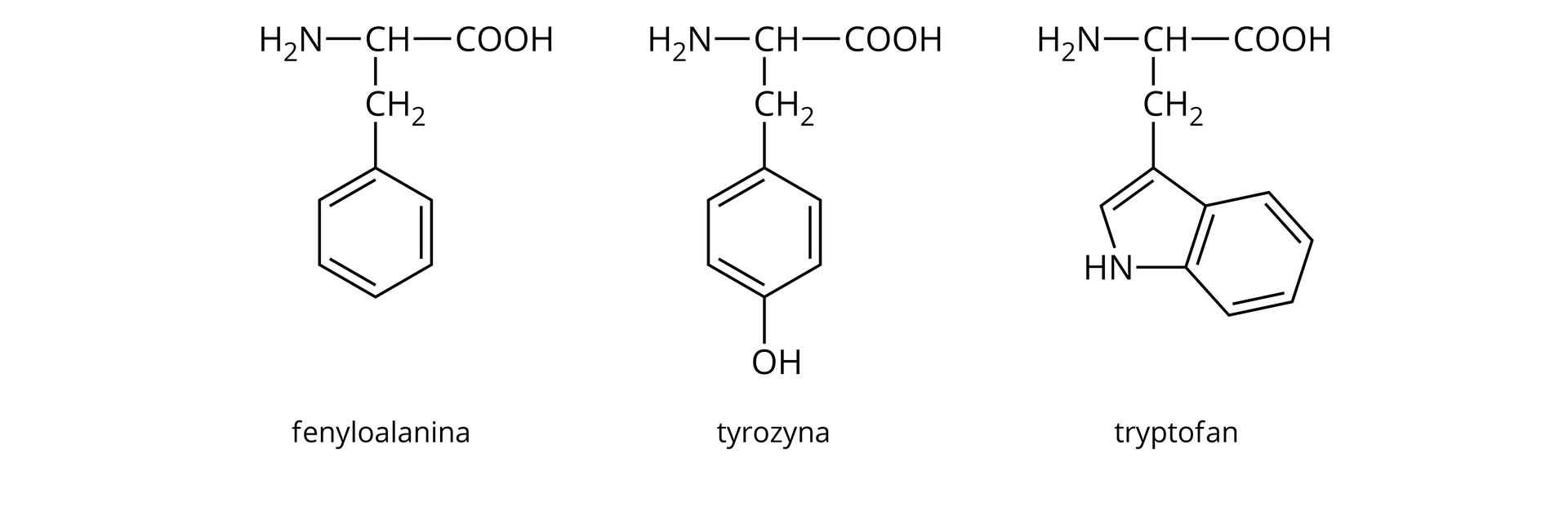
Pierścienie aromatyczne reagują ze stężonym kwasem azotowym() , w wyniku czego zachodzi nitrowanienitrowanie pierścienia benzenowego. Dla przykładu, reakcja nitrowania tyrozyny przebiega według równania:
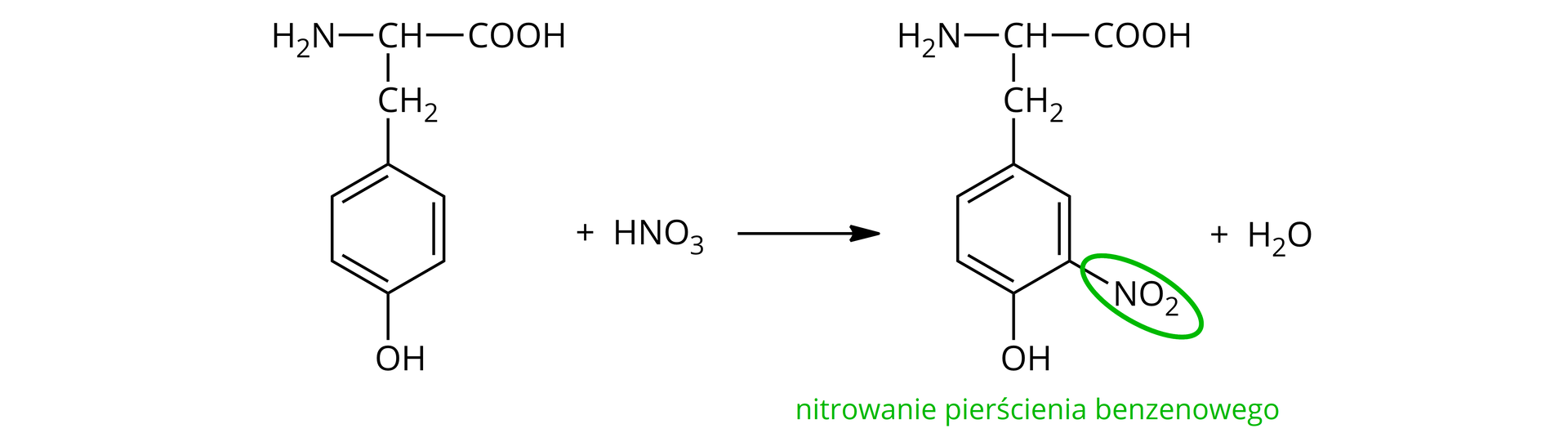
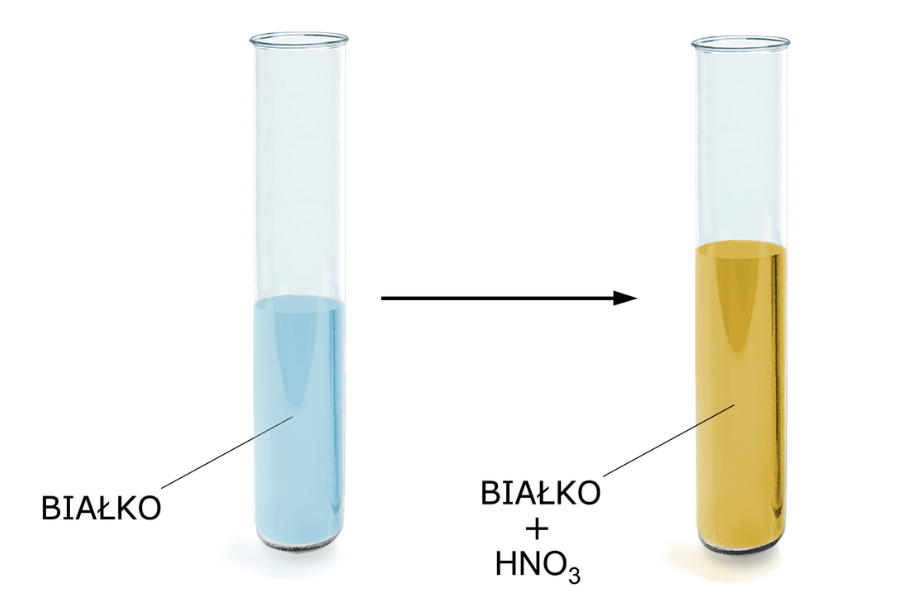
Po dodaniu do badanej próbki zasady (np. roztworu wodorotlenku sodu) pojawi się pomarańczowe zabarwienie. Powstały związek to pochodna aminokwasu, która w swojej budowie posiada wiązania jonowewiązania jonowe i wiązania donorowo‑akceptorowewiązania donorowo‑akceptorowe. Przebieg mechanizmów reakcji został zaprezentowany na rysunku poniżej:
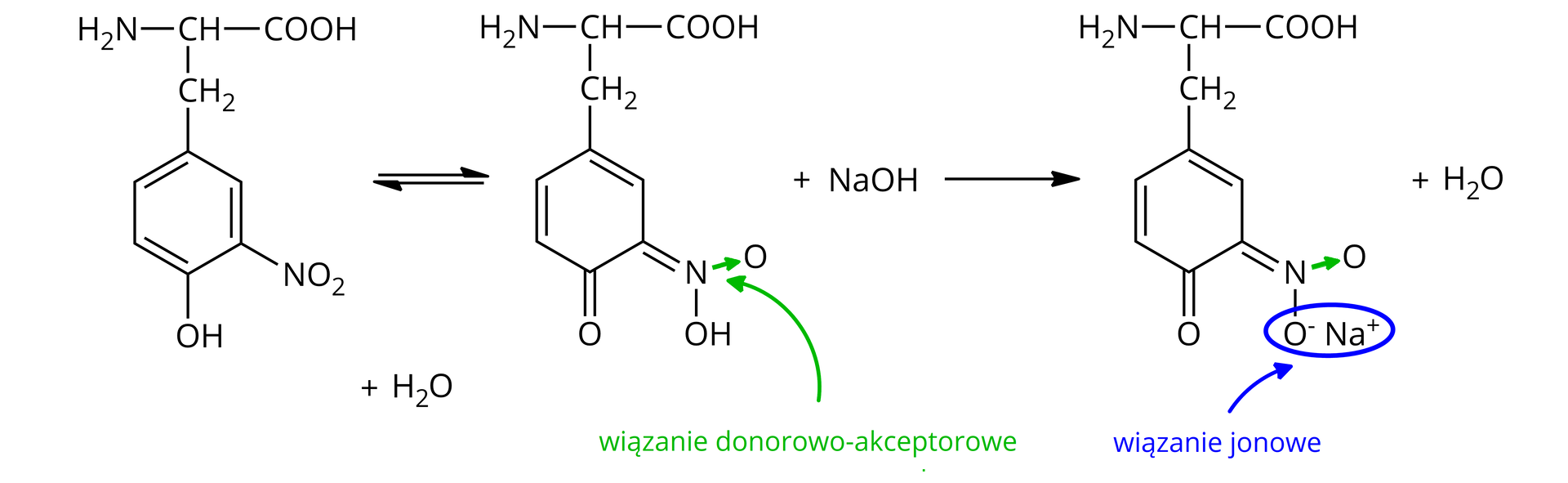
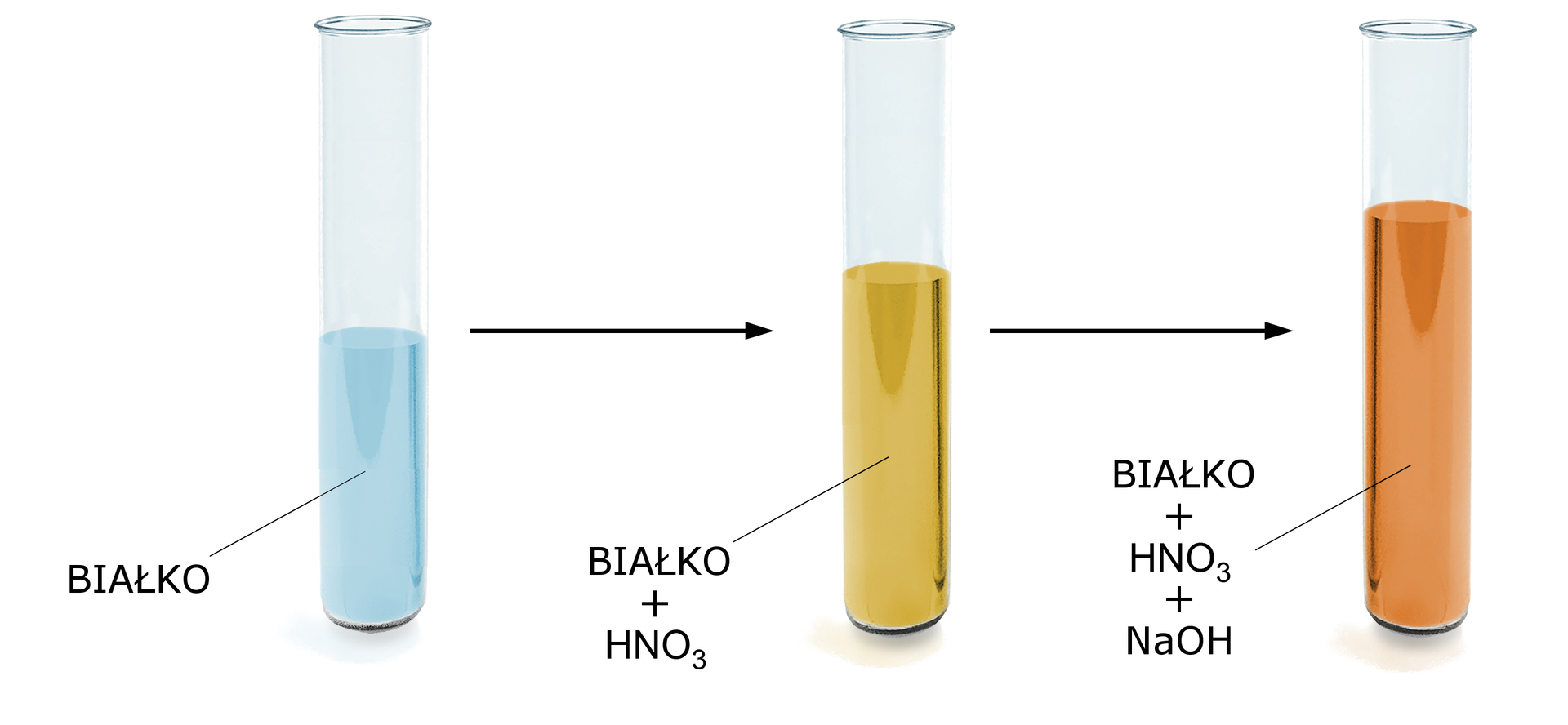
Reakcja ksantoproteinowa nie jest reakcją charakterystyczną tylko dla białek, ale również m.in. dla innych związków aromatycznych. Pozytywny wynik dają również benzen czy fenol. Pod wpływem stężonego kwasu azotowego() zachodzi nitrowanie pierścienia benzenowego i powstaje połączenie o barwie żółtej. Stąd właśnie pochodzi takie zabarwienie skóry, gdy przez nieuwagę obleje się palce stężonym .
Słownik
wiązanie chemiczne, w którym wolna para elektronowa pochodzi tylko od atomu jednego pierwiastka; wyróżnia się dawcę (donora) pary elektronowej i biorcę (akceptora) pary elektronowej
płaski fragment cząsteczki, zbudowany z atomów węgla (a czasem, oprócz atomów węgla, z atomów innych pierwiastków, np. azotu) połączonych w pierścień, który zawiera określoną liczbą elektronów zdelokalizowanych, spełniającą regułę Hückla
reakcja chemiczna, która polega na wymianie atomu wodoru na grupę nitrową w związkach organicznych
reakcja, która jest rozpoznawalna dla konkretnych związków chemicznych
oddziaływanie, które polega na elektrostatycznym przyciąganiu się dwóch różnoimiennych jonów; w białkach występuje najczęściej pomiędzy dodatnio naładowanymi grupami aminowymi a ujemnie naładowanymi grupami karboksylowymi
białka; wielkocząsteczkowe związki zbudowane wyłącznie lub w dużej mierze z aminokwasów; stanowią największą część występujących w żywej komórce związków organicznych
Bibliografia
Doonan S., Zawadzki Z., Białka i peptydy, tłum. Z. Zawadzki, Warszawa 2008.
Stryer L., Berg J. M., Tymoczko J. L., Biochemia. Część 1. Molekularny wzór życia, Warszawa 2009, wyd. 4.