Przeczytaj
Rola żelaza w organizmie człowieka
W organizmie ludzkim żelazo występuje tylko w postaci jonowej bądź jest związane z innymi cząsteczkami, ale nie w formie atomowej. Mimo że często domyślnie używamy formy „żelazo” w miejsce formy „jony żelaza” w czasie opisywania wpływu tego pierwiastka na funkcjonowanie organizmu. Oglądając zatem reklamę telewizyjną, czytając informacje o składzie leku czy nawet analizują treść tej lekcji, pamiętaj, że w istocie żelazo wprowadzane do organizmu ma formę zjonizowaną, nie atomową.
Żelazo jest niezbędne do prawidłowej budowy skóry, włosów, paznokci, ale również prawidłowego funkcjonowania układu odpornościowego. Pierwiastek ten jest także składnikiem wielu enzymów i białek, które biorą udział w metabolizmie.
Jony żelaza wchodzą w skład enzymów: katalaz, oksydaz, peroksydaz, uczestniczących w procesach, takich jak synteza kwasów nukleinowych oraz transport tlenu i elektronów. Jony żelaza(II) są bardzo istotnym składnikiem czerwonego barwnika krwi (hemoglobiny) oraz mioglobiny. Wiążą one tlenek węgla(IV) w hemoglobinie i transportują go do płuc, skąd jest usuwany.
Kolejne, równie istotne funkcje tego pierwiastka to udział w procesie tworzenia czerwonych ciałek krwi w szpiku kostnym czy udział w syntezie DNA i procesach oddychania komórkowego, a także wspomaganie pracy wątroby oraz odporności organizmu.
Białka związane z żelazem
Autor: Zephyris. Źródło: wikipedia.org. Licencja: CC BY‑SA 3.0, Mioglobina Białko występujące w mięśniach. Główną funkcją mioglobiny jest magazynowanie tlenu w mięśniach czerwonych (poprzecznie prążkowanych). Podczas nadmiernego wysiłku mioglobina uwalnia zmagazynowane cząsteczki O indeks dolny, dwa, koniec indeksu dolnego i pozwala mitochondriom na syntezę ATP. Grafika przedstawiająca model mioglobiny. Zbudowany z łańcucha polipeptydowego utworzonego przez osiem podjednostek o strukturze alfa helisy. Grupę prostetyczną w mioglobinie stanowi cząsteczka hemu. Model wstążkowy mioglobiny
Autor: AzaToth. Źródło: wikipedia.org. Licencja: CC 0, Ferrytyna Białko, które kompleksuje jony żelaza(III) F e indeks górny, trzy, plus, koniec indeksu górnego, utrzymując żelazo w dostępnej i nieszkodliwej formie oraz przechowując je w wątrobie. Grafika przedstawiająca model ferrytyny. Białko globularne zbudowane z dwudziestu czterech podjednostek białkowych o strukturze alfa helisy. Model wstążkowy ferrytyny
Źródło: wikipedia.org, Transferryna (TRF) Główne białko, które odpowiada za transport jonów żelaza w osoczu. Każda cząsteczka TRF wiąże tylko utlenioną formę — jon żelaza(III) (F e indeks górny, trzy, plus, koniec indeksu górnego). TRF syntetyzowana jest w wątrobie, a jej stężenie w osoczu regulowane jest w zależności od dostępności żelaza. Grafika przedstawiająca model wstążkowy transferryny. Białko zbudowane jest z dwóch głównych jednostek utworzonych przez strukturę białkową beta harmonijki oraz alfa helisy. Model wstążkowy transferryny
Autor: Emw. Źródło: wikipedia.org. Licencja: CC BY‑SA 3.0, Haptoglobina Białko, które wiąże nieodwracalnie wolną hemoglobinę, a powstały kompleks jest fagocytowany i rozkładany w układzie siateczkowo‑śródbłonkowym. Grafika przedstawiająca model wstążkowy haptoglobiny. Białko zbudowane z dwóch łańcuchów alfa i dwóch beta połączonych mostkami disiarczkowymi. Model wstążkowy haptoglobiny
Autor: Ayacop. Źródło: wikipedia.org. Licencja: CC 0 1.0, Hemosyderyna Białko, które powstaje, gdy pozajelitowe żelazo jest w nadmiarze. Zawiera ono żelazo w formie koloidalnej. Występuje w wątrobie, śledzionie i szpiku., Hepcydyna Hormon peptydowy produkowany w wątrobie, ma działanie przeciwgrzybicze., Laktoferyna Białko, które posiada właściwości przeciwbakteryjne (wyłapuje i blokuje dostępność żelaza dla bakterii). Współtworzy obronę organizmu przed patogenami. Występuje w organizmie w siarze, ślinie, mleku, łzach oraz neutrofilach.

Organizm dorosłego zdrowego człowieka zawiera w przeliczeniu żelaza, z czego ok. są niezbędne do prawidłowego funkcjonowania, reszta to rezerwa znajdująca się w ferrytynie i hemosyderynie w hepatocytach i makrofagach.
Człowiek spożywa żelaza w postaci hemowej i niehemowej, z czego wchłania się do krwi ok. 10%. Większa część żelaza (60–70%) pozostaje związana w hemoglobiniehemoglobinie erytrocytów, wchodzi w skład mioglobiny oraz różnych enzymów.
Dzienna utrata żelaza to , głównie ze złuszczającymi się komórkami, W pożywieniu znajduje się żelazo zarówno dwu-, jak i trójwartościowe. W żołądku jest uwalniane ze związków organicznych i w jego kwasowym środowisku redukowane do postaci , która jest rozpuszczalna w wodzie i wchłaniana w jelicie, przy optymalnym pH.
Zawartość żelaza w organizmie
Pula całkowita | 3‑4 g | 40‑50 |
|---|---|---|
osocze | 3 mg | transferyna |
erytrocyty | 1800 mg | hemoglobina |
szpik | 300 mg | |
mięśnie | 300 mg | mioglobina |
wątroba | 1000 mg | ferrytyna |
Indeks dolny Źródło: Moon J., Weinberg E. D., Iron: The Most Toxic Metal, 2008. Indeks dolny koniecŹródło: Moon J., Weinberg E. D., Iron: The Most Toxic Metal, 2008.
Metabolizm żelaza w ustroju obejmuje żelazo hemowe (produkty zwierzęce), które jest lepiej przyswajalne, i żelazo niehemowe (produkty roślinne).
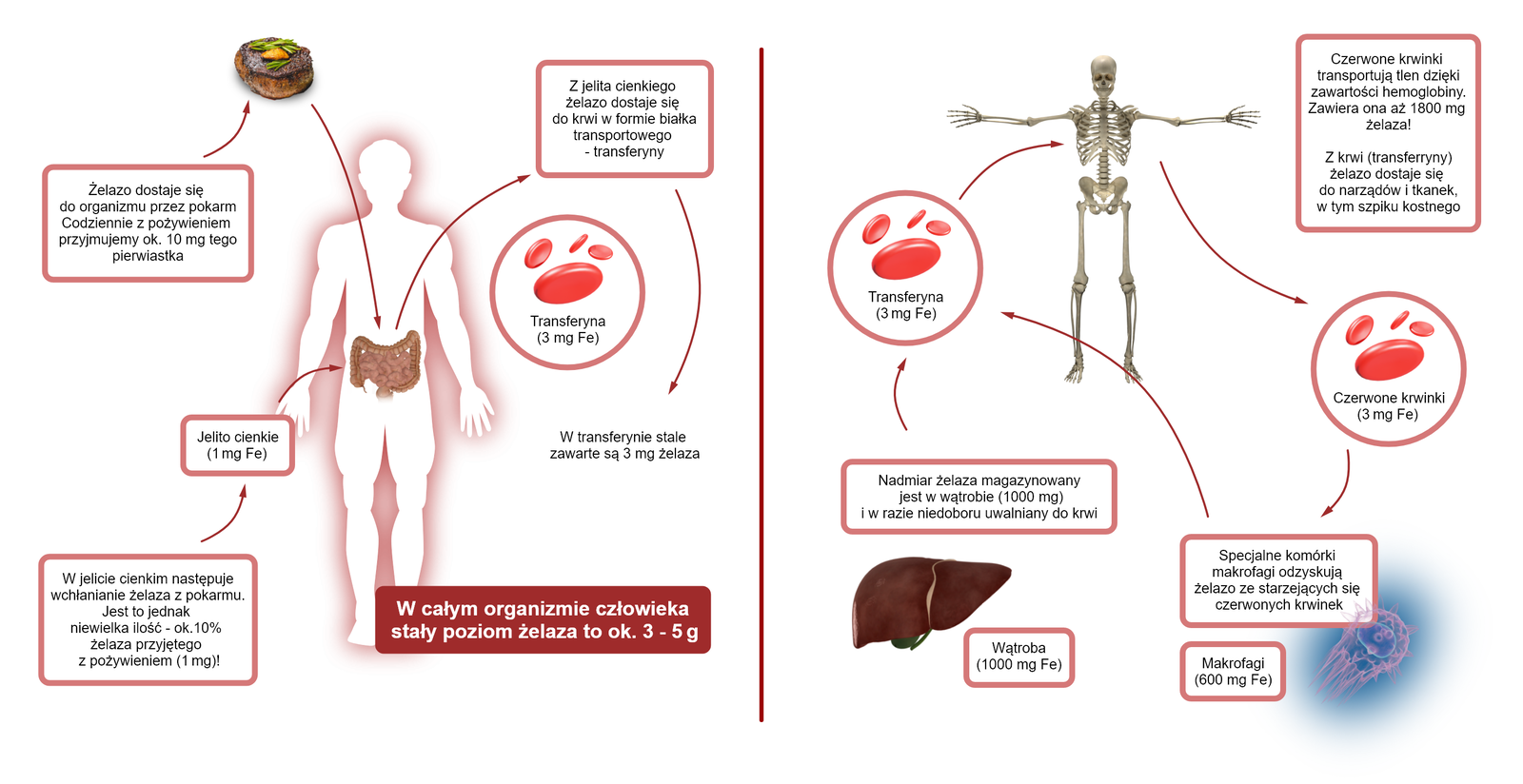
Etapy metabolizmu żelaza
absorpcja w przewodzie pokarmowym – redukcja w żołądku do ();
transport do wszystkich komórek organizmu – wchłanianie przez enterocyty i utlenienie do następnie połączenie z ferrytyną;
przejście żelaza przez błonę komórkową; żelazo, przechodząc z komórek nabłonka do krwi, łączy się z transferyną; transferyna łączy się z receptorem błonowym erytroblastu ( do produkcji erytrocytów w szpiku);
udział w procesach metabolicznych;
odzyskiwanie żelaza z rozpadłych erytrocytów;
procesy magazynowania żelaza – nadmiar magazynowany wewnątrzkomórkowo – ferrytyna.
Słownik
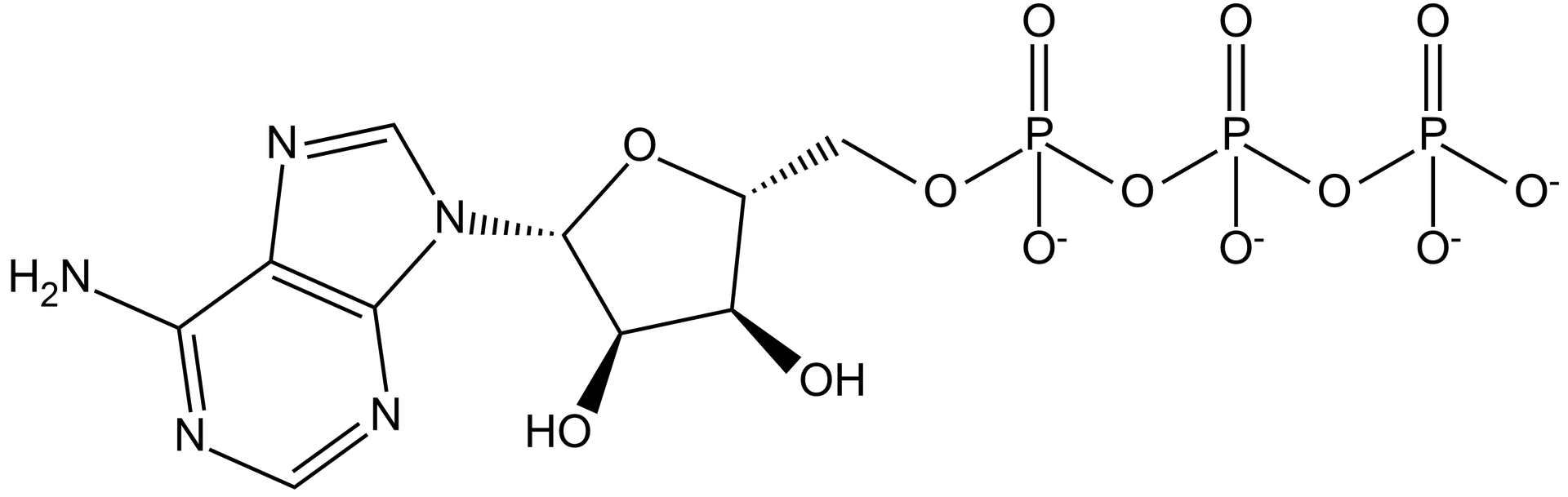
nukleotyd adeninowy, zbudowany z adenozyny z przyłączoną wiązaniem estrowym w pozycji 5′-OH grupą trifosforanową; stanowi nośnik energii chemicznej, używanej w metabolizmie komórki; powstaje jako magazyn energii w procesach fotosyntezy i oddychania komórkowego
białko złożone z grupy metaloproteidów, występujące w mięśniach poprzecznie prążkowanych; posiada zdolność nietrwałego wiązania tlenu i stanowi jego magazyn w tkance mięśniowej poprzecznie prążkowanej
białko z grupy metaloproteidów, pełniące rolę czerwonego barwnika oddechowego; należy do białek złożonych zawierający żelazo ; wiąże się nietrwale z tlenem; występuje u kręgowców w postaci zamkniętej w komórkach krwi – erytrocytach lub w postaci rozpuszczonej w osoczu u niektórych bezkręgowców
Bibliografia
Heiserman D. l., Księga pierwiastków chemicznych, Warszawa 1997.
Jurczyk K., Rola żelaza w chorobach wątroby, „Postępy Nauk Medycznych” 2000, 1.
Shouman B. O., Mesbah A., Aly H., Iron metabolism and lipid peroxidation products in infants with hypoxic ischemic encephalopathy. „Journal of Perinatology” 2008, 28, s. 487‑491.