Przeczytaj
E‑materiały powiązane z tematem
Budowa anatomiczna liścia
Ligustr pospolity

Ligustr pospolity (Ligustrum vulgare) to krzew liściasty z rodziny oliwkowatych (Oleaceae), osiągający ok. 2–3 m wysokości. Ma sezonowe skórzaste liście o eliptycznym kształcie, które z wierzchu są błyszczące i ciemnozielone, a od spodu matowe i jaśniejsze, z widocznym nerwem głównym.
Krzew ten zakwita latem, wydając drobne, kremowobiałe, lekko pachnące kwiaty, zebrane w wiechowate kwiatostany. Jesienią z kwiatów wykształcają się kuliste, błyszczące, czarne, skupione w gronach owoce, które utrzymują się na pędach aż do wiosny. Owoce te są dla człowieka trujące, ale dla wielu zwierząt (głównie ptaków) stanowią ważny składnik diety.
Ligustr dobrze znosi suszę, mróz i zanieczyszczenia miejskie. Znajduje zastosowanie jako roślina ozdobna. Jest doskonałą rośliną na żywopłoty, ponieważ łatwo regeneruje się nawet po ostrym cięciu oraz rzadko bywa atakowany przez choroby i szkodniki.
Sosna czarna

Sosna czarna (Pinus nigra) to gatunek drzewa iglastego, zimozielonego i długowiecznego (szacuje się, że niektóre egzemplarze osiągają wiek ponad 500 lat). Dorasta do 25–45 m wysokości.
Jej liście to sztywne, spiczaste igły zebrane w pęczkach po dwie, w kolorze ciemnozielonym, o długości 8–14 cm i grubości 1–2 mm. Ma również jasnobrązowe szyszki o długości ok. 4–7 cm. Owocuje po 15–40 latach.
Odmiana ta nie wymaga żyznej gleby – rośnie na podłożu suchym, piaszczystym lub gliniastym, bogatym w wapń. Cechuje się wysoką wytrzymałością na ujemne temperatury i bardzo dobrą odpornością na zanieczyszczenia środowiska.
Sosna zwyczajna

Sosna zwyczajna (Pinus sylvestris) to gatunek wiecznie zielonego drzewa iglastego, osiągającego zazwyczaj 30 m wysokości (a w sprzyjających warunkach nawet 40–48 m).
Ma sztywne, twarde i ostro zakończone igły osadzone parami na krótkopędach o długości 3–7 cm i grubości 1–2 mm, zwykle skręcone wzdłuż osi o 180°. Najczęściej są ciemnozielone z odcieniem niebieskawym, sinawym lub srebrzystym. W igłach sosny zwyczajnej znajduje się od 3 do 13 przewodów żywicznych, położonych pod epidermą (skórką), która utworzona jest z małych grubościennych komórek. Przewody żywiczne wysłane cienkościennymi komórkami wydzielniczymi są otoczone grubościenną sklerenchymą. Szyszki sosny zwyczajnej, o długości do 7 cm, osadzone są pojedynczo lub po dwie (a nawet trzy). Początkowo zielone, później brunatnieją i pękają, uwalniając przenoszone przez wiatr uskrzydlone nasiona.
Gatunek ten jest odporny na duże wahania temperatury (dobrze znosi zarówno suszę, jak i mrozy), jednak ma duże wymagania względem światła.
Obserwacja mikroskopowa tkanek roślinnych
Do obserwacji struktur tkankowych i komórkowych używa się głównie mikroskopów (z gr. mikros – mały, skopeo – patrzę, obserwuję) – przyrządów optycznych pozwalających na otrzymywanie powiększonych obrazów obiektów niewidocznych gołym okiem. Najczęściej stosowanym mikroskopem do obserwacji tkanek roślinnych jest mikroskop świetlny, który wykorzystuje wiązkę światła przechodzącą przez specjalny układ optyczny, tworzony przez zestaw soczewek umieszczonych w obiektywie i okularze.
Taka obserwacja jest jednak utrudniona, gdyż komórki i ich elementy nie wykazują różnic w absorpcji promieniowania elektromagnetycznego. Przekłada się to na brak wyraźnego kontrastu między poszczególnymi elementami. Nie ma więc możliwości rozróżnienia szczegółów budowy danej tkanki czy też elementów komórki. Z tego powodu w preparatach mikroskopowych niezbędne jest zastosowanie barwników histologicznych, które wybarwiają komórki wraz z ich elementami strukturalnymi, a tym samym umożliwiają ich dokładną obserwację i identyfikację.
Barwniki histologiczne
Barwniki histologiczne to związki chemiczne wykorzystywane w mikroskopii świetlnej do wybarwiania struktur komórkowych i tkankowych. Typowy barwnik zawiera dwie grupy chemiczne: chwytną i barwną. Część chwytna łączy się z elementami komórkowymi o określonym składzie chemicznym, natomiast barwna absorbuje światło o określonej długości fali, dzięki czemu możliwe jest dostrzeżenie wybarwionych struktur.
W zależności od struktury, jaką się będzie obserwować, należy zastosować odpowiedni barwnik histologiczny. Do wykrywania amyloplastów, czyli leukoplastów magazynujących skrobię, stosuje się jodek w jodku potasu, który barwi skrobię na kolor od jasnoniebieskiego do granatowego. Celulozowe ściany komórkowe wykrywa się za pomocą roztworu chlorku cynku z jodem, pod wpływem którego ściany komórkowe zbudowane z celulozy wybarwiają się na kolor fioletowy. Ściany komórkowe inkrustowane ligniną po zastosowaniu floroglucyny z kwasem solnym barwią się na kolor czerwony. Natomiast ściany komórkowe adkrustowane suberyną pod wpływem sudanu III nabierają barwy żółtoczerwonej.
Barwienie różnicowe
Aby odróżnić od siebie poszczególne struktury komórkowe i tkankowe, dany preparat należy potraktować jednocześnie dwoma różnymi barwnikami – jest to tzw. barwienie różnicowe. Dzięki tej technice można odróżnić m.in. zdrewniałe ściany komórkowe, które pod wpływem safraninysafraniny barwią się na kolor czerwony, od celulozowych ścian komórkowych, które pod wpływem zieleni świetlistej barwią się na kolor niebieskozielony. Innym przykładem barwników stosowanych w barwieniu różnicowym są: karmin ałunowy, barwiący ściany celulozowe na kolor czerwony, oraz zieleń metylenowa, barwiąca zdrewniałe ściany komórkowe na kolor zielony.
Jak przygotować preparat mikroskopowy z liści?
Podczas przygotowywania preparatu istnieje ryzyko pojawienia się artefaktówartefaktów, np. pęcherzyków powietrza. Jest to bardzo częste zjawisko towarzyszące samodzielnemu sporządzaniu preparatów. Duża liczba artefaktów uniemożliwia przeprowadzenie obserwacji mikroskopowych. W takiej sytuacji należy spróbować usunąć pęcherzyki powietrza poprzez delikatne ruchy góra‑dół, lewo‑prawo szkiełka nakrywkowego lub wykonać preparat na nowo.
Barwienie liścia sosny zwyczajnej safraniną z zielenią trwałą
Przygotowanie roztworu do barwienia
Dodaj 20 mg safraninysafraniny w proszku do zlewki o pojemności 100 ml.
Wlej 20 ml wody destylowanej do zlewki i przez ciągłe mieszanie przygotuj 0,1‑procentowy roztwór barwiący safraniny.
Przenieś 20 mg zieleni trwałejzieleni trwałej do innej zlewki o pojemności 100 ml.
Dodaj do niej 20 ml wody destylowanej i przygotuj 0,1‑procentowy roztwór barwiący.
Przefiltruj oba roztwory barwiące.
Przygotowanie szkiełek do obserwacji
Nawodnij preparaty po deparafinizacji (przeprowadź przez szereg alkoholowy, zanurzając je kolejno w alkoholu: 99,8%, 90%, 80%, 70% i 50%, a następnie w wodzie).
Zanurz skrawki w 0,1‑procentowym roztworze zieleni trwałej na 5–10 minut.
Przepłucz szkiełka 0,1‑procentowyn kwasem octowym przez 10–15 sekund.
Zanurz szkiełka w 0,1‑procentowym roztworze safraniny na 20–30 minut.
Wyczyść i odwodnij szkiełka (odwodnienie w etanolu 95% i 100%).
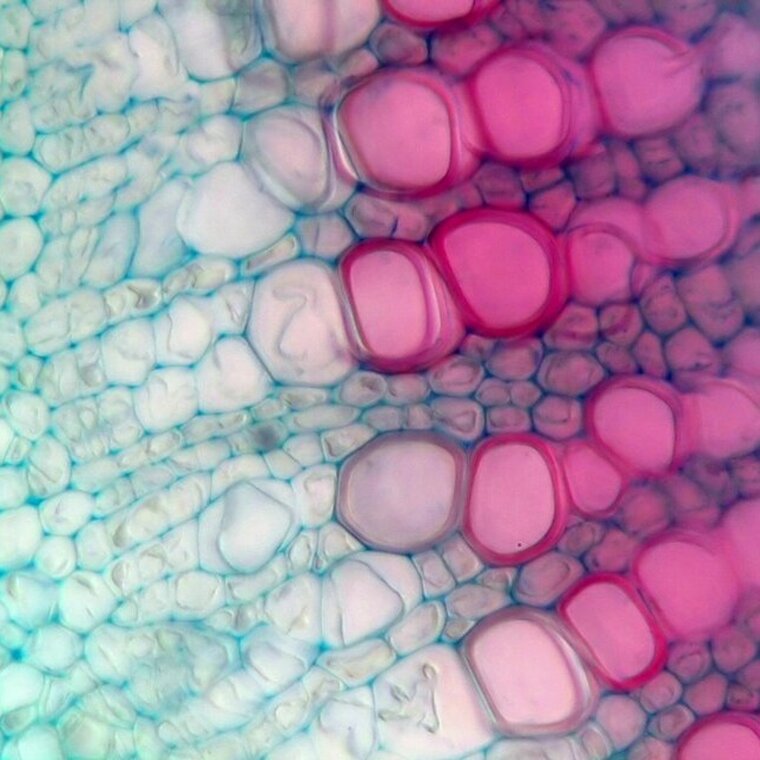
Wyniki barwienia
Ściana komórkowa celulozowa: kolor niebieskozielony
Ściana komórkowa zdrewniała: kolor czerwony
Słownik
struktury obserwowane w preparatach mikroskopowych powstałe podczas przygotowywania preparatów, niewystępujące w żywych komórkach lub tkankach

zasadowy barwnik organiczny, trwały (odporny na działanie światła, wody, mydła itp.), stosowany w histologii i cytologii, używany podczas barwienia kontrastowego; wiąże się z jądrami (DNA) i innymi polianionami tkankowymi oraz składnikami ligniny i plastydami w tkankach roślinnych
niebieskozielony barwnik rozpuszczalny w alkoholu; może być stosowany z safraniną jako barwnik do tkanek roślinnych