Przeczytaj
Związki zawierające grupę karboksylową
Grupa karboksylowaGrupa karboksylowa to organiczna grupa funkcyjna składająca się z atomu węgla związanego z atomem tlenu za pomocą wiązania podwójnego i z grupą hydroksylową za pomocą wiązania pojedynczego.
Grupa karbonylowaGrupa karbonylowa to organiczna grupa funkcyjna, która składa się z atomu węgla połączonego z atomem tlenu za pomocą wiązania podwójnego.
Kwasy karboksylowe
Wszystkie kwasy karboksylowekwasy karboksylowe zawierają w swojej budowie grupę karboksylową, która determinuje ich właściwości chemiczne, ale również wiele właściwości fizycznych.

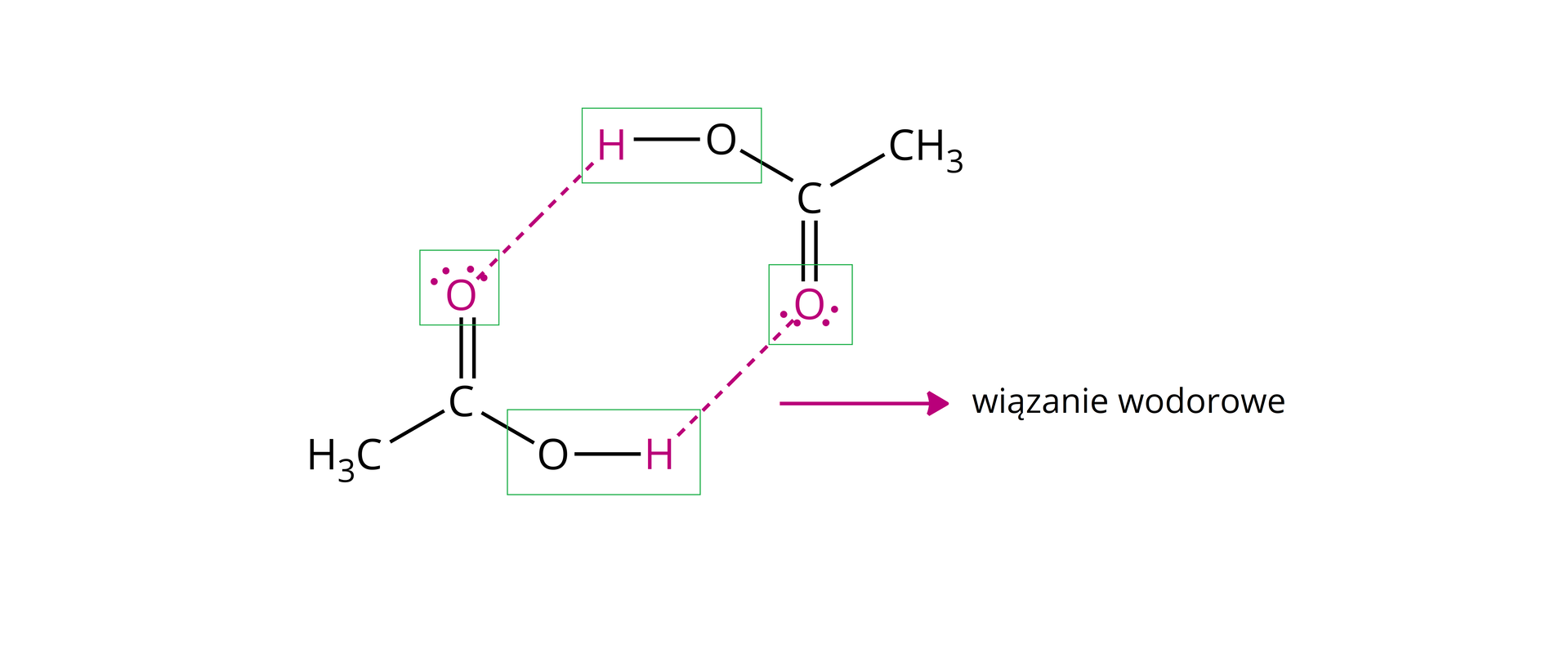
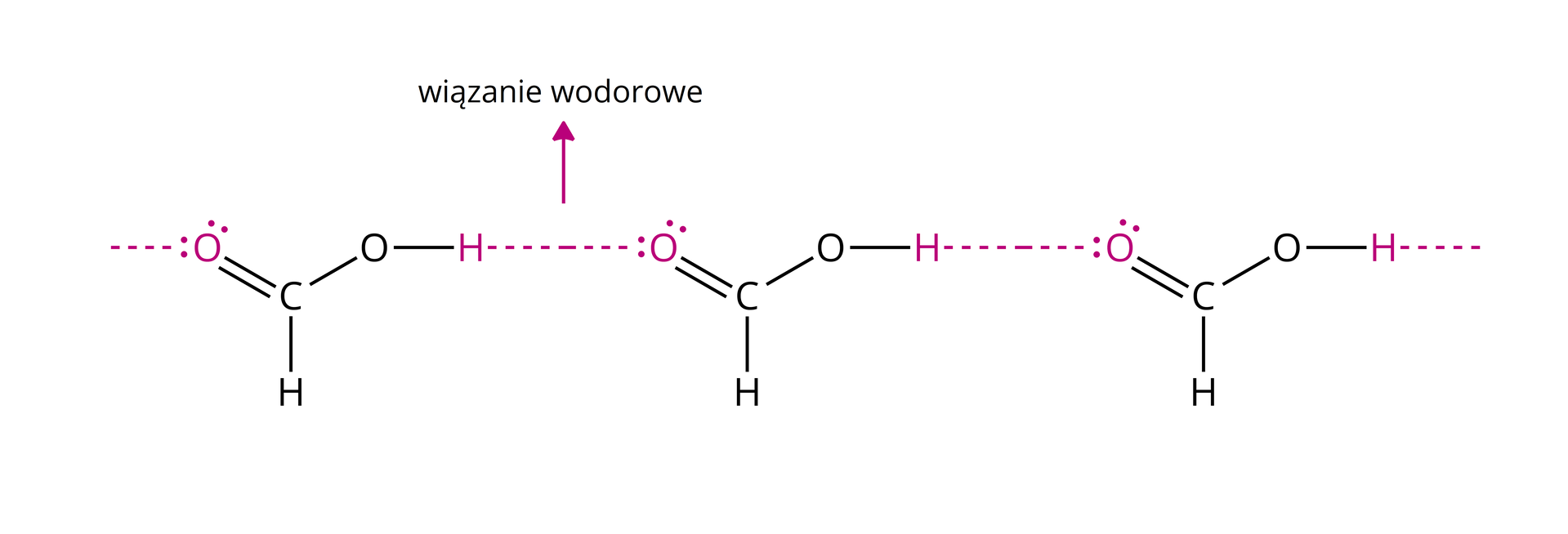
Ponieważ w grupie karboksylowej występuje atom wodoru związany z silnie elektroujemnym atomem tlenu to kwasy karboksylowe zdolne są do tworzenia wiązań wodorowych. Wpływa to na silną asocjację cząsteczek i tworzenie cyklicznych dimerów (agregatów dwucząsteczkowych) lub łańcuchów złożonych z wielu cząsteczek.
Tworzenie wiązań wodorowych wpływa na wysokie temperatury wrzenia kwasów karboksylowych, ponieważ potrzeba więcej energii aby rozerwać tego typu oddziaływania. Kwasy karboksylowe charakteryzują się więc niską lotnością.
Nazwa | Temperatura wrzenia [°C] | Temperatura topnienia [°C] | Stan skupienia |
Kwas metanowy (mrówkowy) | 100,7 | 8,4 | ciecz |
Kwas etanowy (octowy) | 117,9 | 16,6 | ciecz |
Kwas benzenokarboksylowy (benzoesowy) | 249 | 122,1 | ciało stałe |
Kwas oktadekanowy (stearynowy) | 361 | 69,3 | ciało stałe |
Indeks górny Tabela 1. Wybrane właściwości fizyczne kwasów karboksylowych. Indeks górny koniecTabela 1. Wybrane właściwości fizyczne kwasów karboksylowych.
Niższe kwasy karboksylowe to ciecze, natomiast zmiana stanu skupienia w szeregu homologicznym następuje stopniowo, więc wyższe oraz aromatyczne kwasy karboksylowe charakteryzują się stałym stanem skupienia.
Jak grupa karboksylowa wpływa na polarność cząsteczki?
Kwasy karboksylowe o krótkich łańcuchach węglowych bardzo dobrze rozpuszczają się w wodzie ze względu na większy wkład hydrofilowej części, czyli grupy karboksylowej. Dobra rozpuszczalność w wodzie prostych kwasów karboksylowych wynika również z tworzenia wiązań wodorowych pomiędzy cząsteczkami kwasu a cząsteczką wody. Im więcej jednak atomów węgla, oraz im bardziej rozbudowana reszta węglowodorowa, tym coraz większy udział części niepolarnej (hydrofobowej) co powoduje zmniejszenie rozpuszczalności w wodzie, a zwiększenie rozpuszczalności w rozpuszczalnikach niepolarnych. Można więc powiedzieć, że rozpuszczalność kolejnych homologów kwasów karboksylowych zmniejsza się ze wzrostem hydrofobowego łańcucha węglowego.
Aminokwasy
AminokwasyAminokwasy to wielofunkcyjne pochodne węglowodorów, w których cząsteczkach występują takie grupy funkcyjne jak: grupa aminowa (-NHIndeks dolny 22) oraz grupa karboksylowa (-COOH).

Przykłady aminokwasów
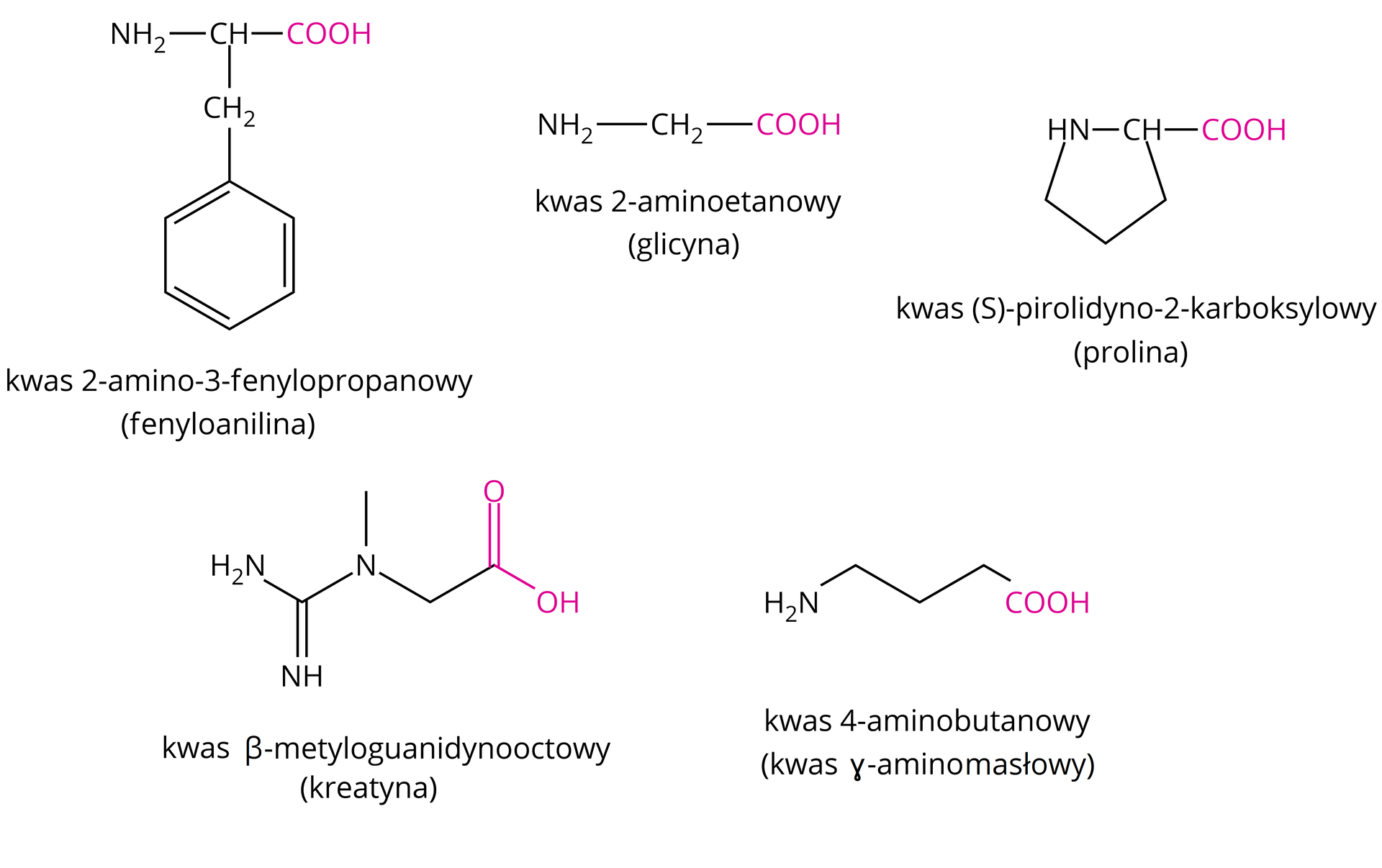
Obie grupy funkcyjne są polarne, co znacząco wpływa na rozpuszczalność aminokwasów w wodzie. Dlatego proste aminokwasy białkowe, które zawierają krótkie łańcuchy węglowe bardzo dobrze rozpuszczają się w wodzie. Jeżeli jednak fragment boczny aminokwasu zawiera grupy niepolarne, czyli część hydrofobowa przeważa nad częścią hydrofilową to rozpuszczalność w wodzie znacząco maleje na rzecz co raz lepszej rozpuszczalności w rozpuszczalnikach niepolarnych.
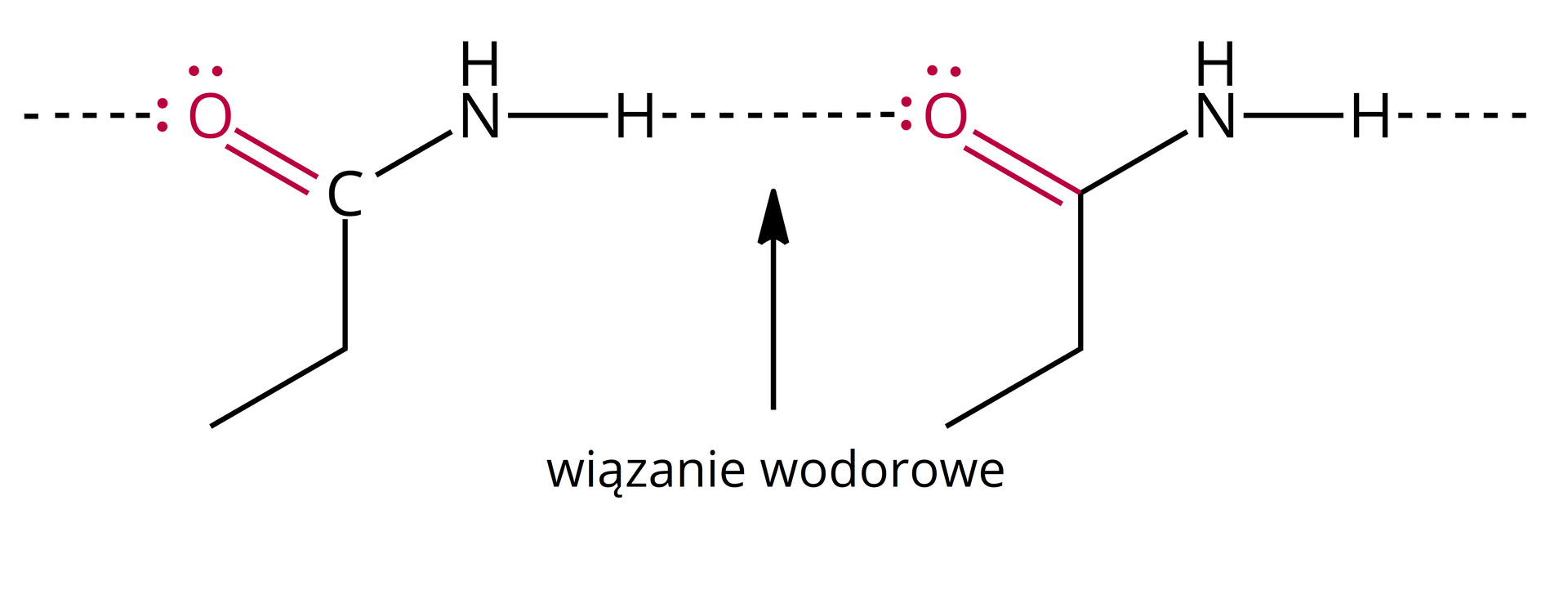
Ze względu na występowanie w obu grupach funkcyjnych atomów wodoru związanych z silnie elektroujemnymi atomami azotu i tlenu, pomiędzy cząsteczkami występują wiązania wodorowewiązania wodorowe. Wiązania te stabilizują drugorzędową strukturę białek tworzonych przez aminokwasy, czyli alfa helisę oraz beta harmonijkę.
Hydroksykwasy
HydroksykwasyHydroksykwasy to wielofunkcyjne pochodne węglowodorów, w których cząsteczkach występują takie grupy funkcyjne jak: grupa hydroksylowa (-OH) oraz grupa karboksylowa (-COOH).
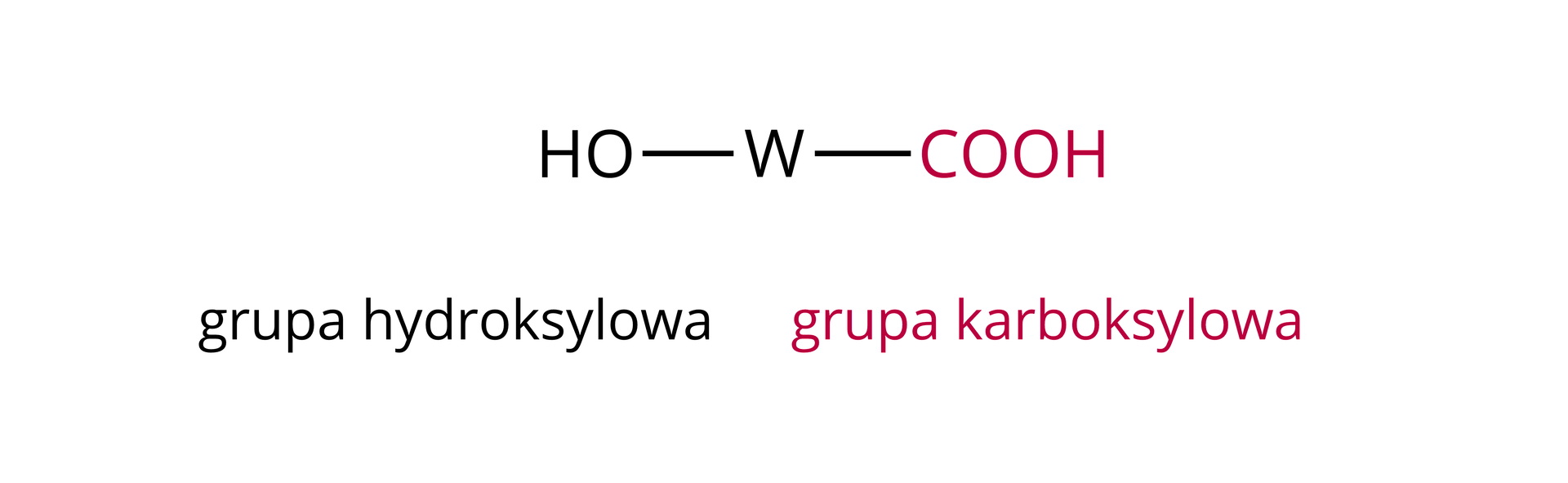
Przykłady wybranych hydroksykwasów

Podobnie jak w przypadku aminokwasów i niższych kwasów karboksylowych, hydroksykwasy bardzo dobrze rozpuszczają się w wodzie, ponieważ zarówno grupa hydroksylowa jak i karboksylowa to grupy polarne. Dobra rozpuszczalność w wodzie wynika również z możliwości tworzenia wiązań wodorowych pomiędzy cząsteczkami hydroksykwasów i cząsteczkami wody.
Jeżeli jednak w cząsteczkach hydroksykwasów występuje większy udział grup hydrofobowych, to znacznie spada ich rozpuszczalność w wodzie.
Wiązania wodorowe tworzą się również pomiędzy cząsteczkami hydroksykwasów, co wpływa na ich wysokie temperatury wrzenia i topnienia.
Słownik
jednowartościowa grupa atomów, składająca się z jednego atomu węgla, dwóch atomów tlenu i jednego atomu wodoru
organiczna grupa funkcyjna, w której atom węgla połączony jest wiązaniem podwójnym z atomem tlenu. Może być zapisywana skrótowo jako CO, -C(O)-, lub >C=O
związki organiczne, których cząsteczki zawierają grupę karboksylową (–COOH) połączoną z grupą alifatyczną, alicykliczną, aromatyczną lub heterocykliczną
związki organiczne powszechnie występujące w organizmach żywych, zawierające w cząsteczce co najmniej jedną grupę karboksylową (–COOH) i co najmniej jedną grupę aminową (–NHIndeks dolny 22)
związki organiczne o cząsteczkach zawierających grupy karboksylowe (–COOH) i jedną lub więcej niż jedną grupę hydroksylową (-OH)
słabe oddziaływania tworzące się pomiędzy atomem wodoru związanym z silnie elektroujemnym pierwiastkiem (np. O, N, F) a wolną parą elektronową silnie elektroujemnego pierwiastka należącego do drugiej cząsteczki; wiązania wodorowe powodują asocjację cząsteczek i wpływają na wysokie temperatury wrzenia i topnienia cząsteczek
Bibliografia
Dudek‑Różycki K., Płotek M., Wichur T., Węglowodory. Repetytorium i zadania, Kraków 2020.
Dudek‑Różycki K., Płotek M., Wichur T., Związki organiczne zawierające azot oraz wielofunkcyjne pochodne węglowodorów. Repetytorium i zadania, Kraków 2021.
Dudek‑Różycki K., Płotek M., Wichur T., Kompendium terminologii oraz nazewnictwa związków organicznych. Poradnik dla nauczycieli i uczniów, Kraków 2020.
McMurry J., Chemia organiczna, Warszawa 2000.