Przeczytaj
Hydroliza peptydów
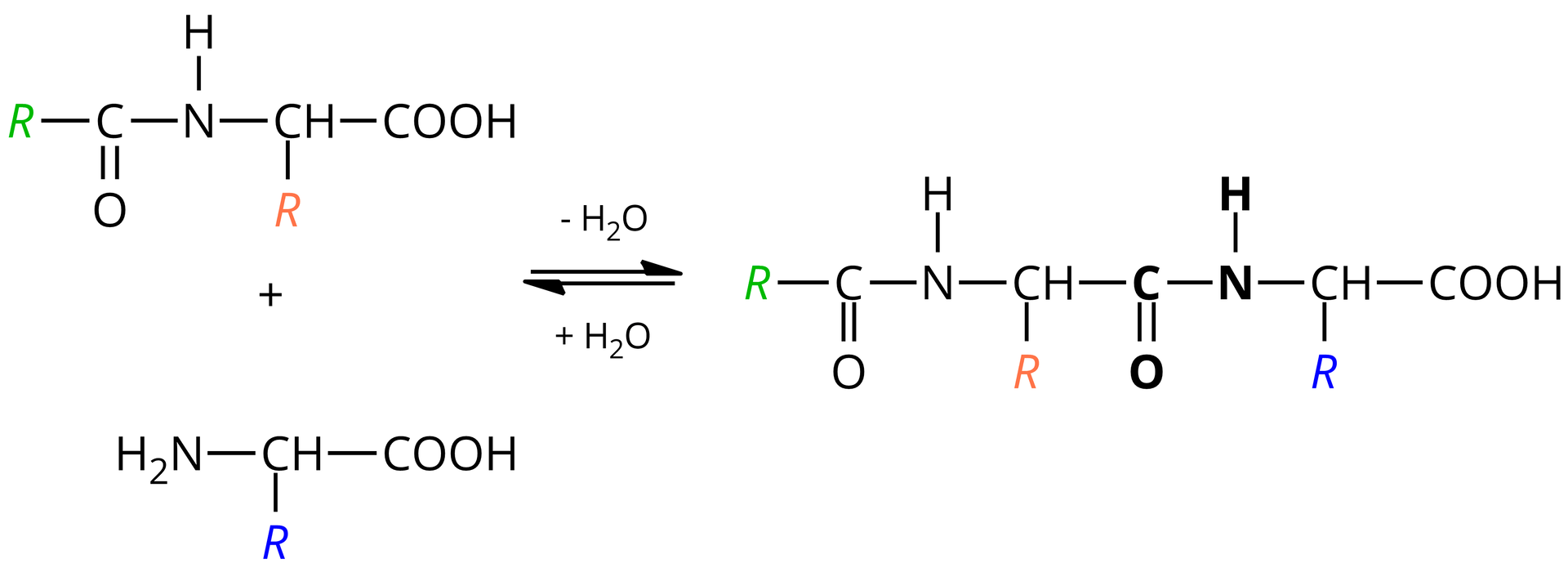
Peptydy powstają w wyniku reakcji kondensacji, podczas której między grupą -karboksylową () i grupą -aminową () tworzy się połączenie zwane wiązaniem peptydowymwiązaniem peptydowym. Produktem ubocznym jest cząsteczka wody.
HydrolizaHydroliza jest reakcją odwrotną do reakcji kondensacji, czyli polega na rozerwaniu utworzonych wiązań peptydowych i odtworzeniu poszczególnych aminokwasów. Bierze w niej udział woda, której cząsteczki rozpadają się na jony hydroksylowe i jony hydroniowe , a następnie łączą się z uwolnionymi wiązaniami substancji wielkocząsteczkowej. Przemiany te można przedstawić uproszczonym schematem:
Peptydy, jak i białka, ulegają hydrolizie w środowisku wodnym i w podwyższonej temperaturze oraz w obecności stężonych kwasów nieorganicznych lub stężonych zasad.
W reakcji tej powstają odpowiednie aminokwasy. Analizując skład otrzymanych produktów hydrolizy, można ustalić, z jakich reszt aminokwasowych składał się dany peptyd.
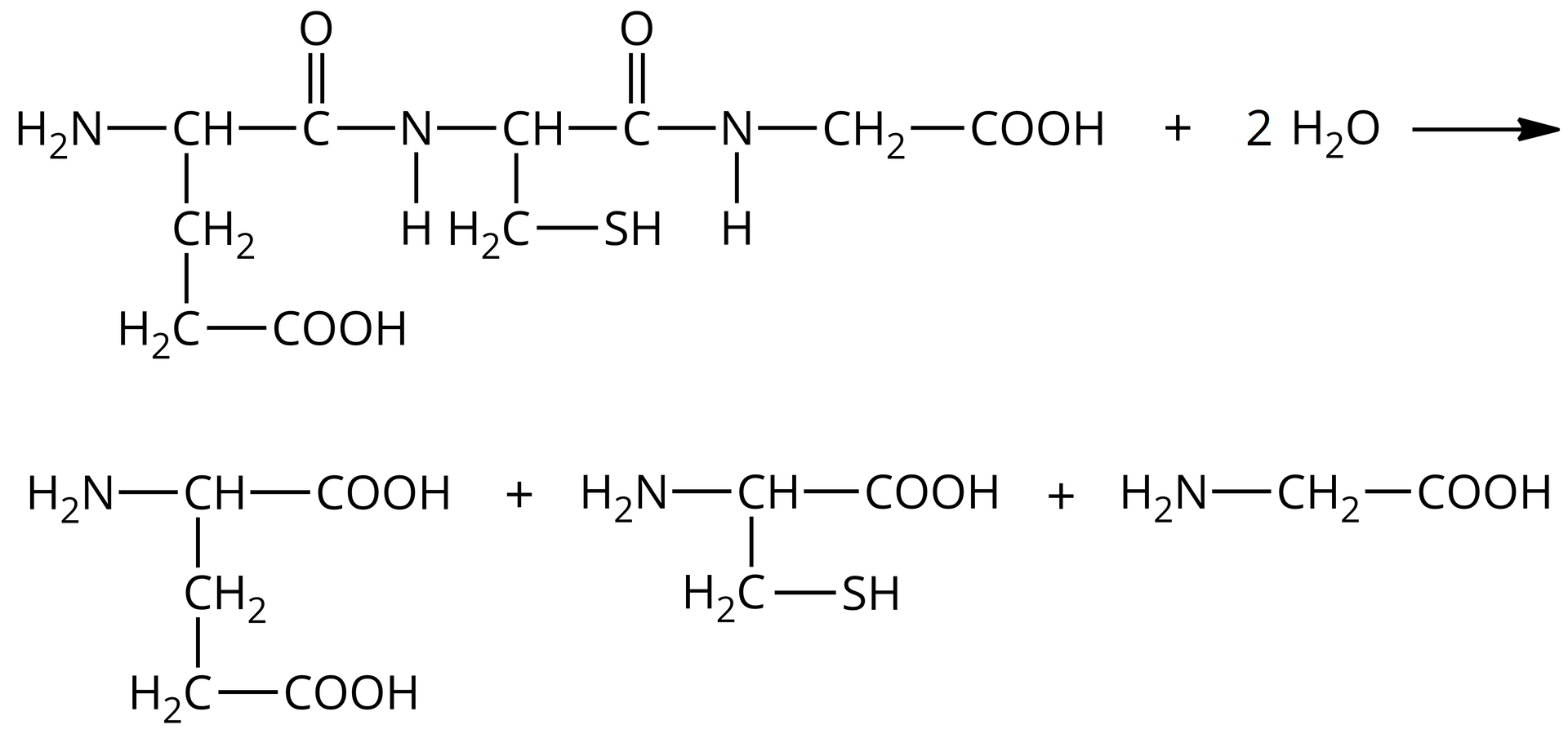
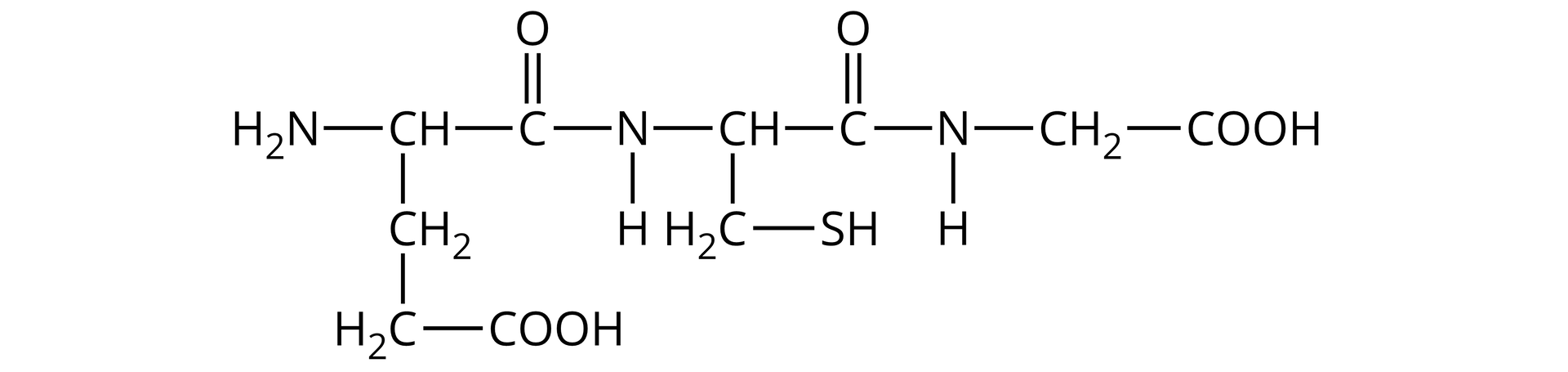
Przykładem peptydu, którego obecność stwierdzono w większości żywych komórek, jest glutation.
Ile i jakie aminokwasy powstaną w wyniku hydrolizy glutationu? Czy potrafisz zapisać tę reakcję?
Sposoby przeprowadzania hydrolizy peptydów i białek
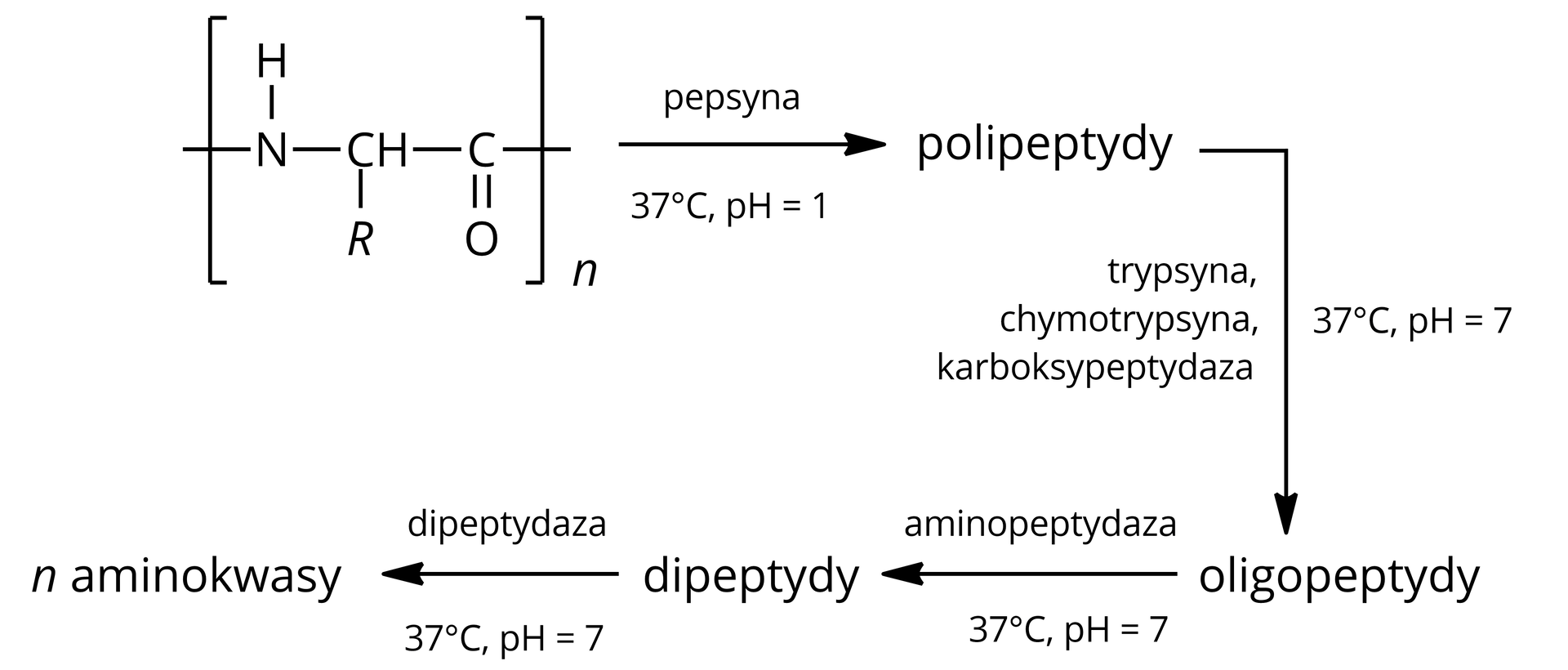
W organizmach żywych hydroliza wiązań peptydowych w peptydach katalizowana jest przez enzymyenzymy zwane proteazamiproteazami i odgrywa istotną rolę we wszystkich procesach fizjologicznych. Jest to reakcja nieodwracalna, regulowana na wielu poziomach (przez ekspresję genów kodujących proteazy oraz kontrolę aktywności proteaz wewnątrz i na zewnątrz komórek).
Proteoliza, zachodząca poza komórką (zewnątrzkomórkowa), jest często kontrolowana przez wyspecjalizowane białka inhibitorowe, które wiążą się z proteazami i blokują ich aktywność. Na przykład inhibitory proteaz stanowią 10% wszystkich białek w surowicy ssaków.
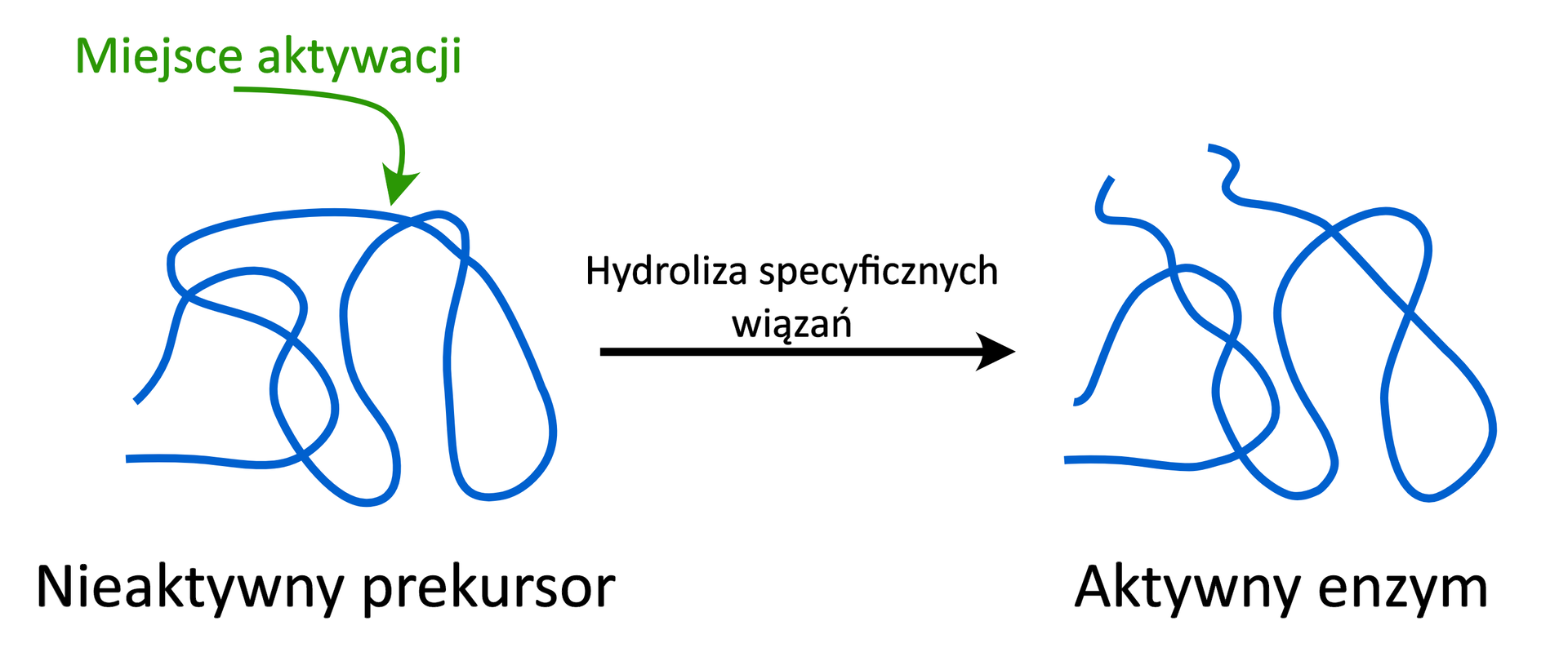
Uproszczony schemat przedstawia aktywację nieaktywnego prekursora enzymu poprzez hydrolizę specyficznych wiązań peptydowych w obrębie katalizatora. Jest to sposób aktywacji charakterystyczny dla niektórych enzymów, np. trypsyny.
Słownik
charakterystyczne ugrupowanie, które powstaje w reakcji kondensacji aminokwasów
liniowa sekwencja kolejnych aminokwasów połączonych wiązaniami peptydowymi
rozerwanie łańcucha polipeptydowego na poszczególne aminokwasy
(z gr. ἔnuzetaupsilonmuomicronnu, od ἔnu en „w” i zetaύmueta dzýmē „zaczyn, (za)kwas”) wielkocząsteczkowe, w większości białkowe, katalizatory, które przyspieszają specyficzne reakcje chemiczne poprzez obniżenie ich energii aktywacji
podklasa enzymów z klasy hydrolaz katalizująca proteolizę, czyli hydrolizę wiązań peptydowych
rozkład wiązania peptydowego z udziałem proteaz; w efekcie z białek powstają peptydy i aminokwasy; proteoliza jest jednym z procesów zachodzących podczas trawienia
Bibliografia
Banaszkiewicz S., Zbiór zadań, Chemia organiczna, Warszawa 2004, s. 82‑89.
Czerwińska A., Jelińska‑Kazimierczuk M., Kuśmierczyk K., Chemia 2, Warszawa 2003, s. 284‑327.
Jakubke H‑D., Jeschkeit H., Aminokwasy, peptydy, białka, Warszawa 1989.
Żak I.,Polipeptydy i białka, [w:] Chemia medyczna, pod red. Iwony Żak, Katowice 2001, s. 244‑274.