Przeczytaj
Charakterystyka i właściwości tłuszczów
Tłuszcze należą do grupy estrów, dlatego, tak jak pozostałe estry, ulegają procesom hydrolizy w odpowiednich warunkach. Są to reakcje hydrolizy zasadowej oraz hydrolizy kwasowej. Przyjrzyjmy się więc, czym się różnią oba procesy.
Hydroliza w środowisku zasadowym
W reakcji zmydlania, czyli zasadowej hydrolizy tłuszczów, powstaje glicerolglicerol (propano‑1,2,3‑triol) oraz sole kwasów tłuszczowych, z których reszt kwasowych zbudowany jest wyjściowy tłuszcz. Spójrzmy, jak właściwie wygląda schematyczne równanie reakcji chemicznej powstawania mydła:

Mydła to nic innego jak właśnie sole sodowe lub potasowe wyższych kwasów karboksylowych (tłuszczowych). Zwykłe znane Ci mydło jest najczęściej mieszaniną soli sodowych wyższych kwasów tłuszczowych, ponieważ tłuszcz, z którego to mydło powstaje, również jest mieszaniną.
Hydroliza zasadowa tłuszczu przebiega wg mechanizmu substytucji nukleofilowej, tak jak typowa hydroliza estru. Dla przejrzystości poniższego schematu, pokazano tylko jedno ugrupowanie estrowe, ale dla dwóch pozostałych grup estrowych w cząsteczce tłuszczu mechanizm przebiega w ten sam sposób. Spójrzmy zatem na schemat i przeanalizujmy, co dzieje podczas każdego etapu.
Hydroliza zasadowa tłuszczu przebiega wg mechanizmu substytucji nukleofilowej, tak jak typowa hydroliza estru. Dla przejrzystości poniższego schematu, pokazano tylko jedno ugrupowanie estrowe, ale dla dwóch pozostałych grup estrowych w cząsteczce tłuszczu mechanizm przebiega w ten sam sposób. Zapoznaj się z opisem schematu i przeanalizuj, co dzieje się podczas każdego etapu.
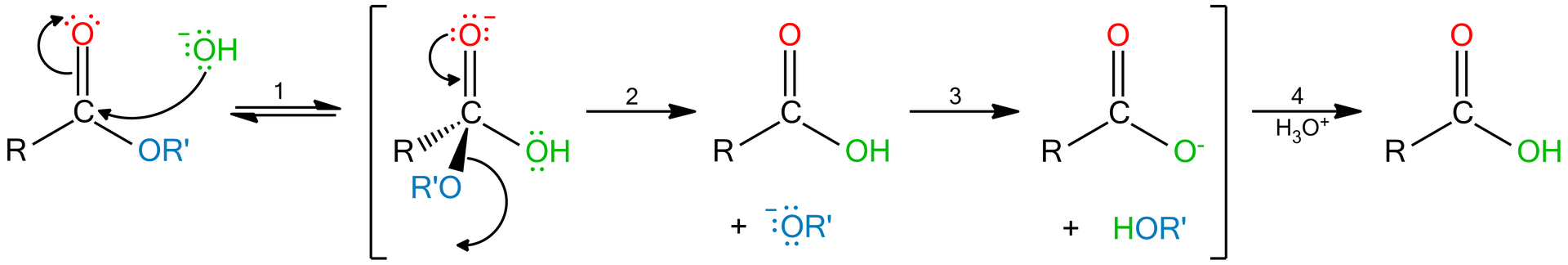
Nukleofilem jest anion wodorotlenkowy, który przyłącza się do atomu węgla grupy karbonylowej tłuszczu w pierwszym etapie. Zauważ przy tym, że kształt cząsteczki jest trygonalny – hybrydyzacja . Po addycji nukleofilowej jonu wodorotlenkowego powstaje typowy, tetraedryczny (hybrydyzacja ) produkt pośredni. W czasie drugiego etapu następuje odszczepienie jonu (jonu alkoksylowego) i powstaje kwas karboksylowy, który ulega deprotonacji w trzecim etapie, tworząc anion karboksylanowy. Zwróć uwagę – jon alkoksylowy ulega protonowaniu przez oderwanie kwasowego protonu z powstałego kwasu karboksylowego. W czwartym etapie następuje protonowanie jonu karboksylanowego przez dodanie wodnego roztworu kwasu nieorganicznego (np. ) lub przyłącza się jon .
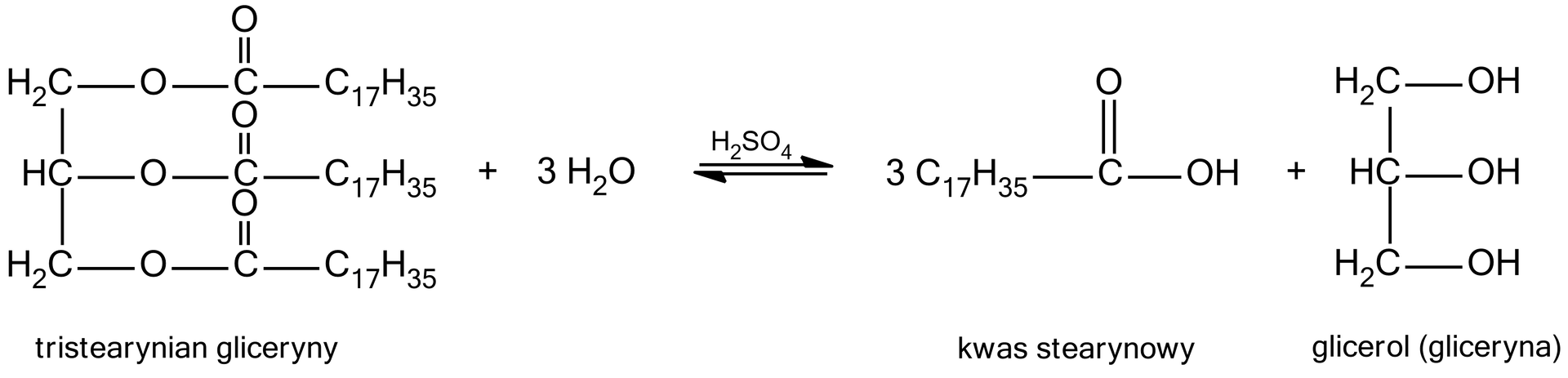
A teraz, na przykładzie hydrolizy zasadowej tristearynianu gliceryny:

W przypadku, gdy grupy R nie są identyczne, możliwe jest również otrzymanie mieszaniny soli kwasów tłuszczowych. W tym przykładzie są to: stearynian sodu, oleinian sodu oraz palmitynian sodu. Wówczas równanie tej reakcji chemicznej wygląda następująco:

Do niedawna jedyną metodą otrzymywania glicerolu i kwasów tłuszczowych było zmydlanie tłuszczów. Obecnie są one produkowane w wyniku obróbki ropy naftowej. Dzięki temu, do procesu zmydlania używa się tylko takich tłuszczów, które nie nadają się do innych celów.
Czy można przygotować właściwy roztwór mydła?
Zauważ, że otrzymywane sole posiadają długie łańcuchy alifatycznełańcuchy alifatyczne, które stanowią część hydrofobową („bojącą się wody”), czyli niepolarną. Z drugiej strony posiadają również polarny koniec jonowy , czyli hydrofilowy („lubiący wodę”). Zatem nie można mówić o właściwym roztworze mydła. W rzeczywistości mydło jest rozproszone w wodzie w postaci kulistych tworów, czyli miceli.
Czy można otrzymać mydło z twardej wody
Na pewno ze szkoły, jak i życia codziennego znasz pojęcie tzw. twardej wody. Jest bogata w sole wapniowe i magnezowe, które, reagując z mydłem, tworzą nierozpuszczalne sole wapniowe i magnezowe wyższych kwasów karboksylowych. To one są odpowiedzialne za brudny pierścień w wannie czy zszarzałą białą odzież. Równanie takiej reakcji chemicznej możemy zapisać następująco:
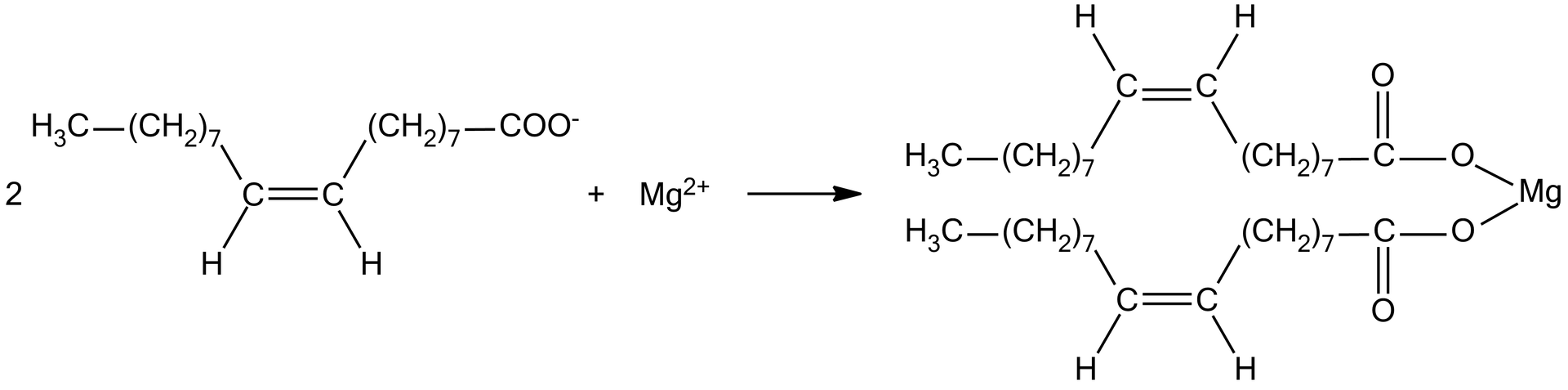
Jak za pomocą hydrolizy w środowisku kwasowym otrzymać kwasy tłuszczowe?
Aby otrzymać kwas tłuszczowy należy przeprowadzić hydrolizę tłuszczu pod wpływem wody w środowisku kwasowym. Podobnie jak w procesie zmydlania, tutaj również otrzymujemy glicerol, ale drugim produktem nie są sole kwasu tłuszczowego, lecz same kwasy tłuszczowe, składające się z reszt kwasowych, które tworzyły tłuszcz wyjściowy.
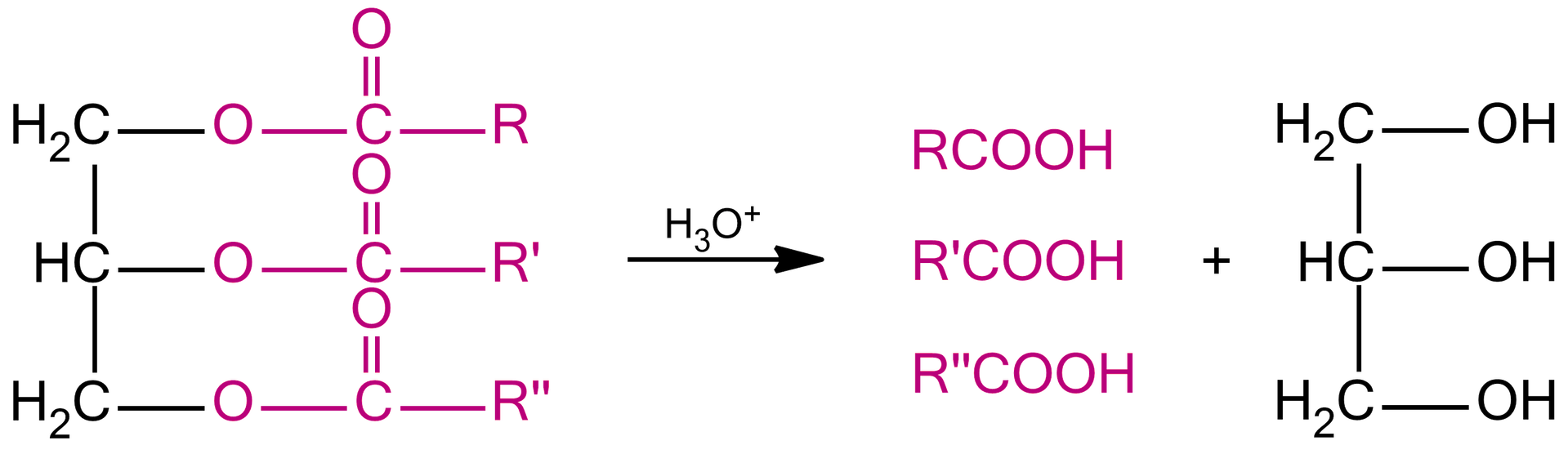
Hydroliza estrów (w tym tłuszczów) w warunkach kwasowych przebiega wg poniższego schematu. Spójrzmy na następujące po sobie etapy.
Hydroliza estrów (w tym tłuszczów) w warunkach kwasowych przebiega wg poniższego schematu. Zapoznaj się z jego opisem.

Cząsteczka estru zostaje najpierw aktywowana przez protonowanie karbonylowego atomu tlenu w pierwszym etapie, dzięki czemu w drugim etapie następuje addycja nukleofilowa cząsteczki wody. Wówczas tworzy się tetraedryczny produkt pośredni i w trzecim etapie następuje przeniesienie protonu. Eliminacja cząsteczki alkoholu w czwartym etapie prowadzi do produktu końcowego, czyli kwasu karboksylowego. Wykorzystany na początku reakcji katalizator kwasowy zostaje odtworzony.
W galerii poniżej przedstawiono konkretne przykłady.
Jeżeli w cząsteczce powstającego kwasu tłuszczowego obecne są wiązania podwójne, to zazwyczaj mają one geometrię cis.
Pamiętaj, że hydroliza tłuszczów zachodzi również w Twoim organizmie. Tłuszcze, przechodząc przez przewód pokarmowy człowieka i zwierząt, ulegają rozkładowi pod wpływem enzymów zwanych lipazami, w wyniku czego również otrzymujemy glicerol oraz kwasy tłuszczowe.
Słownik
x(gr. glykerós „słodki”; eídos „postać”) powszechnie znane jako tłuszcze. Są to estry powstałe w wyniku reakcji glicerolu i wyższych kwasów karboksylowych (nazywanych kwasami tłuszczowymi)
(z łac. glycerolum), gliceryna, propano‑1,2,3‑triol; jest to najprostszy trwały alkohol trójwodorotlenowy
prosty lub rozgałęziony łańcuch węglowodorowy, w których atomy węgla nie tworzą struktur zamkniętych (pierścieni)
roztwór, w którym cząstki substancji rozpuszczonej mają rozmiary mniejsze od 1 nm ( 10Indeks górny −9−9 m).
Bibliografia
Danikiewicz W., Część III. Chemia organiczna, Wydawnictwo Oficyna Edukacyjna, Warszawa, 2009.
Kaznowski K., CHEMIA Vademecum maturalne, Wydawnictwo Oficyna Edukacyjna, Warszawa, 2016.
McMurry J., Chemia organiczna, Wydawnictwo Naukowe PWN, Warszawa, 2000.
McMurry J., Chemia organiczna, Wydawnictwo Naukowe PWN, Warszawa, 2016.
Morrison R.T., Boyd R.N., Chemia organiczna, Wydawnictwo Naukowe PWN, Warszawa, 1985.